биофизика фотосинтеза. Федеральное государственное бюджетное образовательное учреждение высшего образования астраханский государственный университет
 Скачать 1.06 Mb. Скачать 1.06 Mb.
|
|
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «АСТРАХАНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ» Биологический факультет Кафедра физиологии, морфологии, генетики и биомедицины Курсовая работа выполнена в рамках изучения дисциплины «Биофизика» «Биофизика фотосинтеза» Направление подготовки: 06.03.01 Биология Направленность (профиль): Генетика Выполнила: Мухтарова Амина Рауфовна Научный руководитель: кандидат биологических наук; заместитель декана биологического факультета; доцент кафедры Касимова Сауле Куаншевна Астрахань-2019 ОглавлениеМИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ 1 3 Глава 1 ОБЩИЕ ПОНЯТИЯ 4 1.1 Общая характеристика фотосинтеза 4 1.2 Изучение фотосинтеза 4 1.3 Значение фотосинтеза 5 Глава 2 ФОТОСИНТЕТИЧЕСКИЕ ПИГМЕНТЫ 6 2.1 Структурная основа для фотосинтетических процессов 6 2.2 Светособирающие комплексы 7 2.2.1 Фотосинтетические пигменты 8 2.3 Спектры поглощения хлорофиллов 9 Глава 3 ПРОЦЕССЫ ФОТОСИНТЕЗА 10 3.1 Физико-химическая основа фотосинтеза. 10 3.2 БИОФИЗИЧЕСКИЕ МЕХАНИЗМЫ ФОТОСИНТЕЗА. 15 3.3. Основные компоненты электротранспортной цепи 16 3.3.1. Фотосистема I 16 3.3.2. Фотосистема II 16 3.3.3. b6f или b/f-комплекс 18 3.4. Циклический и псевдоциклический транспорт электрона 18 3.5 Основные свойства фотосинтетического аппарата растений 18 3.5.1 Насыщение световой кривой фотосинтеза с ростом освещенности 18 3.5.2 «Эффект усиления» Эммерсона. 19 3.5.3 Эффект Кока-Жолио. 20 3.5.4 Задержанная флуоресценция. 21 ЗАКЛЮЧЕНИЕ 22 Литература 23 ВВЕДЕНИЕ Фотосинтез - один из важнейших механизмов жизни на Земле, поскольку, за его счет образуются как сложные высокоупорядоченные органические вещества, так и кислород, потребляемые другими организмами (бактериями, растениями и животными) в качестве источников строительного материала и энергии. В работе мы более подробно рассматриваем механизм фотосинтеза, а именно обращаем внимание происходящие процессы со стороны биофизики. Фотосинтез – сложный, но вместе с тем интересный и очень красивый процесс. Он появился на ранних этапах эволюции у различных бактерий – пурпурных, цианобактерий, зеленых серных бактерий и других, у одноклеточных эукариот (водорослей) и, наконец, у высших растений. Исследование фотосинтетического аппарата прокариот внесло большой вклад в выяснение основных принципов и механизмов фотосинтеза. Но здесь мы рассмотрим главным образом механизмы фотосинтеза высших растений. Суть фотосинтеза заключается в получении высокоэнергетических электронов за счет энергии квантов света, поглощаемых хлорофиллом. Для того, чтобы предупредить возвращение электрона в исходное состояние и растрату полученной энергии на тепловые процессы, возбужденный электрон очень быстро переносится по электронтранспортной цепи на NADP+, который затем используется в биосинтетических реакциях. Исходным источником электронов является вода, которая при этом расщепляется и выделяет кислород. Этим кислородом, являющимся побочным продуктом фотосинтеза, дышат все аэробные организмы. Глава 1 ОБЩИЕ ПОНЯТИЯ1.1 Общая характеристика фотосинтезаФотосинтез (от греч. φωτο- — свет и σύνθεσις — синтез, совмещение, помещение вместе) — процесс образования органических веществ из углекислого газа и воды на свету при участии фотосинтетических пигментов (хлорофилл у растений, бактериохлорофилл и бактериородопсин у бактерий). В современной физиологии растений под фотосинтезом чаще понимается фотоавтотрофная функция — совокупность процессов поглощения, превращения и использования энергии квантов света в различных эндэргонических реакциях, в том числе превращения углекислого газа в органические вещества. 1.2 Изучение фотосинтезаПервые опыты по фотосинтезу были проведены Джозефом Пристли в 1770—1780-х годах, когда он обратил внимание на «порчу» воздуха в герметичном сосуде горящей свечой (воздух переставал быть способен поддерживать горение, помещённые в него животные задыхались) и «исправление» его растениями. Пристли сделал вывод что растения выделяют кислород, который необходим для дыхания и горения, однако не заметил что для этого растениям нужен свет. Это показал вскоре Ян Ингенхауз. Позже было установлено, что помимо выделения кислорода растения поглощают углекислый газ и при участии воды синтезируют на свету органическое вещество. В 1842 Роберт Майер на основании закона сохранения энергии постулировал, что растения преобразуют энергию солнечного света в энергию химических связей. В 1877 В. Пфеффер назвал этот процесс фотосинтезом. Хлорофиллы были впервые выделены в 1818 П. Ж. Пельтье и Ж. Кавенту. Разделить пигменты и изучить их по отдельности удалось М. С. Цвету с помощью созданного им метода хроматографии. Спектры поглощения хлорофилла были изучены К. А. Тимирязевым, он же, развивая положения Майера, показал что именно поглощенные позволяют повысить энергию системы, создав вместо слабых связей С-О и О-Н высокоэнергетические С-С (до этого считалось что в фотосинтезе используются жёлтые лучи, не поглощаемые пигментами листа). Сделано это было благодаря созданному им методу учёта фотосинтеза по поглощённому CO2, в ходе экспериментов по освещению растения светом разных длин волн (разного цвета) оказалось что интенсивность фотосинтеза совпадает со спектром поглощения хлорофилла. Окислительно-восстановительную сущность фотосинтеза (как оксигенного, так и аноксигенного) постулировал Корнелис ван Ниль. Это означало, что кислород в фотосинтезе образуется полностью из воды, что экспериментально подтвердил в 1941 А. П. Виноградов в опытах с изотопной меткой. В 1937 г. Роберт Хилл установил, что процесс окисления воды (и выделения кислорода), а также ассимиляции CO2 можно разобщить. В 1954—1958 Д. Арнон установил механизм световых стадий фотосинтеза, а сущность процесса ассимиляции CO2 была раскрыта Мельвином Кальвином с использованием изотопов углерода в конце 1940-х, за эту работу в 1961 ему была присуждена Нобелевская премия. В 1955 году был выделен и очищен фермент рибулозобисфосфат-карбоксилаза/оксигеназа.С4 фотосинтез был описан Ю. С. Карпиловым в 1960 и М. Д. Хэтчем и К. Р. Слэком в 1966. 1.3 Значение фотосинтезаФотосинтез является основным источником биологической энергии, фотосинтезирующие автотрофы используют её для синтеза органических веществ из неорганических, гетеротрофы существуют за счёт энергии, запасённой автотрофами в виде химических связей, высвобождая её в процессах дыхания и брожения. Энергия, получаемая человечеством при сжигании ископаемого топлива (уголь, нефть, природный газ, торф), также является запасённой в процессе фотосинтеза. Фотосинтез является главным входом неорганического углерода в биологический цикл. Весь свободный кислород атмосферы — биогенного происхождения и является побочным продуктом фотосинтеза. Формирование окислительной атмосферы (кислородная катастрофа) полностью изменило состояние земной поверхности, сделало возможным появление дыхания, а в дальнейшем, после образования озонового слоя, позволило жизни выйти на сушу. Глава 2 ФОТОСИНТЕТИЧЕСКИЕ ПИГМЕНТЫ2.1 Структурная основа для фотосинтетических процессовФотосинтетические процессы в листьях локализованы в специальных органеллах, называемых хлоропластами. Внутреннее пространство хлоропласта заполнено пластинчатыми гранулами зеленого цвета – гранами. Граны представляют собой стопки сильно сплюснутых мешочков – тилакоидами. Стенки тилакоидов – ламеллы – представляют собой тонкие фосфолипидные мембраны, внутри которых находятся липотропные участники первичных процессов фотосинтеза. К ним относятся белки, пигменты, переносчики электронов и протонов. Внутреннее межмембранное пространство тилакоидов является водной средой, в которой содержатся водорастворимые участники процесса. В межгранальном – стромальном – пространстве (также водном), находятся менее упакованные отдельные тилакоиды и ламеллы.(Рис.1) 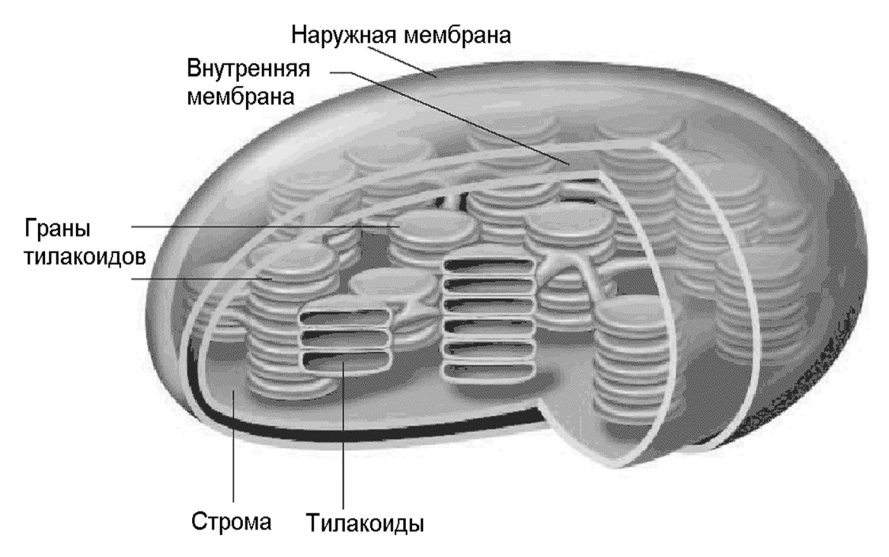 Рис.1. Строение хлоропласта 2.2 Светособирающие комплексыХлорофилл выполняет две функции: поглощения и передачи энергии. Более 90 % всего хлорофилла хлоропластов входит в состав светособирающих комплексов (ССК), выполняющих роль антенны, передающей энергию к реакционному центру фотосистем I или II. Помимо хлорофилла в ССК имеются каротиноиды, а у некоторых водорослей и цианобактерий — фикобилины, роль которых заключается в поглощении света тех длин волн, которые хлорофилл поглощает сравнительно слабо.Передача энергии идёт резонансным путём (механизм Фёрстера) и занимает для одной пары молекул 10−10—10−12 с, расстояние на которое осуществляется перенос составляет около 1 нм. Передача сопровождается некоторыми потерями энергии (10 % от хлорофилла a к хлорофиллу b, 60 % от каратиноидов к хлорофиллу), из-за чего возможна только от пигмента с максимумом поглощения при меньшей длине волны к пигменту с большей. Именно в таком порядке взаимно локализуются пигменты ССК, причём наиболее длинноволновые хлорофиллы находятся в реакционных центрах. Обратный переход энергии невозможен.ССК растений расположен в мембранах тилакоидов, у цианобактерий основная его часть вынесена за пределы мембран в прикреплённые к ним фикобилисомы — палочковидные полипептидно-пигментные комплексы, в которых находятся различные фикобилины: на периферии фикоэритрины (с максимумом поглощения при 495—565 нм), за ними фикоцианины (550—615 нм) и аллофикоцианины (610—670 нм), последовательно передающие энергию на хлорофилл a (680—700 нм) реакционного центра. 2.2.1 Фотосинтетические пигментыОсновной пигмент фотосинтеза - хлорофилл а (Chl a). Он состоит из порфириновой головки размером примерно 1,5х1,5 нм, обладающей гидрофильными свойствами, и длинного гидрофобного хвоста - фитола - длиной около 2,0 нм (Рис.2). В центре порфиринового кольца хлорофиллов находится ион Mg2+, связанный координационными связями с атомами азота (Рис.2). Другие формы хлорофилла - b,c,d, а также бактериохлорофилл - отличаются боковыми заместителями и распределением двойных связей в порфириновом кольце. 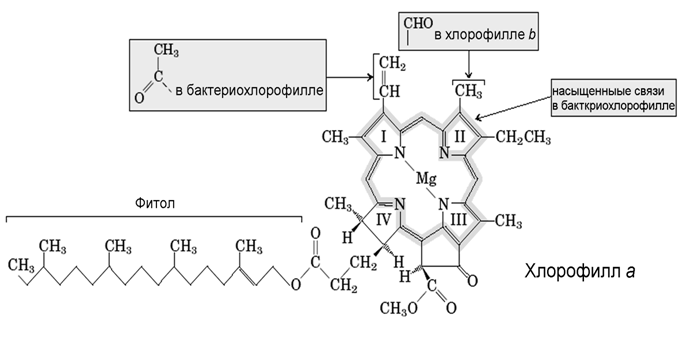 Рис.2. Структура хлорофилла а. Отмечены модификации, характерные для хлорофилла b и бактериохлорофилла. 2.3 Спектры поглощения хлорофилловСпектры поглощения хлорофиллов имеют две интенсивные полосы: характерную для порфиринов полосу Сорэ в синей или ближней ультрафиолетовой части спектра и «красную» полосу поглощения света в области 650-700 нм (у бактериохлорофиллов она смещена в ближнюю инфракрасную область 800-890 нм). Поглощение света в красной области спектра обеспечивается взаимодействием иона магния с сопряженной *-электронной системой порфиринового кольца. (Для сравнения - гем, содержащий в порфириновом кольце не Mg2+, а Fe2+ поглощает свет не в красной, а зелено-желтой части спектра). В клетке "красные полосы" поглощения хлорофиллов сдвинуты в длиноволновую область по сравнению со спектрами, полученными в органических растворителях (Табл.1), что указывает на значительную роль пигмент-пигментных, пигмент-белковых и пигмент-липидных взаимодействий вследствие плотной упаковки хлорофилльных молекул в фотосинтетической мембране.Методами низкотемпературной и дифференциальной спектрофотометрии выявлено до 10 модификаций хлорофилла a, различающихся по спектрам поглощения и флуоресценции (т.е. по расположению энергетических уровней), по экстрагируемости из мембраны (т.е. по гидрофильности/гидрофобности) и т.д. Они называются "нативными формами" хлорофилла а. Так, выделены Р670 (поглощающий свет 670-673 нм), Р680, Р700 и т.д. Основным фактором, обуславливающим свойства этих нативных форм, являются пигмент-пигментные взаимодействия, т.е. образование димеров и более крупных агрегатов. В пигментных агрегатах за счет взаимодействия *-электронных систем происходит "размазывание" электронного облака по двум или нескольким порфириновым кольцам. Соответственно, снижается верхний энергетический уровень и повышается способность поглощать более длинноволновый красный свет. Таблица 1. Полосы поглощения некоторых хлорофиллов в растворах органических растворителей и в клетках.
Кроме хлорофилла в фотосинтезирующих клетках встречаются и другие пигменты: феофитины, каротиноиды, фикоэритрины фикобилины и др. Все они содержат длинные цепочки сопряженных связей, в которых π-электронное облако «размазывается» по всей длине, что также приводит к снижению возбужденных энергетических уровней и позволяет поглощать кванты видимого света. У каротиноидов длина цепочек составляет примерно 40 углеродных атомов. Они поглощают свет в области 400-500 нм и имеют желтый или оранжевый цвет. Фикобилины поглощают свет в области 500-650 нм. Все они дополняют спектр поглощения хлорофилла, поглощая не только красный свет, но и свет других участков спектра, позволяя растениям эффективно улавливать солнечную радиацию. Глава 3 ПРОЦЕССЫ ФОТОСИНТЕЗА3.1 Физико-химическая основа фотосинтеза.Основная продукция фотосинтеза - это соединения с высоким восстановительным потенциалом – углеводы. Рабочим телом фотосинтетической машины в высших растениях и некоторых водорослях является вода. Процесс фотосинтеза включает в себя две стадии: 1. Фотолиз, физическая сущность которого заключается в разложении воды с помощью квантов света на кислород и водород, причем кислород является в этом процессе побочным продуктом; 2.Восстановление – получения глюкозы. Основным уравнением фотосинтеза в высших растениях является: 6CO + 6H2O + Nhν = 6O2 + C6H12O6 + ∆G, то есть, реакция идет только за счет энергии света и в итоге на один шаг реакции в её продуктах запасается ∆G= 686 ккал свободной энергии. Однако, во-первых, это уравнение объединяет два этапа превращения субстратов: световой и темновой, и, во-вторых, в данном уравнении не видны важные промежуточные продукты данной реакции. Поэтому для понимания необходимо записать эти этапы раздельно: 1. 6CO2+12H2O*+48hν+12НАДФ+18АДФ+18Ф → 6CO2+ 12НАДФН2+ 18АТФ + 6 O*2 → 2. → C6H12O6 + 6 O*2 + 6H2O + 12НАДФ +18АДФ +18Ф. Теперь видно, что продуктом световой стадии является восстановленные переносчики НАДФН2 и АТФ, которые в темновой стадии восстановления углекислоты до глюкозы (цикл Кальвина) соответственно окисляются и гидролизуются. Звездочкой отмечен кислород, который получается при фоторазложении воды. Необходимо отметить, что вода, которая образуется в темновой стадии, содержит другой кислород. Первая стадия фотосинтеза протекает на свету с помощью фотокатализатора. Фотокатализатором, или точнее, сенсибилизатором, в растениях является хлорофилл. Хлорофилл имеет гидрофобную часть и гидрофильную. То есть хлорофилл обладает амфотерными свойствами, которые способствуют самосборке агрегатов хлорофилла на границе липид-вода и на поверхности белков, где чередуются гидрофильные и гидрофобные участки. Структура центральной части хлорофилла аналогична гему железа в молекуле гемоглобина или цитохромах и обеспечивает поглощение света в видимом диапазоне. Существует три вида хлорофилла: a,b и c. Спектры поглощения хлорофиллов качественно похожи: в красной области – в районе 660-680 нм, в синей области – в районе длин волн 450 нм. Существование нескольких химически и физически различающихся форм хлорофиллов необходимо для того, чтобы сгладить спектр действия фотосинтеза в видимом участке солнечного спектра.Красная граница фотосинтеза определяется самыми длинноволновыми формами хлорофилла, и у высших растений располагается в районе 700 нм. Свет в зеленой части спектра, поглощают некоторые пигменты, в частности, каротин, так как хлорофиллы имеют относительно малое поглощение в этой части спектра. Кроме этого каротин защищает хлорофилл от деструктивных процессов, которые возникают при длительном нахождении электрона на триплетном уровне.В хлоропластах высших растений имеются две фотосистемы – фотосистема 1 (ФС1) и фотосистема 2 (ФС2), которые различаются по составу белков и пигментов. Светособирающая антенна ФС1 поглощает свет с длиной волны 700-730 нм, а ФС2 – 680 – 700 нм. Индуцированное светом окисление реакционных центров двух фотосистем сопровождается их обесцвечиванием, которое характеризуется изменениями спектров поглощения. Две фотосистемы связаны посредством цепи электронных переносчиков.ФС2 является источником электронов для ФС1. Индуцируемое светом разделение зарядов в фотореакционных центрах обеспечивает перенос электрона от воды, разлагаемой в ФС2, к конечному акцептору электрона – молекуле НАДФ+. Цепь электронного транспорта, соединяющая две фотосистемы, в качестве переносчиков электрона включает в себя молекулы пластохинона, отдельный электрон-транспортный белковый комплекс (так называемый b/f-комплекс) и водорастворимый белок пластоцианин (Рс). В ФС2 от возбужденного центра Р+ 680 электрон переносится сначала на первичный акцептор феофетин (Рhе), а затем на молекулу пластохинона Qа, прочно связанную с одним из белков ФС2. Затем электрон переносится на вторую молекулу пластохинона Qb, а Р+680 получает электрон от первичного донора – молекулы хлорофилла. После двукратного срабатывания реакционного центра ФС2 молекула пластохинона Qb получает два электрона и становится отрицательно заряженной. Эта молекула обладает высоким сродством к протонам, которые она захватывает из стромального пространства. После протонирования восстановленного пластохинона образуется электрически нейтральная форма этой молекулы (QbН2 или просто QН2), которая называется пластохинолом. Пластохинол выполняет роль подвижного переносчика двух электронов и двух протонов: покинув ФС2, молекула QН2 может легко перемещаться внутри тилакоидной мембраны, обеспечивая связь ФС2 с другими электрон-транспортными комплексами. Окислительный реакционный центр ФС2 обладает исключительно высоким сродством к электрону, то есть является очень сильным окислителем. Благодаря этому в ФС2 происходит разложение воды. Входящий в состав ФС2 водорасщепляющий комплекс (ВРК) содержит в своем активном центре группу ионов марганца, которые служат донорами электронов для Р+ 680 . Отдавая электроны окисленному реакционному центру Р+ 680, ионы марганца становятся «накопителями» положительных зарядов, непосредственно участвующих в реакции окисления воды. В результате последовательного четырехкратного срабатывания реакционного центра ФС2 в Mn-содержащем активном центре ВРК накапливаются четыре сильных окислительных эквивалента (четыре «дырки») в форме окислительных ионов марганца, которые, взаимодействуя с двумя молекулами воды, катализируют реакцию её разложения. Таким образом, в результате последовательной передачи электронов от ВРК к Р+ 680 происходит синхронное разложение сразу двух молекул воды, сопровождающееся выделением одной молекулы кислорода и четырех протонов, которые диффундируют во внутритилакоидное пространство хлоропластов. Образовавшаяся при функционировании ФС2 молекула пластихинола QН2 диффундирует внутри липидного бислоя тилакоидной мембраны к b/f-комплексу. При столкновении она связывается с ним и передает ему два электрона, при этом два освободившихся протона выходят во внутри тилакоидное пространство. В свою очередь b/f -комплекс служит донором электрона для пластоцианина, который выполняет роль связующего звена между b/f-комплексом и ФС1. Пластоцианин – это водорастворимый белок, имеющий в составе своего активного центра ион меди. Реакция восстановления и окисления пластоцианина сопровождается изменением валентности иона меди. Молекула пластоцианина быстро перемещается внутри тилакоида, обеспечивая перенос электрона от b/f-комплекса к ФС1. От восстановленного пластоцианина электрон поступает непосредственно к окислительным центрам ФС1. Таким образом, в результате совместного действия ФС1 и ФС2 два электрона от молекулы воды, разлагаемой в ФС2, через цепь электронного транспорта переносятся на молекулу НАДФ+, обеспечивая образование сильного восстановителя НАДФ•Н. Схематически выше описанные процессы представлены на рисунке 3. 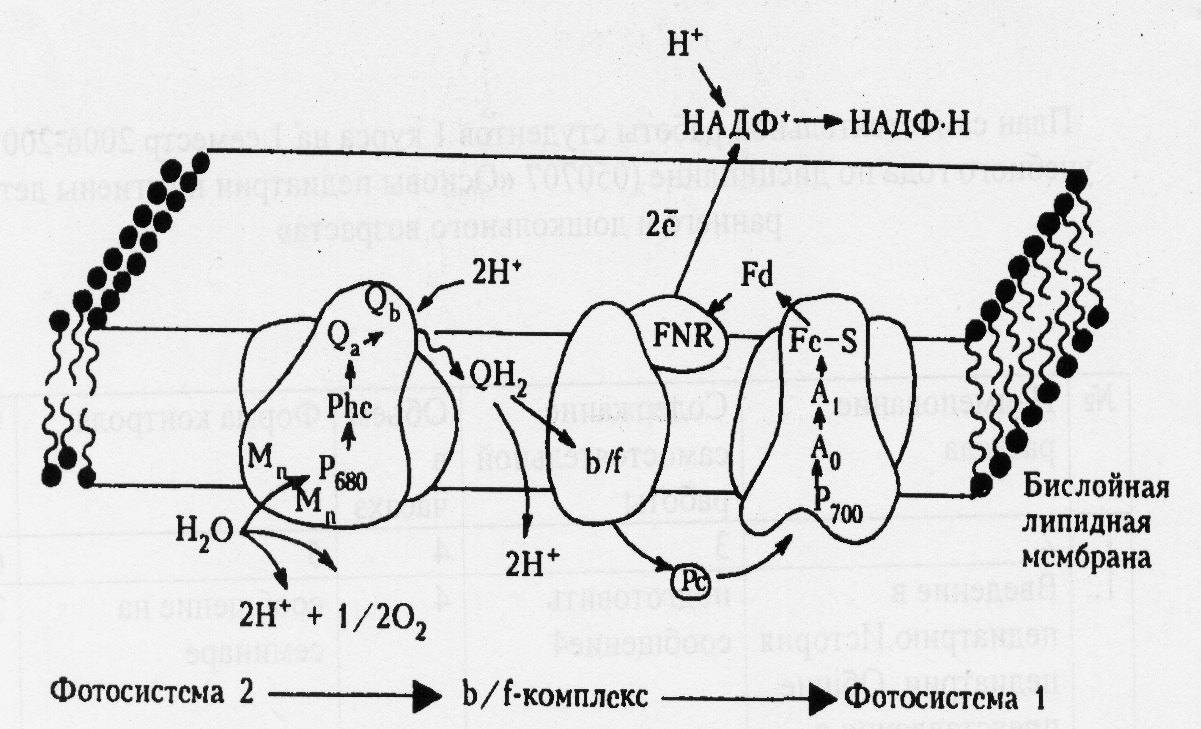 Рис.3. Расположение электрон-транспортных комплексов (ФС1, ФС2 b/f-комплекса) 3.2 БИОФИЗИЧЕСКИЕ МЕХАНИЗМЫ ФОТОСИНТЕЗА.Транспорт возбужденных π-электронов, обеспечивающий аккумулирование (конвертирование) солнечной энергии в макроэргических связях АТФ, свойствен хлорофилл содержащим бактериям и зеленым растениям. Хлорофилл обладает уникальной способностью быть как донором, так и акцептором электронов в зависимости от действия на него солнечного света. В исходном состоянии (когда на него не действует свет) хлорофилл служит донором электронов. Поглотив фотон в видимой области солнечного излучения, этот пигмент теряет электрон, окисляется и приобретает акцепторные свойства. Принимая электрон от сопряженных с ним веществ, он снова испытывает восстановление и становится готовым отдать электроны, если на него вновь подействует свет. Такая цикличность в работе хлорофилла позволяет называть его «электронным насосом», приводимым в действие и регулируемым солнечной энергией. Это важнейшее свойство замечательного пигмента открыто в 1948 г. академиком А. А. Красновским. Его открытие вошло в науку под названием реакции обратимого фотохимического восстановления хлорофилла (реакции Красновского). 3.3. Основные компоненты электротранспортной цепи3.3.1. Фотосистема IСветособирающий комплекс I содержит примерно 200 молекул хлорофилла.В реакционном центре первой фотосистемы находится димер хлорофилла a с максимумом поглощения при 700 нм (П700). После возбуждения квантом света он восстанавливает первичный акцептор — хлорофилл a, тот — вторичный (витамин K1 или филлохинон), после чего электрон передаётся на ферредоксин, который и восстанавливает НАДФ с помощью фермента ферредоксин-НАДФ-редуктазы. Белок пластоцианин, восстановленный в b6f комплексе, транспортируется к реакционному центру первой фотосистемы со стороны внутритилакоидного пространства и передаёт электрон на окисленный П700. 3.3.2. Фотосистема IIФотосистема — совокупность ССК, фотохимического реакционного центра и переносчиков электрона. Светособирающий комплекс II содержит 200 молекул хлорофилла a, 100 молекул хлорофилла b, 50 молекул каротиноидов и 2 молекулы феофитина. Реакционный центр фотосистемы II представляет собой пигмент-белковый комплекс, расположенный в тилакоидных мембранах и окружённый ССК. В нём находится димер хлорофилла a с максимумом поглощения при 680 нм (П680). На него в конечном счёте передаётся энергия кванта света из ССК, в результате чего один из электронов переходит на более высокое энергетическое состояние, связь его с ядром ослабляется и возбуждённая молекула П680 становится сильным восстановителем (E0=-0,7 В).(Рис.4) 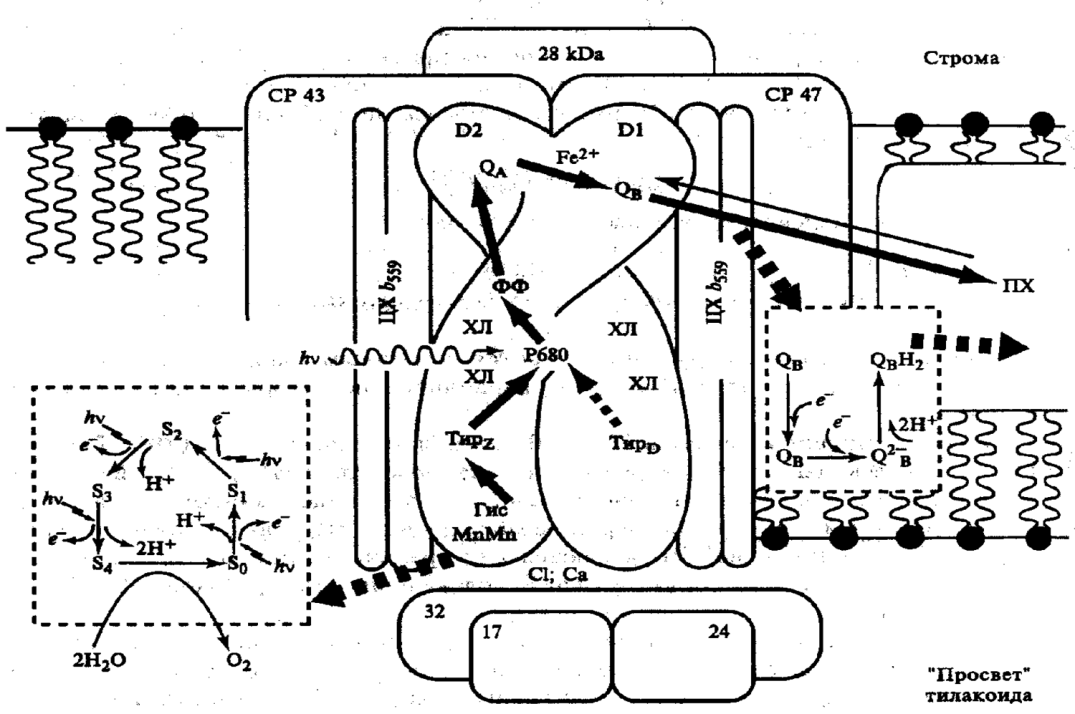 Рис.4.Схема структурной организации фотосистемы II в фотосинтетической мембране (по Рубину, 2000) П680 восстанавливает феофитин, в дальнейшем электрон переносится на хиноны, входящие в состав ФС II и далее на пластохиноны, транспортируемые в восстановленной форме к b6f комплексу. Одна молекула пластохинона переносит 2 электрона и 2 протона, которые берутся из стромы. Заполнение электронной вакансии в молекуле П680 происходит за счёт воды. В состав ФС II входит водоокисляющий комплекс, содержащий в активном центре ионы марганца в количестве 4 штук. Для образования одной молекулы кислорода требуется две молекулы воды, дающие 4 электрона. Поэтому процесс проводится в 4 такта и для его полного осуществления требуется 4 кванта света. Комплекс находится со стороны внутритилакоидного пространства и полученные 4 протона выбрасываются в него. Таким образом, суммарный результат работы ФС II — это окисление 2 молекул воды с помощью 4 квантов света с образованием 4 протонов во внутритилакоидном пространстве и 2 восстановленных пластохинонов в мембране. 3.3.3. b6f или b/f-комплексb6f комплекс является насосом, перекачивающим протоны из стромы во внутритилакоидное пространство и создающий градиент их концентрации за счёт выделяющейся в окислительно-восстановительных реакциях электронтранспортной цепи энергии. 2 пластохинона дают перекачку 4 протонов. В дальнейшем трансмембранный протонный градиент (pH стромы около 8, внутритилакоидного пространства — 5) используется для синтеза АТФ трансмембранным ферментом АТФ-синтазой. 3.4. Циклический и псевдоциклический транспорт электронаПомимо полного нециклического пути электрона, описанного выше, обнаружены циклический и псевдоциклический. Суть циклического пути заключается в том, что ферредоксин вместо НАДФ восстанавливает пластохинон, который переносит его назад на b6f комплекс. В результате образуется больший протонный градиент и больше АТФ, но не возникает НАДФН. При псевдоциклическом пути ферредоксин восстанавливает кислород, который в дальнейшем превращается в воду и может быть использован в фотосистеме II. При этом также не образуется НАДФН. 3.5 Основные свойства фотосинтетического аппарата растений3.5.1 Насыщение световой кривой фотосинтеза с ростом освещенностиНа графике видно, что кривые роста скорости фотосинтеза имеют выраженное насыщение. Предельное значение насыщения растет с ростом концентрации CO2 в воздухе. Причиной этого явления являются ограничения скорости потока электронов в электрон-транспортной цепи, когда скорость их отвода на CO2 лимитируется его диффузией из окружающей среды.(Рис.5) 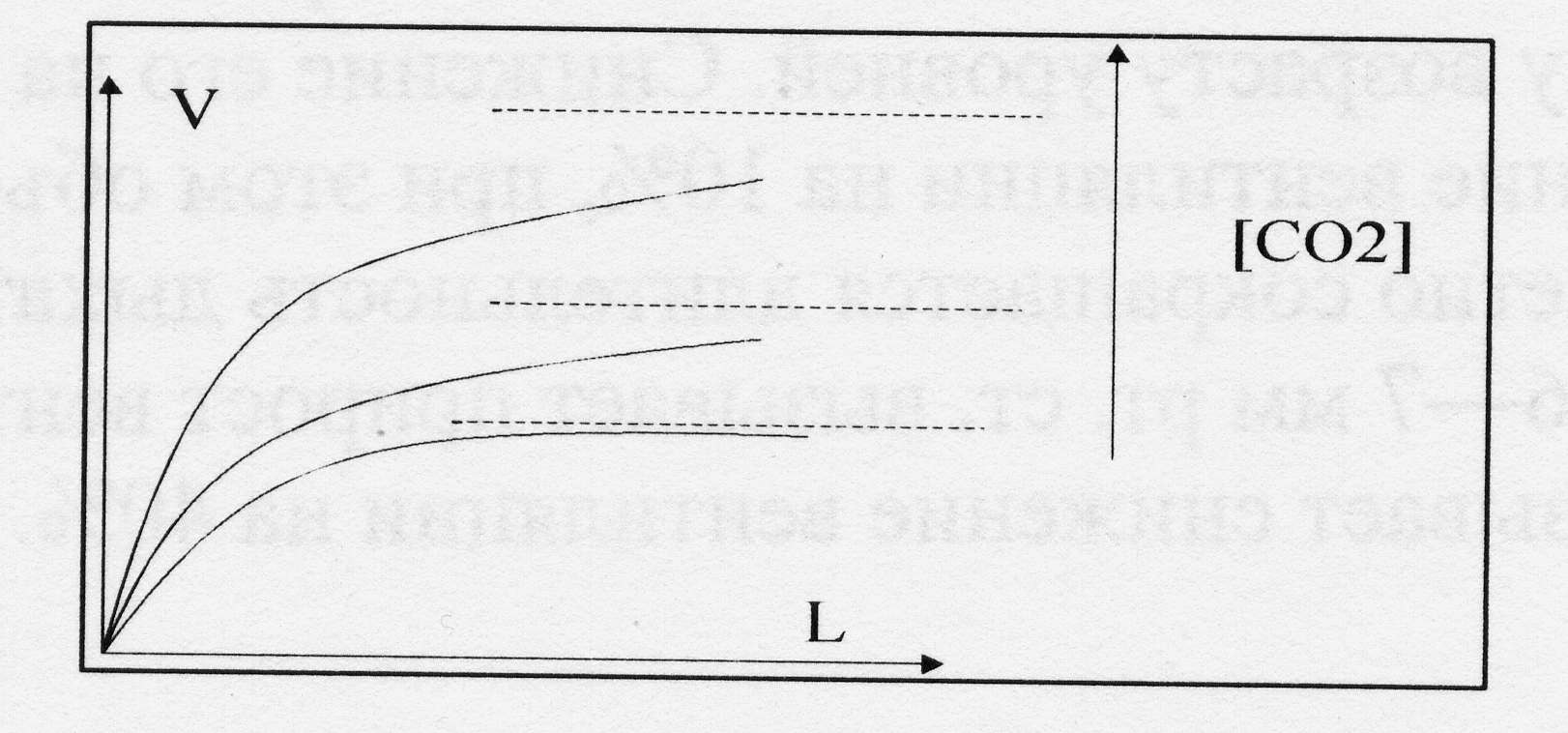 Рис.5. По вертикальной оси – скорость ассимиляции углекислоты V, по горизонтальной оси – освещенность листа L. 3.5.2 «Эффект усиления» Эммерсона.Если измерять интенсивность фотосинтеза от двух монохроматических источников света с длинами волн λ1 < 690 нм и λ2 > 690 нм, то она окажется в несколько раз больше, чем интенсивность фотосинтеза при свете той же мощности, но содержащем лишь одну длину волны λ1 или λ2. Это объясняется тем, что для нормального протекания фотосинтеза необходимо сбалансированное возбуждение фотосистем ФС1 и ФС2. В противном случае поток электронов ослабевает. «Память» «эффекта усиления» составляет 1 секунду. Если освещать лист растения поочередно светом с λ1 и λ2 с интервалом меньше 1 секунды, то скорость фотосинтеза будет неотличима от скорости при одновременном облучении светом с λ1 и λ2 . Это время характеризует время удержания пластохиноном избытка или дефицита электронов между ФС1 и ФС2. Изменение окислительно-восстановительного состояния цитохромов b и f при освещении светом с разными длинами волн. При освещении фотосинтетического аппарата светом с λ1 < 690 нм цитохромы восстанавливаются, а при освещении светом с λ2 > 690 нм цитохромы окисляются. Это происходит потому, что свет с длиной волны λ1возбуждает преимущественно ФС2, направляющую электроны к цитохромам, а свет с длиной волны λ2возбуждает в основном ФС1, отсасывающую электроны от цитохромов. 3.5.3 Эффект Кока-Жолио. Если зеленый лист растения выдержать в темноте около часа, а затем начать освещать короткими вспышками света, то выход кислорода будет иметь следующий вид.(Рис.6) Если зеленый лист растения выдержать в темноте около часа, а затем начать освещать короткими вспышками света, то выход кислорода будет иметь следующий вид.(Рис.6)Рис.6. Количество кислорода, выделяемого на одну вспышку. N – номер вспышки. На две первые вспышки кислород практически не выделяется, на третью вспышку выделение максимально, на четвертую несколько меньше, далее серия повторяется с периодом 4, и через 20-30 вспышек модуляция сглаживается, и выделения становятся одинаковыми. Эффект объясняется дискретностью работы кислород-выделяющего комплекса. Если вспышка достаточно короткая, так что кислород-выделяющий комплекс успевает получить от Р680 за вспышку только одну дырку, то последовательное одноэлектронное окисление реакционного центра ФС2 изменяет каждый раз суммарную валентность ионов Mn на единицу. А так как не все реакционные центры получают возбуждения во время каждой вспышки, то со временем состояния кислород-выделяющих комплексов раз синхронизируются и суммарный эффект сглаживается. 3.5.4 Задержанная флуоресценция.Вслед за затуханием флуоресценции молекулы хлорофилла (несколько наносекунд) в живом листе наблюдается слабое остаточное свечение с характерным временем затухания от нескольких секунд до минуты. Индукция флуоресценции. При включении освещения наблюдается флуоресценция с определенным значением квантового выхода. Через некоторое время начинается рост уровня флуоресценции до нового значения квантового выхода. ЗАКЛЮЧЕНИЕФотосинтез– это весь комплекс процессов ассимиляции фотонов и химических субстратов в растительном организме, которые приводят к его росту и развитию. Кроме этого, в фотосинтез входят: процессы синтеза пигментов, обеспечивающих поглощение фотонов и первичные фотохимические реакции; синтез соединений, отвечающих за формирование органов растительного организма и его приспособление к условиям окружающей среды. В более узком смысле фотосинтез – это синтез углеводов под действием видимого света. Термин фотосинтез был предложен Чарльзом Рейдом Бансом из Чикагского университета в начале прошлого столетия. В Европе этот процесс часто называют ассимиляцией или ассимиляцией углерода. Многие живые организмы способны к фотосинтезу. Даже в кожном слое млекопитающих идет под действием света синтез химических соединений. Но основными объектами исследования фотосинтеза и практического использования его продуктов являются растения, водоросли и микроорганизмы. У высших растений основная масса синтезируемых соединений производится в листьях. В других частях также идут фотосинтетические процессы, управляющие развитием цветков, семян, изменением формы растений и их пространственной ориентацией. ЛитератураВикторов Д.П. Практикум по физиологии растений /Викторов Д.П. под общ. Ред. А.А. Землянухина. – Воронеж: Изд-во Воронеж. ун-та, 1991. - 157 с. Журбицкий З.И. Теория и практика вегетационного метода / З.И. Журбицкий – М.: Наука, 1968. – 260 с. Лебедев, С. И. Физиология растений: учеб. для студентов вузов / С. И. Лебедев. – Изд. 3-е, перераб. и доп.– М.: Агропромиздат, 1988. – 544 с. Летние практические занятия по физиологии растений. Полевая практика. /Ф.Д.Сказкин [и др.]; под ред. М.С. Миллер. – Изд. 3-е, перераб. – М.: Просвещение, 1973. – 208 с. Методы биохимических исследований/под ред. А. И. Ермакова - 2-е изд., перераб. и доп. – Колос, 1972. – 456 с. Плешков, Б. П. Биохимия сельскохозяйственных растений: учеб. для студ. вузов / Б. П. Плешков. – Изд. 5-е, перераб. и доп. – М.: Агропромиздат, 1987. – 486 с. Самойлов В.О. Медицинская биофизика. Санк-Петербург, Спецлит, 2004.- 167 с. Тарасенко, С. А. Физиология и биохимия растений. Практикум : учеб. пособие / С. А. Тарасенко, Е. И. Дорошкевич; Гродненский гос. аграр. ун-т. – Гродно: УО «ГГАУ», 2004. – 210 с. Практикум по физиологии растений: учеб. пособие / Н. Н. Третьяков [и др.]; под ред. Н. Н. Третьякова. – М.: Колос, 2003. – 288 с. Физиология и биохимия сельскохозяйственных растений: учеб. пособие / Н. Н. Третьяков [и др.]; под ред. Н. Н. Третьякова. – Изд. 2-е. – М.: Колос, 2005. – 656 с. Alberts B. et al. Molecular Cell Biology. 4-th edition. Garland Science. New York, 2002. Nelson D.L., Cox M.M. Lehninger Principles of Biochemistry, Fourth Edition, W.H. Freeman & Company; 2005 | ||||||||||||||||||||||||||||||||||||||||||||||||
