Питание и размножение бактерий. 4. Питание и размножение бактерий. Физиология бактерий
 Скачать 197.5 Kb. Скачать 197.5 Kb.
|
|
Конструктивный метаболизм. Обязательной фазой питания бактерий является усвоение питательных веществ, то есть включение их в изменённом или модифицированном виде в синтетические реакции по воспроизведению клеточных компонентов и структур. Белковый обмен у бактерий может протекать в 3 фазы: первичный распад белка, вторичный распад и синтез белка. Первичный распад белковых молекул до пептонов осуществляют экзоферменты – экзопротеазы, выделяемые бактериями в окружающую среду. Вторичный распад происходит под действием эндоферментов (эндопротеаз), которые имеют все бактерии. Этот процесс протекает внутри бактериальной клетки и заключается в расщеплении пептидов до составляющих их аминокислот. Последние могут быть использованы в неизменённом виде или быть подвергнуты химическим преобразованиям (дезаминирование, декарбоксилирование и др.), в результате которых появляются аммиак, индол, сероводород, кетокислоты, спирт, углекислый газ и др. Обнаружение указанных соединений имеет в бактериологии диагностическое значение. Наряду с реакциями расщепления белков, происходят реакции их синтеза. Одни бактерии образуют белки из готовых аминокислот, полученных в результате внешнего питания, другие бактерии самостоятельно синтезируют аминокислоты из простых соединений, содержащих азот и углерод. Синтез аминокислот может осуществляться в реакциях аминирования, переаминирования, амидирования, карбоксилирования. Большинство прокариот способны синтезировать все аминокислоты, входящие в состав клеточных белков. Особенностью биосинтеза аминокислот является использование общих биосинтетических путей: цикл трикарбоновых кислот, гликолиз, окислительный пентозо-фосфатный путь и др. Основным исходным соединением для синтеза аминокислот является пируват и фумарат. Углеводный обмен у автотрофов и гетеротрофов имеет отличия (схема 1). Бактерии-автотрофы все необходимые углеводы синтезируют из углекислого газа. Сырьём для образования углеводов у бактерий-гетеротрофов могут служить: (1) одно-, двух- и трёхуглеродные соединения; и (2) полисахариды (крахмал, гликоген, целлюлоза). Для расщепления последних многие бактерии-гетеротрофы имеют экзоферменты (амилаза, пектиназа и др.), которые проводят гидролиз полисахаридов до образования глюкозы, мальтозы, фруктозы и пр. У 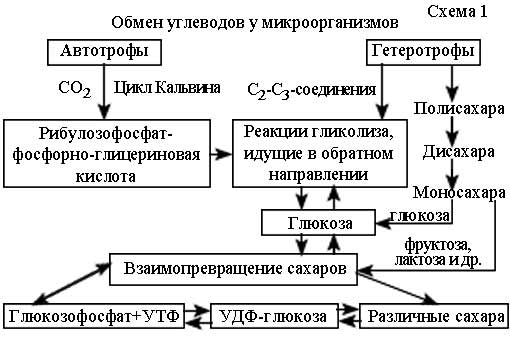 бактерий-автотрофов в цикле Кальвина из углекислого газа образуется рибулозофосфат-фосфорно-глицериновая кислота, которая включается в реакции гликолиза, идущие в обратном направлении. Конечным продуктом обратного синтеза является глюкоза. Бактерии-гетеротрофы образуют глюкозу из одно-, двух- и трёхуглеродных соединений, также включая их в реакции обратного гликолиза. Ввиду того, что некоторые реакции гликолиза необратимы, у гетеротрофов сформировались специальные ферментативные реакции, позволяющие обходить необратимые реакции катаболического пути. При расщеплении бактериями-гетеротрофами полисахаридов образующиеся дисахариды поступают внутрь клеток и под влиянием мальтозы, сахарозы, лактозы подвергаются гидролизу и распаду на моносахара, которые затем сбраживаются либо включаются в реакции взаимопревращения сахаров. Липидный обмен. Исходными материалами для образования липидов у бактерий могут служить как экзогенные липиды, так и амфиболиты межуточного обмена. Экзогенные липиды подвергаются действию бактериальных липаз и других липолитических ферментов. Многие виды бактерий усваивают глицерин, который служит источником пластического материала и энергии. Эндогенными источниками для синтеза липидов могут быть ацетилкоэнзим А, пропионил-АПБ, малонил-АПБ (АПБ – ацетилпереносящий белок), фосфодиоксиацетон и др. Исходным субстратом для синтеза жирных кислот с чётным числом углеродных атомов служит ацетилкоэнзим А, для жирных кислот с нечётным числом углеродных атомов – пропионил-АПБ и малонил-АПБ. Образование двойных связей в молекуле кислоты у аэробных прокариот происходит при участии молекулярного кислорода и фермента десатуразы. У анаэробных прокариот двойные связи вводятся на ранних этапах синтеза в результате реакции дегидратации. Исходным субстратом для синтеза фосфолипидов служит фосфодиоксиацетон (промежуточное соединение гликолитического пути), восстановление которого приводит к образованию 3-фосфороглицерина. К последнему затем присоединяются 2 остатка жирных кислот в виде комплекса с АПБ. Продуктом реакции является фосфатидная кислота, активирование которой с помощью ЦТФ и последующее присоединение к фосфатной группе серина, инозита, глицерина или другого соединения приводят к синтезу соответствующих фосфолипидов. Ауксотрофные и гипотрофные по жирным кислотам микроорганизмы (например, микоплазмы) получают их в готовом виде из клеток хозяина или питательной среды. Мононуклеотидный обмен. Пуриновые и пиримидиновые мононуклеотиды являются важнейшими компонентами ДНК и РНК. Многие прокариоты способны как использовать содержащиеся в питательной среде готовые пуриновые и пиримидиновые основания, их нуклеозиды и нуклеотиды, так и синтезировать их из низкомолекулярных веществ. Бактерии располагают ферментами, катализирующими следующие этапы взаимопревращений экзогенных пуриновых и пиримидиновых производных: азотистое основание – нуклеозид – нуклеотид (моно- – ди- – трифосфат). Синтез пуриновых и пиримидиновых мононуклеотидов denovoосуществляется независимыми путями. При синтезе пуриновых нуклеотидов в результате последовательных ферментативных реакций образуется инозиновая кислота, из которой путём химических модификаций пуринового кольца синтезируются адениловая (АМФ) и гуаниловая (ГМФ) кислоты. Синтез пиримидиновых нуклеотидов начинается с образования оротидиловой кислоты, декарбоксилирование которой даёт уридиловую кислоту (УМФ). Из последней образуется УТФ, ацилирование которого приводит к возникновению ЦТФ. Дезоксирибонуклеотиды образуются в результате восстановления соответствующих рибонуклеотидов на уровне дифосфатов или трифосфатов. Синтез специфического для ДНК нуклеотида – тимидиловой кислоты происходит путём ферментативного метилирования дезоксиуридиловой кислоты. Ионный обмен. Минеральные соединения – ионы, NH3+, К+, Mg2+, Fe2+, SO42-, PO43- и другие бактерии получают из окружающей среды как в свободном, так и в связанном с другими органическими веществами состоянии. Катионы и анионы транспортируются в бактериальную клетку различными способами, описанными в § 3. На скорость проникновения ионов в бактериальную клетку влияют рН среды и физиологическая активность самих микроорганизмов. 4. Дыхание бактерий (энергетический метаболизм). Все процессы жизнедеятельности энергозависимы, поэтому добывание энергии является крайне важной стороной метаболизма прокариот. Они получают энергию при анаэробном и аэробном дыхании. Дыхание, или биологическое окисление – это катаболический процесс переноса электронов от вещества-донора на вещество-акцептор, сопровождающийся накоплением энергии в макроэргических соединениях. Дыхание осуществляется в процессе катаболических реакций, в результате которых сложные органические вещества, расщепляясь, отдают энергию и превращаются в простые соединения. Аккумулированная в макроэргических веществах (АТФ, ГТФ, УТФ и др.) энергия используется в анаболических реакциях. По способу дыхания микроорганизмы подразделяются на облигатные (строгие) аэробы, облигатные анаэробы и факультативные анаэробы. Облигатные аэробы нуждаются в свободном кислороде. Донорами электронов у патогенных для человека аэробов-хемоорганотрофов являются органические соединения (углеводы, жиры, белки), акцептором электронов – молекулярный кислород. Запасание энергии в виде АТФ у аэробов-хемоорганотрофов происходит при окислительном фосфорилировании доноров электронов. Аэробы обладают цитохромами (участвуют в переносе электронов), а также ферментами (каталаза, супероксиддисмутаза, пероксидаза), инактивирующими токсические кислородные радикалы, образующиеся при дыхании. Супероксиддисмутаза инактивирует наиболее токсичный метаболит – супероксидрадикал в Н2О2. Фермент каталаза превращает Н2О2 в Н2О и О2. Особую группу аэробов составляют микроаэрофильные бактерии, которые хотя и нуждаются в кислороде для получения энергии, лучше растут при повышенном содержании СО2, например, бактерии родов Campylobacter и Helicobacter. Облигатные анаэробы не нуждаются в свободном кислороде, напротив, даже в малых количествах кислород оказывает на них токсическое действие. Донорами электронов у патогенных для человека анаэробов-хемоорганотрофов служат различные органические соединения (преимущественно углеводы). Акцептором электронов у анаэробов-хемоорганотрофов являются органические кислородсодержащие соединения – кислоты или кетоны, то есть акцептор электрона - связанный с органическим фрагментом кислород. Запасание энергии у этих прокариот происходит при субстратном фосфорилировании. Облигатные анаэробы, как правило, не имеют цитохромов и ферментов, инактивирующих кислородные радикалы (каталазо- и супероксидисмутазоотрицательны). У непатогенных для человека анаэробов хемолитотрофов акцептором электронов являются неорганические кислородсодержащие соединения – нитраты, сульфаты, карбонаты. Особую группу анаэробов составляют аэротолерантные бактерии, которые способны расти в присутствии атмосферного кислорода, но не используют его в качестве акцептора электронов (например, молочнокислые бактерии). Аэротолерантные прокариоты каталазо- и супероксиддисмутазопозитивны. Факультативные анаэробы способны существовать как в кислородной, так и в бескислородной средах. Донорами электронов у них являются органические вещества; акцепторами электронов, в зависимости от условий среды – молекулярный или связанный в органических и неорганических соединениях кислород. Энергия факультативными анаэробами может аккумулироваться как при окислительном, так и при субстратном фосфорилировании. Как и аэробы, данная группа бактерий имеет цитохромы и ферменты антиоксидантной защиты. Основным субстратом для получения энергии являются углеводы, которые у разных по типу дыхания хемогетеротрофных прокариот могут катаболизироваться до ацетилкоэнзима А («активированная уксусная кислота»). В качестве энергетических субстратов могут выступать липиды и белки, поскольку ацетилкоэнзим А также является одним из промежуточных продуктов их метаболизма (схема 2). Катаболизм углеводов у хемоорганотрофных прокариот включает: (а) анаэробные процессы – гликолиз, пентозофосфатный путь и кетодезоксифосфоглюконатный путь; (б) аэробный процесс – цикл трикарбоновых кислот (цикл Кребса). Анаэробные процессы имеют место у всех прокариот, тогда как аэробный процесс характерен только для облигатных аэробов и факультативных анаэробов. В основе получения энергии анаэробными путями лежит субстратное фосфорилирование, в основе аэробного процесса – окислительное фосфорилирование. Получение энергии путём субстратного фосфорилирования. Брожение. Субстратным фосфорилированием называется процесс бескислородного присоединения к молекуле субстрата остатков фосфорной кислоты с последующим их переносом на АДФ, в результате чего образуется АТФ. Субстратное фосфорилирование составляет сущность гликолиза, кетодезоксифосфоглюконатного и пентозофосфатного путей. Все реакции субстратного фосфорилирования локализованы в цитоплазме бактериальной клетки. Гликолиз (путь Эмдена-Мейерхофа-Парнаса). Это наиболее примитивный способ извлечения энергии, поскольку из субстрата в результате его анаэробного преобразования извлекается лишь незначительная доля той химической энергии, которая в нём содержится. При гликолизе донором электронов является углевод, акцептором электронов – какая-нибудь органическая молекула, образующаяся в процессе последующего брожения. Синтез АТФ при гликолизе осуществляется на уровне субстрата. В результате расщепления 1 молекулы глюкозы при гликолизе расходуется 2 и синтезируются 4 молекулы АТФ (схема 3). Общий полезный выход составляет 2 молекулы АТФ и 2 молекулы НАД*Н2. Ключевым продуктом гликолиза выступает пировиноградная кислота (пируват), которая в зависимости от метаболических особенностей конкретных микроорганизмов может подвергаться дальнейшим ферментативным преобразованиям – брожению. Конечный продукт брожения является восстановленным соединением, акцептировавшим электроны, выделяется из клеток прокариот в окружающую среду и накапливается в ней в значительных количествах. Преобладающий продукт брожения определяет его вид. Молочнокислое брожение. Гомоферментативное молочнокислое брожение вызывают бактерии родов Streptococcus, Lactobacterium, Bifidobacterium. При этом виде брожения акцептором электронов служит пируват. Конечный продукт – молочная кислота. Бактерии родов Escherichia, Proteus, Salmonella, Shigella способны вызывать гетероферментативное молочнокислое брожение. При нём, кроме молочной кислоты, в меньших количествах образуются уксусная, муравьиная, янтарная кислоты, этанол. Пропионовокислое брожение вызывают бактерии родов Clostridium, Propionobacterium, Corynebacterium, некоторые виды из родов Neisseria, Veillonella. Конечными продуктами брожения являются пропионовая, уксусная, янтарная кислоты. Маслянокислое брожение характерно для бактерий родов Butyribacterium, Sarcina, Clostridium, Neisseria. При данном виде брожения образуются масляная кислота, бутанол, ацетон, изопропанол, уксусная кислота, этанол. Бутилен-гликолевое брожение свойственно некоторым видам бактерий родов Aeromonas, Bacillus, Enterobacter. Конечные продукты брожения: ацетон, бутилен-гликоль, молочная кислота, муравьиная кислота. Определение в среде ацетона (ацетилметилкарбинола) в реакции Фогеса-Проскауэра используется при идентификации Enterobacter sp. Спиртовое брожение способны вызывать бактерии родов Sarcina, Erwinia. У многих клостридий и энтеробактерий также среди продуктов брожения обнаруживается этиловый спирт. К альтернативным путям катаболизма углеводов относятся пентозофосфатный и кетодезоксифосфоглюконатный пути. Пентозофосфатный путь возник для обеспечения прокариот пентозами. Суммарно весь процесс можно представить в виде следующего уравнения: глюкозо-6-фосфат + 2 НАДФ+ = рибозо-5-фосфат + СО2 + 2 НАДФ*Н2. Образовавшийся рибозо-5-фосфат используется прокариотами в синтезе нуклеиновых кислот и пентозосодержащих коферментов; молекулы НАДФ*Н2 потребляются в восстановительных биосинтетических процессах. Ни на одном из этапов пентозофосфатного пути АТФ не синтезируется. Пентозофосфатный путь присущ большинству микроорганизмов. Он в 2 точках может смыкаться с гликолизом и, следовательно, оба этих пути взаимно дополняют друг друга при необходимости образования таких ключевых веществ, как глюкозо-6-фосфат и 3-фосфорноглицериновый альдегид, которые могут переключить пентозофосфатный путь на гликолитический. Пентозофосфатный путь позволяет прокариотам сбраживать пентозы. |
