|
|
Абдуллаев СРОП 11 бф. Фотохимическое преобразования днк
МЕББМ ҚАЗАҚСТАН-РЕСЕЙ
|

|
НУО КАЗАХСТАНСКО-РОССИЙСКИЙ
|
МЕДИЦИНАЛЫҚ УНИВЕРСИТЕТІ
|
МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
|
СРОП
Тема: «Фотохимическое преобразования ДНК»
Выполнил: Абдуллаев Абдуллам
Факультет: Общая медицина
Группа: 120-А
Проверил: Дарын Кермакынович
Алматы – 2021
СОДЕРЖАНИЕ
Введение……………………………………………………..3 стр
Первичные фотохимические реакции……………………...4 стр
Фотохимические превращения ДНК……………………….5 стр
Образование (6-4) пиримидиновых аддуктов……………...7 стр
Сшивка с белком……………………………………………..8 стр
Особенности действия высокоинтенсивного лазерного УФ -
Излучения…………………………………………………….9 стр
Люминесцентные метки и зонды и их применение в медицине..11 стр
Заключение…………………………………………………………12 стр
Литература………………………………………………………….13 стр
Приложения…………………………………………………………14 стр

ВВЕДЕНИЕ
Фотохимические реакции -это химические реакции, происходящие под воздействием света; имеют важнейшее общебиологическое значение.
По характеру биологического эффекта фотохимические реакции подразделяют на физиологические иповреждающие. К физиологическим относятся те реакции, которые лежат в основе фотосинтеза, биосинтеза физиологически важных веществ -витаминов, пигментов и др., а также реакции обеспечивающие физиологические функции связанные с получением информации из окружающей среды, - зрение, тропизмы, таксисы. Повреждающие фотохимической реакции имеют в своей основе действие света, особенно УФ-излучения, нануклеиновые кислоты и белки. В результате может наблюдаться гибель клеток, интенсивный мутагенез, инактивация ферментов и др.
ПЕРВИЧНЫЕ ФОТОХИМИЧЕСКИЕ РЕАКЦИИ
В настоящее время доказано, что основной первичной фото-реакции триптофана (АН) в белке является его фотоионозация с образованием катион-радикала и сольватированого электрона:
[1] Приложение
При комнатной температуре эта реакция протекает за 5-20 мкс и исследована с использованием метода флеш-фотолиза. Показано, что через 5 мкс после Уф облучения в растворе триптофана появляются характерные спектры поглощения в красной и дальней красной области спектра, которые принадлежат выбитому сольватированному электрону, т.е. электрону, «выбитому» из молекулы аминокислоты и захваченному дипольными молекулами растворителями. Сольватированный электрон быстро реагирует с другими молекулами, в частности, с молекулами растворителя и, вследствие чего полоса его поглощения исчезает. Однако, если облучать замороженные образцы триптофана при температуре жидкого азота ( в этих условиях сольватированные электроны не рекомбинируют), то поглощение сольватированого электрона (максимум при 600 нм) можно зарегистрировать и на обычном спектрофотометре. Кроме того, наличие некомпенсированного магнитного момента (спин) у сольватированного электрона позволяет обнаружить его методом ЭПР.
ФОТОХИМИЧЕСКИЕ ПРЕВРАЩЕНИЕ ДНК
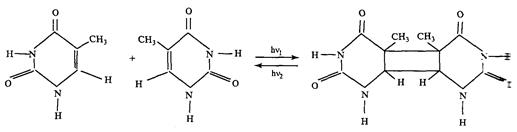
Согласно общепринятому мнению, ДНК основная внутриклеточная мишень при летальном и мутагенном действии коротковолнового УФ излучения. Это в частности, подтверждается совпадением максимума в спектрах действия фотобиологических эффектов (260-265 нм) с максимумом в спектре поглощения ДНК. Основными хромофорами ДНК являются азотистые основания нуклеотидов, причем квантовые выходы фотопревращений пирими-диновых компонентов примерно на порядок выше, чем пуриновых. Поглощение азотистыми основаниями квантов Уф света ( максимум поглощения при 260 нм) приводит к образованию их электронно-возбужденных синглетных и триплетных состояний, которые возникают за счет p–p*-переходов. Электронно-возбужденные состояния пиримидиновых оснований могут вступать в ряд фотохимических реакций, из которых, биологически наиболее важны три реакции присоединения: димеризация, гидратация и образования сшивок с белком. Эта реакция впервые была обнаружена при Уф облучении замороженных растворов тимина. Она состоит в соединении двух оснований по 5,6-двойной углеродной связи с образованием кольца циклобутанового типа:
[2] Приложение
Характерная черта реакции димеризации ее обратимость. Пиримидиновые основания поглощают свет в области 200-300 нм, их димеры примерно в том же диапазоне УФ-спектра (200-285 нм).Поэтому при Уф облучении оснований или ДНК для каждой длины волны возбуждающего света между димерами и основаниями устанавливается динамическое равновесие, определяемое соотношением поперечных сечений димеризации оснований и мономеризации димеров. Так, в случае облучения тимина при 200 нм димеризуется около 65% оснований, а при 280-15%.
Вследствие бимолекулярного характера реакций фотодимеризации ее квантовый выход существенно зависит от степени взаимоориентации мономеров при возбуждении одного из них. Например, квантовый выход димеризации тимина в водном растворе при комнатной температуре - 4,7×10-4, а в замороженном - 1. Квантовый выход димеризации тимина в ДНК - 2×10-2. В соответствии с проведенными расчетами условия для димеризации тимина в ДНК являются оптимальными, если соседние мономеры ориентированы друг к другу под углом в 36 .
Некоторые красители акридинового ряда могут эффективно уменьшать выход УФ- индуцированных димеров в ДНК. Защитное свойство акридинов основано на их способности интеркалировать между парами оснований в молекуле ДНК. Характерная черта взаимодействия акридинов (например акридиновый оранжевый) с ДНК заключается в том, что при образовании комплекса резко увеличивается интенсивность флуоресценции красителя в максимуме спектра при 530 нм. По мнению некоторых авторов, это может быть обусловлено синглет-синглетной миграцией энергии возбуждения с оснований на краситель. Расчеты показывают, что максимальный квантовый выход такой миграции энергии достигается при соотношении 1 молекула красителя / 5 оснований и составляет 32%.
Помимо увеличения интенсивности флуоресценции тестом на связывание акридинов с ДНК может служить так же изменение степени поляризации люминесценции, зависящей от подвижности молекул красителей. С помощью этого метода показано, в частности, что плоскость кольца акридинового оранжевого перпендикулярна длинной оси спирали ДНК и параллельна плоскостям основани
ОБРАЗОВАНИЕ (6-4) ПИРИМИДИНОВЫХ АДДУКТОВ
Эти фотопродукты, характеризующиеся абсорбцией при 315-320 нм и флуоресценцией в области 405-440 нм, были выделены из кислотного гидролизата УФ-облученной ДНК. Структура аддуктов была установлена с помощью УФ-, ИК-, ЯМР-спектроскопии и масс-спектрометрии, Квантовый выход (6-4)-аддуктов порядка 103, т. е. в
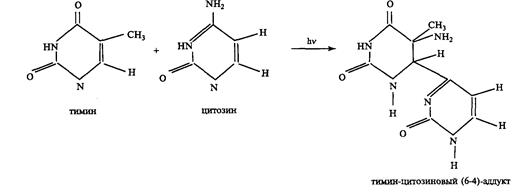
10 раз меньше, чем цикло-бутановых димеров, и следовательно, в летальный эффект УФ-излучения (254 нм) они вносят незначительный вклад. Однако в УФ-мутагенезе они могут играть важную роль. В отличие от летальных повреждений ДНК, мутационные дефекты возникают намного реже, и поэтому для них требование максимального квантового выхода не имеет принципиального значения. Полагают, что реакция образования (6-4) пиримидиновых аддуктов идет по схеме:
[3] Приложение
СШИВКА С БЕЛКОМ
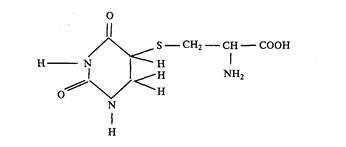
Это пример межмолекулярных взаимодействий, относящихся к третьему типу фотохимических реакций, в которые вступают Пиримидиновые основания ДНК. Акцепторами Уф света являются оба компонента, поскольку облучение как белка, так и ДНК перед сшиванием сопровождается образованием сшивок. Механизм данного процесса, вероятно, заключается в прикреплении аминокислотных остатков белка через SН- или ОН- группы к С5 или С6 цитозина или тимина ДНК. В модельной системе наблюдали образование по такому механизму 5-S-цистеин-6-гидроурацила.
[4] Приложение
Рассмотренные выше фотохимические реакции ДНК протекают с участием низших возбужденных (синглетных и триплетных) состояний пиримидиновых оснований, которые возникают в результате поглощения одного кванта Уф света.
ОСОБЕННОСТИ ДЕЙСТВИЯ ВЫСОКОИНТЕНСИВНОГО ЛАЗЕРНОГО УФ- ИЗЛУЧЕНИЯ
До создания лазерных источников УФ-излучения классическая УФ - фотобиология рассматривала в основном процессы, линейно зависящие от интенсивности УФ-света или исследовались биологические эффекты одноквантовых фотохимических реакций. Лазерное излучение обладает такими замечательными свойствами, как пространственная когерентность, монохроматичность, высокая интенсивность и концентрация энергии в коротком импульсе наносекундной или пикосекундной длительности. Большая мощность и ультракороткое время действия делают лазерное УФ-излучение потенциально новым инструментом для исследования процессов двухквантового возбуждения электронных уровней оснований ДНК и особенностей протекающих при этом фотохимических реакций, а также их проявления на биологическом уровне.
Экспериментальные исследования, в которых водные растворы азотистых оснований облучали пикосекундными или наносекундными импульсами УФ-излученш (266 нм), показали, что при интенсивностях выше 1010 Вт/м2 происходят необратимые фотохимические изменения молекул, причем образующиеся продукты качественно отличаются от фотопродуктов одноквантовых реакций, таких, как пиримидиновые димеры и гидраты. Причем степень деградации оснований квадратично зависит от интенсивности излучения, что свидетельствует о двухквантовом механизме лазер-индуцированных фотохимических превращений.
Лазер-индуцированное двухквантовое возбуждение оснований в составе ДНК приводит к таким ее фотохимическим превращениям, которые не наблюдаются (либо идут с очень низким квантовым выходом) в случае действии низкоинтенсивного УФ-света. Наряду с деградацией оснований в ДНК выявлены разрывы N-гликозидной связи с отрывом тимина от цепи ДНК (при низко интенсивном УФ-облучении такой процесс не происходит) и одноцепочечные разрывы. Показано, что квантовый выход однонитевых разрывов при переходе от низкоинтенсивного УФ-облучения (1 Вт/м2) к высокоинтенсивному пикосекундному УФ-облучению (4 • 1013 Вт/м2) возрастает от (1¸2) • 10-6 до 8 • 10-5.
Вклад двухквантовых фотоповреждений ДНК по сравнению с одноквантовымг (пиримидиновые димеры) в лазерную УФ-инактивацию плазмид, бактериофагов и микроорганизмов значительно выше. Об этом, в частности, свидетельствуют эксперименты по изучению фотореактивации УФ-облученных биологических объектов Они показали, что с ростом интенсивности лазерного УФ-излучения (266 нм) степень фотореактивации резко уменьшается (СЛАЙД 8).
Поскольку при фотореактивации ликвидируются летальные фотопродукты только одного типа — циклобутановые пиримидиновые димеры ДНК, то установленный факт свидетельствует ос уменьшении вклада димеров (и соответственно увеличении вклада двухквантовых фотоповреждений ДНК) в лазерную УФ-инактивацию.
ЛЮМИНЕСЦЕНТНЫЕ МЕТКИ И ЗОНДЫ И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ
В медицине используется применение специальных флуоресцирующих молекул, добавляемых к исследуемым биологическим системам извне, в которых они распределяются в соответствии со своими свойствами. Примером использования флуоресцентных зондов является метод флюоресцентной ангиографии - контрастирование сосудов флуоресцеином и их последующее фотографирование. Этот краситель вводится внутривенно пациентам. Этот краситель не токсичен, обладает очень высоким квантовым выходом флуоресценции. Он разносится с током крови по всему организму и диффундирует в дерму и эпидермис. Флуоресцеин возбуждается невидимым длинноволновым ультрафиолетовым излучением. Люминесценция его наблюдается в видимом свете. Диагностическая значимость этого метода заключается в том, что по скорости появления флуоресценции ( люминесценции) в поверхностных тканях судят об участках тела с пониженным кровообращением, в них флуоресцеин появляется позже, чем в участках тела с нормальным кровообращением.
Применение люминесценции для аналитических целей включает широкую область использования ее для идентификации веществ, для обнаружения малых концентраций веществ; для контроля изменений, претерпеваемых веществом; для определения степени чистоты веществ. Широко применяются измерения люминесценции при изучении кинетики обычных химических реакций. Высокая чувствительность метода позволяет фиксировать малую степень превращения, а иногда по люминесценции промежуточных соединений становится возможным установить механизм химической реакции. Люминесцентные методы используются в биологии, в частности, для исследования структуры белков методом флуоресцентных зондов и меток.
ЗАКЛЮЧЕНИЕ
Фотохимический закон Эйнштейна аналогичен закону Вавилова для выхода люминесценции. Оба закона отражают обстоятельство, что для действия света важна не сама величина светового потока, а число фотонов, содержащихся в этом световом потоке. Чем меньше энергия фотонов, еще способных вызвать реакцию, тем больший эффект вызовет данный световой поток, так как тем больше в нем будет фотонов.
При поглощении света в ряде веществ происходят химические реакции, изменяющие их внутреннюю структуру. Эти реакции называются фотохимическими.
Общеизвестно большое практическое значение фотохимических реакций в твердых телах. Эти реакции лежат в основе фотографии и кинематографии, ими обусловлено зрение человека. Однако в некоторых случаях с ними приходится бороться, например при создании прочных невыцветающихся красителей для тканей.
Всякий источник света представляет собой коллектив, состоящий из огромного числа элементарных излучателей. Существенным свойством люминесценции, неравновесного процесса, является ее конечная длительность.
Первые шаги практического применения люминесценции связаны с открытием радиоактивности и рентгеновых лучей. Роль люминесценции в открытии ядерного ядра. Применение светящихся составов постоянного действия, представляющих собой смесь радиоактивного вещества с сернистым цинком, на светящихся циферблатах часов явилось, по существу, первым практическим использованием ядерной энергии.
Использование люминесценции позволило создать новые источники света, лишенные недостатков ламп накаливания. Прежде всего следует указать на достигнутое при этом резкое повышение экономичности, а затем и на улучшение цветовых характеристик источников света.
ЛИТЕРАТУРА
Физика и биофизика: Учебник / В. Ф. Антонов, Е. К. Козлова, А. М. Черныш. - 3-е изд., испр. и доп. - М.: ГЭОТАР-Медиа, 2013. - 472 с. : ил.
Физика и биофизика. Краткий курс: Учебное пособие для вузов / В. Ф. Антонов, А. В. Коржуев. - М.: ГЭОТАР-Медиа, 2007. - 256 с.: ил.
Физика и биофизика: Курс лекций для медвузов / Антонов, Валерий Федорович, Коржуев А.В. - М.: ГЭОТАР-Медиа, 2007. - 236 с.
Особенности действия высокоинтенсивного лазерного УФ-излучения на ДНК (двухквантовые реакции) (helpiks.org)
Первичный фотохимический акт - Фотохимические превращения ДНК. Люминесцентные метки и зонды (vuzlit.ru)
ПРИЛОЖЕНИЕ
[1]

[2]
[3]
[4]
 |
|
|
 Скачать 151.43 Kb.
Скачать 151.43 Kb.





