Курсовая работа на тему «Расчет основных параметров горения и тушения пожара газового фонтана» Нефтяная и газовая промышленность. Теоретический расчет основных параметров горения и тушения пожар. Горение газов
 Скачать 4.82 Mb. Скачать 4.82 Mb.
|
5. расчет основных параметров горения и тушения газового фонтана1. Дебит газового фонтана ( 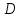 , млн. м3/сутки) может быть рассчитан из высоты факела пламени по формуле (4): , млн. м3/сутки) может быть рассчитан из высоты факела пламени по формуле (4):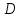 = 0,0025× = 0,0025× 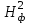 = 0,0025× 132 =0,4225 млн.м3/сутки (19) = 0,0025× 132 =0,4225 млн.м3/сутки (19)Секундный расход газа составит Vг =0,4225/ (246060) = 4,8 м3/с. . Режим истечения газовой струи может быть определен из сравнения эффективной скорости истечения (э) со скоростью звука (0): Э =4Vг /π 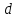 у 2 =(4× 4,8)/ (3,14× 0,252 )= 98 м/с. (20) у 2 =(4× 4,8)/ (3,14× 0,252 )= 98 м/с. (20)где Vг − секундный расход газа, м3/с, 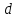 у − диаметр устья скважины, м. у − диаметр устья скважины, м.Скорость звука в метане (0) составляет 430 м/с. Рассчитанная скорость истечения газовой струи меньше скорости звука почти в 4,4 раза. . Для расчета адиабатической (Та) и действительной ( 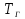 ) температуры процесса горения необходимо определить теплоту сгорания, т.е. количество тепла, выделяемое при полном сгорании 1 м3 фонтанирующего газа с учётом его химического состава. ) температуры процесса горения необходимо определить теплоту сгорания, т.е. количество тепла, выделяемое при полном сгорании 1 м3 фонтанирующего газа с учётом его химического состава.Теоретическая (адиабатическая) температура процесса горения рассчитывается с учётом полного адиабатического сгорания газообразного вещества(теплопотерями в окружающую среду пренебрегают). Остановимся на методике расчета Та, основываясь на анализе энергетического баланса химической реакции. Для его упрощения можно воспользоваться значением стандартной энтальпии сгорания при 298.15 K (- 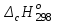 ),а вместо истинных теплоемкостей веществ - их средними значениями, взятыми в температурном интервале 289-2000 К. ),а вместо истинных теплоемкостей веществ - их средними значениями, взятыми в температурном интервале 289-2000 К.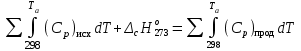 , (21) , (21)где 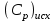 − теплоемкость исходных веществ; − теплоемкость исходных веществ;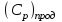 − теплоемкость продуктов горения (в том числе свободного кислорода); − теплоемкость продуктов горения (в том числе свободного кислорода);Та − адиабатическая температура процесса горения. Количество тепла, выделяющееся при полном сгорании одного моля, единицы массы или объёма вещества, называется теплотой сгорания (Qс, ΔсН). Стандартная энтальпия сгорания кислорода, жидкой воды, газообразного диоксида углерода (СО2) и других высших оксидов в стандартных состояниях равна нулю при любой температуре ( 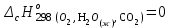 ), так они не способны окисляться. ), так они не способны окисляться.Значения теплот сгорания органических соединений можно найти в справочной литературе или рассчитать, используя первое следствие из закона Гесса, которое гласит: тепловой эффект реакции равен сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ с учетом стехиометрических коэффициентов. Высшей теплотой сгорания Qсв (∆сНв) называют количество теплоты, выделяемое при полном сгорании единицы массы или объёма горючего вещества при условии, что вода выделяется в конденсированном состоянии. Низшей теплотой сгорания Qсн (∆сНн) называют количество теплоты, выделяемое при полном сгорании единицы массы или объёма горючего вещества при условии, что вода выделяется в виде пара и происходит испарение влаги, содержащейся в горючем веществе. В пожарно-технических расчетах обычно используют низшую теплоту сгорания, так как в условиях пожарах вода как продукт реакции находится в парообразном состоянии. Используя справочную литературу для нахождения теплот (энтальпий) образования веществ и проводя теплотехнические расчеты, необходимо помнить, что тепловой эффект реакции ∆rН0т и теплота сгорания Qс. имеют одинаковые численные значения, но разный знак, т.е. Qс = − 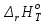 . .Рассчитаем теплоту сгорания (− 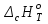 = Qн) метана, этана и сероуглерода, опираясь на первое следствие из закона Гесса. Запишем термохимические уравнения реакции их окисления: = Qн) метана, этана и сероуглерода, опираясь на первое следствие из закона Гесса. Запишем термохимические уравнения реакции их окисления:для метана СН4(г)+ 2О2(г) +2×3,76N2 = СО2(г) + 2Н2О(г) + 2×3,76N2 (22) 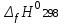 , кДж/моль −74,85 0 −393,51 −241,81 , кДж/моль −74,85 0 −393,51 −241,81Согласно первому следствию из закона Гесса, теплоты сгорания метана будет равна: Qсн=−{ 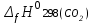 +2 +2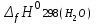 − −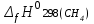 } = } == - {(−393,51)+2(−241,81)−(−74,85)} = 802,28 кДж/моль. Значение низшей теплоты сгорания 1 м3 метана рассчитаем по формуле: Qнс, об = - Qнс×1000/24,45 , (23) где 24,45 л - объем одного моля газа при Т=298 К. Отсюда низшая теплота сгорания 1 м3 метана будет равна: Qнс, об(СН4) = 802,28×1000 / 24, 45 = 32813,5 кДж/м3. · для этана: С2Н6(г) + 3,5О2(г) + 3,5×3,76N2 = 2СО2(г) + 3Н2О(г)+3,5×3,76N2 (24) 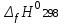 , кДж/моль −84,67 −393,51 −241,81 , кДж/моль −84,67 −393,51 −241,81Низшая теплота сгорания 1 моля этана составит: Qсн=−{2 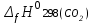 +3 +3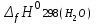 − −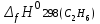 } = } == - {2(−393,51) + 3(−241,81) − (−84,67)} =1427,78 кДж/моль. Рассчитанная по аналогии с метаном теплота сгорания 1 м3 этана будет равна 58397,1 кДж/м3. · для сероводорода: H2S(г)+ 3О2 +3×3,76N2 = 2Н2О(г) + 2SО2(г) + 3×3,76N2 (25) 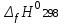 , кДж/моль - 20,60 - 241,81 - 296,90 , кДж/моль - 20,60 - 241,81 - 296,90Низшая теплота сгорания 1 моля сероводорода составит: Qсн=−{2ΔfН0298(Н2О) + 2ΔfН0298(SО2) − 2ΔfН0298(H2S)} = = - {(−241,81) + 2(−296,9)− 2(- 20,6)} = 1036,22 кДж/моль. Рассчитанная по аналогии теплота сгорания 1 м3 сероводорода будет равна 42381,2 кДж/м3. Поскольку в 1 м3 исходной газовой смеси содержится 84 об. % (0,84) метана, 6 об. % (0.06) этана и 7 об. % (0.07) сероводорода, то общая теплота сгорания 1 м3 смеси составит Qсн, об = 32813,5 × 0,84 + 58397,1 × 0,06 + 42381,2×0.07 = 34033,9 кДж/м3. Определим объем (V) и число молей (ν) продуктов горения, образовавшихся при сгорании исходной смеси, содержащей 84 об.% СН4, 6 об.% С2Н6, 7% H2S(г), используя приведённые выше химические уравнения реакций их горения. Учтём также, что смесь в соответствии с заданием содержит дополнительно 3 об.% О2: = (vCO2 / vCH4) × (φCH4 /100) + (vCO2 / vC2H6) × (φC2H6 /100) = 1/1 × 84/100 + 2/1 × 6/100 = 0,96 м3/м3 ; νCO2 = 0,96/ 0,02445 = 39,26 моль/м3 ;O = (vH20 / vCH4) × (φCH4 /100) + (vH20 / vC2H6) × (φC2H6 /100) + (vH20 / vH2S) × (φH2S /100) = 2/1 × 84/100 + 3/1 × 6/100 + 2/2 × 7/100 = 1,93 м3/м3 ; νH20 = 1,93/ 0,02445 = 78,94 моль/м3 ;= (vN2 / vCH4) × (φCH4 /100) + (vN2 / vC2H6) × (φC2H6 /100) + (vN2 / vH2S) × (φH2S /100) = (2×3,76)/1 × 84/100 + (3,5×3,76)/1 × 6/100 + (3×3,76)/2 × 7/100 = 7,501 м3/м3 ; νN2 = 7,501/ 0,02445 = 306,798 моль/м3 ; VSO2 = (vSO2 / vH2S) × (φH2S /100) = 2/2 × 7/100 = 0,07 м3/м3 ; νSO2 = 0,07/ 0,02445 = 2,86 моль/м3 ; = φO2 /100 = 3/100 = 0,03 м3/м3 ; νO2 = 0,03/ 0,02445 = 1,23 моль/м3 . Суммарный объем продуктов горения составит: Vпг = 0,96 + 1,93 + 7,501 + 0,07 +0,03 = 10,49 м3/м3 или 429,04 моль/м3. После интегрирования уравнения (21) получим выражение для расчёта адиабатической температуры горения: = T0 + Qнс, об / Σ νi CP,пг = T0 + Qнс, об / (νCO2 CP,CO2 + νH2O CP,H2O + νN2 CP,N2 + νSO2 CP,SO2 + νO2 CP,O2) (26) Для расчетов воспользуемся следующими средними значениями теплоемкостей для температурного диапазона 298−2000 K (табл. 3) 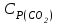 =53,14; =53,14; 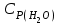 =42,34; =42,34; 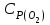 =34,73; =34,73; 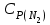 =32,76; CP(SO2)=52,57 Дж/моль.K. =32,76; CP(SO2)=52,57 Дж/моль.K.Подставив приведенные значения теплоемкостей и числа молей продуктов сгорания в формулу (26), получим:= 298 + 34033,9 × 103/(39,26×53,14 + 78,96×42,34+ 1,23×34,73 + 306,798×32,76 + 2,86×52,57 ) = 2470 К. Действительная температура горения всегда ниже адиабатической, так как часть тепла теряется с излучением. При расчете действительной температуры горения учитываются потери тепла в результате химического недожога в зоне горения, когда образуются продукты неполного сгорания (СО, С, CnHm и др.) и потери тепла за счёт излучения факела пламени. 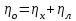 , (27) , (27)где 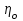 - общие теплопотери при горении газового фонтана, представляющие собой долю от низшей теплоты сгорания - общие теплопотери при горении газового фонтана, представляющие собой долю от низшей теплоты сгорания 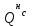 ; ;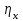 - химический недожог (0,10); - химический недожог (0,10);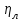 - коэффициент теплопотерь излучением. - коэффициент теплопотерь излучением.Коэффициент теплопотерь излучением от пламени газового фонтана может быть определен в соответствии со следующей формулой: 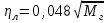 . (28) . (28)Молекулярную массу фонтанирующего газа ( 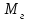 ), состоящего из нескольких компонентов, можно определить по формуле: ), состоящего из нескольких компонентов, можно определить по формуле: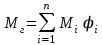 , (29) , (29)где 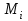 − молекулярная масса i-гo горючего компонента газового фонтана; − молекулярная масса i-гo горючего компонента газового фонтана;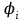 − доля i-гo горючего компонента. − доля i-гo горючего компонента.Молекулярная масса горючего газа, содержащего метан, этан и сероводород, будет равна: Мг = МCH4 φCH4 + МC2H6 φC2H6 + МH2S φH2S =16×0,84 + 30×0,06 + 34×0,07= =17,62 г/моль. Коэффициент теплопотерь за счёт излучения пламени фонтана составит: ηл=0,048 √17,62 = 0,2. Тогда для общих теплопотерь будет равна: η= 0,08 + 0,2 = 0,28. Действительная температура горения газового фонтана будет равна: 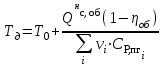 (30) (30)д= 298 + 34033,9 × 103 ×(1 - 0,28)/(39,26×53,14 + 78,96×42,34 + 306,798×32,76 + 2,86×52,57 + 1,23×34,73) = 1862 К. . Интенсивность лучистого потока от факела пламени, приходящаяся на единицу площади поверхности окружающих тел, называют плотностью лучистого потока или облучённостью (Е). Её обычно выражают в кВт/м2. Величина облучённости определяет границы локальных зон теплового воздействия факела пламени, в пределах которого предъявляются определённые требования к экипировке личного состава, выполняющего боевые действия по тушению пожара, и времени пребывания в данных зонах. Расстояние от устья скважины, в пределах которого облучённость не превышает 1,6 кВт/м2, является безопасным для нахождения в течение неопределённо долгого времени. При граничном уровне облучённости 4,2 кВт/м2 допустимо нахождение не более 15 минут бойцов без специального теплозащитного снаряжения при условии защиты открытых кожных покровов (перчатки, защитные щитки). Специальное теплозащитное снаряжение и защита с использованием распылённых водяных струй позволяют вести работу в течение 5 минут при облучённости 14 кВт/м2. Величину облучённости от факела пламени горящего фонтана в зависимости от расстояния до устья скважины можно рассчитать по формулам: 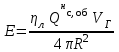 , (31) , (31)где 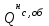 − низшая теплота сгорания фонтанирующего газа, кДж/м3; − низшая теплота сгорания фонтанирующего газа, кДж/м3;VГ − секундный расход газа, м3/с; R − длина гипотенузы в треугольнике, катетами которого являются половина высоты факела фонтана и расстояние от устья скважины до места облучения (L), м. Очевидно, что 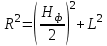 , (32) , (32)Тогда из (31) следует, что 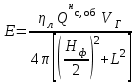 (33) (33)Для установления величины облучённости окружающего пространства факелом пламени в зависимости от расстояния до скважины в формуле (32) необходимо задаваться значениями L, принимая их равными 20, 40, 60, 80, 100, 120, 150 и 200 м. В формулу (32) подставляются также высота факела пламени Нф=13 м, секундный расход газа VГ=4,8 м3/с и коэффициент теплопотерь излучением л= 0,2. В качестве примера проведем расчёт облучённости (Е) на расстоянии L = 20 м: Е = (0,2×34033,9×4,8)/(4×3,14×[(13/2)2 + 202 ] ) = 5,88 кВт/м2 . Остальные значения получим по аналогии, используя формулу (33). Рассчитанные значения облучённости сведём в табл. 8. Таблица 8. Величина облучённости от факела газового фонтана в зависимости от расстояния до устья скважины
Зависимость Е = f(L) в графической форме представлена на рис. 11. Рисунок 11. Зависимость изменения облучённости, создаваемой факелом пламени газового фонтана, от расстояния до устья скважины Построенный график можно использовать для определения границ локальных зон теплового воздействия факела горящего фонтана, на которых уровень облучённости составляет 1,6; 4,2 и 14 кВт/м2, путём нахождения расстояния от точки, имеющей соответствующую облучённость, до устья скважины. Также границы зон можно определить из формулы (34), подставив в неё известные значения Е и положив неизвестной величиной расстояние L. Таким образом, расстояние до соответствующих локальных зон теплового воздействия составляют соответственно 39,8; 24 и 12 м от устья скважины. 5. Определение теоретического расхода воды на тушение газового фонтана производится по формуле (18): nв = 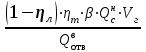 Коэффициент излучения л был рассчитан ранее по формуле (28). Коэффициентт в свою очередь рассчитывается из соотношения: 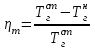 (34) (34)Для определения этого коэффициента необходимо рассчитать действительную температуру горения стехиометрической смеси горючих газов с воздухом (при =1) 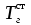 и температуру горения при концентрации горючей смеси, равной нижнему концентрационному пределу и температуру горения при концентрации горючей смеси, равной нижнему концентрационному пределу 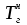 . .Согласно формуле (11): Тгст = Т0 + Qнс, об (1- ηл) / (νCO2 CP,CO2 + νH2O CP,H2O + νN2 CP,N2 + νSO2 CP,SO2) = 298 + 34033,9 × 103 ×(1 - 0,2)/(39,26×53,14 + 306,798×32,76 + 78,96×42,34 + 2,86×52,57) = 2040 К. По формуле (12) находим Тгн: Тгн = Т0 + Qнс, об (1- ηл) / (νCO2 CP,CO2 + νH2O CP,H2O + νN2 CP,N2 + νSO2 CP,SO2 +Δν CP,в). Предварительно находим избыточный объём воздуха: ΔVв =Vв0 (α - 1). Для этого рассчитываем теоретический объём воздуха, необходимый для сгорания газовоздушной смеси заданного нам состава: в0 = (Σi φ i - φ O2)/21. (35) где 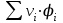 - сумма произведений стехиометрического коэффициента реакций горения каждого компонента горючей смеси (i) на процентное содержание этого компонента (Σi) в смеси; - сумма произведений стехиометрического коэффициента реакций горения каждого компонента горючей смеси (i) на процентное содержание этого компонента (Σi) в смеси;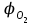 - процентное содержание кислорода в газовой смеси.в0 = (2×84 + 3,5×6 + 3×7 - 3)/ 21=9,9 м3 /м3 . - процентное содержание кислорода в газовой смеси.в0 = (2×84 + 3,5×6 + 3×7 - 3)/ 21=9,9 м3 /м3 .Коэффициент избытка воздуха α определяют из соотношения (13). Нижний концентрационный предел для многокомпонентной газовой смеси рассчитывается по формуле Ле-Шателье: φ нсм = 100/ (Σ φ i / φ iн ), [%] где ji - концентрация i - го горючего газа в смеси; jiн - значение НКПВ i - го компонента (табл. 4). φ нсм = 100/(84/5,3 + 6/2,9 + 7/4,3) = 5,1 %. Отсюда α = (100 - НКПР) / (НКПР×Vв0 ) = (100 - 5,1) / (5,1×9,9) = 1,88. Тогда DVв = 9,9 (1,88 - 1) = 8,7 м3/м3 или Δνв = 8,7/0,02445=355,83 моль/м3 . Среднее значение теплоёмкости воздуха в интервале температур 298-2000 К составляет 32,3 Дж/ (моль К). Отсюда: Тгн = 298 + 34033,9 × 103 ×(1 - 0,2)/(39,26×53,14 + 306,798×32,76 + 78,96×42,34 + 2,86×52,57 + 355,83×32,3) = 1302 К. Определим коэффициент hт: hт = (2040 - 1302)/ 2040 = 0,36. Расход воды, требуемый для прекращения горения газового фонтана, рассчитываем согласно формуле (18): 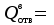 4570 кДж/кг. Низшая теплота сгорания газовой смеси выражена в кДж/м3, поэтому количество тепла, которое вода отнимает из зоны горения, также выразим в кДж/м3. 4570 кДж/кг. Низшая теплота сгорания газовой смеси выражена в кДж/м3, поэтому количество тепла, которое вода отнимает из зоны горения, также выразим в кДж/м3.При 298 К один килограмм воды занимает объём, приблизительно равный 1 л или 10−3 м3. Тогда 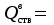 4570 кДж/л или 4570000 кДж/м3 4570 кДж/л или 4570000 кДж/м3Подставив все известные значения в формулу (18), получим:в=(1 - 0,2)×0,36×0,9×34033,9×4,8/4570000 = 0,009 м3/с или 9 л/с. С учетом коэффициента использования воды, равного 0,1, расход воды составит 90 л/с. Выводы Граница локальной зоны теплового воздействия факела пламени газового фонтана, за пределами которой личный состав при выполнении боевых действий может находиться неопределённо долгое время (Е=1,6 кВт/м2), расположена на расстоянии 39,8 м от устья скважины. Граница локальной зоны теплового воздействия факела пламени газового фонтана, на которой личный состав может работать без специального теплозащитного снаряжения не более 15 минут при условии защиты кожных покровов (Е=4,2 кВт/м2), находится на расстоянии 24 м от устья скважины. Граница локальной зоны теплового воздействия факела пламени газового фонтана, на которой личный состав может вести боевую работу в специальном теплозащитном снаряжении под защитой распылённых водяных струй не более 5 минут (Е=14 кВт/м2) находится на расстоянии 13 м от устья скважины. Требуемый секундный расход, обеспечивающий прекращение горения газового фонтана с дебитом 0,4225 млн. м3 /сут., составляет 90 л/с. Библиографический список Абдурагимов И.М., Андросов А.С., Исаева Л.К., Крылов Е.В. Процессы горения М.: РИО ВИПТШ МВД СССР, 1976. 113с. Ахметов Д.Г., Луговцов Б.А. Вихрепорошковый способ тушения пожаров на фонтанирующих газонефтяных скважинах / Тр. школы семинара “Физика нефтяного пласта” 2002. С. 7-14. Боевой устав противопожарной службы (утвержден приказом Председателя Комитета по государственному контролю и надзору в области чрезвычайных ситуаций Министерства по чрезвычайным ситуациям Республики Казахстан от 27.12.05 г. № 373). Драйздейл Д. Введение в динамику пожаров М.: Стройиздат, 1990. 424 с. Краткий справочник физико-химических величин / Под ред. А.А. Ра-вделя и А.М. Пономаревой Л.: Химия, 1983. 332 с. Малеванский В. Д. Открытые газовые фонтаны и борьба с ними / В. Д. Малеванский. - М.: Гостоптехиздат, 1963.- 288 с. Мамиконянц Г. М. Тушение пожаров мощных газовых и нефтяных фонтанов / Г. М. Мамиконянц. - М.: Недра, 1971. - 95 с. Марков В.Ф., Маскаева Л.Н., Миронов М.П., Пазникова С.Н. Физико-химические основы развития и тушения пожаров. Учебное пособие. - Екатеринбург: Изд-во УрО РАН. - 2009. - 274 с. Михеев В. П. Газовое топливо и его сжигание / В. П. Михеев. - Л.: Недра, Ленингр. отд-ние, 1966. - 327 с. Повзик А. Я. Пожарная тактика / А. Я. Повзик. - М.: ЗАО «Спецтехника», 2004. - 416 с. Рекомендации по тушению пожаров газовых и нефтяных фонтанов- М.: РИО ВИПТШ МВД СССР, 1976. 83с. Решетняк В. В. Применение метода Родионова для расчета квазиодномерных движений идеальной сжимаемой жидкости / В. В. Решетняк, А. Н. Семко // Прикладная гидромеханика. - 2009. - Т. 9 (81), № 3. - С. 56-64. Семко А. Н. Внутренняя баллистика порохового водомета и гидропушки / А. Н. Семко // Теорет. и прикл. механика. - Харьков: Основа, 2002. - Вып. 35. - С. 181-185. Семко А. Н. Импульсные струи жидкости высокого давления / А. Н. Семко. Донецк: Вебер (Донецкое отделение), 2007. - 149 с. Чабаев Л. У. Технологические и методологические основы предупреждения и ликвидации газовых фонтанов при эксплуатации и ремонте скважин: автореф. дис. на соискание уч. ст. доктора техн. наук: спец. 05.26.03 «Пожарная и промышленная безопасность (нефтегазовый комплекс)» / Л. У. Чабаев. - Уфа, 2009. - 47 с. Черменский Г. П. Избыточное давление в импульсной струе жидкости / Г. П. Черменский // ПМТФ, 1970. - № 1.- С. 174-176. |
