иммунология. Иммунитет. Благодаря иммунитету организм опознает, связывает, разрушает и выводит вещества и структуры. Вещества, отличающиеся по происхождению от собственных структур, называют чужеродными. Иммунитет
 Скачать 75.19 Kb. Скачать 75.19 Kb.
|
|
Введение. Внешние и внутренние факторы меняют клеточные циклы здорового как животного ,так и человека. В результате образуются аномальные (чужеродные, или синтезированные не так, как свои собственные) молекулы и клетки. Специальные клетки крови и других тканей продуцируют и поддерживают достаточную концентрацию фиксированных на клетках и свободных молекул, которые распознают, связывают (преобразуют) и выводят из организма аномальные молекулы и клетки. Перераспределение частиц и клеток, «иммунного надзора» во все ткани организма происходит через крово- и лимфоток, а также транспорт через гистогематические барьеры. Иммунитет (от лат. immunis) дословно означает свободный от чего- либо. Организм здорового животного непрерывно освобождается от веществ и структур, в том числе болезнетворных, как попадающих в него извне, так и образующихся внутри организма. Источниками внешних (экзогенных) веществ и структур являются компоненты пищи, химические примеси воздуха и капельки жидкости, микроорганизмы, попадающие на кожу, в легкие, желудочно-кишечный тракт. Эндогенными (возникающими в самом организме) веществами, нарушающими постоянство внутренней среды и выводимыми с помощью иммунных механизмов, являются аномальные (мутантные) клетки и их компоненты, появившиеся при делении клеток, внутриклеточном синтезе веществ, метаболиты (шлаки) и др. Тело животного состоит примерно из 1012-1013генотипически похожих клеток. Если принять, что при делении клеток каждая миллионная клетка подвергается мутации, то в любой момент в организме человека есть примерно 10 млн. аномальных клеток, которые могут стать источником смертельных опухолей. Иммунитет. Благодаря иммунитету организм опознает, связывает, разрушает и выводит вещества и структуры. Вещества, отличающиеся по происхождению от собственных структур, называют чужеродными. Иммунитет — способность специальных клеток жидкостей организма опознавать, связывать и удалять (выводить) вещества и структуры, происходящие из клеток других организмов или потерявших сходство с клетками собственного тела. Иммунитет поддерживает жизнедеятельность организма путем выведения изношенных клеток, белков (гемоглобин, др.), шлаков, возобновления специфических для организма белков, клеток, в том числе клеток крови определенной группы, сохранения чужеродного плода во время беременности, и др. Поэтому понятие иммунитет шире способности защищаться от инфекции. Хотя значение инфекции очевидно: около 50% здоровых людей является носителями болезнетворных микроорганизмов (Лебедев К.К., др., 1989). Таким образом, иммунитет поддерживает определенные (молекулярные) показатели гомеостаза и, значит, здоровья животного.человека: динамическое равновесие количества удаляемых и восстанавливаемых клеток, тканей и жидкостей тела. Одним из механизмов гомеостаза является поддержание иммунитета — определенного уровня активности клеток (лимфоцитов, лейкоцитов, эпителиоцитов, др.), синтезирующих и выделяющих естественные антитела (глобулины и др.) в кровь и другие жидкости тела. Сохранение постоянства клеток и их производных есть результат деятельности иммунной системы. Воздействие формирует систему ответа на него. Непрерывность антигенных воздействий на организм поддерживает иммунитет животного. Помещенный в стерильные условия (стерильная пища, вода, окружающая среда) организм (гнотобионт, греч. gnotos- известный, biontos — живой организм) теряет иммунитет. Раздражителями для органов иммунной системы являются антигены — сложные химические вещества, микроорганизмы, появляющиеся в результате деления аномальные клетки или их компоненты. Эти антигенные воздействия вызывают ответы «органов» иммунной системы — костного мозга, тимуса, селезенки, пейеровых бляшек стенки кишечника, лимфоузлов, лимфатических сосудов и др. Степень активности органов иммунной системы, вызванная воздействием внутренних и внешних антигенов, описывается как состояние — иммунный статус организма, или иммунитет. Животное остается здоровым до тех пор, пока не нарушается динамическое равновесие между антигенным воздействием и активностью иммунной системы. Поэтому иммунная система — понятие не столько морфологическое, сколько функциональное.. Гуморальный и клеточный иммунитет Существуют две ветви приобретенного иммунитета с разным составом участников и различным предназначением, но имеющие одну общую цель — устранение антигена. Как мы увидим в дальнейшем, эти две ветви взаимодействуют друг с другом, чтобы достичь конечной цели — устранения антигена. Из этих двух направлений приобретенного иммунного ответа одно определяется участием в основном В-клеток и циркулирующих антител, в форме так называемого гуморального иммунитета (термин «гуморальный» ранее использовали для определения жидких сред организма). Другое направление определяется участием Т-клеток, которые, как мы указывали ранее, не синтезируют антител, но синтезируют и высвобождают различные цитокины, действующие на другие клетки. В связи с этим данный вид приобретенного иммунного ответа называется клеточным или клеточно-опосредованным иммунитетом. Гуморальный иммунитет определяется участием сывороточных антител, которые являются белками, секретируемыми В-клеточным звеном иммунной системы. Первоначально после связывания антигенов со специфическими молекулами мембранного иммуноглобулина (Ig) (В-клеточные рецепторы; В cell receptors — BCR) В-клетки активируются для секреции антител, которые экспрессируются этими клетками. По имеющимся оценкам, каждая В-клетка экспрессирует примерно 105 BCR совершенно одинаковой специфичности. После связывания антигена В-клетка получает сигналы на производство секретируемой формы того иммуноглобулина, который ранее был представлен в мембранной форме. Процесс инициации полномасштабной реакции с участием антител направлен на удаление антигена из организма. Антитела представляют собой гетерогенную смесь сывороточных глобулинов, которые обладают способностью самостоятельно связываться со специфичными антигенами. Все сывороточные глобулины со свойствами антител относят к иммуноглобулинам. Все молекулы иммуноглобулинов имеют общие структурные свойства, которые позволяют им: 1) распознавать и специфически связываться с уникальными элементами структуры антигена (т.е. эпитопами); 2) выполнять общую биологическую функцию после соединения с антигеном. В основном, каждая молекула иммуноглобулина состоит из двух идентичных легких (L) и двух тяжелых (Н) цепей, связанных дисульфидными мостиками. Получающаяся в результате структура показана на рис. 1.2. Рис. 1.2. 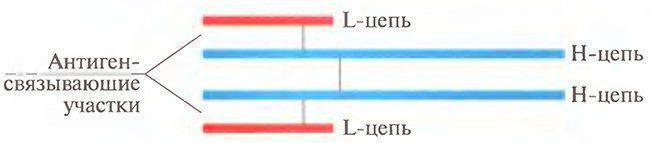 Типичная молекула антитела, состоящая из двух тяжелых (Н) и двух легких (L) цепей. Выделены антигенсвязывающие участки Часть молекулы, которая связывается с антигеном, является зоной, состоящей из терминальных участков аминокислотных последовательностей как на L-, так и на Н-цепях. Таким образом, каждая молекула иммуноглобулина является симметричной и способна связываться с двумя идентичными эпитопами, имеющимися на одной молекуле антигена или на разных молекулах. Кроме различий между участками, связывающими антиген, у разных молекул иммуноглобулина имеются и другие различия, наиболее важные из которых касаются Н-цепей. Существует пять основных классов Н-цепей (называемых у, μ, α, ε и δ). На основании различий в Н-цепях молекулы иммуноглобулина были разделены на пять основных классов: IgG, IgM, IgA, IgE и IgD, каждый из которых характеризуется уникальными биологическими свойствами. Например, IgG является единственным классом иммуноглобулинов, пересекающим плацентарный барьер и передающим материнский иммунитет плоду, в то время как IgA — основной иммуноглобулин, обнаруживаемый в таких секретах желез, как слеза или слюна. Важно отметить, что антитела всех пяти классов могут обладать совершенно одинаковой специфичностью по отношению к антигену (антигенсвязывающие участки), сохраняя в то же время различные функциональные (биологические эффекторные) свойства. Связь между антигеном и антителом нековалентная, она зависит от множества относительно слабых сил, таких как водородные связи, вандерваальсовы силы и гидрофобные взаимодействия. Поскольку эти силы слабы, для успешного связывания антигена с антителом требуется очень близкий контакт на ограниченном участке, наподобие контакта ключа и замка. Другим важным элементом гуморального иммунитета является система комплемента. Реакция между антигеном и антителом активирует комплемент, который составляют ряд сывороточных ферментов, что приводит или к лизису мишени, или усиливает фагоцитоз (поглощение антигена) клетками-фагоцитами. Активация комплемента также приводит к привлечению полиморфно-ядерных (ПМЯ) клеток, обладающих высокой способностью к фагоцитозу и являющихся частью врожденной иммунной системы. Эти события обеспечивают максимально эффективный ответ гуморальной ветви иммунитета на вторжение чужеродных агентов. Клеточно-опосредованный иммунитет Антигенспецифичная ветвь клеточно-опосредованного иммунитета задействует Т-лимфоциты (рис. 1.3). В отличие от В-клеток, вырабатывающих растворимые антитела, которые циркулируют для связывания соответствующих специфичных антигенов, каждая Т-клетка, несущая множество идентичных антигенных рецепторов, называемых TCR (около 105 на клетку), сама направляется непосредственно к месту, где на АПК экспрессируется антиген, и взаимодействует с ней в близком (непосредственно межклеточном) контакте. Рис. 1.3. 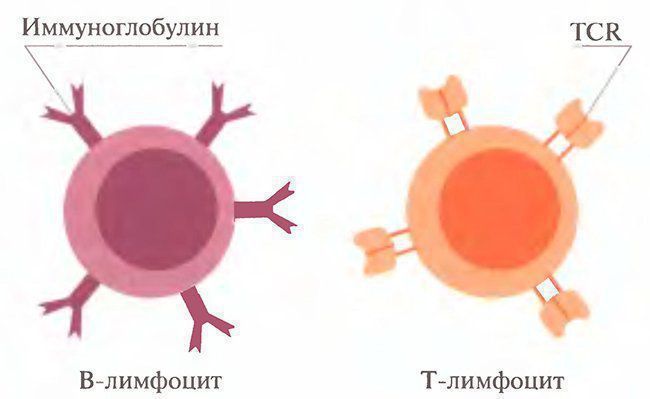 Рецепторы для антигена, экспрессируемые как трасмембранные молекулы на В- и Т-лимфоцитах Существует несколько различающихся по фенотипу субпопуляций Т-клеток, каждая из которых может обладать одинаковой специфичностью по отношению к антигенной детерминанте (эпитопу), но при этом выполнять различные функции. В данном случае можно провести аналогию с разными классами молекул иммуноглобулинов, которые обладают одинаковой специфичностью, но различными биологическими функциями. Имеются две субпопуляции Т-клеток: Т-клетки-хелперы (Тн-клетки), которые экспрессируют молекулы CD4, и цитотоксические Т-клетки (Тс-клетки), которые экспрессируют молекулы CD8 на своей поверхности. Разным субпопуляциям Тн-клеток приписывают различные функции. Взаимодействие с В-клетками для увеличения продукции антител. Такие Т-клетки действуют путем высвобождения цитокинов, которые обеспечивают подачу различных активирующих сигналов В-клеткам. Как указывалось ранее, цитокины являются растворимыми веществами или медиаторами, высвобождаемыми клетками; такие медиаторы, высвобождаемые лимфоцитами, называются лимфокинами. Группе цитокинов с низкой молекулярной массой дали название хемокины. Они, как указывается далее, участвуют в воспалительной реакции. Участие в реакциях воспаления. После активации определенная субпопуляция Т-клеток высвобождает цитокины, индуцируя миграцию и активацию моноцитов и макрофагов, что приводит к возникновению так называемых воспалительных реакций гиперчувствительности замедленного типа. Эту субпопуляцию Т-клеток, участвующих в реакции гиперчувствительности замедленного типа (ГЗТ), иногда называют Тгзт или просто Тн. Цитотоксические эффекты. Т-клетки особой субпопуляции становятся цитотоксическими клетками-киллерами, которые при контакте со своей мишенью способны нанести удар, ведущий к гибели клетки-мишени. Эти Т-клетки называют цитотоксическими Т-клетками (Тс). В отличие от Тн-клеток они экспрессируют молекулы CD8 на своих мембранах и поэтому называются СD8+-клетками. Регуляторные эффекты. Хелперные Т-клетки могут быть разделены на две различные функциональные подгруппы в соответствии с цитокинами, которые они высвобождают. Как вы узнаете из следующих глав, эти субпопуляции (Тн1 и Тн2) обладают различными регуляторными свойствами, которые передаются посредством высвобождаемых ими цитокинов. Более того, Тн1 -клетки могут негативно перекрестно влиять на Тн2-клетки, и наоборот. У другой популяции регуляторных или Т-клеток-супрессоров отмечается коэкспрессия CD4 и CD25 (CD25 является α-цепью рецептора интелейкина-2. Регуляторная активность этих СD4+/СD25+-клеток и их роль в активном подавлении аутоиммунитета обсуждается в гл. 12. Эффекты цитокинов. Т-клетки и другие клетки иммунной системы (например, макрофаги) оказывают различное воздействие на многие клетки, лимфоидные и нелимфоидные, посредством разных цитокинов, которые они высвобождают. Таким образом, прямо или косвенно Т-клетки связываются и взаимодействуют с множеством типов клеток. В результате многолетних иммунологических исследований было установлено, что клетки, активированные антигеном, проявляют целый ряд эффекторных способностей. Однако только за последние несколько десятилетий иммунологи стали осознавать всю сложность событий, которые происходят при активации клеток антигеном и при их взаимодействии с другими клетками. Мы теперь знаем, что простой контакт Т-клеточного рецептора с антигеном недостаточен для активации клетки. В действительности для активации антигенспецифичной Т-клетки должны быть даны по крайней мере два сигнала. Первый сигнал обеспечивается связыванием Т-клеточного рецептора с антигеном, который должен быть соответствующим образом презентирован АПК. Второй сигнал определяется участием костимуляторов, среди которых имеются определенные цитокины, такие как IL-1, IL-4, IL-6, и поверхностные молекулы, экспрессированные на АПК, такие как CD40 и CD86. В последнее время под термином «костимулятор» стали подразумевать и другие стимулы, например продукты жизнедеятельности микроорганизмов (инфекционные, чужеродные) и поврежденная ткань («гипотеза опасности» П. Матзингера (P. Matzinger)), которые будут усиливать первый сигнал, если он относительно слаб. Как только Т-клетки получают достаточно четкий сигнал для активации, происходит ряд событий, и активированная клетка синтезирует и высвобождает цитокины. В свою очередь эти цитокины контактируют с определенными рецепторами на различных клетках и воздействуют на эти клетки. Хотя обе, гуморальная и клеточная, ветви иммунного ответа рассматриваются как самостоятельные и отличные друг от друга компоненты, важно понимать, что реакция на любой специфический патоген может предусматривать сложное взаимодействие между ними, а также участие элементов врожденного иммунитета. Все это нацелено на обеспечение достижения максимально возможного выживания организма за счет удаления антигена и, как мы увидим далее, защиты организма от аутоиммунного ответа на собственные структуры. Взаимосвязь клеточной и гуморальной защиты При клеточном иммунитете оборона опосредована клетками. Понятие о клеточном оборонном механизме было введено и развито выдающимся российским биологом И.И. Мечниковым. Благодаря ему и Паулю Эрлиху, объявившему миру о гуморальном иммунитете, сосредоточенному в плазме крове, иммунология совершила квантовый прыжок в своем развитии. Выдающиеся ученые-биологи являются обладателями Нобелевской премии. Клеточные и гуморальные оборонные механизмы тесно взаимосвязаны. Они не могут существовать автономно друг от друга, отличаются функциональностью. Если гуморальная защита призвана вступать в сражение с бактериями, то клеточная – с грибком, вирусом, раковыми клетками. Иммунная секреторная системаСекреторная иммунная система защищает контактирующие с внешней средой слизистые оболочки. Инфицирование слизистых покровов организма вирусами и бактериями начинается с их адгезиина эпителиальных клетках. Функцию защиты во внешних секретах организма выполняет IgA , подавляя адгезию бактерий к клеткам. Он содержится в слезной жидкости, слюне, секретах слизистой носа, в жидкостях, омывающих слизистую кишечника (так называемые " копроантитела") и слизистую дыхательных путей. Во всех этих секретах IgA, связавшись с бактериями и вирусами, предотвращает их адгезию к поверхности слизистой. Естественно предположить, что для выполнения этой функции молекулы секреторного IgA должны обладать минимальной собственной адгезивностью к клеткам. И до сих пор еще не описаны высокоаффинные Fc-рецепторы этого класса Ig. Если инфекционный агент все же преодолевает барьер из IgA, он встречается со следующей защитной линией секреторной системы, основную роль в которой играет IgE . Следует отметить, что большая часть сывороточного IgE синтезируется плазматическими клетками слизистых облочек и дренирующих их лимфоузлов. Несмотря на низкий уровень IgE в сыворотке, он очень прочно связывается с Fc-рецепторами тучных клеток . Контакт IgE с антигеном приводит к высвобождению медиаторов, привлекающих эффекторные молекулы и клетки иммунного ответа и индуцирующих острое локальное воспаление . Так, гистамин , увеличивая проницаемость сосудов, вызывает приток IgG и комплемента , а хемотаксические факторы привлекают нейтрофилы и эозинофилы , необходимые для удаления инфекционных возбудителей, уже нагруженных специфическими антителами и C3b . Если опсонизированный микроорганизм слишком велик дляфагоцитоза , то фагоциты могут уничтожить его с помощью внеклеточного механизма, прикрепившись к нему своими Fcg -рецепторами. Итак, IgE, связанные с тучными клетками, могут стимулировать привлечение протективных IgG, комплемента и полиморфноядерных лейкоцитов к месту инфекции. Этот феномен называетсяантителозависимой клеточной цитоксичностью , и имеются данные о том, что он играет определенную роль в механизме антипаразитарного иммунитета Мононуклеарная фагоцитирующая система.Мононуклеарная фагоцитарная (МФ) система - это совокупность клеток, происходящих из моноцитов, обладающих фагоцитарной активностью. Кроме того, к фагоцитирующим клеткам относятся полинуклеарные фагоциты (ПМЯЛ) - нейтрофилы, эозинофилы, базофилы, микроглия (на рис. затушеваны). Важную роль в механизмах неспецифичкской защиты играют также ретикулярные, эндотелиальные клетки, которые не выполняют фагоцитарной функции, а поддерживают целостность лимфоидной ткани и кровеносных сосудов (Эндотелиальные клетки выстилают сосуды, ретикурные является основой кроветворных органов, образуются из мезенхимы). Фагоцит, описанный И.И. Мечниковым, состоит из 7 следующих фаз: 1) Хемотаксис - движение клеток в направлении градиента молекул, выделенных микроорганизмами. Хемотаксические факторы упорядочивают движения фагоцитов. Они воздействуют на специфические рецепторы на плазмолемме фагоцитов стимуляция которых передается на элементы его цитоскелета и изменяет экспрессию адгезивных молекул. Вследствие этого формируются псевдоподии, которые обратимо прикрепляются к элементам соединительной ткани, что обеспечивает направленную миграцию клеток. 2) Адгезия (прикрепление) клетки к объекту фагоцитоза Происходит при взаимодействии её рецепторного аппарата с молекулами на поверхности бактерии. Протекает в две стадии: -обратимая и непрочная -необратимая, прочная. 3) Захват бактерии клетки с формированием фагосомы Псевдоподии охватывают бактерию, заключая ее в мембранный пузырек - фагосому. Если бактерия инкапсулирована, то на нее садятся IgG или СЗВ. В таком случае бактерия опсонизирована. 4) Слияние гранул нейтрофила с фагосомой с образованием фаголизосомы Содержимое гранул выливается в просвет фаголизосомы (рН кислая). 5) Повреждение и внутриклеточное переваривание бактерии Гибель бактерии наступает вследствие действия на нее антимикробных веществ, далее он подвергается перевариванию лизосомальными ферментами. Бактерицидный эффект усиливается действием токсичных реактивных биоокислителей (перикисью водорода, молекул. Кислородом, супероксидными радикалами, гипохлоритом...) Фагоцитоз, являясь механизмом неспецифической защиты (фагоцитироваться могут любые инородные частицы независимо от наличия иммунизации), в то же время способствует иммунологическим механизмам защиты. Это связано, во-первых, с тем, что поглощая макромолекулы и расщепляя их, фагоцит как бы раскрывает структурные части молекул, отличающиеся чужеродностью. Во-вторых, фагоцитоз в условиях иммунологической защиты протекает быстрее и эффективнее. Таким образом, явление фагоцитоза занимает промежуточное место между механизмами специфической и неспецифической защиты. Это еще раз подчеркивает условность деления механизмов защиты клеточного гомеостаза на специфические и неспецифические. Нефагоцитарный механизм разрушения микробов характерен для ситуаций, когда микроорганизмы имеют столь большие размеры, что клетки не могут их поглощать. В таких случаях фагоциты скапливаются вокруг бактерии и выбрасывают содержимое своих гранул, уничтожая микроб большими концентрациями антимикробных веществ. Воспалительная реакциия также относится к клеточным неспецифическим реакциям. Она является эволюционно выработанным процессом защиты внутренней среды от проникновения чужеродных макромолекул, поскольку внедрившиеся в ткань чужеродные начала, например, микроорганизмы, фиксируются в месте внедрения, разрушаются и даже удаляются из ткани во внешнюю среду с жидкой средой очага воспаления - экссудатом. Клеточные элементы как тканевого происхождения, так и выходящие в очаг из крови (лейкоциты), образуют вокруг места внедрения своеобразный защитный вал, препятствующий распространению чужеродных частиц по внутренней среде. В очаге воспаления особенно эффективно протекает процесс фагоцитоза Гуморальные факторы внутренней среды, обеспечивающие механизмы неспецифической защиты, представлены пропердиновой системой и системой комплемента, осуществляющие лизис чужеродных клеток. При этом система комплемента, хотя и может активироваться неиммунологическим путем, обычно вовлекается в иммунологические процессы и поэтому скорее должна относиться к специфическим механизмам защиты. Пропердиновая система реализует свой защитный эффект независимо от иммунных реакций. К числу гуморальных факторов неспецифической защиты относят также содержащиеся в плазме крови и тканевой жидкости лейкин ы, плакины, бетализины, л и з о ц м и т.д.. Лейкины выделяются лейкоцитами, плакины - тромбоцитами крови, они оказывают отчетливое бактериолитическое действие. Еще большим литическим эффектом на стафилококки и анаэробные микроорганизмы обладают бета-лизины плазмы крови. Содержание и активность этих гуморальных факторов не меняются при иммунизации, что дает основание считать их неспецифическими факторами защиты. К числу последних следует также отнести и довольно большой спектр веществ тканевой жидкости, обладающих способностью подавлять ферментативную активность микроорганизмов и жизнедеятельность вирусов. Это ингибиторы гиалуронидазы, фосфолипаз, коллагеназы, плазмина и интерферон лейкоцитов. Система мононуклеарных фагоцитов (греч. monox один + лат. nucleos ядро: греч. рhagos пожирающий, поглощающий + гистол. суtus клетка; синоним: макрофагальная система, моноцитарно-макрофагальная система) — физиологическая защитная система клеток, обладающих способностью поглощать и переваривать чужеродный материал. Клетки, входящие в состав этой системы, имеют общее происхождение, характеризуются морфологическим и функциональным сходством и присутствуют во всех тканях организма. Основой современного представления о cистема мононуклеарных фагоцитов является фагоцитарная теория, разработанная И.И. Мечниковым в конце 19 в., и учение немецкого патолога Ашоффа (К. А.L. Aschoff) о ретикулоэндотелиальной системе (РЭС). Первоначально РЭС была выделена морфологически как система клеток организма, способных накапливать витальный краситель кармин. По этому признаку к РЭС были отнесены гистиоциты соединительной ткани, моноциты крови, клетки Купфера печени, а также ретикулярные клетки кроветворных органов, эндотелиальные клетки капилляров, синусов костного мозга и лимфатического узлов. По мере накопления новых знаний и совершенствования морфологических методов исследования стало ясно, что представления о ретикулоэндотелиальной системе расплывчаты, не конкретны, а в ряде положений просто ошибочны. Так, например, ретикулярным клеткам и эндотелию синусов костного мозга и лимфатических узлов длительное время приписывалась роль источника фагоцитирующих клеток, что оказалось неверным. В настоящее время установлено, что мононуклеарные фагоциты происходят из циркулирующих моноцитов крови. Моноциты созревают в костном мозге, затем поступают в кровяное русло, откуда мигрируют в ткани и серозные полости, становясь макрофагами. Ретикулярные клетки выполняют опорную функцию и создают так называемое микроокружение для кроветворных и лимфоидных клеток. Эндотелиальные клетки осуществляют транспорт веществ через стенки капилляров. Непосредственного отношения к защитной системе клеток ретикулярные клетки и эндотелий сосудов не имеют. В 1969 г. на конференции в Лейдене, посвященной проблеме РЭС, понятие «ретикулоэндотелиальная система» было признано устаревшим. Вместо него принято понятие «система мононуклеарных фагоцитов». К этой системе относят гистиоциты соединительной ткани, клетки Купфера печени (звездчатые ретикулоэндотелиоциты), альвеолярные макрофаги легких, макрофаги лимфатических узлов, селезенки, костного мозга, плевральные и перитонеальные макрофаги, остеокласты костной ткани, микроглию нервной ткани, синовиоциты синовиальных оболочек, клетки Лангергаиса кожи, беспигментные гранулярные дендроциты. Различают свободные, т.е. перемещающиеся по тканям, и фиксированные (резидентные) макрофаги, имеющие относительно постоянное место. Макрофаги тканей и серозных полостей, по данным сканирующей электронной микроскопии, имеют форму, близкую к сферической, с неровной складчатой поверхностью, образованной плазматической мембраной (цитолеммой). В условиях культивирования макрофаги распластываются на поверхности субстрата и приобретают уплощенную форму, а при перемещении образуют множественные полиморфные псевдоподии. Характерным ультраструктурным признаком макрофага служит наличие в его цитоплазме многочисленных лизосом и фаголизосом, или пищеварительных вакуолей. Лизосомы содержат различные гидролитические ферменты, обеспечивающие переваривание поглощенного материала. Макрофаги — активные секреторные клетки, которые освобождают в окружающую среду ферменты, ингибиторы, компоненты комплемента. Основным секреторным продуктом макрофагов является лизоцим. Активированные макрофаги секретируют нейтральные протеиназы (эластазу, коллагеназу), активаторы плазминогена, факторы комплемента, такие как С2, С3, С4, С5, а также интерферон. Клетки cистема мононуклеарных фагоцитовобладают рядом функций, в основе которых лежит их способность к эндоцитозу, т.е. поглощению и перевариванию инородных частиц и коллоидных жидкостей. Благодаря этой способности они выполняют защитную функцию. Посредством хемотаксиса макрофаги мигрируют в очаги инфекции и воспаления, где осуществляют фагоцитоз микроорганизмов, их умерщвление и переваривание. В условиях хронического воспаления могут появляться особые формы фагоцитов — эпителиоидные клетки (например, в инфекционной гранулеме) и гигантские многоядерные клетки типа клеток Пирогова — Лангханса и типа клеток инородных тел. которые образуются путем слияния отдельных фагоцитов в поликарион — многоядерную клетку. В гранулемах макрофаги вырабатывают гликопротеид фибронектин, который привлекает фибробласгы и способствует развитию склероза. Клетки cистема мононуклеарных фагоцитов принимают участие в иммунных процессах. Так, непременным условием развития направленного иммунного ответа является первичное взаимодействие макрофага с антигеном. При этом антиген поглощается и перерабатывается макрофагом в иммуногенную форму. Иммунная стимуляция лимфоцитов происходит при непосредственном контакте их с макрофагом, несущим преобразованный антиген. Имунный ответ в целом осуществляется как сложное многоэтапное взаимодействие Г- и В-лимфоцитов с макрофагами. Макрофаги обладают противоопухолевой активностью и проявляют цитотоксические свойства в отношении опухолевых клеток. Эта активность особенно выражена у так называемых иммунных макрофагов, осуществляющих лизис опухолевых клеток-мишеней при контакте с сенсибилизированными Т-лимфоцитами, несущими цитофильные антитела (лимфокины). Клетки cистема мононуклеарных фагоцитов принимают участие в регуляции миелоидного и лимфоидного кроветворения. Так, островки кроветворения в красном костном мозге, селезенке, печени и желточном мешке эмбрионе формируются вокруг особой клетки — центрального макрофага, организующего эритропоэз эритробластического островка. Клетки Купфера печени участвуют в регуляции кроветворения путем выработки эритропоэтина. Моноциты и макрофаги вырабатывают факторы, стимулирующие продукцию моноцитов, нейтрофилов и эозинофилов. В вилочковой железе (тимусе) и тимусзависимых зонах лимфоидных органов обнаружены так называемые интердигитирующие клетки — специфические стромальные элементы, также относящиеся к cистемs мононуклеарных фагоцитов, ответственные за миграцию и дифференцировку лимфоцитов. Обменная функция макрофагов заключается в их участии в обмене железа. В селезенке и костном мозге макрофаги осуществляют эритрофагоцитоз, при этом в них происходит накопление железа в форме гемосидерина и ферритина, которое питом может реутилизироваться эритробластами. Система комплемента Комплементом называют сложную систему ферментативных и рецепторных белков (более 30) сыворотки крови. Основные 13 компонентов системы комплемента обозначаются буквой C с соответствующим номером (C1, С2, С3 и т.д.) Они образуются в печени и секретируются макрофагами. Активация системы комплемента протекает классическим, очень сходным с ним лектиновым, а также альтернативнымпутями. Процесс имеет вид цепной реакции, управляемой регуляторными белками. При этом каждый предыдущий компонент каскада активирует несколько последующих за счет их ферментативного расщепления. При распаде компонентов комплемента обычно образуется 2 фрагмента. Больший фрагмент обозначается малой латинской буквой «b» и является активным, продолжая каскад расщепления. Меньшие фрагменты в дальнейшей активации комплемента обычно не участвуют, однако проявляются многообразными биологическими функциями. Они обозначаются малой латинской буквой «а». Единственное исключение из этого правила – фактор С2. Комплексы активированных компонентов обозначаются сверху чертой. Белки альтернативного пути активации получили название факторов и обозначаются большими латинскими буквами (В, Н, I и т.д.) Среди регуляторных белков различают естественный ингибитор компонента комплемента С1 (С1-ингибитор), который тормозит спонтанную активацию C1q компонента. При его дефиците возникает наследственный ангионевротический отек. Кроме этого существует фактор DAF, ускоряющий деградацию С3b компонента комплемента на мембранах собственных клеток организма, предотвращая их лизис. Классический путь активации запускается комплексом антиген-антитело в присутствии катионов Ca и Mg обычно на поверхности клетки-мишени (см. рис. 1.1.) Эффективными активаторами данного пути являются АТ классов IgG и IgM. Комплекс «антиген-антитело» связывается с компонентом С1q, который присоединяет С1rs, а затем активирует и расщепляет С4 на С4а и С4b (рис.11). С4b присоединяется либо к С1, либо к поверхности клетки-мишени. Далее к нему присоединяется С2. Он, в свою очередь, расщепляется на С2а и С2b предыдущим компонентом. С2а остается связанным с С4b. Этот комплекс получил название конвертазы классического пути активации комплемента. Она расщепляет С3 компонент на С3а и С3b. С3b присоединяется к конвертазе классического пути, образуется конвертаза С5 компонента, и этот макромолекулярный комплекс активирует компонент С5. Он распадается на С5а и С5b. К С5b на мембране клетки-мишени последовательно присоединяются С6, С7, С8. Этот комплекс встраивается в мембрану клетки-мишени и к нему может присоединиться до 20 молекул С9 компонента. Лектиновый путь активации комплемента отличается только природой иммунного комплекса, запускающего начальный этап активации. Со стороны иммунной системы здесь участвуют белки-лектины, связывающие полисахаридные компоненты бактерий (например, маннансвязывающий лектин, С-реактивный белок и т.д.) Активация происходит через компонент С1, и ее ход не отличается от классического пути. Альтернативный путь активациикомплемента является неспецифическим. Центральным звеном альтернативного пути является С3b компонент. Следовые его количества постоянно присутствуют в сыворотке вследствие спонтанного гидролиза С3. Этот процесс запускается и усиливается липополисахаридами клеточной стенки бактерий (эндотоксинами), агрегированными иммуноглобулинами, лекарственными препаратами и т.д. Образующийся при этом С3b-компонент в присутствии ионов магния связывается с фактором В сыворотки (неактивная сериновая протеаза). На комплекс С3bB действует фактор D – активная сывороточная протеаза. Она расщепляет фактор В на Ва и Вb. Образующийся комплекс С3bBb представляет собой конвертазу альтернативного пути активации. В норме она неустойчива, но стабилизируется белком пропердином (белок P). Конвертаза альтернативного пути присоединяет еще одну молекулу С3b, образуется конвертаза С5 компонента С3bBbС3b, которая активирует С5. Дальнейшая активация комплемента не отличается от классического пути. Таким образом, С3-компонент является ведущим в активации комплемента по обоим путям, определяя процессы цитолиза. В процессе активации комплемента образуются биологически активные фрагменты. Функции системы комплемента Лизис клеток-мишеней (бактериальных, зараженных вирусом, опухолевых и др.) Опсонизация, т.е. усиление фагоцитоза через рецепторы комплемента. Растворение иммунных комплексов, что препятствует их отложению в тканях. Заключение Защиту организма от внешней и внутренней биологической агрессии иммунная система обеспечивает путем двух основных механизмов — распознавания и разрушения чужеродных молекул и клеток. Это достигается благодаря слаженной работе иммуноцитов различного функционального предназначения. Основным молекулярным инструментом для реализации иммунного ответа служат антитела и поверхностные рецепторы. Причем те и другие могут выполнять как функцию распознавания, так и функцию разрушения чужеродных тел. Межклеточная связь между иммуноцитами выполняют интерлейкины, интерфероны и другие медиаторы. Нарушение этих механизмов приводит к различным формам иммунопатологии, опасной для здоровья и жизни Министерство сельского хозяйства Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования «КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ АГРАРНЫЙ УНИВЕРСИТЕТ им. И.Т. ТРУБИЛИНА» РЕФЕРАТ На тему: «Секреторный, гуморальный, клеточный иммунитет. Системы мононуклеарных фагоцитов и комплемента. Взаимосвязь реакций и их соотношение в противобактериальной и противовирусной защите.» Выполнила: Студентка 2 курса, группы № ВМ-1733 Конащенко М.Ю. Краснодар,2019 |
