Прапараты, общая характеристика. Иммунобиологические препараты
 Скачать 108.5 Kb. Скачать 108.5 Kb.
|
|
Иммунобиологические препараты: препараты, получаемые из живых или убитых микробов и их продуктов (живые и убитые вакцины, анатоксины, фаги, эубиотики); иммуноглобулины и иммунные сыворотки от иммунизированных животных и человека; диагностические препараты для выявления АТ и АГ, для постановки кожно-аллергических проб, для индикации и идентификации микробов. Вакцины Вакцинация основана на способности организма формировать приобретенный иммунитет и иммунологическую память в отношении возбудителя. Вакцинация – это самое известное и наиболее успешное применение иммунологических принципов в медицине. Первая вакцина была названа так по болезни крупного рогатого скота – vaccinia (коровья оспа). Два столетия назад ее применил английский врач Дженнер. Пастер сформулировал фундаментальный принцип вакцинации: для создания напряженного иммунитета против высоковирулентных микроорганизмов можно применять препараты из тех же микроорганизмов, но с ослабленной вирулентностью. В качестве действующего начала в вакцинах используют: · живые ослабленные возбудители; · инактивированные цельные возбудители; · отдельные АГ (протективные) возбудителей; · вторичные, продуцируемые микробной клеткой метаболиты токсины и их обезвреженные дериваты — анатоксины; · полученные генно-инженерным способом или химическим синтезом молекулярные АГ — аналоги природных АГ бактерий и вирусов. Все вакцины можно разбить на две большие группы — живые и неживые (или убитые, инактивированные) вакцины. Классификация вакцин
Живые вакцины В живых вакцинах используются: · аттенуированные, ослабленные (потерявшие свою патогенность) штаммы природных возбудителей (туляремийная, сибиреязвенная, чумная, бруцеллезная, гриппозная, коревая, полиомиелитная, паротитная); «генетическая рулетка» · дивергентные штаммы непатогенных бактерий и вирусов, имеющие родственные АГ с АГ возбудителей (оспенная вакцина); · рекомбинантные штаммы возбудителей, полученные генно-инженерным способом (векторные вакцины). Живые вакцины при введении в организм, вызывают вакцинальный процесс (размножение в организме вакцинного штамма и воздействии его на иммунокомпетентные клетки). Результатом этого является формирование специфического иммунитета к возбудителю данной инфекционной болезни. Получение живых вакцин: · культивирование вакцинного штамма в производственных условиях (бактерийные штаммы культивируют на питательных средах, вирусные — на куриных эмбрионах или в культурах клеток); · полученную чистую культуру вакцинного штамма стандартизуют и подвергают лиофильной сушке вместе со стабилизатором (альбумин, сахароза с желатиной); · вакцину контролируют по: концентрации живых бактерий или вирусов вакцинного штамма, остаточной влажности, безвредности, аллергенности, иммуногенности и др. Убитые вакцины В результате инактивации возбудители полностью теряют жизнеспособность, но сохраняют антигенные и иммуногенные свойства. Для инактивации возбудителя используют: · физические (нагревание, ультрафиолетовое облучение, ионизирующая радиация); · химические (формалин, спирт, фенол) методы. Убитые вакцины можно разделить на две группы: ·корпускулярные вакцины содержат целые возбудители (цельноклеточные, цельновирионные вакцины), или структурные элементы микробов, несущие специфические протективные антигены (субклеточные, субвирионные вакцины). В состав вакцин на основе протективных антигенов вводят консервант (мертиолят в концентрации 1:10 000) и адъюванты. ·молекулярные вакцинысодержатАГ в молекулярной форме (анатоксины). Получение убитых вакцин: культивирование вакцинного штамма; инактивация (чаще всего 0,4 % формальдегидом при 37—40 ОС в течение 4 нед); очистка от балластных компонентов; стандартизация; лиофильная сушка. Вакцину контролируют по основным показателям: остаточной вирулентности, содержанию бактерий или вирусов вакцинного штамма, остаточной влажности, стерильности, безвредности, аллергенности, иммуногенности и др. Анатоксины Анатоксины – обезвреженные токсины. Токсин обезвреживают формальдегидом (0,4 %) при 37—40 ОС в течение 4 нед. При таком режиме полностью утрачивается токсичность, но сохраняются антигенность и иммуногенность токсинов. Получение анатоксина: · культивирование токсигенного штамма (микроорганизм выделяет в среду экзотоксин); · фильтрование через бактериальные фильтры; · обезвреживание формалином; · очистка и стандартизация; · добавление адъюванта. Анатоксины контролируют по основным показателям: остаточной токсичности, концентрации, стерильности, безвредности, аллергенности, иммуногенности и др. В практике применяются анатоксины против столбняка, дифтерии, ботулизма, газовой гангрены, стафилококковых инфекций. Адъюванты Адъювантами (adjuvant — помощник) называют группу веществ, обладающих свойством повышать иммуногенность при добавлении их к АГ и вакцинам. Адъювантами могут быть: · минеральные соединения; · микробные структуры (белки, нуклеиновые кислоты, липополисахариды); · синтетические вещества (полинуклеотиды, гликопептиды, полиоксидоний); · цитокины и пептиды; Соединения алюминия сорбируют АГ, длительно удерживают его вблизи от места инъекции, что обеспечивает лучшее взаимодействие с представляющими АГ клетками. Иммуногенность сорбированных препаратов повышается в сотни раз. Механизмы действия адъювантов: · создание «депо» АГ в месте введения вакцин; · воспалительная реакция, активирующая иммунокомпетентные клетки; · активация процесса захвата АГ и его переработки фагоцитами. Рекомбинантные вакцины Рекомбинантные вакцины — это препараты, полученные биосинтезом при культивировании рекомбинантных штаммов бактерий и вирусов. Преимущество: использование только тех АГ, которые необходимы для формирования иммунитета; дешевизна, безопасность. Когда возбудитель не может быть культивирован генно-инженерный подход является единственно приемлемым. Принцип создания: ген или гены, кодирующие протективные АГ возбудителя «встраиваются» в геном вирусов, бактерий или эукариотов. При этом, наряду с АГ хозяина нарабатывается и необходимый для получения вакцины протективный АГ. Примером такой вакцины служит вакцина против гепатита В, состоящая из чистого HBs-АГ, полученного генно-инженерным путем (в геном дрожжевой клетки был встроен ген HBs-АГ и клетка получила способность его продуцировать). Ассоциированные вакцины Ассоциированные вакцины состоят из нескольких составляющих и предназначены для одновременной иммунизации против нескольких инфекций. АКДС — адсорбированная на гидроокиси алюминия убитая корпускулярная коклюшная вакцина в ассоциации с дифтерийным и столбнячным анатоксином; секстаанатоксин – сорбированные на гидроокиси алюминия столбнячный, ботулинические типов А, В, Е и гангренозные перфрингенс- и нови-анатоксины; вакцина против полиомиелита – живая вакцина, составленная из трех аттенуированных штаммов вируса I, II и III типов; живая ассоциированная вакцина против кори, паротита и краснухи. Возможна также комбинированная иммунизация, т.е. одновременное раздельное введение в организм нескольких несовместимых в одном препарате моновакцин, например чумной и оспенной вакцины. Схема применения вакцин Живые вакцины, как правило, применяют однократно, убитые — многократно. При первичной вакцинации создаются граунд-иммунитет и повышенная способность реагировать на АГ, в результате чего при повторном введении вакцины организм более активно и быстро отвечает на АГ. Первую ревакцинацию проводят обычно через 3 — 6 мес и более, а последующие — по схемам календаря прививок. Ревакцинации обеспечивают длительное поддержание иммунитета на защитном уровне. В нашей стране в соответствии с календарем прививок, утвержденным государственными органами, проводится обязательная вакцинация против гепатита В, туберкулеза, полиомиелита, кори, коклюша, дифтерии и столбняка. Прививки по эпидемическим показаниям проводятся определенным группам населения (группы риска) против гриппа, чумы, холеры, бруцеллеза, сибирской язвы, туляремии, паротита, краснухи, сыпного тифа, Ку-лихорадки, клещевого энцефалита и др. Патология поствакцинального периода Патологию поствакцинального периода можно подразделить на: · присоединение инфекции; · обострение хронического заболевания; · вакцинальные (прививочные) реакции и поствакцинальные осложнения, вызванные самой вакциной («истинные»). Вакцинальные реакции: общие (повышение температуры тела, недомогание) и местные (отек и воспалительную реакцию на месте введения вакцины). Поствакцинальные осложнения: местные (абсцесс, гнойный лимфаденит, некроз); патология ЦНС (острый паралич, энцефалопатия, энцефалит, менингит, судороги); аллергические реакции, артралгии, остиомиелит, сепсис и т.д. Противопоказания к вакцинации К противопоказаниямк вакцинации относятся острые заболевания сердечно-сосудистой системы, почек, печени, дыхательной и нервной систем, некоторые хронические болезни, иммунодефициты, выраженные явления аллергии и др. Беременность (кроме столбнячного и дифтерийного анатоксинов). Острый инфекционный процесс менее 30 дней назад. Сильная реакция или осложнение на предыдущую дозу. Перечень противопоказаний изложен в инструкциях, прилагаемых к каждой вакцине. Иммуноглобулины и антитоксические сыворотки Вакцинация обеспечивает выработку специфического активного искусственного иммунитета спустя 2—3 нед после первичной прививки и через 2—7 сут после ревакцинации, т.е. вторичного введения вакцины. При необходимости экстренного создания иммунитета, а также для лечения уже развивающейся инфекции используют сывороточные иммунные препараты. Иммунные сыворотки и иммуноглобулины создаютпассивный специфический иммунитет, который сохраняется при введении гомологичных сывороток до 1—1,5 мес и гетерологичных — до 10—20 сут. К сывороточным иммунным препаратам относят иммунные сыворотки и иммуноглобулины, содержащие уже готовые АТ. Действующее начало таких препаратов — специфические АТ. Их можно использовать для профилактики и лечения инфекций, при которых ведущим фактором невосприимчивости является гуморальный иммунитет. Сывороточные препараты 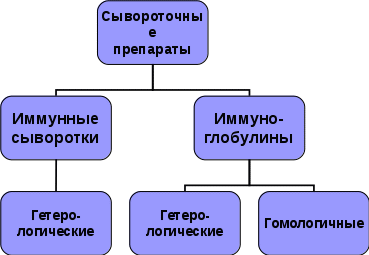 Иммунные сыворотки Гетерологичные сывороткиготовят путем гипериммунизации крупных животных (лошадей, волов, быков, коров, мулов), так как от них можно получить большие количества крови. Принцип получения: · лошадей гипериммунизируют, т.е. многократно вводят большие дозы антигена по разработанной схеме; · на пике антителообразования у иммунных животных забирают кровь, освобождают ее от форменных элементов и фибрина; · сыворотки очищают и концентрируют ферментативным способом в сочетании с диализом (метод «Диаферм»), осаждением спиртом на холоде, хроматографией или иными способами; · стандартизируют по концентрации АТ (антитоксинов) и контролируют. Иммуноглобулины Иммуноглобулины содержат меньше балластного белка и имеют более высокую концентрацию АТ. Для этого из сыворотки выделяют чистую фракцию гаммаглобулинов методом фракционирования разными концентрациями спирта. Гетерологические иммуноглобулины получают из крови лошадей. Для получения гомологичных иммуноглобулинов используют кровь специально вакцинированных доноров или иммунных (переболевших, вакцинированных) людей. Препараты иммуноглобулинов, полученные из человеческой крови для человека не иммуногенны, и в этом их преимущество перед гетерологичными сыворотками и глобулинами. Существующие методы приготовления человеческих глобулинов полностью исключают возможность присутствия в них вирусов, но они могут содержать агрегированные в процессе приготовления реактогенные белки. Поэтому препараты иммуноглобулинов вводят только в мышцу, подкожно или наносят на слизистые. Иммуноглобулины, предназначенные для внутривенного введения, подвергают дополнительной обработке с целью удаления агрегатов и снижения реактогенности. Нормальный иммуноглобулин человека Нормальный иммуноглобулин человека — препарат, приготовленный из смеси образцов крови неиммунизированных доноров, но содержащий АТ к возбудителям банальных инфекций. Используется для больных гипогаммаглобулинемией; для экстренной профилактики и лечения часто встречающихся инфекций и инфекций, от возбудителей которых существует плановая вакцинация. При производстве каждой серии этого препарата в одной реакторной загрузке смешивается плазма крови более 1000 доноров, безопасная в отношении вирусов иммунодефицита человека, а также гепатитов В и С. Правила введения гетерологических сывороточных препаратов Осложнения: сывороточная болезнь, анафилактический шок. Для профилактики анафилактического шока обязательна постановка внутрикожной пробы: введение 0,1 мл разведенного в 100 препарата. Пробу считают отрицательной, если диаметр отека и (или) покраснения меньше 1 см; положительной, если 1 см и более. При отрицательной кожной пробе неразведенную сыворотку вводят в объеме 0,1 мл подкожно. При отсутствии реакции через 30-60 мин внутримышечно вводят назначенную дозу сыворотки, подогретой до температуры 360С. Больной, получивший сыворотку, должен находится под наблюдением врача в течение часа. При положительной кожной пробе препарат применяют только по жизненным показаниям. Для десенсибилизации сыворотку, разведенную 1:100, вводят подкожно последовательно в объеме 0,5; 2,0; 5,0 мл с интервалами 15-20 мин, затем с теми же интервалами вводят подкожно 0,1 и 1,0 мл неразведенной сыворотки и при отсутствии реакции вводят назначенную дозу сыворотки.Метод Безредка. Одновременно с началом десенсибилизации больному вводят средства противошоковой терапии. 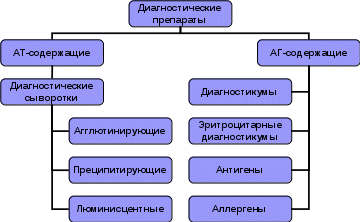 Диагностические сыворотки Диагностические иммунные сыворотки применяются для выявления АГ возбудителей в клиническом материале и для определения вида или типа возбудителя (серологическая идентификация микроорганизмов). Диагностические сыворотки: видовые (видоспецифические), групповые (группоспецифические), типовые (типоспецифические). Устранить групповую агглютинацию можно, удалив из сыворотки АТ против общих АГ. Это достигается добавлением к иммунной сыворотке густой взвеси микробов, дающих групповую агглютинацию, что ведет к адсорбции на их поверхности соответствующих АТ. После центрифугирования в сыворотке остаются только типовые АТ. Этот, так называемый метод рецепторного анализа, был предложен в 1902 году Кастеллани. Иммунные сыворотки, лишенные АТ к групповым АГ и сохранившие лишь АТ к специфическому АГ, получили название монорецепторных. Получение диагностических сывороток Для иммунизации животных (чаще всего кроликов) можно применять живые или убитые микроорганизмы. Из крови получают сыворотку, добавляют консервант, контролируют стерильность, специфичность, высоту титра и при необходимости лиофилизируют. Выпускаются неадсорбированные и адсорбированные агглютинирующие сыворотки. Получение люминисцирующих сывороток Люминисцирующие сыворотки применяют для диагностики ряда инфекционных заболеваний – для определения вирусов, бактерий, риккетсий и простейших в материале от больного в РИФ. РИФ является методом экспресс-диагностики. Люминесцентные сыворотки готовят из специфических иммунных сывороток, которые получают подобно агглютинирующим и преципитирующим сывороткам. Из них извлекают глобулиновую фракцию высаливанием сернокислым аммонием. Полученные глобулины обрабатывают флюорохромами. Обработанные таким образом АТ способны люминесцировать (светится) в ультрафиолетовых лучах люминесцентного микроскопа. Антигенсодержащие препараты Диагностикумы, эритроцитарные диагностикумы, антигены, аллергены. Диагностикумы – это взвесь убитых возбудителей или их отдельных компонентов, чаще всего в физиологическом растворе. Применяемые в качестве АГ для серологических реакций. Диагностикумы, используемые для распознавания инфекционных заболеваний, делятся на бактерийные, риккетсиозные и вирусные. С их помощью в сыворотке больных можно определить наличие АТ по отношению к определенному виду возбудителя или его отдельным АГ. Для приготовления диагностикумов культуру возбудителя инактивируют, очищают, контролируют на стерильность, специфическую активность, разливают в ампулы, при необходимости лиофилизируют. Антигены готовят путем обработки бактерий температурой, УЗ, спиртом, кислотой, многократным замораживанием о оттаиванием и т.д. Принцип приготовления эритроцитарных диагностикумов: дефибринированная кровь фильтруется и отмывается физиологическим раствором, эритроциты обрабатываются формалином, танином и соединяют с АГ. В препарате проверяют густоту взвеси, отсутствие спонтанной агглютинации, специфическую активность с соответствующими иммунными сыворотками. Аллергены. Аллергены при одних заболеваниях (туберкулез, бруцеллез) представляют собой фильтраты бульонных культур, при других (туляремия) – взвесь убитых нагреванием бактерий. В настоящее время выпускают туберкулин, бруцеллин, тулярин, антраксин, токсоплазмин. Туберкулин – белковая вытяжка из культуры туберкулезной палочки в физиологическом растворе с твином в качестве консерванта и фенолом – стабилизатора. Вводят внутрикожно (реакция Манту). Бактериофаги Бактериофаги – это иммунобиологические препараты, состоящие из фагов ( вирусов бактерий). Препараты бактериофагов получают путем инфицирования фагом выращенной в производственных условиях культуры бактерий, чувствительной к данному фагу. Затем их фильтруют, концентрируют, проводят очистку, дозируют по числу вирусных частиц и в ряде случаев – лиофилизируют. Специфичность и титр фагов определяют на культурах чувствительных штаммов бактерий. Бактериофаги выпускают в виде таблеток, в жидком виде. Применение бактериофагов Бактериофаги применяют для профилактики и лечения ряда бактериальных, чаще всего кишечных инфекций (холера, брюшной тиф, дизентерия). Препарат назначают перорально, а в случаях раневых инфекций (газовая гангрена, стафилококковые инфекции) им орошают раны. Фаги используют в диагностике бактериальных инфекций с целью их фаготипирования. По спектру действия выделяют поливалентные (лизирующие родственные бактерии, в том числе близких видов), моновалентные (лизирующие бактерии одного вида) и типоспецифические. Эубиотики Эубиотики состоят из живых микроорганизмов – представителей микрофлоры человека. Они используются для профилактики и лечения дисбактериозов. Эубиотики получают путем выращивания бактерий на искусственных питательных средах, концентрирования, сушки, стандартизации и изготовления готовой формы в виде порошка или таблеток. Используют препараты из кишечной палочки, бифидумбактерий, лактобацилл. Отсюда препараты эубиотиков имеют названия «колибактерин», «бифидумбактерин», «лактобактерин», «бификол» и др. Препараты эубиотиков применяют перорально 2—3 раза в день длительными курсами (1—6 мес). |
