неорг.вещества. Интегрированный урок по теме Химический состав клетки. Неорганические вещества и их роль в клетке
 Скачать 1.77 Mb. Скачать 1.77 Mb.
|
|
Интегрированный урок по теме «Химический состав клетки. Неорганические вещества и их роль в клетке» (10 класс) Учитель биологии: Калугина С.В., МОУ «СОШ № 26» Задачи урока: 1. Расширить знания старшеклассников о химическом составе внутренней среды; строении и значении в жизни клетки различных неорганических соединений (на примере воды и минеральных солей). 2. Научить школьников выявлять связь между составом, строением молекулы, химического соединения и его функциями в клетке. 3. Убедить учащихся в том, что для понимания сущности протекающих в клетке процессов необходимы знания из разных областей естественных наук (биологии, химии, физики). Оборудование: презентация. Ход урока: Орг. Момент. Изучение нового материала. – Одним из основных общих признаков живых организмов является единство их элементарного химического состава. Независимо от того, к какому царству, типу или классу принадлежит то или иное живое существо, в состав его тела входят одни и те же, так называемые универсальные химические элементы. Сходство в химическом составе разных клеток свидетельствует о единстве их происхождения. Но количественное содержание тех или иных элементов в живых организмах и в окружающей их неживой среде существенно отличается. – Что такое химический элемент? (Химический элемент – это определенные вид атомов с одинаковым зарядом ядра.) Какие химические элементы преобладают в земной коре? (Кислород, кремний, алюминий, железо, магний, натрий, кальций – эти элементы составляют ≈ 98% массы земной коры) (презентация, 2 слайд) 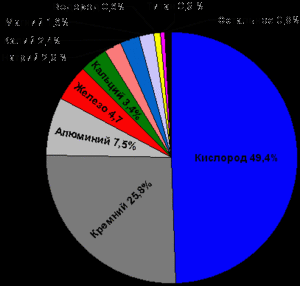 А какие химические элементы преобладают в живых организмах? (слайд 3) 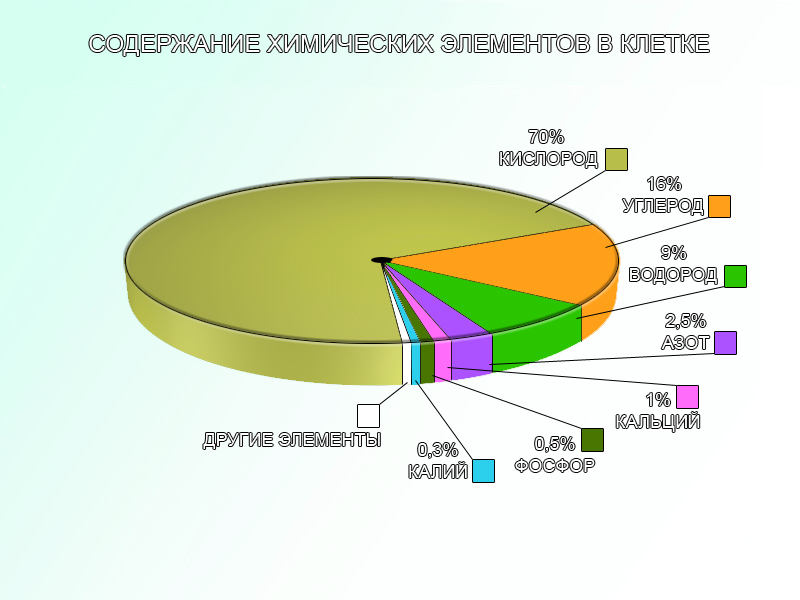 В клетках живых организмов встречается 90 различных химических элементов, из них 25 обнаружены практически во всех клетках. Эти химические элементы необходимы для их жизнедеятельности. Остальные элементы, вероятно, попадают в организм с водой, пищей, воздухом и не участвуют в жизнедеятельности. Задача: (слайд 4) Подсчитайте, сколько в человеке массой 85 кг будет составлять каждый элемент. ( Ответ: (слайд 5) кислород – 59,5 кг; углерод – 13,6 кг; водород – 7,65 кг; азот – 2, 125кг; кальций – 0, 85 кг; фосфор – 0,425кг; калий – 0,255 кг.) Мы с вами выяснили, какова масса биогенов в организме человека определенной массы. Давайте посмотрим какие еще элементы есть в живых организмах. По количественному содержанию в живых системах все химические элементы подразделяются на четыре группы: макроэлементы, мезоэлементы, микроэлементы, ультрамикроэлементы. (слайд 6)  Ультрамикроэлементы – бор, бром, серебро, золото, селен, мышьяк и др. Эти элементы составляют менее 0,000001%. Функции ультрамикроэлементов еще полностью не изучены, имеются лишь отдельные сведения о них: например, выяснено, что недостаток селена приводит к развитию раковых заболеваний. Обратимся к таблице и посмотрим роль в организме некоторых элементов-биогенов. (слайд 7)
Учитель обращает внимание учащихся на то, что именно макроэлементы – кислород, углерод, водород и азот – обеспечивает большинство функций в организме, и задает вопрос: – Почему данные элементы-биогены подходят для выполнения биологических функций? 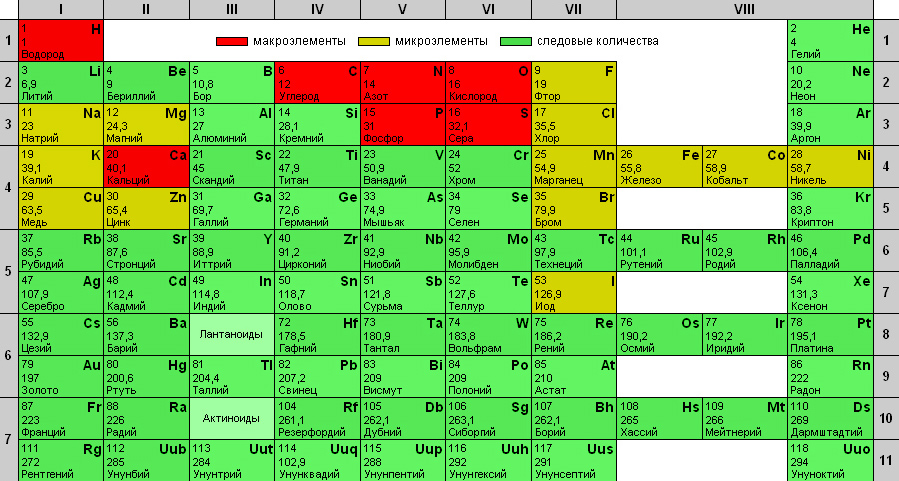 Учащиеся из курса химии вспоминают о строении атомов биогенов, их расположении в первых периодах периодической системы Д.И.Менделеева, их общих свойствах – способности к образованию ковалентных связей посредством спаривания электронов с отдачей или присоединением при этом от одного до шести электронов. Кроме того, органеллы могут легко реагировать друг с другом, образуя при этом разнообразные химические соединения. Эти элементы имеют малую атомную массу (относительно малый радиус), то есть они сочетают легкость с прочностью ковалентных связей между ними. (слайд 8) Ковалентно связанные атомы углерода образуют «каркас» органических молекул, на котором как бы «крепятся» разнообразные функциональные группы, содержащие водород, кислород, серу, азот и другие элементы. Отсюда можно сделать вывод, что свойства органогенов так разнообразны, что названных элементов достаточно для образования множества органических молекул. Следовательно, атомы, из которых состоят вещества клетки и неживой природы, идентичны. Это указывает на тесную связь и единство живой и неживой природы. Содержание тех или иных элементов в организме определяется не только особенностями данного организма, но также составом среды, в которой он обитает, и той пищей, которую он использует. Геологическая история нашей планеты, особенности почвообразовательных процессов привели к тому, что на поверхности Земли сформировались области, которые отличаются друг от друга по содержанию химических элементов. Резкий недостаток или, наоборот, избыток какого-либо химического элемента вызывает в пределах таких зон возникновение биогеохимических эндемий – заболеваний растений, животных и человека.  Во многих районах нашей страны – на Урале и Алтае, в Приморье и в Ростовской области количество йода в почве и воде значительно снижено. Если человек не получает с пищей нужного количества йода, у него снижается синтез тироксина. Щитовидная железа, пытаясь компенсировать нехватку гормона, разрастается, что приводит к образованию так называемого эндемического зоба. Особенно тяжелые последствия от недостатка йода возникает у детей. Сниженное количество тироксина приводит к резкому отставанию в умственном и физическом развитии. Чтобы предотвратить заболевания щитовидной железы, врачи рекомендуют подсаливать пищу специальной солью, обогащенной иодидом калия, употреблять рыбные блюда и морскую капусту. Одни и те же химические элементы входят в состав как неорганических веществ (воды и минеральных солей), характерных и для живых организмов и существующих в неживой природе, так и органических веществ – углеводов, липидов, белков, нуклеиновых кислот, витаминов и др., характерных только для живых организмов. 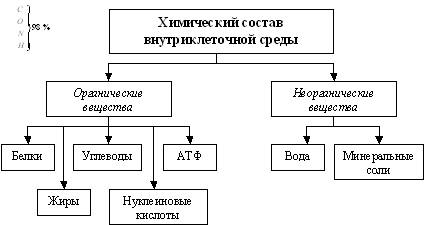 Рассмотрим самое распространенное в живых организмах неорганическое соединение – воду, её роль в клетке. Вода абсолютно необходима для всех известных форм жизни – не случайно человеческое тело на 60–70 % состоит из воды. Кроме того, она является средой обитания для многих организмов. Содержание воды в организме колеблется: В слюне, желудочном соке, грудном молоке содержится 90 – 99%. В клетках развивающего зародыша её более 90%. В крови – около 83%. Клетки взрослого организма – 80%. В костях всего лишь 15 – 20%. Время обновления количества воды, равного весу тела, колеблется в зависимости от окружающей среды, к которой адаптирован организм; для амебы оно составляет 7 дней; для человека 4 недели; для верблюда 3 месяца; для черепахи 1 год; для кактуса 29 лет.
Вода играет очень важную роль в жизни любого живого организма. Следует помнить основные свойства и функции воды. Давайте вспомним физические свойства воды. Вода – это бесцветная прозрачная жидкость, без цвета, запаха и вкуса, максимальная плотность — при 4 °С, высокая теплоемкость, практически не сжимается; чистая вода плохо проводит тепло и электричество, замерзает при 0 °С, кипит при 100 °С, обладает высокой испаряемостью за счет слабых водородных связей, текучесть. Какие химические элементы входят в состав молекулы воды? Напишите молекулярную формулу, структурную, электронную. 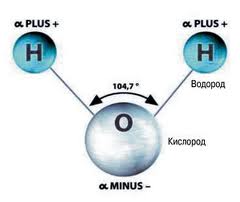 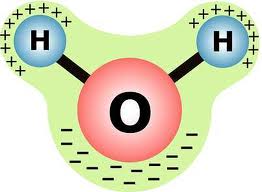 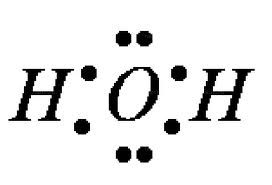 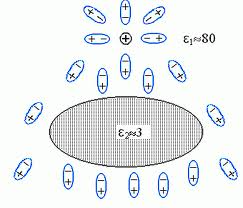 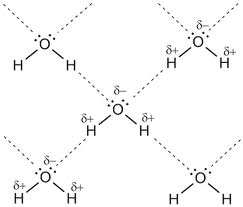 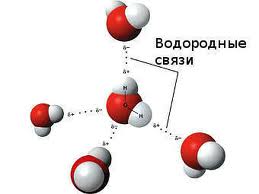 Какая химическая связь в молекуле воды? (полярная, неполярная?) Чему равен угол между атомами водорода и кислорода? (104,5ᵒ) Диполь. (Атом кислорода сильно электроотрицательный по отношению к атому водорода, что обеспечивает полярность ковалентной связи; при этом кислород оттягивает на себя электроны общей электронной пары. Следовательно кислород отрицательно заряжен, а водород – положительно. Между атомами О и Н соседних молекул возникает водородная связь). Каковы химические свойства воды? (хороший растворитель, реагируют с металлами, оксидами, гидролиз солей и органических соединений; по отношению к способности растворяться в воде различают: гидрофильные вещества — хорошо растворимые, гидрофобные вещества — практически нерастворимые в воде.) Свойства воды в живом организме: Текучесть; Вода – хороший растворитель; Высокая теплопроводность и теплоемкость; Высокая испаряемость за счет слабых водородных связей; Гидролиз – разложение под действием воды; Высокая сила поверхностного натяжения воды. Функции воды в живом организме: является средой обитания для многих организмов, является основой внутренней и внутриклеточной среды; вода обеспечивает тургор клетки, гидроскелет; обеспечивает поддержание пространственной структуры, транспорт крови, межклеточного вещества, цитоплазмы, лимфы; служит растворителем и средой для диффузии; пищеварение, многие химические реакции в организме идут с растворенными в воде веществами; регуляция тепла в организме; способствует охлаждению организма, гидратирует полярные молекулы, участвует в реакциях фотосинтеза и гидролиза, способствует миграциям и распространению семян, плодов, личиночных стадий, является средой, в которой происходит оплодотворение, у растений обеспечивает транспирацию и прорастание семян, способствует равномерному распределению тепла в организме и мн. др. Другие неорганические соединения клетки Другие неорганические соединения представлены в основном солями, которые могут содержаться или в растворенном виде (диссоциированными на катионы и анионы), или твердом. Важное значение для жизнедеятельности клетки имеют катионы K+, Na+, Ca2+, Mg2+ и анионы HPO42—, Cl—, HCO3—, Многие ионы неравномерно распределены между клеткой и окружающей средой, так, например, в цитоплазме концентрация ионов калия в 20 – 30 раз выше, чем с наружи, а концентрация ионов внутри клетки, наоборот, в 10 раз ниже. Именно благодаря существованию подобных градиентов концентраций осуществляются многие важные процессы жизнедеятельности, такие как возбуждение нервных клеток, сокращение мышечных волокон. После гибели клетки концентрация катионов снаружи и внутри быстро выравнивается. Анионы слабых кислот (НСО3-, НРО42-) обеспечивают буферные свойства клетки. Буферность — способность поддерживать рН на определенном уровне (рН — десятичный логарифм величины, обратной концентрации водородных ионов). Величина рН, равная 7,0, соответствует нейтральному, ниже 7,0 — кислому, выше 7,0 — щелочному раствору. Для клеток и тканей характерна слабощелочная среда. За поддержание этой слабощелочной реакции отвечают фосфатная (1) и бикарбонатная (2) буферные системы: Низкий рН ⇔ Высокий рН (1) НРО42— + Н+ Н2РО4— Гидрофосфат Дигидрофосфат Низкий рН ⇔ Высокий рН (2) НCО3— + Н+ Н2CО3 Гидрокарбонат Угольная кислота В твердом нерастворенном состоянии находятся в костной ткани, в раковинах моллюсков карбонаты и фосфаты кальция и магния, в зубной эмали — фторид кальция и т.д. Закрепление: По предложенной схеме назовите слово: А) __ __ Л __ __ __ __ С __ __ Характерная черта молекулы воды (полярность); Б) __ О __ __ __ __ __ __ Н __ __ Вид химической связи внутри молекулы воды (ковалентная); В) __ __ Д __ О __ И __ __ __ __ Е Вещества, хорошо растворимые в воде (гидрофильные); Г) __ А __ __ __ __ Результат диссоциации солей в клетке (катион). Домашнее задание: п.6–8 читать и отвечать на вопросы |
