алхимия. Научное шоу. Исследовательская работа От алхимии к экспериментальной химии или химические опыты в домашних условиях
 Скачать 2 Mb. Скачать 2 Mb.
|
|
КРАЕВАЯ ИТОГОВАЯ НАУЧНО-ПРАКТИЧЕСКАЯ КОНФЕРЕНЦИЯ ДЛЯ ОДАРЕННЫХ ШКОЛЬНИКОВ И МОЛОДЕЖИ «БУДУЩЕЕ АТАЯ» Исследовательская работа От алхимии к экспериментальной химии или химические опыты в домашних условиях Автор: Бергер Арсений Николаевич Ученик 6 Б класса МБОУ «СОШ №13» Научный руководитель: Бергер Елена Иосифовна, учитель химии Славгород, 2022 Оглавление Введение 4 I.Теоретическая часть 4 Алхимия – наука прошлого. 4 Происхождение названия «Алхимия» 5 Периоды алхимии 6 Александрийский период 6 Арабский период 7 Европейский период 8 Методы и средства обучения химии 11 Техника безопасности в лаборатории 11 Что нам понадобится для проведения опытов 13 Научное шоу 14 II. Практическая часть 14 Описание, результат и научное объяснение опытов 15 Опыт № 1. Магическое тушение свечей содержимым пустого стакана 15 Опыт № 2. Как надуть шарик содой и уксусом. 15 Опыт № 3. Резиновое яйцо. 16 Опыт № 4. Обесцвечивание раствора марганцовки 16 Опыт № 5. Зубная паста для слона 17 Опыт № 6. Светящийся помидор. 18 Опыт № 7. Секретное послание 18 Опыт №8. Светофор. 19 Опыт № 9.Фараонова змея из соды и сахара 20 Заключение 20 Выводы 20 Список литературы 22 1.Химические опыты для детей. [Электронный ресурс]: Занимательная химия. - Режим доступа: http://www.alto-lab.ru/himicheskie-opyty- Загл. с экрана. 22 2.Зав. каф. химии и геоэкологии С.В. Бортников. Научно-познавательные шоу для детей. [Электронный ресурс]: Бизнес портал. Фабрика манимейкеров. - Режим доступа: http://moneymakerfactory.ru/biznes-idei/nauchno-poznavatelnyie_shou_dlya_detey/ - Загл. с экрана. 22 3.В. А. Крицман, В. В. Станцо Энциклопедический словарь юного химика. 2-е изд., испр. М.: Педагогика, 1990г. 22 4.История химии. [Электронный ресурс]: Википедия — свободная энциклопедия. – Режим доступа: https://ru.wikipedia.org/wiki/ История_химии. 22 ВведениеХимия - удивительная наука, полная разнообразных чудес. Она интересна как сама наша жизнь, ведь всё что происходит с нами можно рассматривать с точки зрения химии. Нужно узнать химию, чтобы объяснить многие явления в нашей жизни. Ведь вещества, окружающие нас в быту, имеют интересную историю и необычные свойства. А желание познать неизвестное очень велико и есть у каждого человека. Сделать скучные и непонятные химические формулы и уравнения очень интересными возможно, стоит лишь немного изменить точку своего зрения. Поэтому у нашего проекта есть еще одна особенность – это чудеса. Может, и действительно, чудо бывает только в сказках и в нашем воображении, может его и вовсе не бывает… Но знания могут сделать все невозможное возможным и реальным. И многие чудеса можно легко объяснить, опираясь лишь на химические знания. Итак, мы готовы постичь тайну всех земных и неземных превращений, готовы окунуться с головой в бушующее море интересных фактов нашей повседневной жизни! Актуальность Данный проект не только существенно расширяет кругозор, но и раскрывает материальные основы окружающего мира, дает химическую картину природы. Знакомство с характеристикой веществ и химических процессов, которые можно наблюдать в обычной жизни, в домашних условиях позволяет окунуться в загадочный мир научных экспериментов и совершить увлекательную экскурсию по химии. Гипотеза Химия доступна всем и каждому, кто стремится познать эту интересную науку, «чудеса» можно не только увидеть своими глазами, но и сделать своими руками. Объект исследования: химические домашние препараты. Предмет исследования: химические опыты. Цель В интересной форме рассказать о тех химических веществах и процессах, с которыми мы сталкиваемся в нашем доме и доказать, что «чудеса» можно сделать своими руками. Задачи: Проанализировать информацию о химических веществах в Интернете и научно-популярной литературе. Выбрать опыты приемлемые для проведения в домашних условиях. Провести опыты и осуществить "чудеса" своими руками. Объяснить происходящие процессы, обработать результаты и сделать выводы. Теоретическая частьАлхимия – наука прошлого.Традиции экспериментальной химии складывались веками. Еще тогда, когда химия не была точной наукой, в древние времена и в эпоху средневековья, ученые и ремесленники иногда случайно, а иногда и целенаправленно открывали способы получения и очистки многих веществ, находивших применение в хозяйственной деятельности: металлов, кислот, щелочей, красителей и т. д. Так возникла алхимия. Алхимия (лат. alchimia, alchymia) — это старинная химия, представляющая собой смешение экспериментальной химии в современном смысле этого слова и общих, наглядно интуитивных, частью религиозных спекуляций о природе и человеке. Алхимики во всех культурах ставили перед собой цель найти способы осуществления изменений внутри одушевленных и неодушевленных предметов. С помощью этих изменений предмет, по мнению алхимиков, сможет перейти на новый уровень или вовсе переродиться. Алхимия подразделялась на 2 вида: внутренняя и внешняя. Поиском способов получения золота из других металлов, а также созданием пилюль бессмертия занималась внешняя алхимия. В свою очередь, поиском абсолютного здоровья или вовсе бессмертия, при помощи разных упражнений, занималась внутренняя алхимия. Во всех алхимических традициях важную роль играют ртуть и ее сульфид, сера, 6 известных на тот момент металлов (свинец, железо, медь, олово, серебро, золото), соединения мышьяка, сурьма, селитры, щелочи. Алхимия включает несколько философских традиций, охватывающих четыре тысячелетия и три континента. Общая склонность этих традиций к загадочному и символическому языку затрудняет прослеживание их взаимного влияния и «генетических» отношений. Можно выделить, по крайней мере, три основных направления, которые кажутся в значительной степени независимыми на более ранних этапах: китайская алхимия, сосредоточенная в Китае и его зоне культурного влияния; индийская алхимия, сосредоточенная на индийском субконтиненте; и западная алхимия, которая произошла вокруг Средиземноморья и центр которой сместился в течение тысячелетий от греко-римского Египта к исламскому миру и, наконец, к средневековой Европе. Китайская алхимия была тесно связана с даосизмом и индийская алхимия с дхармическими верованиями, в то время как западная алхимия разработала свою собственную философскую систему, которая была в значительной степени независима, но находилась под влиянием различных западных религий. Остается открытым вопрос, имеют ли эти три нити общее происхождение и в какой степени они влияют друг на друга. Происхождение названия «Алхимия»Алхимия считалась тайной деятельностью жрецов в Египте. Из Египта она проникла в Европу, а оттуда в Азию. Как и сама наука, слово алхимия формировалось по кусочкам. В Египте она называлась "Кем" (Khem), что означало плодородную почву возле реки Нил. После того, как Египет был завоёван Александром Македонским в 332 году до н. э., образовалось слово "Кемия" (Khemia) — так на древнегреческом языке назывался Египет. Впервые термин «алхимия» встречается в рукописи Юлия Фирмика, астролога 4 века. Другое толкование слова алхимия (позднелатинское alchemia, alchimia, alchymia) восходит через арабское к греческому chemeia от cheo -- лью, отливаю, что указывает на связь алхимии с искусством плавки и литья металлов. Периоды алхимииПервые сведения о химических превращениях люди получили, занимаясь различными ремеслами, когда красили ткани, выплавляли металл, изготавливали стекло. Тогда появились определённые приёмы и рецепты, но химия ещё не была наукой. Уже тогда химия была нужна человечеству в основном для того, чтобы получать от природы все необходимые для жизнедеятельности человека материалы – металлы, керамику, известь, цемент, стекло, красители, лекарства, драгоценные металлы. Основной задачей было получение веществ с необходимыми свойствами. Можно выделить основные периоды наивысшего развития алхимии: александрийский (греко-египетский); арабский; европейский. Александрийский периодРодина алхимии, как и многих наук, Египет, где время она считалась божественной наукой, ее секреты тщательно оберегались жрецами. Несмотря на это, некоторые сведения просачивались за пределы страны и доходили до Европы через Византию. В то время цель алхимических исследований – нахождение средства для превращения неблагородных металлов в благородные, как результат наблюдений над приготовлением искусственных драгоценных камней и эмалей. Но эта мысль не подкреплялась никакой научной теорией или гипотезой, которая оправдывала бы ее существование, и потому эта мысль не могла служить стимулом для дальнейших исследований в этом вопросе. После завоевания Александром Македонским Египта, основания новой столицы и Александрийской академии в 332 г до н. э. в Египет проникли идеи греческих философов о природе вещей (натурфилософию). Влияние этих идей тотчас сказалось в появлении теории состава металлов, основные черты которой мы находим уже у писателей I и II века нашей эры: Диоскорида и Зосимы Панаполитанина. Познания египтян в прикладной химии поразили греков, и, перенимая их конкретные знания, греки восприняли многое и из мистики – отождествили египетского бога Осириса с греческим богом Гермесом. Простые люди страшились тех, кто занимался алхимией и это заставляло ученых писать свои труды туманными символами, что усиливало таинственность. Эта неясность языка приводила к торможению прогресса, так как работавший в этой области пребывал в неведении того, чем же занимаются его коллеги. А также, любой мошенник мог выдать себя за серьезного ученого. Именно в Александрийской академии произошло соединение теории античной натурфилософии и практических знаний о веществах, их свойствах и превращениях и из этого соединения и родилась новая наука – химия. Эта теория в общих чертах состояла в следующем: все металлы имеют два общих начала, из которых они состоят, это меркурий и сера. Именем меркурия и серы алхимики того времени называли отвлеченные понятия металличности и изменяемости. При внимательном наблюдении все металлы оказались обладающими многими общими свойствами. Так, все они имеют особый блеск и цвет, все более или менее ковки; будучи расплавлены, превращаются в жидкости и в этом виде чрезвычайно похожи друг на друга и в особенности на ртуть, ставшую уже известной в то время. Будучи выставлены на воздух или подвергнуты нагреванию, они, за исключением золота, изменяются и превращаются в землистые вещества – ржавчины или, по-нынешнему, окиси. Эти общие для всех металлов свойства были соединены, за исключением последнего, в одно понятие – металличности, и ртуть, по своей идеальной ковкости, по сильному блеску, естественно, стала считаться типом всех металлов, и ее алхимическое имя «меркурий» выразило эту типичность, соединив в себе все общие свойства металлов, за исключением изменяемости на воздухе и при нагревании. Эта последняя способность металлов дала повод к установлению другого общего для всех начала — изменяемости, и сера, сгорающая без остатка, дала свое имя для выражения названного свойства. Сообразно этому все металлы считались результатом соединения двух начал: металличности и изменяемости, меркурия и серы, в различном относительном количестве, в различной степени чистоты и в различной силе соединения друг с другом. Вдумываясь глубже в эту теорию, легко понять, что неизбежным выводом из нее являлась мысль о возможности превращения одних металлов в другие и всех их в золото, самый совершенный из них. Арабский периодВ 758 г. халифат Абассидов принимал широкие меры для распространения просвещения в своем государстве. Во многих городах были основаны высшие школы, библиотеки, астрономические обсерватории. В научном центре Багдаде сосредоточились самые известные арабские врачи и ученые. Слово «химия» преобразовалось в арабском языке в «алхими». Влияние ислама в арабских университетах было сравнительно слабым; кроме того, изучение трудов античных авторов не противоречило трём обязательным исламским догматам – вере в Аллаха, в его пророков и загробный суд. Благодаря этому на Арабском Востоке могли свободно развиваться научные представления, в основе которых лежало научное наследие античности, в том числе и александрийская химия. «Их химики были наблюдателями и искусными техниками; они увеличили объем науки и избавили её от посторонних элементов: Магии, Кабаллы и Мистики. Арабы поставили Алхимию, так сказать, на ноги». Абу Муса Джабир ибн Хайан, в европейской литературе известный под именем Гебер придавал первостепенное значение практике в химии. Он очень подробно описывает все операции – кристаллизацию, возгонку, растворение, перегонку, обжигание и т.д. В его сочинениях точные и подробные предписания добычи и приготовления металлов и их очистки, окраски тканей, изготовления лаков. Он первый получил азотную кислоту. У него впервые говорится об азотносеребрянной соли, о хлорной ртути, о производстве нашатыря. Джабир изучал возможность трансмутации металлов, и эти его исследования оказали сильнейшее влияние на последующие поколения алхимиков. Джабир полагал, что ртуть является особым металлом, так как благодаря своей жидкой форме она содержит очень мало примесей. Столь же необычными свойствами обладает и сера: она способна воспламеняться. Джабир считал, что все остальные семь металлов образуются из смеси ртути и серы, «созревающей» в недрах земли. Труднее всего образуется золото — наиболее совершенный металл. Поэтому, чтобы получить золото, необходимо найти вещество, ускоряющее «созревание» золота. В старинных преданиях говорилось, что это вещество представляет собой сухой порошок. Греки называли его xerion, или «сухой», арабы изменили его на al-iksir, и в конце концов в европейских языках появилось слово эликсир. В Европе это удивительное вещество получило название философского камня. Эликсир должен был обладать и другими чудесными свойствами: излечивать от всех болезней и, самое главное, давать бессмертие. Другой арабский алхимик Ар-Рази (865—925), ставший известным в Европе под именем Разес, занимался медициной и алхимией. Он завоевал почти такую же известность, как и Джабир. Ар-Рази описал методику приготовления гипса и способа наложения гипсовой повязки для фиксации сломанной кости. Он изучил и описал металлическую сурьму. Джабир рассматривал серу как принцип горючести, ртуть как принцип металличности, Ар-Рази добавил к этим двум принципам третий — принцип твердости, или соль. Летучая ртуть и воспламеняющаяся сера образовывали твердые вещества только в присутствии третьего компонента — соли. Ар-Рази интересовался медициной больше, чем Джабир, но самым знаменитым врачом был бухарец Ибн-Сина (ок. 980—1037), гораздо более известный под латинизированным именем Авиценна. Его сочинения служили важнейшими руководствами для врачей в течение многих веков. Авиценна единственный из алхимиков не верил в возможность получения золота из других металлов. Главная же заслуга алхимиков арабского периода состоит в том, что они, сочетая наблюдение, опыт и практические задачи в исследованиях, значительно приблизили к практике достижения «тайной науки» эллинистического Египта и тем самым на несколько столетий рассеяли туман, окутывавший химические знания, оставшиеся в наследие от представителей «тайной науки» Александрийской академии. Вместе с тем алхимия арабского периода исторически оказалась промежуточным звеном между алхимией древнего мира и позднейшей западноевропейской химией. Начиная с XI в. арабские алхимические сочинения в латинских переводах получили распространение в различных европейских странах и стали первыми пособиями для изучения химии европейцами. Таким образом, развитие химии и алхимии в Европе началось благодаря приобщению европейцев к арабской культуре. Европейский периодПоявление алхимии на Западе стало возможным прежде всего благодаря крестовым -походам. Тогда европейцы позаимствовали у арабов многие научно-практические знания и среди них алхимию, которая получила быстрое распространение и способствовала расширению знаний о препаратах, необходимых в медицине. Европейская алхимия находилась в этот период под покровительством астрологии и поэтому приобрела характер тайной науки. Политические условия, сложившиеся в средневековой Европе, и острое соперничество многочисленных королевских дворов благоприятствовали развитию алхимии. В период с XI до XVI века, то есть в течение пяти веков, западная алхимия дала много крупных мыслителей, оставивших глубокий след в развитии химии. Начиная с 1200 года европейские ученые могли близко познакомиться с наследием алхимиков прошлого и дальше развивать их исследования. Имя самого видного из средневековых алхимиков осталось неизвестным, но, вероятно, он был испанцем и жил в XIV веке. Его заслуга перед химией состояла в том, что он первый описал серную кислоту - одно из самых важных соединений современной химии (после воды, воздуха, угля и нефти). Он также описал, как образуется азотная кислота. Ее открытие также связано с попытками получить золото. Было замечено важное свойство царской водки (получаемой при взаимодействии азотной кислоты с раствором нашатыря) воздействовать на золото, считавшееся до тех пор неподдающимся изменению. Открытие сильных минеральных кислот было самым важным достижением химии после успешного получения железа из ртути примерно за 3000 лет до того. Используя сильные минеральные кислоты, европейские химики смогли осуществить многие новые реакции и, в частности, сумели растворить такие вещества, которые древние греки и арабы считали нерастворимыми. Минеральные кислоты дали человечеству гораздо больше, чем могло бы дать золото, если бы его научились получать с помощью трансмутации. Если бы золото перестало быть редким металлом, оно мгновенно бы обесценилось. Ценность же минеральных кислот тем выше, чем они дешевле и доступнее. В XIV веке западные алхимики, разочаровавшись в попытках получить философский камень, вернулись к теории, которая рассматривала ртуть и серу как основные составные части металлов, но при этом они ввели третью составную часть -«соль». Под солью здесь подразумевалось соляное основание металлов, которое должно было дополнить две другие составные части и придать ртути свойство затвердевать и противостоять огню. Таким образом были изучены соли, число которых значительно возросло. Их различали по происхождению: хлористый натрий называли морской солью, селитру - каменной солью и т.д. Западные алхимики не внесли значительного усовершенствования в металлургию, они лишь применили то, что было известно арабским алхимикам, к условиям европейских стран и, главным образом, к переработке руд металлов. Из достижений европейских алхимиков особого упоминания заслуживает изучение продуктов брожения (вино, уксус), поскольку именно в западной алхимии берет начало изготовление чистого спирта путем перегонки крепких вин и водки. Перегонные аппараты применялись в Италии с XI века и быстро нашли распространение в других европейских странах. Заслугой западных алхимиков является также значительное расширение знаний в области практической и прикладной химии. В этот период были созданы аппараты, применяемые при различных операциях, связанных с нагреванием на прямом огне, на песчаной бане, на водяной бане, применяемые при перегонке, выпаривании, фильтровании, кристаллизации, настаивании и возгонке. Василий Валентин (XV век)открыл сурьму и создал соляную кислоту, описал в своих трудах азотную и серную кислоты, царскую водку, нашатырь, сулему и другие соли ртути, некоторые соединения цинка, олова, свинца, кобальта. Многие принципы работы Василия позаимствовал позже и последствии применял Парацельс. Парацельс известен абсолютному большинству читателей как врач и предтеча фармакологии, но он также занимался медицинской алхимией. Этот ученый был новатором. Наша медицина многим обязана Парацельсу. Именно он предсказал современную гомеопатию, начал рассматривать процессы, протекающие в организме человека, с точки зрения химии и использовать минералы в изготовлении лекарств. Таким образом были подготовлены соответствующие условия для исследований химических соединений, их применения в медицине и практической науке. Поиск золота стал делом многих мошенников, хотя некоторые великие ученые даже в просвещенном XVII веке (Бойль, Ньютон) не смогли устоять от соблазна попытаться получить золото посредством трансмутации. И вновь изучение алхимии было запрещено. Запрещение преследовало две цели: нельзя было допустить обесценивания золота и необходимо было бороться против мошенничества. Изучив теоретические аспекты проекта, решив все задачи, мы пришли к выводу, что алхимия – это самостоятельно развивавшееся направление науки, которое дало начало современной химии. Алхимией занимались многие ученые того времени. Сам факт преобладания теоретического интереса и полного отсутствия интереса к получению золота выводит ученых за пределы алхимии как элемента средневековой культурной традиции, дает толчок к развитию экспериментальной химии. История экспериментальной химии. Наукой, в современном смысле этого слова, химия начала становиться только в XIX в., когда был открыт закон кратных отношений и разрабатывалось атомно-молекулярное учение. С этого времени химический эксперимент стал включать в себя не только изучение превращений веществ и способов их выделения, но и измерения различных количественных характеристик. Современный химический эксперимент включает множество разнообразных измерений. Изменились и оборудование для постановки опытов, и химическая посуда. В современной лаборатории не встретишь самодельных реторт — на смену им пришло стандартное стеклянное оборудование, производимое промышленностью и приспособленное специально для выполнения той или иной химической процедуры. Методы изучения вещества сделались не только более универсальными, но и гораздо более разнообразными. Все большую роль в работе химика играют физические и физико-химические методы исследования, предназначенные для выделения и очистки соединений, а также для установления их состава и строения. Стали стандартными и приемы работы, которые в наше время уже не приходится каждому химику изобретать заново. Описание наилучших из них, проверенных многолетним опытом, можно найти в учебниках и руководствах. Методы и средства обучения химииХимия повсюду. И в предметах, которые нас окружают (многие из которых изготовлены из материалов, получаемых на химических заводах и фабриках), и в производимых в повседневной жизни действиях (например, приготовление пищи или мытье волос), и, наконец, внутри самих людей. Важнейший метод и средство обучения химии – это химический эксперимент. Подавляющее большинство сведений о веществах, их свойствах и химических превращениях получено с помощью химических и физико-химических экспериментов. Поэтому химический эксперимент следует считать основным методом, применяемым химиками. Самое главное: работая в химической лаборатории, всегда необходимо помнить об осторожности, не торопиться, знать и соблюдать основные правила техники безопасности. Техника безопасности в лабораторииТехника безопасности в лаборатории - это комплекс обязательных правил, которые нужно выполнять при обращении с химическими веществами и при любых работах в химических лабораториях. Множество веществ, применяемых в химической лаборатории, в большей или меньшей степени ядовиты, некоторые из них способны вызывать ожоги при попадании на кожу и в глаза. Практически все органические и многие неорганические вещества огнеопасны. Есть химические вещества, которые приятно пахнут и не вызывают ожогов, но через некоторое время после вдыхания таких паров у человека появляется аллергия или заболевание внутренних органов. Однако без химии обойтись нельзя: она составляет одну из основ современного производства. И с самым ядовитым веществом можно безопасно работать, если хорошо знать его свойства. В химической лаборатории особенно осторожно следует работать с веществами, свойства которых незнакомы. Ничего нельзя пробовать на вкус, нюхать реагенты нужно с большой осторожностью. Начинать работу с маленькими порциями вещества. Прежде чем начать опыт, продумать до мелочей, что и как делать, какие могут быть опасности и как их избежать или нейтрализовать. Нельзя курить в пожароопасных и взрывоопасных местах. Не следует пить из лабораторной посуды, приносить в лабораторию пищевые продукты. Нужно пользоваться специальными рукавицами, защитной маской или противогазом, когда это необходимо. Закончив опыты, тщательно вымыть руки. При всех биологических исследованиях и экспериментах следует всегда соблюдать законы охраны окружающей среды и защиты биологических видов. Ответственное обращение с биологическим материалом, а также с приборами и химическими реактивами предупреждает несчастные случаи: При работе с щелочами и кислотами следует надевать защитные очки. При попадании химикалий в глаза или на кожу нужно незамедлительно промыть их большим количеством воды. Если это были кислоты, используйте 1%-ный гидрокарбоната натрия (питьевая сода), а если щелочи - 1%-ный раствор уксусной кислоты. После оказания первой помощи следует обратиться к врачу. Кислоту при разбавлении всегда добавляют в воду малыми порциями. Никогда не храните химические реактивы в бутылках или банках, обычно используемых для пищевых продуктов или напитков; химическая посуда всегда должна быть снабжена нестирающейся надписью, соответствующей ее содержанию. При обращении с горючими жидкостями следите за тем, чтобы вблизи не было открытого огня. Под рукой всегда должны быть песок и вода. Опыты с ядовитыми газами или едкими парами проводите только под тягой или на открытом воздухе. При нагревании жидкостей в пробирках отверстие пробирки должно быть направлено от себя и от человека, работающего рядом с вами. Отходы или продукты химических реакций ни в коем случае нельзя сливать в одну посуду. В ходе опыта не наклоняться близко во избежание повреждения глаз и кожи. Что нам понадобится для проведения опытовПри выполнении домашних опытов можно обойтись без громоздкого и дорогого лабораторного оборудования. Понадобятся лишь скромно оснащенное рабочее место и ограниченный набор химических реактивов. Многое из специального дорогостоящего оборудование, можно, заменить предметами домашнего обихода. Так же обстоит дело и с химическими реактивами. Вместо коллекционирования дорогостоящих экзотических реактивов и красителей и, разумеется, ядов начнем работать с небольшим, разумно подобранным набором наиболее употребительных реактивов, которые можно найти на собственной кухне или в аптеке. Всегда нужно иметь под рукой: Одни защитные очки (а если опыты проводят вместе с товарищами, то защитные очки для каждого). На приобретении очков ни в коем случае нельзя экономить. Темные очки для защиты от солнца не подойдут, потому что они не защищают глаз сбоку. Промывалка, всегда заполненная водой. С помощью промывалки можно, например, быстро удалить попавшие на кожу брызги кислоты. Небольшое количество перевязочных материалов Бутылки с 3%-ным уксусом и 3%-ным раствором питьевой соды (гидрокарбоната натрия). Если немного кислоты или щелочи прольется, то с помощью этих растворов их можно быстро нейтрализовать. Склянка с 5% -ным раствором сульфата меди. Эта соль служит быстродействующим рвотным средством при отравлении. Тряпки для вытирания стола, фильтровальная бумага. Научное шоуЛюдям, а особенно детям всегда было и будет интересно посмотреть, а также поучаствовать в научных экспериментах. Прозрачное превращается в цветное, твёрдое в жидкое, жидкое улетает белым туманом, оранжевый порошок превращается в действующий вулкан - настоящая магия на глазах восхищённых зрителей! Научные шоу – это познавательное и развлекательное мероприятие для детей, с проведением химических опытов и экспериментов. В процессе шоу можно производить эффектные, но безопасные взрывы; создавать молнии и вихри; вместе со зрителями превращать жидкости в полимеры и светящиеся «тянучки», замораживать предметы и многое другое. Организация научных развлекательных шоу формирует в детях тягу к познанию и занятиям наукой. Научные шоу можно проводить в стиле интерактивных уроков химии, веселых праздников, стилизованных вечеринок или познавательных экспериментов. Такие шоу начали проводиться не так давно, их новизна и оригинальность обеспечат успех мероприятия. Шоу может состоять из разных опытов и экспериментов, быть стилизованным под персонажей популярных книг и фильмов. Каждое отдельно взятое представление может быть не похожим на предыдущие, для того, чтобы дети каждый раз могли открывать для себя что-то новое. После просмотра шоу дети будут в восторге, они будут рассказывать о празднике всем друзьям и одноклассникам. Научные шоу и эксперименты помогают развивать в детях стремления к познанию и обучению. Мы решили провести научное химическое шоу в нашей школе в рамках проведения "Дней науки", чтобы участники смогли окунуться в загадочный мир научных экспериментов и совершить увлекательную экскурсию по химической лаборатории. Школьники с большим интересом наблюдали за опытами, чудесными превращениями и удивительными явлениями, а, в некоторых случаях, и сами в них участвовали. II. Практическая частьИ вот, мы подошли к самой удивительной части нашего исследования - проведению химических опытов. Их особенность в том, что каждый из них можно повторить дома. Так что мы постараемся в интересной форме рассказать о тех химических веществах и процессах, с которыми мы сталкиваемся чуть ли не каждый день и без которых уже и не представляем нашу жизнь. Здесь собраны самые замечательные домашние опыты, целью которых будет доказать, что и чудеса можно «сделать» своими руками. В химической лаборатории мы сталкиваемся с веществами, которые впоследствии смешиваем, нагреваем и окисляем… В общем, делаем так, чтобы произошла химическая реакция. А используем для этой цели жидкости, газы, порошки и прочие состояния различных веществ. Результат довольно предсказуем. Зная основные химические свойства веществ, можно предвидеть, что получится в результате реакции. Но в живой природе вещества в чистом виде встречаются не часто, а химические процессы идут постоянно. Это создает некоторые трудности в прогнозировании результатов. Поэтому в нашем эксперименте мы сначала сделаем, а потом будем думать, отчего же так получилось. Описание, результат и научное объяснение опытовОпыт № 1. Магическое тушение свечей содержимым пустого стаканаПеред постановкой эксперимента спросите у детей, как затушить пламя свечи. Они, конечно же, вам ответят, что свечку надо задуть. Спросите, верят ли они, что вы сможете загасить огонь пустым стаканом, произнеся волшебное заклинание? Цель: Поместив в стакан соду и уксус, полить полученным газом на зажженную свечу и погасить ее. Для проведения эксперимента понадобятся: уксус 3 чайные ложки; сода 2 чайные ложки; стаканы; свечи 3-4; спички. Постановка опыта. Насыпьте в стакан соды и залейте ее уксусом. Зажгите несколько свечей. Поднесите стакан с содой и уксусом к другому стакану, немного переклонив его, чтобы полученный в процессе химической реакции углекислый газ перетек в пустой стакан. Пронесите стакан с газом над свечами, как бы поливая им пламя. Результат и научное объяснение. При взаимодействии соды и уксуса выделяется углекислый газ, который, в отличие от кислорода, не поддерживает горение: CH3—COOH + Na+[HCO3]− → CH3—COO− Na+ + H2O + CO2 CO2 тяжелее воздуха, а потому не улетает вверх, а оседает вниз. Благодаря этому свойству мы имеем возможность собрать его в пустой стакан, а потом «вылить» на свечи, тем самым загасив их пламя. Опыт № 2. Как надуть шарик содой и уксусом.Что делать если нет насоса для надувания воздушных шариков, а нужно надуть много больших шаров в домашних условиях? Цель: наполнить воздушный шарик углекислым газом, который выделяется при добавлении соды в уксус (гашение соды). Для проведения эксперимента понадобятся: бутылка; воздушный шарик; пищевая сода; уксус. Постановка опыта. Насыпаем немного соды в шарик (не более 3-4 чайных ложек). Для удобства можно использовать воронку или обычную ложку. В бутылку заливаем небольшое количество уксуса и осторожно надеваем шарик на горлышко бутылки таким образом, чтобы сода не просыпалась в бутылку. После подготовительного процесса приподнимите шарик так, чтобы сода высыпалась в бутылку. Уксус начнет булькать и пенится, не стоит этого бояться, это выделяется углекислый газ, который в итоге и надует наш шарик. Несколько секунд и шарик надут, только придерживайте его, а то улетит! Оказывается вот так просто можно надуть шарик содой и уксусом! Результат и научное объяснение. Опыт основан на взаимодействие кислоты (уксус) и соли (сода). Происходит реакция нейтрализации: т.е выделяется углекислый газ и вода. CH3COOH+NaHCO3 → CH3COONa+H2O+CO2 Газ, выделяющийся в процессе реакции, постепенно заполняет все пространство и, не помещаясь в заданном объеме, начинает давить на стенки шарика. Резина растягивается, шарик надувается. Опыт № 3. Резиновое яйцо.Как всем известно, куриное яйцо имеет внешнюю тонкую оболочку (скорлупу), основным химическим компонентом которой является кальций. Проведём интересный химический опыт с яйцом в домашних условиях. Эксперимент нужно проводить заранее. Цель: рассмотреть, как скорлупа полностью растворится, если поместить куриное яйцо в уксус и продержать там около 3-х дней. Для проведения эксперимента понадобятся: стакан; уксус; сырое куриное яйцо. Постановка опыта. Наливаем в стакан уксус пищевой.Помещаем сырое куриное яйцо в стакан с уксусом. Оставляем яйцо в стакане на 3 дня. После этого можно показывать "резиновое яйцо" зрителям. Результат и научное объяснение. Если поместить куриное яйцо в уксус и продержать там около 3-х дней, то скорлупа полностью растворится. Скорлупа растворяется из-за того, что состоит она из кальция, который вступает в реакцию с уксусом. Яйцо, при этом, сохранит свою форму, благодаря наличию пленки между скорлупой и содержимым яйца. Если выключить свет и поднести к нему фонарик, то яйцо превращается в светящуюся капсулу. Кальций, находящийся в скорлупе яйца, прореагировал с уксусной кислотой, образовав раствор ацетата кальция, а белок и желток денатурировали (изменили форму белковых молекул) под действием кислой среды (денатурация белка происходит при температуре, когда яйцо, например, варится). C  3COOH + CaCO3 (CH3COO)2 Ca + CO2 + H2O 3COOH + CaCO3 (CH3COO)2 Ca + CO2 + H2OОпыт № 4. Обесцвечивание раствора марганцовкиКаждый может чистую прозрачную воду сделать цветной, добавив в нее какой-нибудь краски, а вот наоборот, сделать грязную воду прозрачной может не каждый. Цель: Показать на опыте реакцию нейтрализации перманганата калия. Для проведения эксперимента понадобятся: марганцовка (KMnO4) активированный уголь стакан с водой Постановка опыта. Сделать раствор перманганата калия. Положить в стакан с раствором таблетку активированного угля. Визуально, как результат, мы видим обесцвечивание окрашенного раствора! Результат и научное объяснение. Этот опыт является самым простым и наглядным способом показать явление сорбции. Как известно, активированный уголь имеет очень шероховатую и разрыхленную поверхность. Суть опыта в том, что если погрузить (закинуть) уголь в раствор, окрашенный каким то красителем, или же марганцовкой, он поглощает растворенное вещество на свою поверхность. Мы совершили показательную реакцию нейтрализации соли марганцевой кислоты. Опыт № 5. Зубная паста для слонаВы когда-нибудь видели «пенный вулкан», много - много густой пены? Нет? Тогда этот эксперимент для вас! Для проведения эксперимента понадобятся: 6% раствор перекиси водорода, иодид калия, жидкое мыло или средство для мытья посуды, 5 капель любого пищевого красителя, 2 ложки теплой воды, литровая пластиковая бутылка, воронка, тарелка, поднос. Постановка опыта. Внимание! 6% раствор перекиси водорода может отбелить кожу или даже вызвать ожог! Поэтому не пренебрегайте правилами техники безопасности и используйте перчатки. Зубная паста для слона оставляет пятна, поэтому будьте уверены, что испачканную поверхность можно будет отмыть. Не пробуйте на вкус получившуюся пену и тем более не глотайте. Важно. Использовать менее, чем 6% раствор перекиси водорода не нужно. Ничего не получится. Чем выше концентрация, тем лучше. Но чем выше концентрация, тем опаснее становится раствор перекись водорода. Возьмем поднос и стакан. . Нальем в стакан 50 мл 30%-ной перекиси водорода, добавим несколько капель средства для мытья посуды и 2 г пищевого красителя. Перемешаем полученный раствор. Прильем 50 мл концентрированного раствора йодида калия и наблюдаем «пенный вулкан». Результат и научное объяснение. Перекись водорода разлагается на воду и кислород. Иодид калия выступает в качестве катализатора и ускоряет эту реакцию. Выделяющийся кислород вспенивает средство для мытья посуды, образуя густую пену, а пищевой краситель придает ей цвет. Пена получается плотной и долго не оседает из-за низкого содержания воды 2H₂O₂ –> 2H₂O + O₂ Опыт № 6. Светящийся помидор.Попробуйте сделать очень простой, но в тоже время очень эффектный химический опыт «светящийся помидор». Полученный в результате эксперимента светящийся томат категорически нельзя употреблять в пищу. Цель: сделать светящийся помидор. Для проведения эксперимента понадобятся: помидор; шприц с иголкой; сера со спичек (1 коробок); «Белизна» 2-3 мл; 30% перекись водорода – 3-4 мл. Постановка опыта. Перекись водорода свободно продается в аптеках, важно чтобы она была не менее 30%. Если не найдете такого, то можно использовать крепкий раствор таблеток гидроперита. «Белизну» можно заменить на Гипохлорит натрия. Когда все готово, в небольшую емкость засыпаем серу со спичек и добавляем «Белизну». Оставляем на 20 минут этот раствор в покое, до момента пока не образуется 2 слоя. Набираем раствор в шприц и со всех сторон обкалываем нашего пациента, он же помидор. После инъекции аккуратно вводим в самый центр помидора перекись водорода, выключаем свет и наслаждаемся результатом! Результат и научное объяснение. В данном случае мы имеем дело с разновидностью люминесценции получившим название - хемилюминесценция - свечение, использующее энергию химических реакций, другими словами, хемилюминесценция это люминесценция (свечение) тел, вызванная химическим воздействием. Происходит реакция окисления фосфора пероксидом водорода. А помидор получается просто необычной емкостью для реагентов :) Согласитесь если бы реактивы смешивали просто в пробирке или стакане то все выглядело бы не столь эффектно. Опыт № 7. Секретное посланиеНевидимые чернила представляют собой раствор для письма на бумаге. Изначально надпись нельзя увидеть, но до тех пор пока к чернилам не будет применено какое-то химическое воздействие. Существует множество всевозможных рецептов невидимых чернил, однако большинство из них все-таки оставляют следы на бумаге, которые можно увидеть невооруженным взглядом. Сегодня же мы с вами приготовим настоящие шпионские невидимые чернила, которые невозможно заметить до проявления. Цель: написать секретное послание. Для проведения эксперимента понадобятся: лимон; бумага; аптечный йод; ватная палочка; стакан с водой; кисточка. Постановка опыта. Написать письмо лимонным соком или раствором лимонной кислоты. Чтобы его прочесть, растворить в воде несколько капель аптечного йода и слегка смочить текст. Результат и научное объяснение. Получилось написать послание невидимыми чернилами, которые под воздействиями паров воды и йода становятся видимыми. OH OH H  OOC – CH2 – C – CH2 – COOH + 2I2 HOOC – CH – C – CH – COOH + 2HI OOC – CH2 – C – CH2 – COOH + 2I2 HOOC – CH – C – CH – COOH + 2HICOOH I COOH I Опыт №8. Светофор.Еще один занимательный и очень красивый химический опыт под названием Светофор. Этот эксперимент можно смело отнести к лучшим химическим фокусам для детей. Главным действующим веществом в химическом опыте Светофор является краситель индигокармин. Это его простое название, настоящее звучит так: динатриевая соль индиго-5,5′-дисульфокислоты. Индигокармин применяют как пищевые красители в производстве напитков и выпечки, которым нужно придать синий цвет, он даже зарегистрирован как пищевая добавка Е132 или индиготин. В химии используется как реагент. Его способность служить индикатором мы используем проводя опыт Светофор. Для проведения эксперимента понадобятся: индигокармин, глюкоза, каустическая сода, горячая вода, 2 стеклянных сосуда,защитные перчатки Постановка опыта, результат и научное объяснение. Обратите внимание, что для этого опыта мы обязательно должны использовать перчатки. Во-первых, можно испачкать руки индигокармином, а во-вторых, каустическая сода (гидроксид натрия) очень сильная щелочь способная нанести химический ожог. Для начала в одном стеклянном сосуде растворим 4 таблетки глюкозы в небольшом количестве горячей воды. 4 таблетки это 2 грамма. Приливаем к раствору глюкозы раствор около 10 мг раствора каустической соды. Получили щелочной раствор глюкозы. Отставляем его пока в сторонку. Во втором сосуде растворяем некоторое количество индигокармина. Получается синий раствор. Теперь осторожно вливаем в синий раствор щелочной раствор глюкозы. Жидкость изменит цвет на зеленый. Это синий индигокармин окисляется кислородом воздуха, т.к. жидкость насыщается этим газом при переливании. Постепенно зелёный раствор будет становиться красным, а затем жёлтым. Действительно, как светофор! Если жёлтый раствор резко встряхнуть, то он вновь станет зелёным, т.к. жидкость насытит кислород. Опыт № 9.Фараонова змея из соды и сахараФараонова змея — это собирательное название химических реакций, результатом которых является многократное увеличение объема реактивов. Во время реакции результирующее вещество быстро увеличивается, при этом извиваясь как змея. А почему змея фараонова? Видимо тут существует отсылка на библейский сюжет, когда Моисей продемонстрировал фараону чудо, бросив свой посох на землю, превратившийся в змею. Безопасный опыт в домашних условиях нам помогут провести обычная сода и сахар! Для проведения эксперимента понадобятся: просеянный песок, 95% спирт, сахарная пудра, пищевая сода. Постановка опыта. Из песка насыпаем небольшую горку, пропитанную спиртом, на вершине этой горки делаем небольшое углубление. Затем смешиваем чайную ложку сахарной пудры и четверть ложки соды. Полученную смесь засыпаем в «кратер». Поджигаем спирт (это может занять некоторое время). Постепенно смесь начнет превращаться в черные шарики, а после того как весь спирт прогорит, смесь резко почернеет и из неё начнет выползать фараонова змея! Результат и научное объяснение. Во время горения спирта происходит реакция разложения соды и сахара. Сода разлагается на углекислый газ и водяной пар. Газы вспучивают массу, поэтому наша «змея» ползет и извивается. Тело змеи состоит из продуктов горения сахара. 2NaHCO3 = Na2CO3 + H2O + CO2, C2H5OH + 3O2 = 2CO2 + 3H2O Диоксид углерода CO2, выделяющийся при разложении гидрокарбоната натрия и горении этилового спирта, а также водяные пары вспучивают горящую массу, заставляя ее ползти, как змея. Чем дольше горит спирт, тем длиннее получается «змея». Она состоит из карбоната натрия Na2CO3, смешанного с мельчайшими частичками угля, образованного при горении сахара. ЗаключениеТаким образом, мы совершили различные химические реакции. Наша практическая работа является неоспоримым доказательством того, что химия – это интереснейшая из наук, а эксперименты являются ее неотъемлемой частью, помогающей интереснее получить новые знания. В ходе работы все задачи выполнены полностью. ВыводыХимия удивительна, в этом мы убедились точно. Нашей целью было доказать, что химию может понять каждый, кто хоть немного заинтересован ей. Показательность – один из главных методов пропаганды чего угодно. Именно на этом методе была основана наша работа. Эксперименты. Они были самой важной частью и работы алхимиков, и ученых XIX века, и в наше время. И мы поступили также. На наших глазах происходили самые разные реакции: мы увидели, как жидкости меняют свой цвет, потушили свечу содержимым пустого стакана, куриное яйцо превратили в резиновое. Неужели это нельзя назвать чудом? Но эти чудеса мы легко объяснили, опираясь лишь на химические знания. В заключение, хотелось бы сказать: верьте в чудеса, знайте, что весь наш мир состоит из них и все живое - уже великое чудо. В нашем проекте нам удалось познать малую часть того, что может совершить наука, но жизнь непременно еще много раз будет сталкивать нас с такими поистине волшебными явлениями химии. «Для меня химия — это волшебство, это приключение». Список литературыХимические опыты для детей. [Электронный ресурс]: Занимательная химия. - Режим доступа: http://www.alto-lab.ru/himicheskie-opyty- Загл. с экрана.Зав. каф. химии и геоэкологии С.В. Бортников. Научно-познавательные шоу для детей. [Электронный ресурс]: Бизнес портал. Фабрика манимейкеров. - Режим доступа: http://moneymakerfactory.ru/biznes-idei/nauchno-poznavatelnyie_shou_dlya_detey/ - Загл. с экрана.В. А. Крицман, В. В. Станцо Энциклопедический словарь юного химика. 2-е изд., испр. М.: Педагогика, 1990г.История химии. [Электронный ресурс]: Википедия — свободная энциклопедия. – Режим доступа: https://ru.wikipedia.org/wiki/ История_химии.Приложение        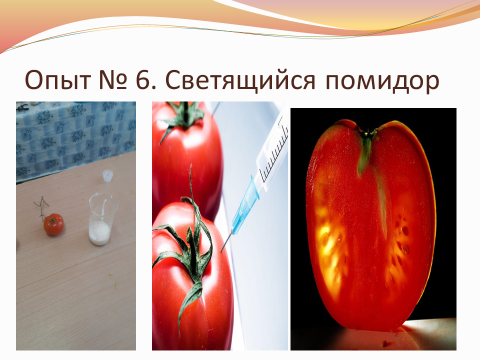 |
