Казанский национальный исследовательский технологический университет Кафедра общей химической технологии
 Скачать 428 Kb. Скачать 428 Kb.
|
МИНОБРНАУКИ РОССИИФедеральное государственное бюджетное образовательное учреждение высшего образования «Казанский национальный исследовательский технологический университет»Кафедра общей химической технологииМЕТОДИЧЕСКИЕ УКАЗАНИЯ к лабораторной работе для студентов «ПИРОЛИЗ НЕФТЕПРОДУКТОВ» Казань 2017 г. Цель работы: Изучение основных закономерностей гомогенных ХТП с протекающей сложной некаталитической обратимой реакцией на примере пиролиза жидких нефтепродуктов. Пиролиз – высокотемпературный ( 7000С) крекинг (термическое разложение) углеводородов, протекающий при низких давлениях. Целевые продукты пиролиза – олефиновые продукты. По масштабам потребления первое место занимают ЭТИЛЕН (С2H4) и ПРОПИЛЕН (C3H6) Основные области их использования следующие :   полиэтилен полиэтилен   этилбензолстиролполистирол этилбензолстиролполистирол окись этиленаэтиленгликольполиэфирное волокно окись этиленаэтиленгликольполиэфирное волокноэтилен   дихлорэтанвинилхлоридполивинилхлорид дихлорэтанвинилхлоридполивинилхлорид  этиловый спиртацетальдегидуксусная кислота этиловый спиртацетальдегидуксусная кислотавинилин (волокно)  и др. и др.   полипропилен полипропилен окись пропиленапропиленгликоль окись пропиленапропиленгликоль акрилонитрилполиакрилаты акрилонитрилполиакрилаты пропилен пропилен глицеринполиглицерин глицеринполиглицерин н-бутиловый спирт н-бутиловый спирт изопренизопреновый каучук изопренизопреновый каучуки др.  Сырье пиролиза (в лаборатории ОХТ) – керосин, бензин, лигроин. В промышленности используют этан-этиленовую, пропан-пропиленовую фракции. Закономерности процесса пиролиза При пиролизе протекают две группы сложных обратимых реакций. Первичные (реакции расщепления): - распад молекул предельных углеводородов с разрывом связи С - С (преимущественно в середине молекулы); СпН2п+2 - дегидрирование предельных и нафтеновых углеводородов; СпН2п+2  - деалкилирование с отрывом боковой цепи;  и другие. Голоядерная ароматика (бензол, нафталин и пр.) не подвергается распаду. Вторичные (реакции уплотнения, приводящие к образованию смол и кокса): - изомеризация предельных углеводородов; н - СпН2п+2 - полимеризация: п С2Н4 - циклизация: 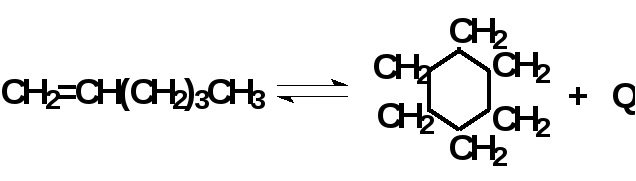 - дегидрирование олефинов с образованием диолефинов:СН2=СН-СН2–СН3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Свойства сырья | бензин | лигроин | керосин |
| Пределы выкипания, оС | 70-180 | 120-212 | 180-330 |
| Средняя длина углеводородной цепи | С6-С9 | С9-С12 | С12-С19 |
При одинаковом времени пребывания реагентов в зоне реакции и при одной и той же температуре легкое сырье успевает разложиться до газообразных углеводородов, тогда как тяжелые углеводороды, главным образом, только до жидких парафинов и олефинов.
Основными параметрами, от которых зависят скорость, конверсия избирательность процесса, являются: фракционный состав и химическая природа сырья, температура, давление и время пребывания в зоне реакций. Скорость пиролиза возрастает с повышением температуры выкипания углеводородов и с понижением их термостойкости (следующая последовательность : парафины нафтены олефины ароматика).
В пределах одного и того же класса термостойкость уменьшается с увеличением молекулярной массы.
Как первичные, так и вторичные реакции обратимы, поэтому процессом пиролиза управляют на основе принципа Ле-Шателье:
«Если на систему, находящуюся в равновесии, воздействовать извне, изменяя какое-нибудь из условий, определяющих положение равновесия, то равновесие смещается в том направлении, при котором эффект произведенного воздействия уменьшается». Иными словами, система как бы противодействует внешнему воздействию. Так, повышение температуры способствует ускорению эндотермических (первичных) и замедлению экзотермических (вторичных) реакций. Следовательно, чтобы увеличить выход продуктов расщепления (газа, содержащего низшие олефины) и снизить выход продуктов уплотнения (кокса, смолы), в реакционной зоне следует поддерживать высокую температуру. Для пиролиза жидкого сырья требуется более мягкий температурный режим (700-7500С), чем для газообразного сырья (более 8000С).
Повышение давления способствует замедлению первичных реакций, идущих с увеличением объема, и ускорению вторичных, протекающих с уменьшением объема. С повышением давления место разрыва цепи смещается к середине. Поэтому, если необходимо увеличить выход жидких продуктов, то процесс проводят при повышенном давлении, если необходимо увеличить выход газообразных продуктов, то процесс ведут при пониженном давлении. Парциальное давление паров углеводородов снижают за счет подачи перегретого водяного пара в количестве 10-20% масс. для газообразного сырья и 50-70% масс. для жидкого сырья.
Продолжительное время пребывания сырья в зоне реакции способствует протеканию вторичных реакций и глубокому разложению первичных продуктов (до С и Н2). Поэтому степень конверсии сырья за один проход через реактор ограничивают 50-70%. На промышленных установках время пребывания жидкого сырья в реакционной зоне составляет около 1 с, а газообразного сырья - менее 1 с.
Процесс пиролиза проводится в реакторах идеального вытеснения. Реактор идеального вытеснения представляет собой длинный канал, через который реакционная смесь движется в поршневом режиме (рис.1, поз.3). Каждый элемент потока, условно выделенный двумя плоскостями, перпендикулярными оси канала, движется через него как твердый поршень, вытесняя предыдущие элементы потока и не перемешиваясь ни с предыдущими, ни с последующими за ним элементами потока.
В реакторе с постоянной площадью поперечного сечения канала линейная скорость потока U будет величиной постоянной, равной отношению объемного расхода V к площади сечения S (U=V/S).
В реальном реакторе можно приблизиться к режиму идеального вытеснения, если длина канала существенно превышает его поперечный размер.
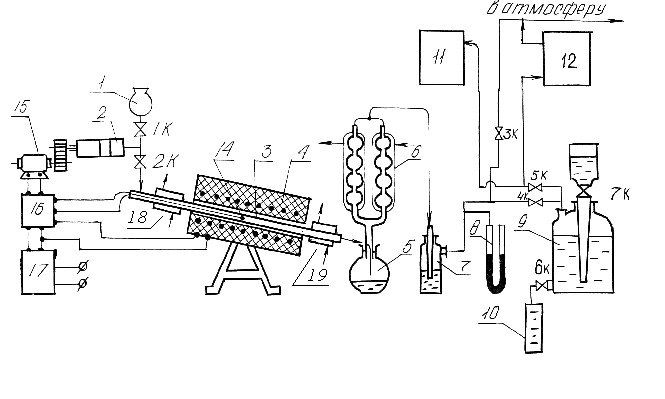
Рис.1. Схема установки пиролиза нефтепродуктов
1 – емкость для сырья; 2 – шприц-насос микропроцессорный «ВЭДА – 5»; 3 – реактор; 4 – электропечь;
5 – сборник жидкого продукта; 6, 18, 19 – холодильники; 7 – абсорбер; 8 – манометр; 9 – газометр;
10 – мерный цилиндр; 11 – газоанализатор; 12 – хроматограф; 14 – термопара; 15 – электромотор;
16 – потенциометр; 17 – ЛАТР; 1к – 7к – краны.
Описание установки и методика проведения работы
Установка (рис.1) состоит из емкости сырья 1, дозатора 2, реактора 3, электропечи 4, сборника жидкого продукта 5, холодильника 6, абсорбера 7, манометра 8, газометра 9, мерного цилиндра 10, газоанализатора 11, хроматографа 12, термопары 14, электромотора дозатора 15, потенциометра 16, автотрансформатора 17, кранов 1к-6к.
Порядок проведения работы
Круглодонную или коническую колбу на 150 мл взвешивают вместе с пробкой, затем герметично соединяют с холодильником 6, собирают всю установку по схеме. Снимают зажимы 3к, 4к открывают кран 7к газометра (другие краны закрыты) и заливают в газометр из верхнего колокола водопроводную воду до верхней красной метки (тем самым газ из газометра вытесняют в атмосферу). Зажимом 3к закрывают выход в атмосферу и закрывают кран 7к. Проверяют установку на герметичность, для чего, пользуясь зажимом 6к, сливают воду (не более 0,5 л) из газометра до поднятия уровня жидкости в манометре до красной метки. Установка считается герметичной, если в манометре в течение 1-2 минут не изменяются уровни жидкости. Далее заливают в емкость 1 сырье . Открывают кран 1к, и, отодвигая назад поршень дозатора 2, засасывают 30мл сырья, закрывают кран 1к. Подают воду в холодильники. На потенциометре устанавливают температуру проведения опыта и включают электрообогрев печи. При достижении в реакторе заданной температуры (на щите управления зажигается красная лампочка) начинают подачу сырья: открывают кран 2к и включают электромотор дозатора, фиксируют время начала опыта.
В системе поддерживают атмосферное давление за счет слива воды из газометра через зажим 6к в мерный цилиндр. Время начала опыта и отбора очередного объема воды записывают в рабочий журнал. После подачи в реактор заданного количества сырья заканчивают опыт: выключают электрообогрев печи, мотор дозатора и закрывают кран 2к. Через некоторое время после прекращения поступления пирогаза из реактора снимают приемник 5 и определяют массу смолы (взвешивают, плотно закрыв пробкой).
Аналитическая часть
Определение качественного и количественного состава пирогаза производят хроматографическим методом. На хроматографе ЛХМ-80 определяют полный состав пирогаза (при отборе газа снимают зажим 5к, зажимом 4к отсоединяют газометр от реактора, через кран 7к в газометр поступает вода). После анализа пирогаза из газометра вытесняют газ в атмосферу (сняты зажимы 3к, 4к, хроматограф отсоединен зажимом 5к, через кран 7к поступает вода).
Расчетная часть
Массу поданного в реактор сырья рассчитывают по формуле:
G = ·V , г
где - плотность сырья , г/мл (табл.2) ; V - объем сырья, мл.
Таблица 2
-
Наименование сырья
бензин
лигроин
керосин
Плотность при 20оС,
г/мл
0,75
0,81
0,87
Расчет содержания отдельных компонентов пирогаза по хроматограмме производят, используя формулу:
где Si - площадь пика , мм2 ;
Mi - масштаб записи на хроматографе;
Ki - поправочный коэффицент на теплопроводность i – го компонента
пирогаза (cм. табл. 3);
Таблица 3










Наименование СН4 С2 Н6 , С3Н8 , i- С4Н10 , н-С4 Н10 , н-С5Н12 ,
веществ С2 Н4 С3Н6 н-С4 Н8 н-С5Н10


Коэффициент, Ki 2,33 1,67 1,30 1,03 1,00 1,00

* для веществ, отсутствующих в таблице, принять Ki = 1,00.
Для определения площади пика (рис.2а) замеряют высоту Н от базовой линии до вершины и ширину пика а на расстоянии Н/2 с учетом толщины самой линии. Площадь пика вычисляют по уравнению:
S = а H , мм2
При неполном разделении пиков (рис.2б) площадь каждого вычисляют так, как будто они не накладываются друг на друга.
Массу пирогаза вычисляют как сумму масс его компонентов :
Gпг = Gi = Vпг 10-2 i Сi , г
где Vпг - объем пирогаза, л; равный объему вытесненной воды из газометра;
где
Опытные и расчетные данные сводят в таблицу материального баланса:
Таблица 4 – Материальный баланс процесса пиролиза
| ПРИХОД РАСХОД | |||||||
| п/п | Наименование веществ | г | % | п/п | Наименование веществ | г | % |
| 1. | Бензин | | | 1. 2. 3. | Пирогаз Смола Кокс и потери | | |
| ИТОГО: 100 ИТОГО: 100 | |||||||
Техника безопасности
Проверить герметичность собранной установки.
Не допускать утечки жидкости и паров.
Промывные воды сливать в специальную бутыль.
В случае возникновения пожара тушить песком и асбестовым одеялом или углекислотным огнетушителем.
З А Д А Н И Е 1
Изучить влияние температуры на процесс пиролиза. Сырье – бензин.
Температура опыта: t = 600, 650, 7000С. Объем сырья, подаваемого в реактор -10 мл. Скорость подачи сырья – 50мл/час.
З А Д А Н И Е 2
Изучить влияние природы сырья на процесс пиролиза. Сырье – бензин, керосин, лигроин. Температура опыта t = 6500С, объем сырья, подаваемого в реактор – 10 мл. Скорость подачи сырья – 50 мл/час.
З А Д А Н И Е 3
Изучить влияние температуры на процесс пиролиза. Сырье – керосин.
Температура процесса t = 550, 600, 6500С. Объем сырья, подаваемого в реактор, - 10 мл. Скорость подачи сырья – 25 мл/час.
З А Д А Н И Е 4
Изучить влияние природы сырья на процесс пиролиза. Сырье – бензин, лигроин, керосин. Температура процесса t = 6500С. Объем сырья, подаваемого в реактор, - 10 мл. Скорость подачи сырья – 25 мл/час.
Построить;
1. Графические зависимости изменения объема (накопления) пирогаза во времени.
2. Графические зависимости массового состава продуктов (пирогаз, смола, кокс и потери), от переменных параметров.
3. Графическую зависимость изменения суммарного содержания непредельных соединений в пирогазе от переменных параметров.
Сделать выводы по работе.
Контрольные вопросы
Процесс пиролиза для углеводородов различных классов.
Первичные и вторичные реакции пиролиза.
Простые и сложные реакции.
Закономерности управления процессом пиролиза: влияние температуры и давления на протекание первичных и вторичных реакций пиролиза. Принцип Ле-Шателье.
Влияние природы сырья на эффективность процесса пиролиза.
Влияние времени пребывания сырья в зоне реакции на эффективность процесса пиролиза.
Процесс пиролиза нефтяного сырья и его место в современной нефтепереработке.
Основные продукты пиролиза и направления их использования.
Характеристика реактора пиролиза.
Технологические критерии эффективности процесса пиролиза.
Принципы хроматографического анализа газа.
Методика проведения работы и выполнения анализов.
Рекомендуемая литература.
Мухленов И.П. Практикум по общей химической технологии /И.П. Мухленов. –М.: Высшая школа. -1979.
Паушкин Я.М. Технология нефтехимического синтеза. Часть 1 /Я.М. Паушкин. – М.: Химия. -1975.
Адельсон С.В. Технология нефтехимического синтеза /С.В.Адельсон, Т.П.Вишнякова, Я.М.Паушкин –М.:Химия. - 1985.
К.А. Гольберт, М.С. Вигдергаус. Курс газовой хроматографии. –М.: Химия. -1977.
Иванов В.Г. Введение в теорию химико-технологических систем. Части I, II. Учебник для вузов /В.Г. Иванов, И.М. Кузнецова, Х.Э.Харлампиди, Э.В. Чиркунов. –Казань, КГТУ.- 1997 г.
Рис.2. Замер площади пика хроматограммы.
а- полное разделение пика; б- неполное разделение пика.

