БА. Классификация бронхиальной астмы
 Скачать 127.74 Kb. Скачать 127.74 Kb.
|
1 2 Бронхиальная астма – это хроническое неинфекционное заболевание дыхательных путей воспалительного характера. Хронические воспалительные процессы в органах дыхания ведут к их гиперактивности, в результате которой при контакте с аллергенами или раздражителями, мгновенно развивается обструкция бронхов, что ограничивает скорость потока воздуха и вызывает удушье. Приступ бронхиальной астмы часто развивается после предвестников и характеризуется коротким резким вдохом и шумным длительным выдохом. Обычно он сопровождается кашлем с вязкой мокротой и громкими свистящими хрипами. Бронхиальная астма может привести к развитию эмфиземы легких и легочного сердца, возникновению астматического статуса. Классификация бронхиальной астмы По происхождению: бронхиальная астма аллергическая бронхиальная астма неаллергическая бронхиальная астма смешанная бронхиальная астма неуточненная По степени тяжести: 1.интермиттирующая, то есть эпизодическая 2.персистирующая легкой степени тяжести 3.персистирующая средней степени тяжести 4.персистирующая тяжелой степени тяжести По состоянию: 1.обострение 2.ремиссия 3.нестабильная ремиссия 4.стабильная ремиссия По уровню контроля: 1.контролируемая 2.частично контролируемая 3.неконтролируемая Лечение бронхиальной астмы Поскольку бронхиальная астма является хроническим заболеванием вне зависимости от частоты приступов, то основополагающим моментом в терапии является исключение контакта с возможными аллергенами, соблюдение элиминационных диет и рациональное трудоустройство. Если же удается выявить аллерген, то специфическая гипосенсибилизирующая терапия помогает снизить реакцию организма на него. Для купирования приступов удушья применяют бета-адреномиметики в форме аэрозоля, для того чтобы быстро увеличить просвет бронхов и улучшить отток мокроты. Это фенотерола гидробромид, сальбутамол, орципреналин. Доза в каждом случае подбирается индивидуально. Так же хорошо купируют приступы препараты группы м-холинолитиков – аэрозоли ипратропия бромида и его комбинации с фенотеролом. Ксантиновые производные пользуются среди больных бронхиальной астмой большой популярностью. Они назначаются для предотвращения приступов удушья в виде таблетированных форм пролонгированного действия. В последние несколько лет препараты, которые препятствуют дегрануляции тучных клеток, дают положительный эффект при лечении бронхиальной астмы. Это кетотифен, кромогликат натрия и антагонисты ионов кальция. При лечении тяжелых форм БА подключают гормональную терапию, в глюкокортикостероидах нуждается почти четверть пациентов, 15-20 мг Преднизолона принимают в утренние часы вместе с антацидными препаратами, которые защищают слизистую желудка. В условиях стационара гормональные препараты могут быть назначены в виде инъекций. Особенность лечения бронхиальной астмы в том, что нужно использовать лекарственные препараты в минимальной эффективной дозе и добиваться еще большего снижения дозировок. Для лучшего отхождения мокроты показаны отхаркивающие и муколитические препараты. Глюкокортикоиды при бронхиальной астме используются для достижения мощного противоаллергического и противовоспалительного эффекта. Механизм действия этих эффектов является комплексным и достаточно сложным. Глюкокортикоиды оказывают следующие, нужные при бронхиальной астме, эффекты: уменьшают отек слизистой оболочки бронхов, уменьшают синтез в ней лейкотриенов и простагландинов в бронхах, усиливают бронходилатационный эффект эндогенного адреналина, восстанавливают чувствительность бета-адренорецепторов к их стимуляторам, снижают активацию клеток воспалительной реакции, снижают продукцию лимфокинов Т клетками, снижают концентрацию эозинофилов и мастоцитов в слизистой оболочке бронхов. Глюкокортикоиды используются как для профилактики возникновения, так и для купирования тяжелых приступов бронхиальной астмы. Глюкокортикоиды, которые применяются при бронхиальной астме, разделяются на системные (метилпреднизолон, преднизолон) и ингаляционные (беклометазон, флунисолид, триамцинолон, будезонид, мометазон, флутиказон). СТАБИЛИЗАТОРЫ МЕМБРАН ТУЧНЫХ КЛЕТОК – кромоглициевая кислота, недокромил, кетотифен. Препараты этой группы не оказывают прямого расслабляющего действия на ГМК бронхов. Они подавляют высвобождение гистамиа из сенсибилизированных тучных клеток и синтез лейкотриенов в дыхательных путях вследствие блокирования трансмембранного тока ионов кальция, а также ингибируют фосфодиэстеразу, что приводит к повышению внутриклеточного содержания цАМФ, снижению сократимости миофибрилл. Недокромил препятствует высвобождению гистамина, лейкотриена и других биологических активных веществ не только из тучных клеток, но и из эозинофилов, нейтрофилов, макрофагов, тромбоцитов, лимфоцитов, участвующих н воспалительной реакции бронхов. Кетотифен также блокирует Н1-рецепторы гистамина. Препараты этой группы предупреждают развитие как самой аллергической реакции немедленного типа, обусловленной выделением медиаторов анафилаксии в результате контакта сенсибилизиро- ванной тучной клетки с соответствующим аллергеном, так и поздней иммунологической реакции. Поскольку фармакологический эффект ЛСэтой группы проявляется до взаимодействия Аг с Ат, их назначают с профилактической целью. Фармакокинетика. Кетотифен хорошо и полностью всасывается при пероральном применении; подвергается процессам деметилирования и глюкуронирования в печени, метаболиты приблизительно в равных соотношениях выводятся с мочой и жёлчью. После однократного назначения бронхорасширяющего действия не оказывает. Кромоглициевая кислота практически нерастворима в липидах, поэтому, в отличие от кетотифена, плохо всасывается при приёме внутрь. В основном её применяют путём ингаляции порошка или аэрозольного раствора. При ингаляции через спинхалер 10% дозы препарата достигает бронхиол и альвеол, о стальная часть проглатывается и в неизменённом виде выводится через ЖКТ. Абсорбированная часть дозы не подвергается биотрансформации и выводится в основном почками. При ингаляции недокромила со слизистой оболочки дыхательных путей всасывается 5% дозы, дополнительно абсорбируется 2 — 3% препарата, поступившего в ЖКТ, Недокромил связывается с белками крови на 80%, не подвергаетсяметаболизму в печени и выводится из организма в неизменённом виде почками и с жёлчью. Показания. Бронхиальная астма (атопическая форма, астма физического усилия, астматическая триада), аллергический ринит, аллергический конъюнктивит, пищевая аллергия и аллергические заболевания ЖКТ (внутрь). Профилактика приступов удушья, бронхоспастических реакций, (вызываемых, например, химическими, газообразными веществами, пылью, холодным воздухом). После снижения частоты приступов рекомендовано уменьшение кратности приёма препаратов. Побочные эффекты. Незначительны, редко они вызывают раздражение слизистой оболочки глотки и трахеи, сухость во рту, охриплость голоса. В начале лечения иногда возникают кашель и кратковременный бронхоспазм (после ингаляции сухого порошка). Кашель купируют приёмом стакана воды сразу после ингаляции, а при повторяющемся бронхоспазме показана предварительная (за 15 — 20 мин) ингаляция бета-адреностимуляторов. Кетотифен может вызвать сонливость, сухость во рту, снижение секреции бронхиальных желёз. Противопоказания. При индивидуальной непереносимости, в 1 триместре беременности; кромоглициевая кислота и недокромил — при астматическом статусе; кетотифен с осторожностью назначать пациентам, занятым на работе, требующей концентрации внимания. Взаимодействия. Кромоглициевая кислота и недокромил оказывают более сильное действие при предварительном копировании бронхоспазма адреномиметиками. Кетотифен усиливает седативный эффект препаратов, угнетающих ЦНС. Метилксантины – это препараты со сложным механизмом действия, к которым относятся теофиллин и его водорастворимый эфир – аминофиллин (эуфиллин). Применяются метилксантины (как препараты резерва) для профилактики и купирования приступов бронхиальной астмы. Механизм действия Метилксантины ингибируют фосфодиэстеразу, функция которой заключается в разрушении циклического аденозинмонофосфата (ц-АМФ). Это способствует накоплению ц-АМФ и расслаблению гладкой мускулатуры бронхов. В большей степени ингибируется фосфодиэстераза 4 типа, которая содержится в тучных клетках и в бронхах. Что играет на руку при лечении бронхиальной астмы – патологический очаг находится именно в бронхах. 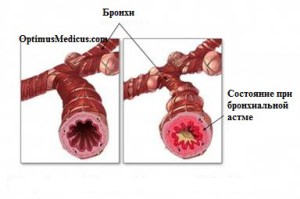 Бронхи в нормальном состоянии и при приступе бронхиальной астмы. Накопление ц-АМФ может приводить к побочному эффекту – увеличение силы и частоты сердечных сокращений. Из-за этого сердце больше нуждается в кислороде, так как начинает больше работать. При увеличении работы сердца повышается выделение мочи и скорость клубочковой фильтрации. В целом этот побочный эффект не имеет какого-либо весомого значения в клинической практике. Метилксантины блокируют рецепторы аденозина, благодаря чему увеличивается выделение катехоламинов в синаптическую щель и, как следствие, расширяются бронхи. Метилксантины тормозят выделение медиаторов аллергии из тучных клеток. Препараты К метилксантинам относятся 2 основных представителя: теофиллин и его водорастворимый эфир – аминофиллин, более известный как эуфиллин. Теофиллин является токсичным препаратом. Его дозирование при приеме внутрь может быть неточным, так как имеются сильные индивидуальные колебания биодоступности, поэтому при применении необходимо контролировать уровень теофиллина в плазме крови. Благодаря этому можно адекватно корректировать дозу и избежать токсического воздействия на организм. Теофиллин, чаще всего, используются в пролонгированной форме. Препарат близок по строению с кофеином, поэтому раздражает слизистую оболочку желудка. Теофиллин метаболизируется в печени при помощи микросомальных ферментов. Из-за этого имеет большое количество лекарственных взаимодействий: применение ингибиторов микросомальных ферментов (таких как циметидин, эритромицин, ципрофлоксацин и др.) с теофиллином увеличивают его токсичность; применение индукторов микросомальных ферментов (рифампицин, фенитоин и др.) с теофиллином – снижают его эффективность. Метилксантины применяются для профилактики (теофиллин) и купирования (аминофиллин) приступов бронхиальной астмы. Аминофиллин (эуфиллин) при купировании приступов гораздо менее эффективен чем ингаляционные бета-2-адреномиметики и подкожное введение эпинефрина. Побочные эффекты Метилксантины имеют серьезные и разнообразные побочные эффекты, зачастую из-за них прекращается лечение: со стороны центральной нервной системы – тревога, раздражительность, головная боль, бессонница и судороги; со стороны сердечно-сосудистой системы – предсердные тахиаритмии и тахикардия; со стороны желудочно-кишечного тракта – рвота, тошнота, анорексия, понос, гастроэзофагальный рефлюкс. Условия применения Метилксантины являются препаратами резерва, из-за их умеренной эффективности и токсичности. Применяются в следующих случаях: по экономическим соображениям – метилксантины являются самыми дешевыми средствами для лечения бронхиальной астмы; отсутствие эффекта при назначении ингаляционных глюкокортикоидов; отсутствие должной эффективности при применении бета-2-адреномиметиков и ипратропия бромида. Терапия бронхиальной астмы (БА) может быть условно разделена на два основных направления. Первое – симптоматическая терапия, быстро и эффективно купирующая бронхоспазм, ведущий клинический симптом БА. Второе – противовоспалительная терапия, способствующая модификации главного патогенетического механизма заболевания, а именно, воспаления слизистой дыхательных путей (ДП). Терапия бронхиальной астмы (БА) может быть условно разделена на два основных направления. Первое – симптоматическая терапия, быстро и эффективно купирующая бронхоспазм, ведущий клинический симптом БА. Второе – противовоспалительная терапия, способствующая модификации главного патогенетического механизма заболевания, а именно, воспаления слизистой дыхательных путей (ДП). Центральное место среди средств симптоматического контроля БА, очевидно, занимают b2–агонисты, характеризующиеся выраженной бронхолитической активностью (и бронхопротективным действием) и минимальным числом нежелательных побочных явлений при их правильном использовании. Впервые симпатомиметик адреналин (эпинефрин) был использован в лечении больных БА в 1900 г. Поначалу адреналин широко применялся как в инъекционной форме, так и в виде ингаляций. Однако неудовлетворенность кратковременностью действия (1–1,5 ч), большим количеством негативных побочных эффектов препарата явилась стимулом к дальнейшему поиску более «привлекательных» лекарственных средств. В 1940 г. появился изопротеренол – синтетический катехоламин. Он разрушался в печени так же быстро, как и адреналин (при участии фермента катехол–о–метилтрансферазы – КОМТ), и поэтому характеризовался небольшой продолжительностью действия (1–1,5 ч), а образующиеся в результате биотрансформации изопротеренола метаболиты (метоксипреналин) обладали b–адреноблокирующим действием. В то же время изопротеренол был свободен от таких нежелательных явлений, присущих адреналину, как головная боль, задержка мочи, артериальная гипертензия. Изучение фармакологических свойств изопротеренола привело к установлению гетерогенности адренорецепторов. По отношению к последним адреналин оказался универсальным прямым a–b–агонистом, а изопротеренол – первым короткодействующим неселективным b–агонистом. Первым селективным b2–агонистом стал появившийся в 1970 г. сальбутамол, характеризовавшийся минимальной и клинически незначимой активностью в отношении a– и b1–рецепторов. Он по праву приобрел статус «золотого стандарта» в ряду b2–агонистов. За сальбутамолом последовало внедрение в клиническую практику других b2–агонистов (тербуталин, фенотерол). Эти препараты оказались столь же эффективны в качестве бронхолитиков, как и неселективные b–агонисты, поскольку бронхолитический эффект симпатомиметиков реализуется только через b2–адренорецепторы. Вместе с тем b2–агонисты демонстрируют существенно менее выраженное стимулирующее воздействие на сердце (батмотропное, дромотропное, хронотропное) по сравнению с b1–b2–агонистом изопротеренолом . Некоторые различия в селективности b2–агонистов не имеют серьезного клинического значения. Большая частота нежелательных кардиоваскулярных эффектов при приеме фенотерола (по сравнению с сальбутамолом и тербуталином) может быть объяснена большей эффективной дозой препарата и, отчасти, более быстрой системной абсорбцией. У новых препаратов сохранилось быстродействие (наступление эффекта в первые 3–5 минут после ингаляции), характерное для всех предшествующих b–агонистов при заметном увеличении продолжительности их действия до 4–6 часов (менее выраженном при тяжелой БА). Это улучшало возможности контроля за симптомами БА в течение дня, но «не спасало» от ночных приступов. Появившаяся возможность приема отдельных b2–агонистов внутрь (сальбутамол, тербуталин, формотерол, бамбутерол) в некоторой степени решала проблему контроля ночных приступов БА. Однако необходимость принимать значительно более высокие дозы (почти в 20 раз больше, чем при ингаляционном применении) способствовала появлению нежелательных явлений, связанных со стимуляцией a– и b1–адренорецепторов. Кроме того, была выявлена и более низкая терапевтическая эффективность этих препаратов. Значительно изменило возможности терапии БА появление пролонгированных ингаляционных b2–агонистов – сальметерола и формотерола. Первым появился на рынке сальметерол – высокоселективный b2–агонист, демонстрирующий продолжительность действия, по крайней мере, в течение 12 часов, но с медленным началом действия. Вскоре к нему «присоединился» формотерол, также являющийся высокоселективным b2–агонистом с 12–часовым действием, но со скоростью развития бронходилатационного эффекта, аналогичной таковой сальбутамола. Уже в первые годы применения пролонгированных b2–агонистов было отмечено, что они способствуют урежению обострений БА, уменьшению количества госпитализаций, а также снижению потребности в ингаляционных кортикостероидах (ИГКС). Наиболее эффективным путем введения лекарственных препаратов при БА, в том числе и b2–агонистов, признан ингаляционный. Важными преимуществами этого пути являются возможность непосредственной доставки лекарственных препаратов к органу–мишени (что в значительной степени обеспечивает быстродействие бронходилататоров) и минимизация нежелательных эффектов. Из известных в настоящее время средств доставки наиболее часто используются дозированные аэрозольные ингаляторы (ДАИ), реже дозированные порошковые ингаляторы (ДПИ) и небулайзеры. Пероральные b2–агонисты в виде таблеток или сиропов применяются крайне редко, главным образом как дополнительное средство при частых ночных симптомах БА или высокой потребности в ингаляционных короткодействующих b2–агонистах у больных, получающих высокие дозы ИГКС (эквивалентные 1000 мкг беклометазона в сутки и более) Механизмы действия b2–агонистов b2–агонисты вызывают бронходилатацию в первую очередь в результате непосредственной стимуляции b2–адренорецепторов гладких мышц ДП. Доказательства этого механизма были получены как in vitro (при воздействии изопротеренола происходило расслабление бронхов человека и отрезков легочной ткани), так и in vivo (быстрое падение сопротивления ДП после ингаляций бронхолитика). Стимуляция b–адренорецепторов приводит к активации аденилатциклазы, образущей комплекс с G–протеином, под воздействием которого повышается содержание внутриклеточного циклического аденозин–3,5–монофосфата (цАМФ). Последнее приводит к активации специфической киназы (протеинкиназы А), которая фосфорилирует некоторые внутриклеточные белки, в результате чего происходит снижение внутриклеточной концентрации кальция (активное его «перекачивание» из клетки во внеклеточное пространство), тормозится гидролиз фосфоинозитида, ингибируются киназы легких цепей миозина и, наконец, «открываются» большие кальций–активируемые калиевые каналы, обусловливающие реполяризацию (расслабление) гладкомышечных клеток и секвестрацию кальция во внеклеточное депо. Нужно сказать, что b2–агонисты могут связываться с калиевыми каналами и непосредственно вызывать релаксацию гладкомышечных клеток независимо от повышения внутриклеточной концентрации цАМФ. 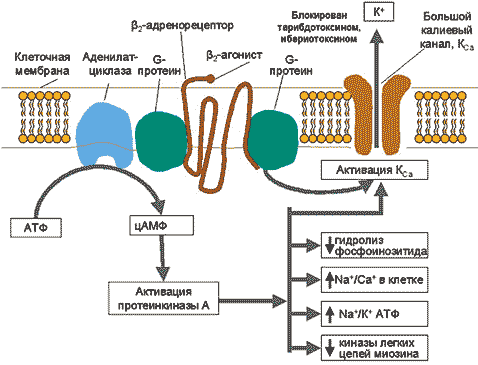 Рис.1. Молекулярные механизмы, участвующие в бронходилатационном эффекте b2-агонистов. КСа - большой кальцийактивируемый калиевый канал; АТФ - аденозинтрифосфат; цАМФ - циклический аденозин-3,5-моносфат b2–агонисты рассматриваются как функциональные антагонисты, обусловливающие обратное развитие бронхоконстрикции вне зависимости от имевшего место констрикторного воздействия. Это обстоятельство представляется чрезвычайно важным, поскольку многие медиаторы (медиаторы воспаления и нейротрансмиттеры) обладают бронхоконстрикторным действием. В результате воздействия на b–адренорецепторы, локализующиеся в различных отделах ДП, выявляются дополнительные эффекты b2–агонистов, которые объясняют возможность профилактического использования препаратов. В их числе угнетение высвобождения медиаторов из клеток воспаления, уменьшение проницаемости капилляров (предотвращение развития отека слизистой бронхов), угнетение холинергической передачи (уменьшение холинергической рефлекторной бронхоконстрикции), модуляция продукции слизи подслизистыми железами и, следовательно, оптимизация мукоцилиарного клиренса. 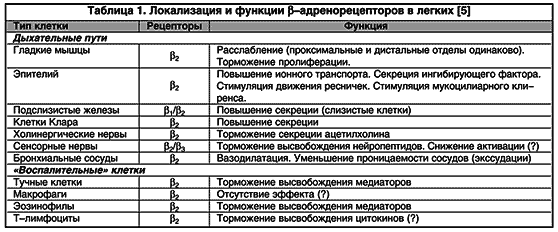 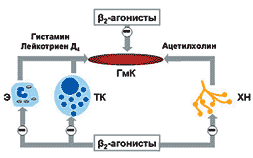 Рис. 2. Прямой и непрямой бронходилатационный эффект b2-агонистов. Э - эозинофил; ТК - тучная клетка; ХН - холинергический нерв; ГмК - гладкомышечная клетка Согласно микрокинетической диффузионной теории продолжительность и время начала действия b2–агонистов связаны с их физико–химическими свойствами (в первую очередь липофильностью/гидрофильностью молекулы) и особенностями механизма действия. Сальбутамол – гидрофильное соединение. Попадая в водную среду внеклеточного пространства, он быстро проникает в «сердцевину» рецептора и после прекращения связи с ним удаляется путем диффузии. Сальметерол, созданный на основе сальбутамола, высоко липофильный препарат, быстро проникает в мембраны клеток дыхательных путей, выполняющих функцию депо, и затем медленно диффундирует через мембрану рецептора, обусловливая его длительную активацию и более позднее начало действия. Липофильность формотерола меньше, чем у сальметерола, поэтому он образует депо в плазматической мембране, откуда диффундирует во внеклеточную среду и затем одновременно связывается с b–адренорецептором и липидами, что обусловливает и быстроту наступления эффекта, и увеличение его продолжительности. Продолжительный эффект сальметерола и формотерола объясняется их способностью длительное время находиться в бислое клеточных мембран гладкомышечных клеток в непосредственной близости от b2–адренорецепторов и взаимодействовать с последними. 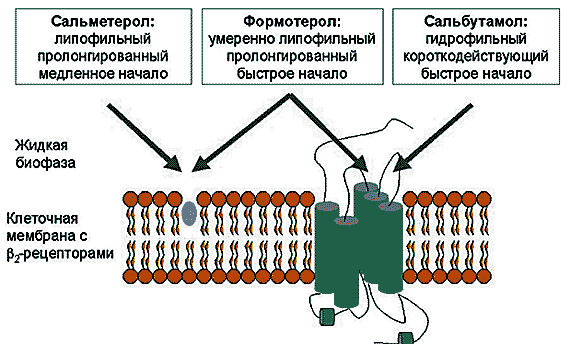 Рис. 3. Механизм действия b2-агонистов [10] (объяснения в тексте) При исследовании in vitro спазмированная мышца расслабляется быстрее при добавлении формотерола, нежели сальметерола. Это подтверждает то, что сальметерол является частичным агонистом b2–рецепторов относительно формотерола. Рацематы Селективные b2–агонисты представляют из себя рацемические смеси (50:50) двух оптических изомеров – R и S. Установлено, что фармакологическая активность R–изомеров в 20–100 раз выше, чем S–изомеров. Показано, что R–изомер сальбутамола проявляет свойства бронхолитика. В то же время S–изомер проявляет прямо противоположные свойства: провоспалительное действие, увеличение гиперреактивности ДП, усиление бронхоспазма, кроме того, он значительно медленнее метаболизируется. Недавно был создан новый препарат, содержащий только R–изомер (левалбутерол). Он существует пока только в растворе для небулайзеров и имеет лучший терапевтический эффект, чем рацемический сальбутамол, так как эквивалентный эффект левалбутерол демонстрирует в дозе, равной 25% рацемической смеси (нет противодействующего S–изомера, уменьшено и количество нежелательных явлений). Селективность b2–агонистов Цель применения селективных b2–агонистов состоит в том, чтобы обеспечить бронходилатацию и при этом избежать нежелательных явлений, индуцируемых стимуляцией a– и b1–рецепторов. В большинстве случаев умеренное применение b2–агонистов не ведет к развитию нежелательных эффектов. Однако селективность не может полностью устранить риск их развития, и тому есть несколько объяснений. Прежде всего, селективность к b2–адренорецепторам всегда относительна и дозозависима. Незначительная активация a– и b1–адренорецепторов, незаметная при обычных среднетерапевтических дозах, становится клинически значимой при увеличении дозы препарата или частоты его приема в течение дня. Дозозависимый эффект b2–агонистов необходимо учитывать при лечении обострений БА, особенно жизнеугрожающих состояний, когда повторные ингаляции в течение короткого времени (нескольких часов) в 5–10 раз превышают допустимую суточную дозу. b2–рецепторы широко представлены в ДП (табл. 1). Плотность их увеличивается по мере уменьшения диаметра бронхов, а у больных БА плотность b2–рецепторов в дыхательных путях выше, чем у здоровых. Многочисленные b2–адренорецепторы найдены на поверхности тучных клеток, нейтрофилов, эозинофилов, лимфоцитов. И в то же время b2–рецепторы находят в разнообразных тканях и органах, особенно в левом желудочке, где они составляют 14% всех b–адренорецепторов, и в правом предсердии – 26% всех b–адренорецепторов. Стимуляция этих рецепторов может привести к развитию нежелательных явлений, включая тахикардию, трепетание предсердий и ишемию миокарда. Стимуляция b2–рецепторов скелетных мышц может вызвать мышечный тремор. Активация больших калиевых каналов может способствовать развитию гипокалиемии и, как следствие этого – удлинению интервала QT и нарушениям сердечного ритма, в т.ч. фатальным. При системном введении больших доз препаратов могут наблюдаться метаболические эффекты (увеличение уровня свободных жирных кислот в сыворотке крови, инсулина, глюкозы, пирувата и лактата). При стимуляции сосудистых b2–рецепторов развивается вазодилатация и возможно снижение диастолического артериального давления. Особенно выражены нежелательные кардиальные эффекты в условиях тяжелой гипоксии во время обострений БА – увеличение венозного возврата (особенно в положении ортопноэ) может вызвать развитие синдрома Bezold–Jarisch с последующей остановкой сердца. Связь между b2–агонистами и воспалением в ДП В связи с широким использованием b2–агонистов короткого действия, а также внедрением в клиническую практику пролонгированных ингаляционных b2–агонистов стал особенно актуальным вопрос о том, обладают ли эти препараты противовоспалительным действием. Несомненно, противовоспалительным эффектом b2–агонистов, способствующим модификации острого воспаления бронхов, можно считать угнетение высвобождения медиаторов воспаления из тучных клеток и уменьшение проницаемости капилляров. В то же время при биопсии слизистой бронхов больных БА, регулярно принимающих b2–агонисты, было установлено, что число клеток воспаления, в т.ч. и активированных (макрофаги, эозинофилы, лимфоциты) не уменьшается. При этом теоретически регулярный прием b2–агонистов может даже привести к усугублению воспаления в ДП. Так, обусловливаемая b2–агонистами бронходилатация позволяет осуществить более глубокий вдох, результатом чего может стать более массивная экспозиция аллергенов. Кроме того, регулярное применение b2–агонистов может маскировать развивающееся обострение, тем самым задерживая начало или усиление истинной противовоспалительной терапии. Потенциальный риск использования b2–агонистов Толерантность Частое регулярное применение ингаляционных b2–агонистов может привести к развитию толерантности (десенситизации) к ним. Накопление цАМФ способствует переходу рецептора в неактивное состояние. Чрезмерно интенсивная стимуляция b–адренорецепторов способствует развитию десенситизации (уменьшению чувствительности рецепторов в результате разобщения рецептора с G–протеином и аденилатциклазой). При сохранении избыточной стимуляции уменьшается число рецепторов на поверхности клетки («down»–регуляция). Нужно отметить, что b–рецепторы гладких мышц ДП имеют довольно значительный резерв и поэтому они более устойчивы к десенситизации, чем рецепторы нереспираторных зон (например, скелетной мускулатуры или регулирующие метаболизм). Установлено, что у здоровых лиц быстро развивается толерантность к высоким дозам сальбутамола, а к фенотеролу и тербуталину – нет. Вместе с тем у больных БА толерантность к бронхолитическому эффекту b2–агонистов появляется редко, гораздо чаще развивается толерантность к их бронхопротективному действию. Уменьшение бронхопротективного действия b2–агонистов при их регулярном, частом применении в равной степени касается и короткодействующих, и пролонгированных препаратов даже на фоне базисной терапии ингаляционными кортикостероидами. В то же время речь идет не о полной потере бронхопротекции, а о небольшом снижении ее первоначального уровня. H.J.van der Woude et al. установили, что на фоне регулярного применения больными БА формотерола и сальметерола бронхолитический эффект последних не снижается, бронхопротективное действие оказывается выше у формотерола, но при этом значительно меньше выражено бронхолитическое действие сальбутамола. Десенситизация развивается длительно, в течение нескольких дней или недель, в отличие от тахифилаксии, которая развивается очень быстро и не связана с функциональным состоянием рецепторов. Это обстоятельство объясняет снижение эффективности лечения и требует ограничения частоты применения b2–агонистов. Индивидуальную вариабельность ответа на b2–агонисты и развития толерантности к их бронходилатирующему эффекту многие исследователи связывают с генетическим полиморфизмом генов. Ген b2–адренорецепторов локализуется на 5q хромосоме. Существенное влияние на течение БА и эффективность лечения оказывает изменение аминокислотной последовательности b2–адренорецепторов, в частности, перемещение аминокислот в 16 и 27 кодонах. Влияние полиморфизма генов не распространяется на вариабельность бронхопротективного эффекта. Справедливости ради надо отметить, что эти данные подтверждаются не во всех работах. b2–агонисты и смертность больных БА Серьезные сомнения в безопасности ингаляционных b–агонистов возникли в 60–х годах ХХ столетия, когда в ряде стран, в том числе Англии, Австралии, Новой Зеландии разразилась «эпидемия смертей» среди больных БА. При этом высказывалось предположение о связи между терапией симпатомиметиками и увеличением смертности от БА. Причинно–следственные взаимоотношения между применением b–агонистов (изопротеренола) и возросшей смертностью тогда не были установлены, а по результатам ретроспективных исследований доказать их было практически невозможно. Связь же между приемом фенотерола и повышением смертности от БА в Новой Зеландии в 80–е годы удалось доказать, поскольку было установлено, что этот препарат чаще назначался в случаях фатальной БА, по сравнению с хорошо контролируемым заболеванием. Эта связь была косвенно подтверждена и снижением смертности, совпавшей с отменой широкого приема фенотерола (при общем увеличении продаж других b2–агонистов). В этом плане показательны результаты эпидемиологического исследования в Канаде, ставившего своей целью изучить возможную связь между частотой летальных исходов и назначаемыми лекарственными средствами. Было показано, что возрастание частоты летальных исходов ассоциируется с высокодозной терапией любым из доступных ингаляционных b2–агонистов. Риск фатального исхода был наибольшим при применении фенотерола, однако при упорядоченном сравнении с эквивалентными дозами сальбутамола показатели смертности достоверно не отличались. В то же время связь между высокодозной терапией b2–агонистами и увеличением смертности от БА надежно доказать не удается, поскольку больные с более тяжелой и плохо контролируемой БА чаще прибегают к помощи высоких доз b2–агонистов и, напротив, реже – к помощи эффективных противовоспалительных лекарственных средств. Кроме того, высокие дозы b2–агонистов маскируют признаки нарастающего фатального обострения БА. Режим дозирования Ингаляционные короткодействующие b2–агонисты Ингаляционные короткодействующие b2–агонисты являются препаратами выбора для ситуационного симптоматического контроля БА , а также для предупреждения развития симптомов астмы физического усилия (АФУ). Регулярное же применение ингаляционных b–агонистов может привести к утрате адекватного контроля над течением заболевания. Так, в исследовании, проведенном M.R. Sears et al. в Новой Зеландии, изучались бронхиальная гиперреактивность, утренняя ПСВ, ежедневные симптомы и потребность в ИГКС у пациентов, использующих b2–агонисты «по требованию», по сравнению с больными, применяющими фенотерол регулярно 4 раза в день. В группе больных с регулярным приемом фенотерола наблюдался плохой контроль над симптомами БА, кроме того, отмечались более частые и тяжелые обострения по сравнению с группой больных, применяющих b2–агонисты «по требованию» в течение полугода. У последних же наблюдались улучшение показателей функции внешнего дыхания, утренней ПСВ, снижение ответа на бронхопровокационную пробу с метахолином. Повышение гиперреактивности бронхов на фоне регулярного приема короткодействующих b2–агонистов, скорее всего, связано с наличием S–энантомеров в рацемической смеси препарата. В отношении сальбутамола подобные закономерности установить не удалось, хотя, как и в случае с фенотеролом, его регулярный прием сопровождался незначительным возрастанием бронхиальной гиперреактивности. Имеются отдельные доказательства того, что регулярное применение сальбутамола сопровождается возрастанием частоты эпизодов АФУ и увеличением выраженности воспаления в ДП. Короткодействующие b2–агонисты должны использоваться (в т.ч. и в рамках монотерапии) только «по требованию». Маловероятно, что обычно рекомендуемый режим дозирования b2–агонистов «по требованию» может ухудшить контроль над течением БА, однако при использовании высоких доз препарата ухудшение контроля становится реальным. Более того, многие больные становятся особенно чувствительными к агонистам при наличии полиморфизма b2–адренорецепторов, что обусловливает более быстрое ухудшение контроля. Связь, установленная между повышением риска смерти у больных БА и применением высоких доз ингаляционных b2–агонистов, отражает лишь степень тяжести заболевания. Возможно также, что высокие дозы ингаляционных b2–агонистов оказывают вредоносное воздействие на течение БА. Больные, получающие высокие дозы b2–агонистов (более 1,4 баллончика аэрозоля в месяц), безусловно, нуждаются в эффективной противовоспалительной терапии, в т.ч. и с целью уменьшения дозы b2–агонистов. При увеличении потребности в бронходилататорах (чаще трех раз в неделю) показано дополнительное назначение противовоспалительных препаратов, а при употреблении b2–агонистов более 3–4 раз в день для купирования симптомов – увеличение их дозы. Прием короткодействующих b2–агонистов с целью бронхопротекции также ограничивается «разумными пределами» (не более 3–4 раз в сутки). Пролонгированные ингаляционные b2–агонисты Доступные в настоящее время пролонгированные ингаляционные b2–агонисты – формотерол и сальметерол оказывают свое действие в течение 12 часов с равноценным бронхолитическим эффектом. Тем не менее различия между ними есть. В первую очередь, это быстродействие формотерола (в форме ДПИ), сопоставимое со временем начала действия сальбутамола (в форме ДАИ), что позволяет использовать формотерол в качестве средства скорой помощи, вместо короткодействующих b2–агонистов. В то же время нежелательных явлений при использовании формотерола существенно меньше, чем при применении сальбутамола. Эти препараты могут использоваться в качестве монотерапии у больных с легким течением БА в качестве бронхопротекторов при АФУ. При использовании формотерола чаще 2 раз в неделю «по требованию» необходимо добавлять к лечению ИГКС. Следует отметить, что монотерапия пролонгированными b2–агонистами на регулярной основе не рекомендуется, так как до сих пор нет надежных доказательств их противовоспалительного, модифицирующего заболевание действия. Есть научно обоснованные доказательства целесообразности комбинированного применения ИГКС и бронходилататоров. Кортикостероиды усиливают экспрессию b2–рецепторов и уменьшают потенциальную десенситизацию, в то время как пролонгированные b2–агонисты увеличивают чувствительность кортикостероидных рецепторов к ИГКС. Проведенные к настоящему времени исследования свидетельствуют о возможности более раннего назначения пролонгированных ингаляционных b2–агонистов.У больных с неадекватным контролем астмы на фоне приема 400–800 мкг ИГКС дополнительное назначение сальметерола обеспечивает более полный и адекватный контроль по сравнению с увеличением дозы ИГКС. Формотерол демонстрирует сходный эффект и одновременно способствует уменьшению частоты обострений заболевания. Эти и ряд других исследований свидетельствуют о том, что добавление пролонгированных ингаляционных b2–агонистов к низко–среднедозовой терапии ИГКС у больных с неадекватным контролем БА равноценно удвоению дозы стероидов. В настоящее время рекомендовано использовать пролонгированные ингаляционные b2–агонисты только у больных, одновременно получающих ИГКС. Многообещающими представляются фиксированные комбинации, такие как сальметерол с флютиказоном (Серетид) и формотерол с будесонидом (Симбикорт). При этом отмечается лучшая комплаентность, исключается риск использования только одного из препаратов в рамках длительной терапии заболевания. 2. М-ХОЛИНОЛИТИКИ Препараты блокируют действие ацетилхолина на М-холинергические рецепторы, которые представлены преимущественно в крупных воздухоносных путях. Соответственно, эффект препаратов более выражен при бронхитах, чем при астме, которая характеризуется преимущественным вовлечением периферических бронхов. В связи с этим традиционно признаны как более эффективные в лечении бронхоконстрикции, связанной с хроническим бронхитом у пациентов, не отвечающих на терапию b2-агонистами. Наряду с расслаблением мускулатуры бронхов, холинолитические препараты оказывают ряд эффектов, затрудняющих их применение: вызывают сухость слизистых оболочек носоглотки и верхних дыхательных путей, снижают секрецию бронхиальных желез и подвижность ресничек эпителия, то есть угнетают эвакуаторную функцию бронхов, увеличивают число сердцебиений, стимулируют расширение зрачка, покраснение кожи. Общие показания для преимущественного применения холинолитиков при БА: являются средством выбора при преобладании признаков бронхита, служащего клиническим эквивалентом астмы, в первую очередь, у пожилых людей, в т.ч. "поздняя астма" (важно использовать препараты совместно с муколитическими и отхаркивающими средствами); при "кашлевой астме" (кашель как эквивалент приступа астмы), при бронхиальной обструкции, провоцируемой физической нагрузкой, холодом, вдыханием пыли, газов; при бронхообструктивном синдроме с выраженной бронхореей ("влажная астма"); у больных БА с противопоказаниями к назначению b2-адреностимуляторов; холинолитики более эффективны для профилактики, чем для "снятия" уже развившегося бронхоспазма; при психогенной астме и особенностях гормонального фона (предменструальная астма, сочетание астмы с тиреотоксикозом) применение комплекса холинолитических и успокаивающих средств имеет преимущество по сравнению с b-адреномиметиками; как антидот при ошибочном назначении больному b-блокаторов (при этом b-адреномиметики действуют на уже блокированные рецепторы и поэтому не снимают спазм). После ингаляции ипратропиума бромида достигается максимальный эффект через 30-60 мин. Продолжительность действия от 3 до 6 часов. Окситропиума бромид имеет схожие характеристики. Представляется перспективным введение в практику нового препарата этой группы - тиотропиума, обладающего пролонгированным действием. Показания: обратимая бронхиальная обструкция, частично обратимая при хроническом бронхите. Предостережения: глаукома, гипертрофия предстательной железы, беременность. Побочные эффекты: сухость во рту, редко - задержка мочи. ЛЕКАРСТВЕННЫЕ ФОРМЫ ИПРАТРОПИУМА БРОМИДА 1) ДИ (аэрозоль), 20 мкг/доза. Режим дозирования: Взрослые: по 2-4 дозы аэрозоля 3-4 раза в день. Дети: до 6 лет - 20 мкг 3 раза в день; 6-12 лет - 40 мкг 3 раза в день. 2) Раствор для ингаляций (через небулайзер) 0,25 мг/мл (0,025%) во флаконах по 20 мл. Режим дозирования: Взрослые: лечение обострений - 2,0 мл (0,5 мг, 40 капель), возможно в сочетании с b2-агонистами; поддерживающая терапия - 2,0 мл 3-4 раза в день. Дети: до 6 лет - по 0,4-1 мл (8-20 капель) до 3 раз в день под наблюдением врача; 6-12 лет -по 1 мл (20 капель) 3-4 раза/сут. Первая ингаляция должна проводиться под наблюдением медицинского персонала. Астматический статус – это приступ бронхиальной астмы, намного сильнее, чем обычно, при этом он не купируется даже повышенными дозировками бронходилататоров, которые принимает пациент. Происходит ярко-выраженное нарушение проходимости бронхов из-за отека слизистой, спазмов мускулатуры бронхов и обструкции слизью. Это ведет к затруднению вдоха и к активному удлиненному выдоху. Классификация астматического статуса По патогенезу: медленно развивающийся астматический статус анафилактический астматический статус анафилактоидный астматический статус По стадиям: стадия относительной компенсации стадия декомпенсации, когда проведение по легким отсутствует кома, наступившая вследствие гипоксии 1 2 |
