коллоквиум гормоны. Классификация межклеточных регуляторов Анатомофизиологическая
 Скачать 1.57 Mb. Скачать 1.57 Mb.
|
1. Дайте классификацию межклеточных регуляторов. Различают: 1. Внутриклеточную регуляцию (ауторегуляцию) 2. Дистантную регуляцию (межклеточную) Классификация межклеточных регуляторов 1. Анатомо-физиологическая: а) Гормоны – межклеточные регуляторы, доставляемые к клеткам-мишеням током крови. Вырабатываются в эндокринных железах или рассеянных железистых клетках. б) Нейрогормоны вырабатываются нервными клетками и выделяются в синаптическую щель, то есть в непосредственной близости от клетки-мишени. Нейрогормоны делятся на медиаторы и модуляторы. Медиаторы обладают непосредственным пусковым эффектом. Модуляторы изменяют эффект медиаторов. Примерами медиаторов являются ацетилхолин и норадреналин; модуляторов – гамма-ааминомасляная кислота, дофамин. в) Локальные гормоны – это межклеточные регуляторы, действующие на близлежащие к месту их синтеза клетки. Пример: гормоны, производные жирных кислот. 2. Классификация по широте действия: а) Гормоны универсального действия действуют на все ткани организма (например, катехоламины, глюкокортикостероиды) б) Гормоны направленного действия действуют на определенные органы-мишени (например, АКТГ действует на кору надпочечников). 3. Классификация по химическому строению: а) Белково-пептидные гормоны: Олигопептиды (кинины, АДГ), Полипептиды (АКТГ, глюкагон), Белки (СТГ, ТТГ, ГТГ) б) Производные аминокислот: Катехоламины и йодтиронины - образуются из тирозина, Ацетилхолин - образуется из серина, Серотонин, триптамин, мелатонин - образуются из триптофана. в) Стероидные гормоны (гормоны коры надпочечников и половые гормоны) 2. Как действуют гормоны через рецепторы находящиеся на клеточной мембране. В этом случае гормон не проникает в клетку, а взаимодействует с рецептором на поверхности мембраны. Далее, возможны два варианта событий: 1. Первый вариант – с рецептором связан фермент, который из специфического субстрата образует второй посредник. Второй посредник далее связывается со своим рецептором в клетке. Чаще всего рецептором посредника является протеинкиназа, которая за счет фосфата АТФ, фосфорилирует белки. В результате изменяются их свойства, возникает биохимический и физиологический эффект. 2. Второй вариант – рецептор связан не с ферментом мембраны, а с ионным каналом. При связывании гормона с рецептором, канал открывается, ион поступает в клетку и выполняет функции второго посредника. Хорошо изученными вторыми посредниками являются циклические нуклеотиды (цАМФ, цГМФ) и Ca2+. Механизм действия гормонов через цАМФ Когда соответствующий гормон связывается с рецептором, в мембране активируется фермент аденилатциклаза, который из АТФ образует цАМФ. цАМФ является аллостерическим активатором протеинкиназы, которая фосфорилирует белки и изменяет их свойства. Например, фосфорилирование фосфорилазы приводит к повышению ее активности, а фосфорилирование гликогенсинтетазы – к снижению. цАМФ расщепляется до АМФ фосфодиэстеразой. Содержание цАМФ в клетке увеличивают: глюкагон, катехоламины (через бета-рецепторы), антидиуретический гормон, гистамин (Н2-рецепторы), простагландин-Е, простациклин, тиреотропный гормон, АКТГ, холерный токсин. Содержание цАМФ в клетке снижают: ацетилхолин (М-холинорецепторы), катехоламины (H2-рецепторы), соматостатин, ангиотензин-II, опиаты, коклюшный токсин. Функции цАМФ Как второй посредник участвует в регуляции: проницаемости мембран; синтеза макромолекул; активности ферментов; процессов деления; в нейронах – увеличения возбудимости; в сердце – стимуляции; в гладких мышцах – расслабления; в железах – увеличения секреции изменения иммунных реакций; дезагрегации тромбоцитов. Механизм действия гормонов через Са2+ Когда гормон связывается с рецептором, в мембране открывается кальциевый канал. В результате содержание кальция в клетке возрастает. Кальций связывается с белком клеток – кальмодулином, образуется комплекс, который может действовать непосредственно на белки, вызывая эффекты, или действовать на кальмодулин-зависимую протеинкиназу. Эта протеинкиназа фосфорилирует белки, в результате изменяются их свойства. Са2+ в качестве второго посредника выполняет те же функции, что и цАМФ, за исключением того, что в гладких мышцах вызывает сокращение, тромбоцитах – агрегацию. Содержание кальция в клетке повышают: катехоламины через 1-рецепторы, ацетилхолин через М-холинорецепторы, гистамин через Н1-рецепторы, тромбоксан, ангиотензин-II. 3. Какие механизмы внутриклеточной регуляции вы знаете? Расскажите об аденилатциклазной системе передачи сигнала. Какие гормоны ее используют? Все механизмы передачи гормонального сигнала условно можно разделить на 3 группы: Механизм передачи сигнала путем образования вторичных посредников (мессенджеров): Аденилатциклазная система, Гуанилатциклазная система, Инозитолфосфатная система Механизм передачи сигнала путем активации киназной активности рецептора Механизм передачи сигнала через внутриклеточные рецепторы Аденилатциклазная система передачи гормонального сигнала 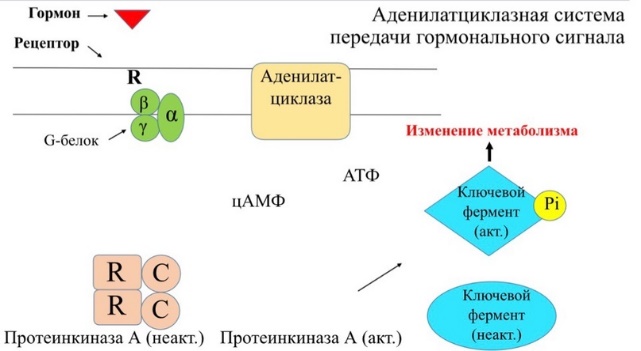 Вторичный посредник (мессенджер) — циклический АМФ (цАМФ) Гормоны, использующие аденилатциклазную систему: Адреналин (через Бетта-адренорецепторы), Глюкагон, Адренокортикотропный гормон (АКТГ), Паратгормон, Тиреотропный гормон (ТТГ), Лютеинизирующий гормон (ЛГ), Меланоцит-стимулирующий гормон (МСГ), Дофамин, Антидиуретический гормон (через V2-рецепторы) 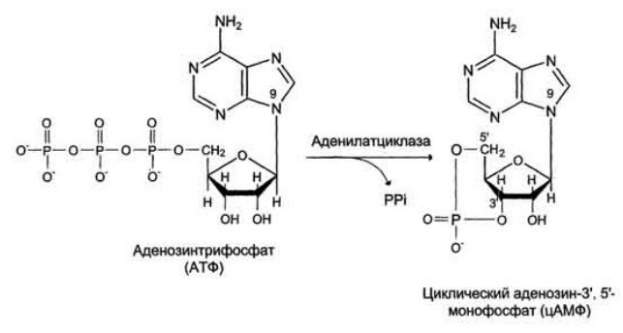 Пример: Адреналин — гормон, выделяющийся надпочечниками при стрессе. Глюкагон — гормон, выделяющийся поджелудочной железой при голодании. Оба гормона повышают уровень глюкозы в крови. Источник глюкозы крови при голодании и стрессе — печень. Глюкоза образуется в ходе процесса распада гликогена (гликогенолиза). Ключевой фермент распада гликогена — гликогенфосфорилаза. 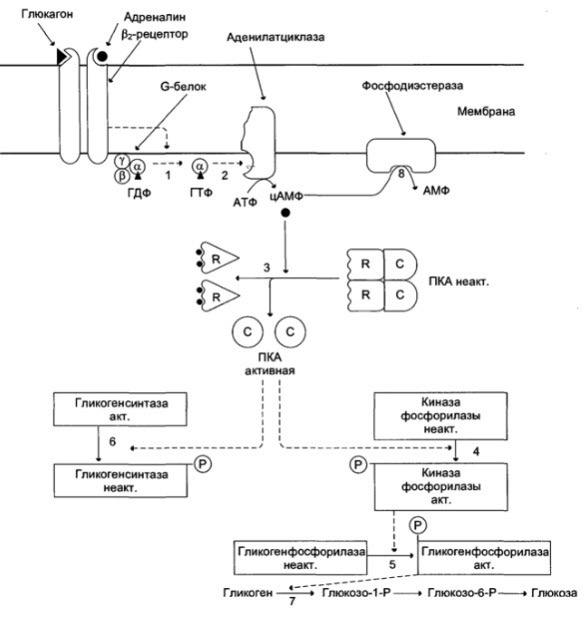 4. Какие механизмы внутриклеточной регуляции вы знаете? Расскажите о гуанилатциклазной системе передачи сигнала. В каких процессах она используется? Все механизмы передачи гормонального сигнала условно можно разделить на 3 группы: Механизм передачи сигнала путем образования вторичных посредников (мессенджеров): Аденилатциклазная система, Гуанилатциклазная система, Инозитолфосфатная система Механизм передачи сигнала путем активации киназной активности рецептора Механизм передачи сигнала через внутриклеточные рецепторы Гуанилатциклазная система передачи гормонального сигнала 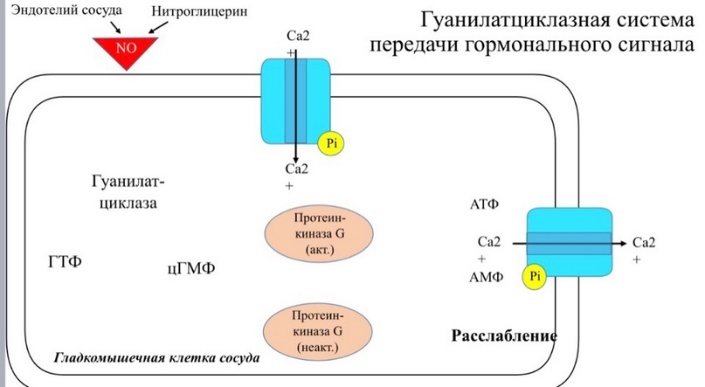 Вторичный посредник (мессенджер) — циклический ГМФ (цГМФ) Гормоны, использующие гуанилатциклазную систему: Предсердный натрийуретический гормон (пептид/фактор), Оксид азота (NО) 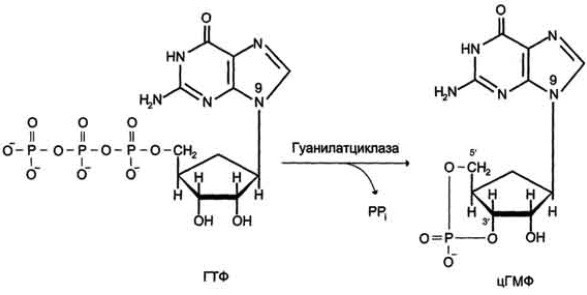 5. Какие механизмы внутриклеточной регуляции вы знаете? Расскажите о инозитолфосфатной системе передачи сигнала. Какие гормоны ее используют? Все механизмы передачи гормонального сигнала условно можно разделить на 3 группы: Механизм передачи сигнала путем образования вторичных посредников (мессенджеров): Аденилатциклазная система, Гуанилатциклазная система, Инозитолфосфатная система Механизм передачи сигнала путем активации киназной активности рецептора Механизм передачи сигнала через внутриклеточные рецепторы Инозитолфосфатная система передачи гормонального сигнала 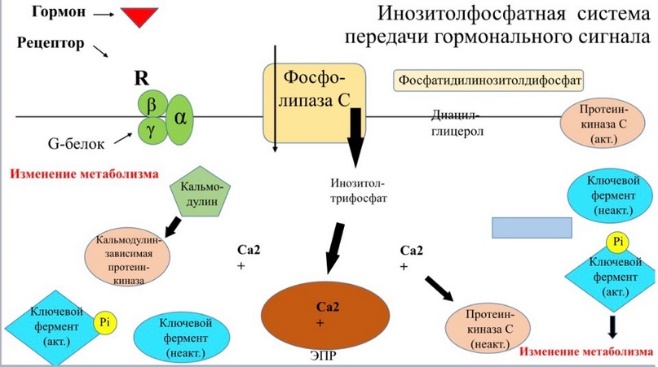 Вторичный посредник (мессенджер) — инозитолтрифосфат, диацилглицерол, Са2+ Гормоны, использующие инозитолфосфатную систему: Адреналин (через Альфа1-адренорецепторы), Ангиотензин II, Вазопрессин (через V1-рецепторы), Ацетилхолин (через М1-рецепторы), Гистамин (через Н1-рецепторы), Серотонин, Тиреолиберин, Гонадолиберин, Окситоцин 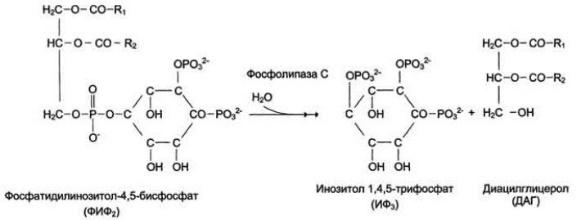 Пример: Адреналин — гормон, выделяющийся надпочечниками при стрессе. Повышает уровень глюкозы в крови путем активации ключевого фермента распада гликогена — гликогенфосфорилазы. Вызывает увеличение ЧСС, сокращение гладкой мускулатуры сосудов (вазоконстрикция) за счет повышения концентрации Са2+ в крови (Са2+ необходимый участник мышечного сокращения). 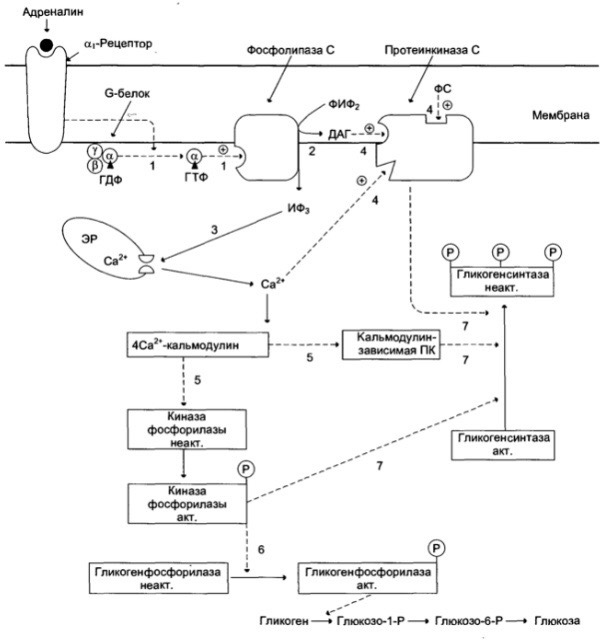 6. Расскажите о механизме действия гормонов через внутриклеточные рецепторы.   Механизм действия гормонов через внутриклеточные рецепторы. Механизм действия гормонов ч/з внутриклеточные регуляторы. Гормон проникает в клетку, связывается с рецептором. Образованный таким образом гормон-рецепторный комплекс перемещается в ядро и действует на генетический аппарат клетки. В результате меняется процесс транскрипции, а в дальнейшем, синтез белков. Таким образом, данные гормоны влияют на количество ферментов в клетке. 7. Как регулируется выработка периферических гормонов через гипоталамус-гипофиз? Когда концентрация периферического гормона в крови снижается, тогда из гипоталамуса выделяются либерины, которые действуют на гипофиз и стимулируют освобождение тропинов. Тропины действуют на периферические железы и усиливают освобождение из них гормонов, концентрация которых возрастает. Это фиксируется рецепторами гипоталамуса. Он прекращает освобождение либеринов, но усиливает выброс статинов, которые тормозят гипофиз. Белково - пептидные гормоны. 1. Либерины, статины, андидиуретический гормон, окситоцин – гормоны гипоталамуса. 2. Тропины (соматотропин, тиреотропин, кортикотропин, фоликулостимулирующий, лютеонизирующий, пролактин) – гормоны гипофиза. 3. Тиреокальцитонин – гормон щитовидной железы. 4. Паратгормон - гормон паращитовидной железы. 5. Тимозин – гормон тимуса. 6. Инсулин – гормон В-клеток поджелудочной железы. 7. Глюкагон – гормон А-клеток поджелудочной железы. 8. Гастрин, секретин, холецистокинин, энтерогастрон – гормоны ЖКТ. 9. Гормоны предсердий. 10. Факторы роста клеток, нервов, сосудов. 11. Ангиотензин-II, кинины – гормоны крови. Соматотропный гормон (СТГ, гормон роста) СТГ – простой белок (молекулярная масса 21000). Обладает высокой видовой специфичностью. СТГ выполняет следующие функции: 1. Стимулирует синтез белка на уровне транскрипции и трансляции; 2. Активирует триглицеридлипазу, окисление жирных кислот; 3. Стимулирует освобождение глюкагона, что приводит к гипергликемии. Выработку СТГ усиливает соматолиберин, снижает – соматостатин. Действие СТГ на клетки осуществляется через цАМФ и ростстимулирующие факторы (соматомедины). Патология, вызванная нарушением образования СТГ. 1. Акромегалия возникает при избыточном образовании СТГ у взрослого человека. Признаки: чрезмерный рост костей рук, ног и лица, мягких тканей носа, губ, подбородка, волос на теле. Акромегалия обычно обусловлена наличием опухоли аденогипофиза или снижением выработки статинов. 2. Гигантизм развивается при гиперсекреции СТГ у людей до завершения окостенения. Происходит общий чрезмерный рост скелета. 3. Гипофизарная карликовость (нанизм) наблюдается при гипосекреции СТГ в детском возрасте. Карлики обычно не имеют признаков деформации скелета, не страдают умственным недоразвитием. Рост взрослого человека 110-130 сантиметров. 8. АКТГ, место и условия образования, мишени, эффекты. Кортикотропин (АКТГ) — пептидный гормон; состоит из 39 аминокислотных остатков; синтезируется в клетках передней доли гипофиза под влиянием кортиколиберина (синтезируется кортикотрофами аденогипофиза.) Активаторы секреции: Кортиколиберин, стресс (физический и психологический), гипогликемия, гипоксия, боль, травмы. Ингибиторы секреции: АКТГ, глюкокортикостероиды. Мишень: Кора надпочечников Кортикотропин секретируется в импульсивном режиме. Скорость секреции составляет 5-25 мкг/сут. При стрессе концентрация АКТГ в крови возрастает во много раз. У здоровых людей наименьший уровень АКТГ в крови отмечается в конце дня и непосредственно перед сном. Т1/2 в крови составляет 15 — 25 мин. Механизм действия АКТГ включает взаимодействие с рецептором плазматической мембраны клеток, активацию аденилатциклазы и фосфорилирование белков. Эти эффекты усиливаются в присутствии ионов Са2+. В клетках коры надпочечников АКТГ стимулирует гидролиз эфиров холестерола, увеличивает поступление в клетки холестерола в составе ЛПНП; стимулирует превращение холестерола в прегненолон; индуцирует синтез митохондриальных и микросомальных ферментов, участвующих в синтезе кортикостероидов. Функция: Стимулирует рост надпочечников и синтез кортикостероидов. Стимуляция секреции глюкокортикостероидов, минералокортикоидов и половых стероидов (в меньшей степени). Избыток: Болезнь Иценко-Кушинга Недостаток: Болезнь Аддисона. 9. ТТГ, место и условия образования, мишени, эффекты. Тиреотропин (ТТГ) синтезируется в тиреотрофных клетках передней доли гипофиза (аденогипофиза). состоит из 2 субъединиц; α-субъединицы всех 4 гормонов идентичны; β-субъединицы различаются первичной структурой, строением олигосахаридных фрагментов и участков гпикозипирования и определяют биологическую активность; α- и β-субъединицы содержат опигосахаридные фрагменты. Стимуляция секреции тиреотропина происходит под влиянием тиреолиберина, эстрагенов и холода, а основное ингибирующее действие оказывает повышение уровня тиреоидных гормонов, а так же соматостатинов. Пик секреции ТТГ отмечается в часы, непосредственно предшествующие сну, с последующим снижением в течение ночи. Мишень: Щитовидная железа Основная биологическая функция тиреотропина — стимуляция синтеза и секреции йодтиронинов (Т3 и Т4) в щитовидной железе. Трансдукция сигнала тиреотропина в клетки щитовидной железы происходит через рецепторы плазматической мембраны и активацию аденилатциклазы. Рецептор тиреотропина состоит из 2 доменов, один из которых представляет собой гликопротеин, а второй — ганглиозид (гликолипид, содержащий сиаловую кислоту). Для проявления биологического действия необходимо связывание тиреотропина с обоими доменами рецептора. Тиреотропин оказывает на щитовидную железу 2 типа эффектов. Одни проявляются быстро (в течение нескольких минут) и включают стимуляцию всех стадий синтеза и секреции йодтиронинов. Проявление других требует нескольких дней. К ним относят стимуляцию синтеза белков, фосфолипидов, нуклеиновых кислот, увеличение размеров и количества тиреоидных клеток. Избыток: приводит к избытку тиреоидных гормонов (гипертиреоз). Недостаток: приводит к недостатку тиреоидных гормонов (гипотиреоз). 10. ЛГ и ФСГ, место и условия образования, мишени, эффекты. Гонадотропные гормоны: ФолликулоСтимулирующийГ, ЛютеинзирующийГ — гликопротеины, состоящие из 2 субъединиц; α-субъединицы всех 4 гормонов идентичны 96 а/к; β-субъединицы (из 121 а/к у ЛГ, 120 у ФСГ) различаются первичной структурой, строением олигосахаридных фрагментов и участков гпикозипирования и определяют биологическую активность; α- и β-субъединицы содержат опигосахаридные фрагменты. Синтезируется гонадотрофами аденогипофиза. Мишень: половые железы (яичники и яички) Активаторы секреции: Гонадолиберин. Ингибиторы секреции: тестостерон (ингибирует выработку ЛГ), эстрогены, ингибин (секретируется клетками Сертоли) ингибируют выработку ФСГ. Функции ЛГ: У женщин индуцирует овуляцию У мужчин индуцирует синтез андрогенов в клетках Лейдига ФСГ: У женщин стимулирует рост фолликулов У мужчин стимулирует сперматогенез 11. СТГ, место синтеза, механизм действия, регуляция синтеза. СТГ- это пептидный гормон, вырабатываемый в передней доле гипофиза. Место синтеза: аденогипофиз (передняя доля гипофиза), а точнее - специальная разновидность хромофильных ацидофильных клеток - соматотрофы, накапливающие данный гормон в виде гранул внутри своей цитоплазмы. Механизм действия: СТГ связывается с рецептором на мембране клетки-мишени, происходит димеризация рецептора и его активация. После этого включаются внутриклеточные процессы фосфорилирования рецептора: выработка ДАГ (1,2-диацилглицерола) и активация протеинкиназы С (ПКС). Рецептор, связанный с тирозинкиназной активностью. Существенную роль в рост-стимулирующих эффектах гормона играет инсулиноподобный фактор роста-1 (ИФР-1, соматомедин С), вырабатываемый в клетке после воздействия на нее СТГ. Вызывает положительный азотистый баланс, повышает транспорт аминокислот в печень, мышечную, хрящевую и костную ткани, активирует все стадии биосинтеза белка. Рост-активирующее действие гормона на кости и мышцы наиболее отчетливо проявляется в детском и подростковом возрасте. ТГ стимулирует гидроксилирование и активацию витамина D в почках. Формирует положительный баланс ионов Mg2+, Ca2+, Na+, К+, Cl–, SO42–, фосфатов. Активирует липолиз, что вызывает накопление жирных кислот в крови и, при недостатке инсулина, кетогенез. В целом СТГ переводит ткани на использование жирных кислот. Регуляция синтеза: Активируют: 1)гипогликемия (при физической нагрузке и кратком голодании), 2)гормоны – эстрогены и андрогены, трийодтиронин (особенно у детей, через высвобождение соматолиберина), вазопрессин, инсулин, 3)медленная фаза сна (вскоре после засыпания, особенно у детей). Уменьшают: гипотиреоз, глюкокортикоиды, ИФР-1, соматостатин, свободные жирные кислоты. Дополнительно можно назвать гипергликемию, ожирение, β-адреномиметики. 12. Перечислите основные эффекты СТГ. Объясните их. Соматотропный гормон (СТГ, гормон роста) СТГ – простой белок (молекулярная масса 21000). Обладает высокой видовой специфичностью. СТГ выполняет следующие функции: Стимулирует синтез белка на уровне транскрипции и трансляции; Активирует триглицеридлипазу, окисление жирных кислот; Стимулирует освобождение глюкагона, что приводит к гипергликемии. Выработку СТГ усиливает соматолиберин, снижает – соматостатин. Действие СТГ на клетки осуществляется через цАМФ и ростстимулирующие факторы (соматомедины). Основные эффекты СТГ являются анаболическими, связаны со стимуляцией синтеза белка. Рецептор, связанный с тирозинкиназной активностью. Существенную роль в рост-стимулирующих эффектах гормона играет инсулиноподобный фактор роста-1 (ИФР-1, соматомедин С), вырабатываемый в клетке после воздействия на нее СТГ. Вызывает положительный азотистый баланс, повышает транспорт аминокислот в печень, мышечную, хрящевую и костную ткани, активирует все стадии биосинтеза белка. Рост-активирующее действие гормона на кости и мышцы наиболее отчетливо проявляется в детском и подростковом возрасте. ТГ стимулирует гидроксилирование и активацию витамина D в почках. Формирует положительный баланс ионов Mg2+, Ca2+, Na+, К+, Cl–, SO42–, фосфатов. Активирует липолиз, что вызывает накопление жирных кислот в крови и, при недостатке инсулина, кетогенез. В целом СТГ переводит ткани на использование жирных кислот 13. Какие патологии, связанные с выработкой СТГ, вы знаете? Гипофункция 1. При снижении синтеза СТГ и его концентрации в крови возникает гипофизарный нанизм (карликовость). Проявляется в раннем детстве (на 1-4 году), критерием служит снижение скорости роста до 4 см в год и менее. 2. При наличии в мишеневых клетках дефектов рецепторной и пострецепторной передачи сигнала (резистентность к СТГ) развивается синдром Ларона (карликовость Ларона, частота 0,5-1 на 1 млн). Концентрация СТГ при этом высока из-за отсутствия обратной отрицательной связи со стороны ИФР-1. 3. При наследственном уменьшении в клетках продукции ИФР-1 снижаются рост-стимулирующие эффекты гормона – тело развивается пропорционально, но недостаточно. Примером выраженной нехватки ИФР-1 могут служить пигмеи, племена Центральной Африки. 4. При нарушении синтеза у взрослых отмечается снижение мышечной массы и тенденция к гипогликемии. Гиперфункция возникает в результате аденомы гипофиза или СТГ-продуцирующей опухоли гипофиза (соматотрофинома), также вследствие избыточной секреции соматолиберина. У детей – гигантизм, так как еще нет зарастания эпифизарных щелей и возможен ускоренный рост кости. Происходит общий чрезмерный рост скелета. У взрослых – акромегалия. Происходит непропорциональное увеличение костей у взрослых (увеличение кистей и стоп, носа и нижней челюсти, промежутки между зубами), огрубление черт лица. Из-за роста мягких тканей возникают толстые кожные складки, лобные и носогубные морщины. Акромегалия обычно обусловлена наличием опухоли аденогипофиза или снижением выработки статинов. 14. Расскажите о месте синтеза, химической природе, мишенях, регуляции секреции и механизме действия глюкагона. Глюкагон — одноцепочечный полипептид, состоящий из 29 аминокислотных остатков. Биосинтез глюкагона происходит в α-клетках островков Лангерганса, в нейроэндокринных клетках кишечника и в некоторых отделах ЦНС. Неактивный предшественник проглюкагон в результате частичного протеолиза превращается в несколько пептидов. В клетках поджелудочной железы главный пептид — глюкагон; в клетках кишечника образуются глюкагоноподобные пептиды: GLP-1, GLP-2, глицентин и другие. GLP-1 ингибирует секрецию глюкагона и стимулирует синтез и секрецию инсулина. На секрецию глюкагона влияют и многие другие соединения, включая аминокислоты, жирные кислоты, кетоновые тела и нейромедиаторы. В плазме крови глюкагон не связан с каким-либо транспортным белком. Т1/2 гормона составляет 5 мин. В печени глюкагон быстро разрушается под действием специфических протеаз. Основные клетки-мишени глюкагона — печень и жировая ткань. 15. Перечислите основные эффекты глюкагона на углеводный, липидный и белковый обмен. Эффекты глюкагона в основном противоположны эффектам инсулина. Основные клетки-мишени глюкагона — печень и жировая ткань. Связываясь с рецепторами на плазматической мембране клеток-мишеней, глюкагон повышает содержание цАМФ. В гепатоцитах это приводит к активации фосфорилазы гликогена и к снижению активности гликоген- синтазы. В результате ускоряется мобилизация гликогена. Фосфорилирование пируваткиназы и БИФ вызывает торможение гликолиза и ускорение глюконеогенеза. Кроме того, глюкагон стимулирует глюконеогенез, индуцируя синтез ферментов: глюкозо-6-фосфатазы, фосфоенол- пируваткарбоксикиназы, фруктозо-1,6-бисфосфатазы. В клетках жировой ткани глюкагон через аденилатциклазный каскад активирует гормончувствительную ТАГ-липазу и стимулирует липолиз . Таким образом, в противоположность инсулину глюкагон стимулирует мобилизацию основных энергоносителей — углеводов и жиров. 16. Дайте характеристику инсулину (химическая природа, активация, место синтеза, регуляция секреции, мишени, механизм действия) Инсулин — полипептид, состоящий из двух полипептидных цепей (А и В). Обе цепи соединены между собой двумя дисульфидными мостиками. Инсулин может существовать в нескольких формах: мономера, димера и гексамера. Гексамерная структура инсулина стабилизируется ионами цинка Биосинтез инсулинавключает образование двух неактивных предшественников, препроинсулина и проинсулина, которые в результате последовательного протеолиза превращаются в активный гормон. Биосинтез препроинсулина начинается с образования сигнального пептида на полирибосомах, связанных с ЭР. Проинсулин поступает в аппарат Гольджи, где под действием специфических протеаз расщепляется в нескольких участках с образованием инсулина и С-пептида Инсулин и С-пептид включаются в секреторные гранулы. В гранулах инсулин соединяется с цинком, образуя димеры и гексамеры. Зрелые гранулы сливаются с плазматической мембраной, и инсулин и С-пептид секретируются во внеклеточную жидкость в результате экзоцитоза. После секреции в кровь олигомеры инсулина распадаются. Разрушение инсулина происходит под действием фермента инсулиназы в основном в печени и в меньшей степени в почках. Регуляция синтеза и секреции инсулина. Глюкоза — главный регулятор секреции инсулина, а β-клетки ПЖ — наиболее важные глюкозо-чувствительные клетки в организме. Глюкоза регулирует экспрессию гена инсулина. При стимуляции глюкозой инсулин быстро освобождается из секреторных гранул, что сопровождается активацией транскрипции мРНК инсулина. Синтез и секреция инсулина не являются строго сопряжёнными процессами. Синтез гормона стимулируется глюкозой, а секреция его является Са 2+-зависимым процессом и при дефиците Са2+ снижается даже в условиях высокой концентрации глюкозы, которая стимулирует синтез инсулина. На секрецию инсулина влияют другие гормоны. Адреналин через α2-рецепторы тормозит секрецию инсулина даже на фоне стимуляции глюкозой, β-адренергические агонисты её стимулируют, вероятно, в результате повышения концентрации цАМФ. Этот механизм, полагают, лежит в основе действия гормонов ЖКТ, таких как секретин, холецистокинин и желудочный ингибирующий пептид (GIP), которые повышают секрецию инсулина. Высокие концентрации гормона роста, кортизола, эстрогенов также стимулируют секрецию инсулина. Механизм действия инсулина, клетки-мишени Действие инсулина начинается с его связывания со специфическим гликопротеиновым рецептором на поверхности клетки-мишени. Рецепторы инсулина обнаружены почти во всех типах клеток, но больше всего их в гепатоцитах и клетках жировой ткани. Инсулиновый рецептор (IR) постоянно синтезируется и разрушается. Т1/2 рецептора составляет 7 — 12 ч. Снижение чувствительности клеток к гормону опосредуется 2 механизмами. Первый включает утрату рецепторов путём их интернализации. Комплекс инсулин-рецептор захватывается внутрь клетки эндоцитозом. В результате интернализации часть рецепторов подвергается разрушению в лизосомах, а часть возвращается в плазматическую мембрану. Второй механизм десенситизации — ковалентная модификация рецептора в результате фосфорилирования. Так, фосфорилирование IR по остаткам серина и треонина снижает его сродство к инсулину. Рецептор инсулина относят к типу рецепторов, обладающих тирозинкиназной активностью. Стимулированное инсулином аутофосфорилирование β-субъединицы IR по остаткам тирозина приводит к фосфорилированию других внутриклеточных белков — субстратов инсулинового рецептора (IRS). Известно несколько таких субстратов: IRS-1, IRS-2, а также некоторые белки семейства STAT. Главную роль в формировании ответной реакции клетки на инсулиновый сигнал играет IRS-1. IRS-1 — фосфопротеин, состоящий из более чем 1200 аминокислотных остатков. Часть остатков серина, тирозина и треонина фосфорилирована. При стимуляции инсулином степень фосфорилирования IRS-1 увеличивается и придаёт ему способность соединяться с другими цитозольными белками. Это приводит к активации нескольких сигнальных путей, представляющих каскад реакций активации специфических протеинкиназ. В результате активации протеинкиназ происходит фосфорилирование ферментов и факторов транскрипции, что составляет основу многочисленных эффектов инсулина. 17. Как инсулин влияет на обмен углеводов, липидов, белков? Влияние инсулина на углеводный обмен: Увеличивает проницаемость клеточных мембран для глюкозы; индуцирует синтез глюкокиназы, тем самым ускоряет фосфорилирование глюкозы в клетке; повышает активность и количество ключевых ферментов гликолиза (фосфофруктокиназы, пируваткиназы), стимулирует синтез гликогена за счет активации гликогенсинтазы и уменьшает распад гликогена; ингибирует глюконеогенез, подавляя синтез ключевых ферментов глюконеогенеза; повышает активность пентозофосфатного пути. Влияние инсулина на метаболизм липидов: ингибирует липолиз (распад триацилглицеролов) в жировой ткани и печени; стимулирует синтез триацилглицеролов в жировой ткани; активирует синтез жирных кислот; в печени ингибирует синтез кетоновых тел. Влияние инсулина на метаболизм белков: стимулирует транспорт аминокислот в клетки мышц, печени; активирует синтез белков в печени, мышцах, сердце и уменьшает их распад; стимулирует пролиферацию и число клеток в культуре и, вероятно, может участвовать в регуляции роста in vivo. 18. Какие типы сахарного диабета существуют? Причины. Различия. Диагностика. Диабет I типа (инсулинозависимый сахарный диабет) – аутоиммунное заболевание. Он возникает, если в результате каких-либо сбоев, происходящих в организме, иммунные клетки начинают воспринимать β-клетки поджелудочной железы как чужеродные элементы и уничтожать их. Подобная ситуация приводит к постепенной гибели β-клеток, из-за чего перестает синтезироваться инсулин – гормон, понижающий концентрацию глюкозы в крови. Главные причины диабета 1 типа – наследственная предрасположенность и перенесенные в детстве инфекционные заболевания (коревая краснуха, ветряная оспа, паротит, гепатит). ИЗСД проявляется обычно в детском или подростковом возрасте. Начало заболевания обычно бурное, с развитием кетоацидоза и значительным повышением уровня глюкозы крови. Диабет II типа (инсулинНЕзависимый диабет) поджелудочная железа вырабатывает достаточное количество инсулина, но клетки организма теряют чувствительность к нему (инсулинорезистентность). Развивается в основном у людей среднего и старшего возраста, имеющих лишний вес. Основные причины болезни – наследственность, малоподвижный образ жизни, неправильное питание, частые стрессы. Следует знать, что 1 и 2 типы сахарного диабета не могут переходить друг в друга. В некоторых случаях при патологии 2 типа поджелудочная железа перестает вырабатывать инсулин из-за его неусвояемости клетками. В результате дополнительно развивается сахарный диабет 1 типа. Диагностика: Глюкозотолерантный тест, определение гликированного гемоглобина, Инсулин и С-пептид в крови 19. Как изменяется обмен углеводов, липидов и белков при сахарном диабете? Нарушения обмена углеводов: 1. Гипергликемия, которая возникает в результате: а) снижения проницаемости клеточных мембран для глюкозы. Глюкоза накапливается в крови. б) усиления процессов, поставляющих глюкозу в кровь (распад гликогена печени, глюконеогенез). в) торможение процессов, потребляющих глюкозу (синтез гликогена, гликолиз, пентозофосфатный путь). В норме концентрация глюкозы в крови составляет 3,3-5,5 ммоль/л, при сахарном диабете — 6,7 ммоль/л и выше, при 8,9 ммоль/л возникает глюкозурия. 2. Заторможен пентозофосфатный путь. В результате этого снижено образование НАДФН, что приводит к катаракте. 3. Гипергликемия вызывает неферментативное гликозилирование белков, в том числе белков клеточных мембран всех органов и систем, в первую очередь, сосудов. Возникают микроангиопатии (ранний признак сахарного диабета). Нарушения обмена липидов: Нарушения обмена липидов характерны для инсулинзависимого диабета. 1. Усиливается липолиз, в крови повышается концентрация НЭЖК. Больные в этом случае худеют. 2. Усиливается окисление жирных кислот и образование ацетил-КоА. 3. Возрастает синтез кетоновых тел, накопление которых опасно, так как приводит к метаболическому ацидозу. 4. Возрастает синтез холестерина, что является фактором риска для развития атеросклероза. 5. Увеличивается содержание атерогенных липопротеидов, снижается содержание антиатерогенных. 6. Усиливается перекисное окисление липидов. Нарушения обмена белков: 1. Увеличивается синтез гликопротеидов. 2. Усиливается распад белков, синтез мочевины, возрастает остаточный азот. 20. Назовите и объясните осложнения при сахарном диабете. Осложнения при сахарном диабете 1. Полиурия и полидипсия. 2. Диабетическая кома. Признаки: гипергликемия (14-16 ммоль/л), резкое увеличение содержания кетоновых тел, повышение уровня холестерина, ЛПНП, рН крови сдвигается до 6,8. Это приводит к снижению связанности инсулина с рецептором. 3. Ангиопатии (микро- и макро -). Микроангиопатия сосудов сетчатки глаза снижает остроту зрения, микроангиопатия сосудов почек приводит к тяжелой почечной недостаточности. Макроангиопатия — нарушение крупных сосудов — характеризуется атеросклерозом, поражением сосудов нижних конечностей. 4. Гиперосмолярная кома возникает при концентрации глюкозы в крови 50-60 ммоль/л. В результате повышается осмотическое давление крови, что приводит к обезвоживанию организма. 5. Гипогликемическая кома может возникнуть при передозировке инсулина. Диагностика сахарного диабета. Различают: преддиабет, латентный диабет и явный диабет (легкий и тяжелый). Наличие диабета определяют по содержанию глюкозы в крови. Для диагностики сопутствующих заболеваний определяют содержание холестерина, ЛПНП (наличие атеросклероза), сиаловых кислот (наличие воспаления), кетоновых тел (диабетическая кома). При латентном диабете проводят пробу с сахарной нагрузкой. 21. Назовите отделы симпато-адреналовой системы и катехоламины, которые в них образуются. Перечислите эффекты катехоламинов в центральном отделе симпато-адреналовой системы. Катехоламины: Образуются из тирозина в клетках хромаффинной ткани. Для синтеза требуются: тирозин, S-аденозилметионин (активный метионин), витамины РР, С и В6. К катехоламинам относятся: ДОФамин (диоксифениламин), норадреналин и адреналин. В центральном отделе симпатоадреналовой системы (головной мозг) образуются дофамин (ДА) и норадреналин (НА). В медиаторном отделе (окончания симпатических нервов) образуется норадреналин. В гормональном отделе симпатоадреналовой системы (мозговое вещество надпочечников) образуется адреналин (А). Дофамин выполняет следующие функции: Является тормозным модулятором головного мозга. Тормозит эффекты ацетилхолина. При недостатке дофамина возникает паркинсонизм. Симптомы паркинсонизма: скованная походка, маскообразное лицо, дрожание конечностей;При избытке дофамина возникают некоторые формы шизофрении;Дофамин тормозит выделение гормонов аденогипофиза. Функции норадреналина: Тормозной модулятор. Участвует в центральной регуляции кровяного давления и дыхания. Тормозит мозговое вещество надпочечников и изменяет деятельность коры надпочечников, регулирует эндокринные железы. Стимулирует умственную работоспособность и запоминание. Стимулирует высшие чувства: эмоции, поведение, мышление. Через α1-адренорецепторы катехоламины вызывают сокращение мышц, в том числе сердца, сосудов, матки, ЖКТ, расширение зрачка, повышают артериальное давление Через α2- рецепторы катехоламины повышают агрегацию тромбоцитов, снижают освобождение норадреналина и ацетилхолина. Через β1-рецепторы катехоламины стимулируют липолиз, окислительно-восстановительные процессы, работу сердца, расслабляют гладкие мышцы ЖКТ. Через β2-рецепторы катехоламины расслабляют гладкие мышцы сосудов, бронхов, матки, усиливают распад гликогена в мышцах. 22. Напишите в формулах синтез катехоламинов. Дайте понятие о депонировании, мобилизации и метаболизме катехоламинов.  Депонирование - это накопление катехоламинов в везикулах-депо. После синтеза молекулы катехоламинов накапливаются в ВЕЗИКУЛАХ (пузырьках, окружённых мембраной, секреторных гранулах), в которых хранятся до тех пор, пока не понадобится секреция данного катехоламина. Эти везикулы выполняют функцию запасных депо катехоламинов. Как происходит поступление молекул катехоламинов в везикулы? Молекулы катехоламинов поступают внутрь «пузырьков» (секреторных гранул) с помощью специальных белков, против градиента концентрации катехоламинов. Мобилизация (в инете не могу найти шо это таке) Мобилизация (освобождение) катехоламинов происходит под влиянием нервного импульса. Метаболизм катехоламинов – это реакции, в которые вступают катехоламины (уже после своего синтеза). В результате этих реакций катехоламины превращаются в неактивные вещества, то есть метаболизм приводит к инактивации катехоламинов и именно для этой инактивации и нужен. Значение метаболизма катехоламинов – оно инактивирует катехоламины, что позволяет организму быстро снизить концентрацию катехоламинов в крови или синапсах, что предотвращает избыточное влияние катехоламинов на организм, в том числе предотвращает патогенное действие катехоламинов: например, защищает сердце от повреждения катехоламинами. 23. Перечислите биохимические эффекты катехоламинов на углеводный, липидный и белковый обмен. 1. Увеличивают потребление кислорода (калоригенный эффект). 2. Повышают концентрацию глюкозы в крови за счет усиления распада гликогена в печени и глюконеогенеза. 3. Адреналин усиливает гликогенолиз в мышцах, что, приводит к гиперлактатемии 4. Усиливают липолиз, окисление жирных кислот, синтез кетоновых тел и холестерина. 5. Способствуют распаду белка, усиливают дезаминирование аминокислот, синтез мочевины, повышают остаточный азот. 24. Какие адренорецепторы вы знаете? При воздействии на них, через какие посредники передается сигнал? Какие эффекты достигаются? Адренорецепторы — рецепторы к адренергическим веществам (Адренергические средства, или адреномиметики, имитируют действие норадреналина или адреналина, взаимодействуя и возбуждая адренорецепторы). Реагируют на адреналин и норадреналин. Различают несколько групп рецепторов, которые различаются по опосредуемым эффектам, локализации, а также аффинитету к различным веществам: α1-, α2-, β1-, β2, β3-адренорецепторы.
Эффекты катехоламинов при действии на разные типы рецепторов: α1-адренорецепторы (инозитолфосфатная система, Са2+) – сокращение сосудов, ↑АД α2-адренорецепторы (аденилатциклазная система, ингибирование) – ↓ АД β1-адренорецепторы (аденилатциклазная система, активация) - ↑ЧСС β2-адренорецепторы (аденилатциклазная система, активация) – расширение бронхов, ↑ распад гликогена β3-адренорецепторы (аденилатциклазная система, активация) - ↑ липолиз, теплопродукция 25. Какие стероидные гормоны вы знаете? Где и как они синтезируются? Стероидные гормоны синтезируются из холестерина в коре надпочечников, клетках Лейдига семенников, в фолликулах и желтом теле яичников, а также в плаценте. Стероидные гормоны содержатся в составе липидных капель адипоцитов и в цитоплазме в свободном виде. В связи с высокой липофильностью стероидных гормонов относительно легко диффундируют через плазматические мембраны в кровь, а затем проникают в клетки-мишени. Гормоны коркового слоя надпочечников (кортикостероиды). Секретируются корковым веществом надпочечников. Специфическим стимулятором биосинтеза глюкокортикоидов является адренокортикотропный гормон гипофиза, а регуляторами биосинтеза альдостерона — ангиотензин, ионы К+ и Na+, серотонин. Минералокортикоиды (Альдостерон, а еще дезоксикортикостерон, кортикостерон) Глюкокортикоиды (Кортизол, а еще деоксикортизол, кортизон) Кальцитриол. Гормональные формы витамина D3 образуются в печени и почках из этого витамина, поступающего с пищей, под контролем паратгормона, кальцитонина, ионов Ca2+ и некоторых анионов. Основным физиол. эффектом гормональных форм витамина D3 является регуляция обмена кальция и фосфора, они обладают также антирахитическим действием. В клин, практике для лечения рахита используют витамины группы D — предшественники их гормональных форм. Гормоны половых желез (гонадостероиды) Андрогены (Тестостерон, а еще андростендиол, дигидротестостерон). Тестостерон синтезируется семенниками и яичниками под специфическим контролем лютеинизирующего гормона. В корковом веществе надпочечников под контролем АКТГ образуются малоактивные андрогены, способные отчасти активироваться в периферических тканях. Основные физиол. эффекты андрогенов: программирование вторичных половых признаков мужского пола и регуляция активности органов мужской половой сферы, общий анаболический эффект, антиэстрогенное действие. Эстрогены (Эстрадиол, а еще эстрон, эстриол). Эстрогены секретируются яичниками, плацентой и семенниками под контролем лютеинизирующего гормона и хорионического гонадотропина. Некоторая часть эстрогенов образуется на периферии из андрогенов. Основные физиол. эффекты эстрогенов: программирование и регуляция проявления вторичных женских половых признаков, стимуляция роста и развития женских половых органов и формирования белочной оболочки яйца, торможение оогенеза, сенсибилизация тканей к действию ряда гормонов, антиандрогенный эффект. Прогестогены (прогестины) (Прогестерон, а еще прегненолон, аллопрегненолон). Их биосинтез специфически стимулируется лютеинизирующим гормоном гипофиза и хорионическим гонадотропином плаценты. Основные физиол. эффекты прогестинов: стимуляция беременности, регуляция половых циклов, стимуляция оогенеза, формирование белочной оболочки яйца, дифференцировка молочных желез, антиандрогенное и антиэстрогенное действие, натрийуретический эффект. 26. Объясните механизм действия, физиологические и биохимические эффекты глюкокортикостероидов. Механизм передачи гормонального сигнала через внутриклеточные рецепторы 1. проникновение гормона через билипидный слой мембраны в клетку; 2. образуется комплекс гормон-рецептор, который перемещается в ядро клетки и взаимодействует с регуляторным участком: ДНК-энхансером или сайленсером; 3. при взаимодействии с энхансером увеличивается (при взаимодействии с сайленсером - уменьшается) доступность промотора для РНК-полимеразы; 4. соответственно увеличивается (уменьшается) скорость транскрипции структурных генов и скорость трансляции; 5. изменяется количество белков (в том числе ферментов), которые влияют на метаболизм и функциональное состояние клетки.  Белковый обмен: значительное повышение катаболизма белков в лимфоидной, эпителиальной, мышечной, соединительной и костной тканях. (получить гликогенные АК) Углеводный обмен: В целом вызывают повышение концентрации глюкозы крови: усиление мощности глюконеогенеза из кетокислот (за счет гликогенный АК, пришедших из мышц) за счет увеличения синтеза фосфоенолпируват-карбоксикиназы, увеличение синтеза гликогена в печени за счет активации фосфатаз и дефосфорилирования гликогенсинтазы, снижение проницаемости мембран для глюкозы в инсулинзависимых тканях. Липидный обмен: стимуляция липолиза (расщепление, много ЖК и глицерина) в жировой ткани благодаря увеличению синтеза ТАГ-липазы, что усиливает эффект АКТГ, СТГ, глюкагона, катехоламинов, т.е. кортизол оказывает пермиссивное действие. |
