конспект. Конспект по топливу. Конспект по топливу doc
 Скачать 1.79 Mb. Скачать 1.79 Mb.
|
Воспламенение технических газов с инертными примесями.Для инертных газов пределы воспламенения определяются по ранее приведённой зависимости Ле-Шателье с учётом экспериментальных данных по зависимости пределов воспламенения от содержания балластных компонентов. При этом формулу Ле-Шателье записывают с расшифровкой: 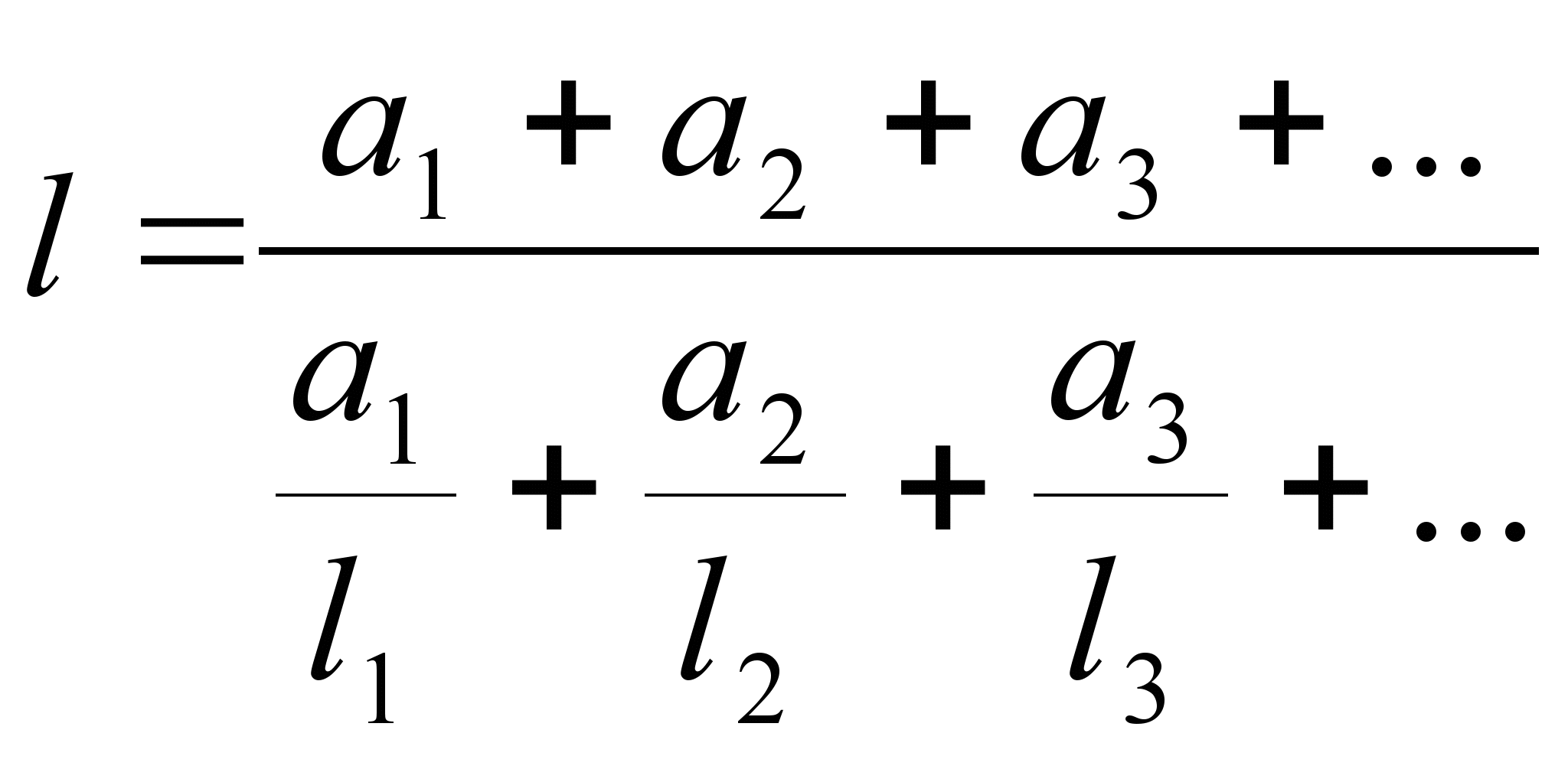 , ,(а1 + а2 + а3) ≠ 100% Экспонента зависимости предела воспламенения в зависимости от балластных примесей получены на основе экспериментальных данных и приведены в специальных справочниках. По этим графикам можно определить количество присутствующего инертного газа или который необходимо подмешать к горючему, чтобы данная смесь не воспламенилась. Чтобы определить пределы воспламенения газа, содержащего инертные примеси, необходимо сгруппировать горючие компоненты с инертными примесями попарно и для каждой пары определить пределы воспламенения пользуясь зависимостью вышеприведённых графиков. Затем, по формуле Ле-Шателье определить пределы воспламенения сложного газа. 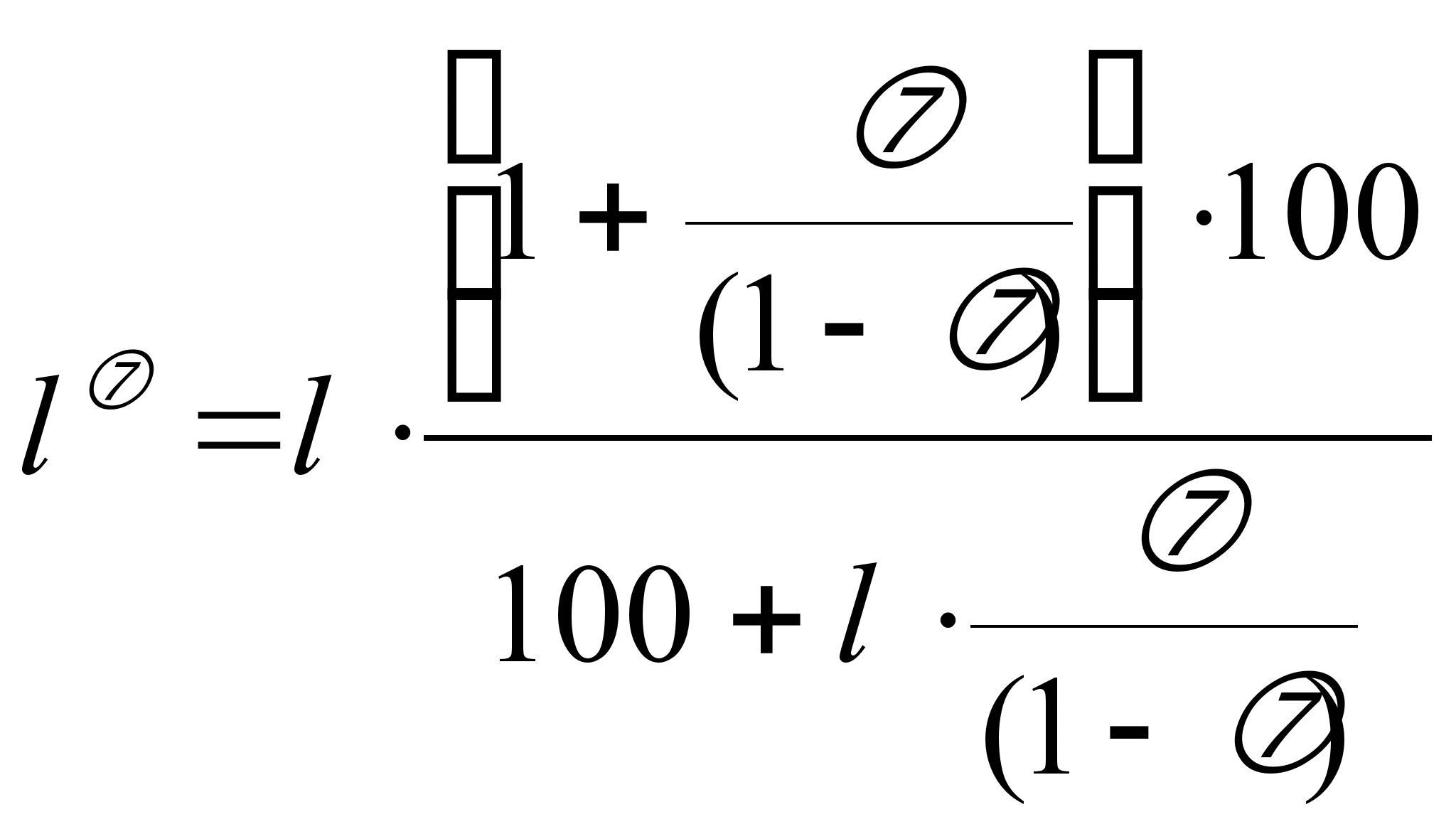 , ,δ = СО2 + N2, где lδ – верхний или нижний предел воспламенения с наличием балласта. ^ Альтернативное топливо1.Необходимость использования альтернативного топливаВозрастающая выработка и потребление электроэнергии, транспорт, промышленность требуют всё большего количества ископаемого топлива, природные запасы которого ограничены. В настоящее время имеются чёткие научнообоснованные расчёты, показывающие, когда человечество их исчерпает. Анализ доказывает, что основные источники энергии на планете по самым позитивным подсчётам имеют довольно чёткие сроки истощения ресурсов. Они могут быть неточными, но сам факт их существования вызывает тревогу: Эра дешёвого топлива кончается. За ним приходится отправляться в малообжитые и труднодоступные районы. Сегодня каждая пятая тонна нефти добывается с морского дна, а к 2050 г. эта цифра увеличится до трёх тонн. К проблеме дефицитности топлива добавляется проблема экологическая, связанная с засорением биосферы. Процессы горения топлива в теплосиловых установках осуществляются за сравнительно короткие промежутки времени, в течении которого не представляется возможным до конца осуществить окисление химических реакций. Образуются токсичные продукты неполного сгорания топлива, среди них следует выделить СО, альдегиды СНО, несгоревшие углеводороды СН, сажа С, оксиды азота (NО)х, соединения серы с кислородом (SOx) и водородом (H2S), соединения свинца в случае применения в качестве антидетонационной присадки тетраэтилсвинца. При горении топлива из атмосферы потребляется большое количество кислорода, необходимого для жизнедеятельности (автомобиль «Жигули» за 1000 км пробега уничтожает столько же кислорода, сколько человеку необходимо в год). В связи с этим программой ООН в настоящее время получили широкое развитие исследования, направленные на снижение потребления нефтяных видов топлива и увеличению использования альтернативных видов топлива. Решение этой проблемы весьма сложно, так как новое горючее должно удовлетворять следующим требованиям: -иметь необходимые сырьевые ресурсы -низкую стоимость -не ухудшать работу теплосиловых установок -как можно меньше загрязнять атмосферу -по возможности сочетаться со сложившейся системой снабжения топливом. На приведённой ниже схеме представлена классификация возможных альтернативных топлив. Данную классификацию можно разделить на две группы. К первой относятся нефтяные бензины, дизельное и котельное топливо с добавками растительных масел, твёрдого органического топлива, спиртов, эфиров, аммиака, водяных эмульсий. Ко второй группе относят топлива, не содержащие нефть и продукты её переработки. ^ Альтернативные смесевые топлива.Под альтернативными смесевыми топливами подразумевают такие традиционные топлива, примесь к которым из возобновляемых источников поможет продлить срок их использования. Как показывает практика сжигания смесевых топлив, они не требуют для этого процесса значительных переделок существующих двигателей внутреннего сгорания, а так же теплосиловых установок. Из этих видов топлив наиболее известен «газохол» – смесь бензина с 10 –20% этилового спирта (этанол). Газохол получил широкое распространение в Бразилии, где количество применяющихся автомобилей достигло 2.7 млн. шт. Для получения газохола используют дешёвый этанол, получаемый из сахарного тростника. Основным источником этанола служит восстанавливаемоё растительное сырьё (сахарный тростник, свекла, кукуруза, картофель и др.). При переработке этого сырья разложением и брожением получаются СН4 и этанол. По данным исследований учёных выход этанола с 1 га посадок сахарного тростника равен4400 литров, с 1 га сахарной свеклы – 2800 литров, с 1 га картофеля и кукурузы – 1664 и 830 литров соответственно. В странах с умеренным климатом производство из биомасс спиртового топлива ограничено. Так, если весь урожай сахарной свеклы ФРГ переработать в спиртовое топливо, то это составит 5.5% от общей потребности в топливе. Поэтому в Европе этанол получают из более дорогого сырья (природного газа, угля, горючих сланцев, и различных органических отходов). Добавки спиртов к бензину улучшают антидетонационные качества, повышает КПД двигателя и снижает в выхлопных газах содержание вредных веществ (СО и NxOy). Из недостатков этанола следует выделить низкую калорийность, отслоение от бензина при пониженной температуре и выпадении влаги. С дизельным топливом этанол не смешивается, однако с повышением молекулярной массы спиртов создание стабильных смесей становится более вероятным. Начиная с пропанола они смешиваются с дизельным топливом в любых пропорциях. В связи с этим возможно приготовление углеродоспиртовых смесей по следующей методике: смешивается метан с высокомолекулярными спиртами, а затем двухкомпонентная композиция растворяется в дизельном топливе. Подобное топливо было синтезировано со следующим составом: 50% дизельного топлива, 25% метилового и 25% изобутилового спиртов. При сравнении этого топлива с дизельным в 1.3 раза уменьшилось содержание углеводородов, в основном за счёт повышения содержания кислорода при постоянном содержании водорода. Метанол как присадку к дизельному топливу можно применять в газообразном виде. При этом метанол должен поступать сначала в в испаритель, а затем в каталитический реактор. Полученный синтез-газ может вводится в опускной трубопровод трубовоздуходувной системой дизельного двигателя с турбонаддувом. Исследования и практика эксплуатации теплосиловых установок показали, что применение добавок воды снижает токсичность продуктов сгорания и повышает эффективность самих установок. Исследования В ФРГ показали, что сгорание водно-магнитных эмульсий в топках КУ даёт следующие результаты: -Содержание сажи в уходящих газах снижается с 1-3% до 0-1%; -Содержание СО снижается с 0.001% до 0.0005%; -Содержание SO3 снижается с 10 мг/м3 до 7 мг/м3; -Содержание твёрдых частиц снижается с 91 мг/м3 до 7 мг/м3. Существует мнение, что присутствие воды присутствие воды в двигателях внутреннего сгорания нежелательно. Однако мнение о плохой работе ДВС на оводнённом топливе несправедливо. Всё зависит от того, в каком виде вода находится в топливе. Если она присутствует в виде отдельных скоплений т. е. в неорганизованном виде или неравномерно вводится в камеру сгорания, то это действительно вызывает перебои в работе двигателя. Вода в топливе не всегда является вредной механической примесью. Опытами с тяжёлокислородной водой было показано, что вода не только участвует в процессе теплообмена, отбирая часть тепла на своё испарение, парообразование и перегрев паров, но и участвует непосредственно в процессах горения, являясь активным участником горения углеводородного топлива. Поскольку вода и жидкое топливо взаимно нерастворимы, необходимо эти системы превратить в эмульсии механическим путём. Имеющиеся данные о влиянии воды справедливы и для сжигания мазута. Это связано с тем, что устойчивые водномазутные смеси (эмульсии) можно получить используя простейшие средства. Перспективными могут считаться также смеси топлива с размельчённым углём. При этом возможно создание стабильных суспензий с содержанием влаги 25 – 30%. Такие топлива следует рекомендовать для сжигания в топочных устройствах КУ и камерах сгорания газовых турбин. Снижение расхода нефтяных топлив за счёт смешивания с другими компонентами – это частичное решение проблемы. В перспективе человечеству придётся отказаться от нефти и перейти на другие альтернативные топлива. ^ Тепловой баланс камеры сжигания топливаТепловой баланс представляет собой равенство, левая часть которого представляет приходную часть, т. е. то тепло, которое расходуется на полезные и неполезные нужды: QpH + Qв + QT = Q1 + Q2 + Q3 + Q4 + Q5 + Q6 где Qв – тепло, необходимое для очистки воздуха; QТ – тепло, приносимое топливом. Qв V = t (Ct)в В QT C= B T tT Тепловыделение в камере сгорания – то тепло, которое выделяется в камере сгорания и не учитывает потери топлива под химическим и механическим недожогом. По тепловыделению в топке определяется теоретическая температура горения топлива. Методика определения тепловыделения в топке 1.Определяем энтальпию дымовых газов для температур 500, 1000, 2000оС. 2.Строится графическая зависимость, причём по вертикали откладывается энтальпия дымовых газов. 3.Определяем тепловыделение в топке. 4.На графической зависимости откладываем тепловыделение топки и по нему определяем адиабатную или теоретическую температуру. ^ Процессы горения топливаИзучая кинетику и динамику горения твёрдого топлива, сследует выделить несколько этапов процесса горения: -Подготовка топлива к процессу горения – подсушка топлива, подогрев, выделение летучих веществ. -Смесеобразование – перемешивание летучих веществ с окислителями, воспламенение, гомогенное выгорание и горение летучих веществ. -Образование кокса и его гетерогенное горение. При этом осуществляются следующие реакции горения: С + О2 = СО2 + Q1 2C +O2 = 2CO +Q2 2CO2 + O2 = 2CO2 + Q3 Q1 > Q2 > Q3 СО2 + С = 2СО (-Q4) CO + H2O = CO2 + H2 (-Q5) Основу этих ракциях составляют гетерогенные процессы, наиболее длительные по времени. При сравнительно низких температурах до 800оС скорость химических реакций мала. Поэтому скорость поглощения кислорода во много раз меньше скорости, с которой кислород поставляется к поверхности горения. Скорость процесса горения лимитируется скоростью химической реакции, которая подчиняется закону Аррениуса и может быть определена в виде произведения постоянной скорости горения на концентрацию кислорода у поверхности или в потоке. Период горения, в котором скорость реакции определяется скоростью окисления вещества называется кинетическим периодом горения. При увеличении температуры в пределах 800 - 900оС скорость химической реакции становится соизмеримой и равна скорости доставки кислорода к окисляемой поверхности: vд=д(Со– Сs), где д – коэффициент массообмена, характеризующий скорость переноса кислорода из потока за счёт молекулярной или турбулентной диффузии. В области горения 800 - 900оС происходит как кинетическое, так и диффузионное горение. Ближе к 800оС k > д и скорость горения определяется скоростью реакции окисления. Ближе к 900оС наблюдается обратный процесс, т. е. скорость горения определяется диффузией поступающей к поверхности частицы окислителя (вторая область процесса горения). При высоких температурах (900 - 1500оС) происходит процесс выхода СО с поверхности частиц, т. е. процесс диссоциации. В результате скорость реакции замедляется из-за развития вторичных реакций. Кроме того, поверхность частицы уменьшается из-за поступления СО через их поры (III период горения). При температурах более 1500оС изменяется характер химической реакции, и начинают преобладать вторичные (восстановительные) реакции. В этом периоде углеродные частицы газифицируются, т. к. кислород не достигает их поверхности, а химическая реакция перемещается в газовый поток. Перемещение процесса горения в газовый поток несколько повышает скорость реакции по сравнению с III периодом горения (IV период горения). С дальнейшим ростом температуры (>2000оС) начинает сказываться нехватка кислорода в зоне вторичных реакций, т. е. происходит торможение горения (V период горения). В натуральном топливе стадия подготовки происходит при 1000С. Водяной пар, выделяющийся при этом, поднимает объём продуктов сгорания и снижает температуру горения. Образование летучих веществ зависит от состава топлива и его возраста. Для торфа выделение летучих веществ начинается при 1000С, бурого угля – 150 – 1700С, газового угля – 2100С, тощего угля и антрацита – 300 – 4000С. Наибольшее количество летучих веществ образуется при температуре 200 – 4000С и продолжается до 1000 – 11000С. Летучие вещества оказывают большое влияние на горение кокса. Зольность топлива снижает Qрн, что требует затрат тепла на его подогрев. Также зашлаковываются поверхности нагрева котлоагрегата. В существующих топочных устройствах температура горения находится в диапазоне до 16000С из-за неравномерного распределения процесса горения. При расчёте топочных устройств эти отклонения учитываются с помощью специальных коэффициентов и эмпирических зависимостей. |
