материаловедение. КР_В50. Контрольная работа по дисциплине Материаловедение Выполнил студент Специальность
 Скачать 299.86 Kb. Скачать 299.86 Kb.
|
|
| Дата сдача работы | | Регистрационный номер работы | |
| Дата оценки работы | | оценка | |
Проверил: доцент__________________________Комаров А.П.
Уссурийск, 2021

Раздел №1 «Железоуглеродистые сплавы»
10. Что называется степенью переохлаждения при кристаллизации металлов? Какое практическое значение она имеет? Приведите примеры.
Ответ
Переход металла из жидкого состояния в твердое (кристаллическое) называется кристаллизацией. Процесс кристаллизации может протекать только при переохлаждении металла ниже равновесной температуры Тп. Разность между температурами Тп и Тк, при которых может протекать процесс кристаллизации, носит название степени переохлаждения:
ΔТ=Тп-Тк.
Большинство металлов кристаллизуется с переохлаждением, причем степень переохлаждения у разных металлов различна. Обычная степень переохлаждения металлов при кристаллизации в производственных условиях колеблется от 10 до 30 °С; при больших скоростях охлаждения она может достигать сотен градусов [3].
Практическое значение: степень переохлаждения является важнейшим фактором, влияющим на величину зерна при кристаллизации.
Пример: если степень переохлаждения невелика, то число центров получается небольшое, а скорость роста кристаллов велика. Поэтому при медленном охлаждении получаются крупные зерна. При большой степени переохлаждения образуется большое число центров, а скорость роста невелика. Следовательно, при быстром охлаждении зерна будут мельче.
Это подтверждается данными практики: при отливке тонкостенных изделий получается мелкозернистая структура, при отливке толстостенных— крупнозернистая.
Размер зерна металла сильно влияет на его механические свойства. Эти свойства, особенно вязкость и пластичность, выше, если металл имеет мелкое зерно [1].
Задача
1. Начертить диаграмму состояний «железо-цементит», провести на ней ординату, соответствующую заданному сплаву, обозначить на ней все критические точки.
2. Рядом с диаграммой справа начертить кривую охлаждения данного сплава, показав связь критических точек на диаграмме и кривой охлаждения.
3. Описать сущность превращений, происходящих в сплаве при медленном охлаждении от температуры в жидком состоянии до комнатной. Обязательно пояснить причины вызывающие превращения.
4. На ординате сплава отметить точку, соответствующую заданной температуре и провести через нее коноду. Пользуясь правилом отрезков, определить фазы, составляющие сплав при заданной температуре; их количество (в %) и состав (содержание компонентов в %) [4].
Исходные данные:
Количество углерода 2,00;
Температура 1350 С
Решение
Диаграмма состояния «железо - карбид железа» показана на рисунке 1.
Основными компонентами, от которых зависит структура и свойства железоуглеродистых сплавов, являются железо и углерод. Чистое железо - металл серебристо-белого цвета; температура плавления 1539°С. Железо имеет две полиморфные модификации: α и γ. Модификация α существует при температурах ниже 911°С и выше 1392°С; γ-железо- при 911-1392°С [3].
В зависимости от температуры и концентрации углерода железоуглеродистые сплавы имеют следующие структурные составляющие.
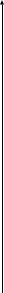




Сплав с 2%С
Ж
С=2+1-1=2
Т,0С


1
1



c
А+Ж
С=2+1-2=1






a
b


2
2


3
А
С=2+1-1=2



3

А+Ц
С=2+1-2=1





4
4
4,



А → П
С=2+1-3=0

Ц+П(Ф+ Ц)
С=2+1-2=1


τ, мин
Рисунок 1 – Диаграмма состояния железо-цементит и кривая охлаждения сплава с содержанием 2% С
Феррит (Ф) - твердый раствор внедрения углерода в α-железе. Растворимость углерода в α-железе при комнатной температуре до 0,005%; наибольшая растворимость - 0,02% при 727°С. Феррит имеет незначительную твердость (НВ 80-100) и прочность (σв=250 МПа), но высокую пластичность (δ=50%; φ=80%).
Аустенит (А) - твердый раствор внедрения углерода в γ-железе. В железоуглеродистых сплавах он может существовать только при высоких температурах. Предельная растворимость углерода в γ-железе 2,14% при температуре 1147°С и 0,8% - при 727°С. Эта температура является нижней границей устойчивого существования аустенита в железоуглеродистых сплавах. Аустенит имеет твердость НВ 160-200 и весьма пластичен (δ=40-50%).
Цементит (Ц) - химическое соединение железа с углеродом (карбид железа Fe3C). В цементите содержится 6,67% углерода. Температура плавления цементита около 1600°С. Он очень тверд (НВ800), хрупок и практически не обладает пластичностью. Цементит неустойчив и в определенных условиях распадается, выделяя свободный углерод в виде графита.
Графит - это свободный углерод, мягок (НВ 3) и обладает низкой прочностью. В чугунах и графитизированной стали содержится в виде включений различных форм (пластинчатой, шаровидной и др.). С изменением формы графитовых включений меняются механические и технологические свойства сплава.
Перлит (П) - механическая смесь (эвтектоид, т. е. подобный эвтектике, но образующийся из твердой фазы) феррита и цементита, содержащая 0,8% углерода. Перлит может быть пластинчатым и зернистым (глобулярным), что зависит от формы цементита (пластинки или зерна) и определяет механические свойства перлита. При комнатной температуре зернистый перлит имеет предел прочности σв=800 МПа; относительное удлинение δ=15%; твердость НВ 160.
Ледебурит (Л) - механическая смесь (эвтектика) аустенита и цементита, содержащая 4,3% углерода. Ледебурит образуется при затвердевании жидкого расплава при 1147°С. Ледебурит имеет твердость НВ 600-700 и большую хрупкость. Поскольку при температуре 727°С аустенит превращается в перлит, то это превращение охватывает и аустенит, входящий в состав ледебурита. Вследствие этого при температуре ниже 727°С ледебурит представляет собой уже не смесь аустенита с цементом, а смесь перлита с цементитом [1].
Построим кривую охлаждения стали с содержанием 2% С (рис.1) с использованием правила фаз Гиббса.
Правило фаз устанавливает зависимость между числом степеней свободы, числом компонентов и числом фаз и выражается уравнением:
C = K + 1 – Ф,
где С – число степеней свободы системы;
К – число компонентов, образующих систему;
1 – число внешних факторов (внешним фактором считаем только температуру, так как давление за исключением очень высокого мало влияет на фазовое равновесие сплавов в твердом и жидком состояниях);
Ф – число фаз, находящихся в равновесии [3].
Этот сплав относится к заэвтектоидным сталям (стали - сплавы содержащие более 0,8% С ). При температуре выше 1430°С (точка 1 на кривой охлаждения) сплав находится в жидком состоянии. В равновесии находится одна фаза-Жидкость. Согласно правилу фаз Гиббса, количество степеней свободы равно
С=k-f + 1 =2-1+ 1=2,
где k- количество компонентов в сплаве, k=2 (Железо и углерод),
f-количество фаз, f=1 (Жидкость).
В интервале т.1-2 до температуры 11800С весь жидкий расплав кристаллизуется в γ-фазу (аустенит), и в интервале т.2-3 до 10950С происходит его охлаждение.
В интервале т.3-4 из аустенита, вследствие уменьшения растворимости в нем углерода, выделяется цементит.
Количество фаз – 2,
С=k-f + 1 =2-2+ 1=1,
При постоянной температуре 7270С т.4-4/ происходит эвтектоидное превращение γ-фазы (аустенита) в феррито-цементитную смесь.
f=3, С=0.
Перлит образуется следующим образом. Пластинка цементита начинает расти или от границы зерна аустенита, или центром кристаллизации является неметаллическое включение. При этом соседние области обедняются углеродом и в них образуется феррит. Этот процесс приводит к образованию зерна перлита, состоящего из параллельных пластинок цементита и феррита. Чем грубее и крупнее выделения цементита, тем хуже механические свойства перлита.
Ниже 7270С в структуре сплава присутствует две фазы – α-фаза и цементит.
f=2, С=1.
Определение состава и количественное соотношение фаз в определенной точке диаграммы
Обозначим т. а, соответствующую состоянию данного сплава при 6500С и рассмотрим состав фаз, т.е. процентное содержание углерода в фазах при этой температуре; количественное соотношение фаз.
В данной точке присутствует две фазы – аустенит и жидкость.
Проведем через точку а горизонтальную линию – коноду.
Для определения процентного содержания углерода в фазах из точек b и c опустим перпендикуляры на ось концентраций.
Получаем содержание углерода в фазах:
СA = 0,9%; Сж = 2,7%.
Для определения количественного соотношения фаз воспользуемся правилом отрезков:
А = аc/bс·100% = (2,7-2)/(2,7-0,9)·100% = 39%;
Ж = 100-39= 61%.
Сплав с 2,0% углерода представляет собой заэвтектоидную сталь, имеющую при комнатной температуре структуру перлит+цементит в виде сетки. В данном сплаве при комнатной температуре присутствует две фазы – α-фаза (феррит в составе перлита) и цементит.
Работа по разделу №2 «Термическая обработка стали»
10. Что называется мартенситом и как он образуется в стали? Каково влияние углерода на положение области начала и конца образования мартенсита? Чем отличается мартенсит, полученный при критической скорости закалки и при скорости выше критической.
Ответ
Мартенсит — микроструктура игольчатого (пластинчатого), а также реечного (пакетного) вида, наблюдаемая в закалённых металлических сплавах и в некоторых чистых металлах, которым свойственен полиморфизм. Мартенсит — основная структурная составляющая закалённой стали; представляет собой упорядоченный пересыщенный твёрдый раствор углерода в α-железе такой же концентрации, как у исходного аустенита [3].
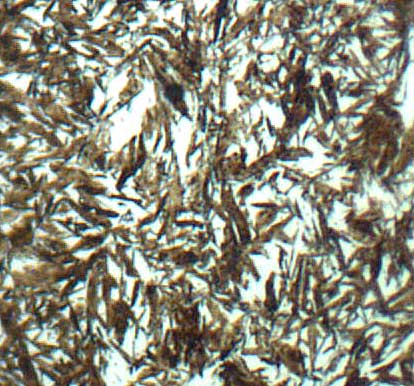
Рисунок 2 - Микроструктура мартенсита
Физический механизм образования мартенсита принципиально отличается от механизма других процессов, происходящих в стали при нагреве и охлаждении. Другие процессы диффузионны, то есть атомы перемещаются с малой скоростью, например, при медленном охлаждении аустенита создаются зародыши кристаллов феррита и цементита, к ним в результате диффузии пристраиваются дополнительные атомы и, наконец, весь объём приобретает перлитную или феррито-перлитную структуру. Мартенситное превращение бездиффузионно (сдвиговое превращение), атомы перемещаются с большой скоростью по сдвиговому механизму, скорость распространения порядка тысячи метров в секунду [3].
При увеличении скорости закалки выше критической возрастает дисперсность мартенситной структуры.
Влияние содержания углерода на мартенситные точки показано на рисунке 3 [2].
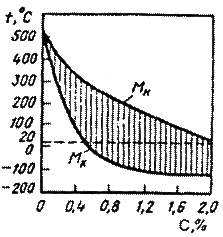
Рисунок 3 - Влияние содержания углерода в стали на температуру начала Мн и конца Mк мартенситного превращения
Задача
1. Выбрать и обосновать наиболее рациональный вид термической или химико-термической обработки, дающий возможность получения требуемой твердости материала заданной детали. Изложить его сущность.
2. Подробно изложить основные этапы технологического процесса обработки:
– выбрать и обосновать необходимую температуру нагрева;
– назначить время выдержки;
– выбрать и обосновать охлаждающую среду.
3. Начертить необходимый участок диаграммы «железо-цементит» и нанести на нем ординату сплава заданного изделия. На ординате отметить температуры нагрева для соответствующих этапов принятого технологического процесса термообработки.
4. Начертить график разработанного технологического процесса термообработки в координатах «температура-время». Масштаб времени допускается принимать условно.
5. Описать структурные превращения, происходящие в обрабатываемой стали на каждом этапе технологического процесса.
Исходные данные
Наименование детали - Болт крышки шатуна.
Марка стали - 40ХН.
Требуемая твердость - 28 HRC
Решение
Сталь 40ХН является доэвтектоидной конструкционной легированной сталью. Применяется в промышленности для изготовления ответственных нагруженных деталей, подвергающихся вибрационным и динамическим нагрузкам, к которым предъявляются требования повышенной прочности и вязкости. Химический состав стали 40ХН представлен в таблице 1 [5].
Таблица 1 – Химический состав стали 40ХН (ГОСТ 4543–71)
| C | Si | Mn | Ni | S | P | Cr | Cu |
| 0.36-0.44 | 0.17-0.37 | 0.5-0.8 | 1-1.4 | до 0.035 | до 0.035 | 0.45-0.75 | до 0.3 |
Температура критических точек материала 40ХН, 0С [5]:
| Ac1 = 735 , Ac3(Acm) = 768 , Ar3(Arcm) = 700 , Ar1 = 660 , Mn = 305 |
Для получения заданных свойств выбираем тип термообработки – закала и высокий отпуск.
Закалка - термическая обработка стали, заключающаяся в нагреве стали выше температуры фазовых превращений, изотермической выдержке при заданной температуре и последующем охлаждении со скоростью выше критической [2].
Выбор температуры нагрева под закалку.
Начертим необходимый участок диаграммы «железо-цементит» и нанем на нем ординату сплава заданного изделия (рис. 4).
Рисунок 4 – Стальной угол диаграммы железо - углерод
На ординате отметим температуры нагрева для принятого технологического процесса термообработки.
Доэвтектоидные стали подвергают полной закалке, при этом оптимальной температурой нагрева является температура Асз + (30- 50 °С).
Точка А3 соответствует температуре полной аустенизации стали и лежит на пересечении линии сплава с GS. В процессе нагрева стали в интервале между точками А1 и А3 структура стали состоит из аустенита и перлита, а выше точки А3 - полностью из аустенита [2].
Для стали 40ХН точка А3 соответствует 7680С.
Нагрев под закалку производится при температуре 800-8200С.
Температуру выдержки выбираем из расчета 1 мин. на 0С на 1 мм сечения детали [2].
Закалка производится в масло.
Превращения в стали при закалке: в результате охлаждения со скоростью выше критической происходит бездиффузионное превращение с образованием структуры мартенсита.
Следующий этап термообработки – отпуск стали.
Превращения в стали при отпуске.
Отпуск проводят при температурах ниже температур фазовых превращений. При нагреве закалённых сталей до температур порядка 200°С избыточный углерод частично выходит из мартенсита и образуются необособленные карбиды. В результате тетрагональность решётки мартенсита уменьшается и получается мартенсит отпуска. Он отличается меньшей твёрдостью и большей пластичностью. При температуре нагрева стали порядка 400°С избыточный углерод полностью покидает мартенсит и образует цементит. В результате формируется структура троостита отпуска (т.е. мелкозернистая смесь феррита с цементитом). При нагреве закалённых сталей до температур порядка 600°С наблюдается укрупнение (путём объединения) зёрен образующего цементита, в результате формируется структура сорбита отпуска [1].
Температуру отпуска выбираем 550-650ºС, охлаждение на воздухе.

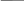




6000С
Т,0С
8200С
Структура после отпуска – сорбит. HRC 28-35 .


τ, мин
Рисунок 5 – График режима термообработки стали 40ХН.
Список литературы
Адаскин, А.М. Материаловедение и технология металлических, неметаллических и композиционных материалов: Учебник / А.М. Адаскин, А.Н. Красновский. - М.: Форум, 2018.
Баранов Е.М. Термообработка стали: метод. Пособие – Хабаровск; Изд-во ДВГУПС, 2004
Волков, Г.М. Материаловедение: учебник. 2 изд / Г.М. Волков. - М.: Academia, 2017.
Комаров А.П. Материаловедение: метод. Указания по выполнению расчетно-графических работ – Хабаровск; Изд-во ДВГУПС, 2019.
Марочник сталей и сплавов / под ред. А.С. Зубченко. 2-е изд. М. : Машиностроение, 2003.
