контрольная по онхл. Контрольная работа ОХНЛВ. Контрольная работа по дисциплине Основы химии неорганических лекарственных веществ
 Скачать 24.7 Kb. Скачать 24.7 Kb.
|
|
Контрольная работа по дисциплине «Основы химии неорганических лекарственных веществ» (модуль 1-2) 1.Классификация и топография элементов. 2.Взаимосвязь между электронным строением, биологической ролью элементов и их токсичностью. 3.Роль биогенных элементов в организме. 4.Токсикологическая роль элементов и их неорганических соединений. 5.Применение неорганических соединений в медицине и фармации. Биогенные элементы р-семействар-Элементы III группы: бор, алюминий, таллий 6.Биологическая роль бора (В), алюминия (Al). 7.Лечебное действие неорганических соединений бора и алюминия. 8.Применение соединений бора и алюминия в медицине и фармации. 9.Токсическое действие соединений бора, алюминия и таллия на живой организм. 10.Реакции качественного обнаружения соединений бора, алюминия и таллия р-Элементы IV группы: углерод, кремний, олово, свинец 11.Биологическая роль углерода (С) и кремния (Si). 12.Лечебное действие неорганических соединений углерода, кремния и свинца. 13.Применение углерода, неорганических соединений углерода, кремния, свинца в медицине и фармации. 14.Токсическое действие соединений углерода, кремния, олова и свинца на живой организм. 15.Реакции качественного обнаружения СО2, SiO32-, Pb2+ р-Элементы V группы: азот, фосфор, мышьяк, сурьма, висмут 16.Биологическая роль азота (N), фосфора (Р), мышьяка (Аs), сурьмы (Sb), висмута (Bi). 17.Лечебное действие неорганических соединений азота, фосфора, мышьяка и висмута. 18.Применение неорганических соединений азота, фосфора, мышьяка, висмута в медицине и фармации. 19.Токсическое действие соединений азота, фосфора, мышьяка, сурьмы и висмута на живой организм. 20.Реакции качественного обнаружения соединений мышьяка, сурьмы и висмута. p-Элементы VI группы: кислород. Озон, вода, пероксид водорода 21.Биологическая роль кислорода, озона (О3), воды (Н2О), пероксида водорода (Н2О2). 22.Применение кислорода, озона, воды, пероксида водорода в медицине и фармаци. 23.Токсическое действие кислорода, озона, пероксида водорода на живой организм. р-Элементы VI группы: сера, селен 24.Биологическая роль серы (S) и селена (Sе). 25.Лечебное действие неорганических соединений серы. Пероксид водорода как промежуточный продукт метаболизма. Способность пероксида водорода образовывать свободные радикалы. Роль свободных радикалов в развитии опухолевых процессов, в старении организма. Лекарственные препараты кислорода, воды, пероксида водорода. Химические основы антисептического и дезодорирующего действия пероксида водорода 26.Применение неорганических соединений серы и селена в медицине и фармации. 27.Токсическое действие соединений серы и селена на живой организм. р-Элементы VII группы: фтор, хлор, бром, йод 28.Биологическая роль фтора, хлора, брома и йода. 29.Лечебное действие неорганических соединений фтора, хлора, брома и йода. 30.Применение соединений фтора, хлора, брома, йода в медицине и фармации. 31.Токсическое действие соединений фтора, хлора, брома и йода на живой организм. 32.Качественные реакции на галогенид ионы. Биогенные элементы d-семейства d-Элементы VI группы:хром, молибден, вольфрам33. Биологическая роль хрома (Cr), молибдена (Мо), вольфрама (W). 34. Лечебное действие неорганических соединений молибдена. 35. Применение неорганических соединений хрома и молибдена в медицине и фармации. 36. Токсическое действие соединений хрома на живой организм. d-Элементы VII группы: марганец 37.Биологическая роль марганца. 38.Лечебное действие неорганических соединений марганца. 39.Применение неорганических соединений марганца в медицине и фармации. 40.Токсическое действие соединений марганца на живой организм. d-Элементы VIII группы: железо, кобальт, никель 41. Биологическая роль железа (Fe), кобальта (Co), никеля (Ni). 42.Лечебное действие соединений железа и кобальта. 43. Применение соединений железа и кобальта в медицине и фармации. 44.Токсическое действие соединений железа, кобальта, никеля на живой организм. d-элементы I, II группы: медь, серебро, цинк, ртуть 45.Биологическая роль меди (Сu), серебра (Ag), цинка (Zn), ртути (Hg). 46.Лечебное действие неорганических соединений меди, серебра, цинка, ртути. 47.Применение неорганических соединений меди, серебра, цинка, ртути в медицине и фармации. 48.Токсическое действие соединений меди, серебра и ртути на живой организм. Биогенные элементы s-семейства.s–Элементы I и II групп: литий, натрий, калий, магний, кальций, стронций, барий 49.Биологическая роль s-элементов I и II групп: лития (Li), натрия (Nа), калия (К), магния (Мg), кальция (Са), стронция (Sr), бария (Ва). 50.Лечебное действие неорганических соединений s-элементов I и II групп. Применение неорганических соединений s-элементов I и II групп в медицине и фармации. 51.Токсическое действие соединений s-элементов на живой организм. Ситуационные задачи 1.Тетраборат натрия (бура) применяется в качестве антисептика. Объясните её фармакологическое действие. Ответ подтвердите уравнениями реакций. 2. Гидроксид алюминия используется как лекарство при повышенной кислотности желудка. Объясните его фармакологическое действие. Ответ подтвердите уравнениями реакций. 3. 8% - ый раствор ацетата алюминия входит в состав лекарственного средства , обладающего вяжущим действием и используемого как кровеостанавливающее средство при порезах (свертывание крови). Вяжущее действие солей алюминия основано на образовании ионами алюминия и белками гелеобразных комплексов. Ответ подтвердите уравнениями реакций. 4. Монооксид углерода (СО- угарный газ) очень биологически активен в живом организме, он ядовит и чрезвычайно опасен еще и потому, что не имеет запаха. В чем заключается причина биологической активности угарного газа? Какие препараты можно использовать при отравлении угарным газом ? 5. Циановодород или синильная кислота, является обязательным компонентом табачного дыма. Циановодород и его соли обладают высокой токсичностью. При поступлении в организм оказывает действие на процесс дыхания. В чем заключается причина влияния синильной кислоты на дыхательные органы? Какие антидоты рекомендуются в качестве первой помощи при отравлении цианидами.? 6. Среди лекарственных азотсодержащих веществ хорошо известен нитрит натрия NaNO2. Однако в последнее время он практически не применяется в лечебных целях из – за токсичности. Объясните токсичность нитрита натрия с позиций окисления – восстановления. 7.Соединения мышьяка со степенью окисления +3 и + 5 очень токсичны. Объясните механизм токсического действия соединений мышьяка 8.Таллий очень токсичен. При попадании в организм даже незначительных количеств соединений Tl+ происходит выпадение волос. Объясните биологическую активность Tl+, какое вещество можно использовать в качестве противоядия? 9.Гидроксиапатит (Са10(РО4)6(ОН)2) - основное вещество и костной, и зубной ткани. Излишек кальция в более зрелом возрасте служит причиной образования камней и выводится из организма с помощью солей этилендиаминтетрауксусной кислоты и её производных. 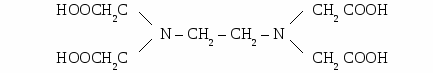 этилендиаминтетрауксусная кислота Объясните, почему этот препарат используют для выведения излишка ионов кальция из организма. Приведите уравнение соответствующей реакции. 10.Соляная кислота является необходимым компонентом желудочного сока, ее массовая доля составляет 0,3%. Присутствие соляной кислоты необходимо для нормального пищеварения и для борьбы с болезнетворными микроорганизмами. Для образования соляной кислоты в желудке необходима поваренная соль - натрий хлорид NaCl. Напишите уравнение химической реакции образования соляной кислоты HCl в желудке. 11.Тиосульфат натрия применяют для детоксикации при отравлениях тяжелыми металлами, например ртутью. Это действие обусловлено способностью тиосульфата разлагаться и впоследствии давать нерастворимые соли. Продемонстрируйте с помощью уравнений реакций на примере отравления солями двухвалентной ртути. 12.Повышенная кислотность в желудке может привести к язвенной болезни. Объясните, почему натрий гидрокарбонат можно применять в качестве антацида - средства против повышенной кислотности. 13.Ионы хрома (III) и гидроксида хрома (III) являются малотоксичными. Какие свойства подтверждают малую токсичность Сr3+ и Сr(0Н)з? 14.Хроматы и дихроматы, поступившие в организм, токсичны, приводят к образованию опухолей легких, т. к. хром (VI) канцерогенен только при ингаляционном попадании в организм. Предельно допустимые концентрации (ПДК) для Сr03 в воздухе производственных помещений - 0,1 мг/м3. Напишите методом полуреакций уравнение окисления-восстановления между дихроматом калия и соляной кислотой, происходящего в желудке. 15.Одной из основных функций марганца (II) является антиоксидантная защита клетки. Однако при избыточном поступлении марганца в организм должен возникать марганцевый токсикоз. Почему это происходит крайне редко? Какой механизм лежит в основе регуляции содержания марганца в организме? 16.Калий перманганат обладает антисептическим и дезинфицирующим действием. Применяют препарат в растворах для полосканий, орошения ран, обработки ожоговых поверхностей и т. д. Объясните принцип действия этого препарата. Напишите уравнение реакции, подтверждающее антисептическое и дезинфицирующее действие калий перманганата. 17.Растворимые соли серебра, попадая в организм в больших дозах, вызывают острое отравление, сопровождающееся отмиранием слизистой оболочки желудочно-кишечного тракта. На чем основано промывание желудка раствором NaCl при отравлении Ag+? 18.Бионеорганические комплексы серебра с белками являются коллоидными растворами. Коллоидное серебро (колларгол) используется в медицине при конъюнктивитах, инфекционных заболеваниях слизистых оболочек (носа, зева и др.) и болезнях кожи. На чем основано их применение? 19.Потребность человека в меди составляет 2-3 мг в сутки. В больших концентрациях растворимые соли меди токсичны. Сульфат меди (II) массой до 2 г, поступивший с пищей, вызывает сильное отравление с возможным летальным исходом. Объясните механизм токсичности. Какое свойство меди проявляется при отравлении ее солями 20.Что образуется при взаимодействии Си2+ с дитиоловыми группами ферментов микроорганизмов? На чем основана способность Си2+ вступать в такие реакции? Напишите схематично уравнение реакции. 21.Растворимые соединения бария очень токсичны. Механизм действия ионов бария состоит в том, что они конкурируют с ионами калия, т. к. имеют близкие по величине радиусы. Какие антидоты можно применить, основываясь на правиле диагонального сходства химических элементов 22.Две соли бария - карбонат и сульфат - одинаково плохо растворимы в воде (Кs = 10-10). Объясните, почему сульфат используется как рентгеноконтрастное вещество при исследовании желудочно-кишечного тракта, а карбонат очень токсичен? 23.Объясните, почему при отравлении солями бериллия вводят избыток солей магния. 24. На чем основано применение комплексонов как лечебных препаратов при отравлении соединениями цинка, кадмия и ртути? 25. Почему калий перманганат в больших концентрациях является ядом для организма? Каким свойством должно обладать вещество, которое используется как противоядие перманганату? 26.В пробирку поместили оксид магния и прибавили 3-4 капли раствора, имитирующего желудочный сок. Составьте уравнение протекающей реакции Что следует ожидать (укажите ожидаемый эффект) .Сделайте вывод. Укажите, какой лекарственный препарат предпочтительней применять в качестве антацидного средства: MgO или NaHCO3?Ответ обоснуйте. В состав какого лекарственного препарата входит оксид магния? 27.Опишите химические основы токсического действия соединений ртути. Какие соединения ртути (II) применялись в медицинской практике ? Опишите их лечебное действие. 28. Какая равновесная система образуется при растворении аммиака в воде? Как доказать его начие в растворе? Напишите уравнение реакции и укажите ее аналитический эффект. С какой целью применяется 10% раствор аммиака в медицинской пр 29.Составьте молекулярное уравнение гидролиза нитрата висмута (III). Как используя принцип Ле Шателье, можно сместить равновесие в сторону образования исходных веществ? Какой препарат висмута (III) применяется в медицинской практике? Запишите его название на латинском и русском языках. 30. Напишите аналитические реакции как можно отличить карбонат натрия от гидрокарбоната натрия. Укажите аналитический эффект. На чем основано лечебное действие гидрокарбоната натрия?
|
