вопросы. Контрольные вопросы Сформулируйте определение средней теплоемкости. Средняя теплоемкость это теплоемкость газов в заданном интервале температур от t 1 до t 2
 Скачать 29.5 Kb. Скачать 29.5 Kb.
|
|
3.2. Контрольные вопросы 6. Сформулируйте определение средней теплоемкости. Средняя теплоемкость – это теплоемкость газов в заданном интервале температур от t1 до t2. Определяется средняя теплоемкость по формуле: где q - количество теплоты, сообщенной газу за процесс, Дж/кг.
Средняя теплоемкость - это отношения теплоты, сообщенной газу за процесс, к разнице конечной и начальной температуры. Для практических расчетов используют таблицы, в которых средняя теплоемкость определена от нуля до интересующей температуры. 7. Почему средние теплоемкости газов в справочниках даются от 0 оС? Средней теплоемкостью можно пользоваться только на интервале температур от t1 до t2. Это очень неудобно, т.к. для практических расчетов необходимо в таблицах экспериментальных данных по средним теплоемкостям предусмотреть все возможные температурные интервалы. Выход из этой ситуации был найден введением средней теплоемкости, определенной от одинаковой начальной температуры. В качестве такой температуры приняли 0 OС. Расчетное выражение средней теплоемкости, определенной от 0 OС, имеет вид:
8. По каким формулам рассчитываются удельные теплоемкости газовых смесей? Под удельной массовой теплоемкостью ссм газовой смеси понимают количество теплоты, необходимое для нагревания 1 кг смеси на 1К. Очевидно, что это количество теплоты можно получить путем суммирования количества теплоты, необходимое для нагревания каждого компонента, входящего в состав смеси: ссм = Σ cimi, где: ci – удельная массовая теплоемкость i-го компонента смеси; mi - массовая доля этого компонента в смеси. Аналогично можно определить удельную объемную теплоемкость газовой смеси – как сумму удельных объемных теплоемкостей ее компонентов. Удельная киломольная теплоемкость смеси газов определяется по формуле: μсм ссм = Σ μiciri, где: μi – молекулярная масса компонента смеси; ri – объемная доля компонента в составе смеси. Удельная мольная теплоемкость смеси газов равна сумме произведений объемных долей на удельные мольные теплоемкости газов, составляющих смесь: сµсм = Σ cµiri 4.2. Контрольные вопросы 1. Для какой термодинамической системы записано уравнение δ δ q = du + ? Данное уравнение относится к первому закону термодинамики. Первое начало термодинамики утверждает, что изменение внутренней энергии термодинамической системы (тела) может быть осуществлено двумя путями: путём совершения механической работы и путём теплопередачи. Энергия, переданная системе путём теплопередачи, называется количеством теплоты. Первое начало термодинамики может быть сформулировано следующим образом: Теплота Если к термодинамической системе подводится элементарное количество теплоты 2. Какие виды энергетического взаимодействия тел рассматриваются в технической термодинамике? В технической термодинамике в качестве рабочего тела принимается идеальный газ — условное газообразное вещество, силами взаимодействия, между молекулами которого пренебрегают. В реальных же газах учитываются силы притяжения между молекулами, а молекулы имеют объем. Если реальные газы сильно разряжены, их свойства близки к свойствам идеального газа. В качестве идеальных газов могут рассматривать такие газы, как азот, гелий, водород. 3. В чем состоит сущность принципа эквивалентности теплоты и работы? В основе закона сохранения и превращения энергии лежит принцип эквивалентности различных форм движения материи. Было установлено, что различные формы движения материи (тепловая, механическая, электрическая, химическая и т. п.), количественными мерами которых являются количества соответствующих видов работ и теплоты, могут переходить в другие формы в строго определенных эквивалентных количествах, не зависящих ни от характера процесса преобразования, ни от условий протекания этого процесса. Различие между теплотой и работой состоит в том, что они являются различными формами передачи энергии. Теплота представляет собой такую форму передачи энергии, которая определяется либо непосредственным контактом между телами, либо лучистым переносом энергии. Работа представляет собой иной механизм передачи энергии, при котором обязательно имеет место изменение объёма тела. 4. В каких случаях считается теплота величиной положительной? Количество теплоты считается положительным, если тело поглощает определенную энергию. 5. В каких случаях считается работа изменения объема величиной положительной? Работа изменения объема - есть мера механического энергетического взаимодействия тела и внешней среды, являющаяся результатом изменения объема тела. Иногда эту работу называют работой расширения, хотя тело в результате этого энергетического взаимодействия может, как увеличивать, так и уменьшать свой объем. В технической термодинамике принято, что работа изменения объема положительна, когда тело совершает работу над внешней средой при увеличении его объема dv>0 6. Какое принципиальное различие между понятиями «внутренняя тепловая энергия» и «теплота»? В термодинамических процессах изменяется только кинетическая энергия движущихся молекул. Следовательно, фактически подвнутренней энергией в термодинамике подразумевают энергию теплового хаотического движения молекул. Внутренняя энергия зависит только от температуры. Теплота - мера энергии, переходящей от одного тела к другому в процессе теплопередачи. Теплота Q зависит от того, каким образом совершен переход из состояния 1 в состояние 2 (изохорически, адиабатически и т.д.), а внутренняя энергия U не зависит. 7. Какая принципиальная разница между уравнениями f(р, v, Т)=0 и δ δ q = du + ? Уравнение состояния — соотношение, отражающее для конкретного класса термодинамических систем связь между характеризующими её макроскопическими физическими величинами, такими как температура, давление, объём и др. Уравнения состояния необходимы для получения с помощью математического аппарата термодинамики конкретных результатов, касающихся рассматриваемой системы. Термическое уравнение состояния для закрытой термодеформационной системы связывает между собой её давление, объём и температуру. Таким образом, чтобы задать термическое уравнение состояния необходимо конкретизировать вид функции f{\displaystyle f}. Это уравнение выражает первое начало термодинамики: теплота, подводимая к системе, расходуется на изменение ее внутренней энергии и на совершение работы против внешних сил. Знак δ в δQ и δА означают, что данные элементарные приращения не являются полными дифференциалами и, следовательно, А и Q не являются функциями состояния. 8. Для каких процессов целесообразно использовать первый закон термодинамики в виде уравнения δq = dh - vdp ? Уравнение δq = du + pdv в случае, когда единственным видом работы является работа расширения, с учетом очевидного соотношения pdv = d(pv)—vdp может быть записано в виде δq = dh — vdp. Из этого соотношения следует, что если давление системы сохраняется неизменным, т.е. осуществляется изобарный процесс (dp = 0), то δqp = dh и qp = h2 - h1, т. е. теплота, подведенная к системе при постоянном давлении, идет только на изменение энтальпии данной системы. 9. Сколько дифференциальных уравнений первого закона термодинамики можно записать ? В дифференциальной форме первый закон термодинамики записывается следующим образом: δQ = dU + δA. Если δА – работа при расширении, то δQ = dU + PdV. Для изохорных процессов (V = const) δQV = dU; для изобарных процессов (P = const) δQP = dH; где H – энтальпия (H = U + PV). 5.4. Контрольные вопросы 1. Какая величина характеризует закономерность энергетического взаимодействия газа и внешней среды в политропном процессе? В термодинамике рассматриваются закономерные процессы. Закономерность процесса может быть выражена закономерным энергетическим взаимодействием газа и окружающей среды. Следствием такого энергетического взаимодействия будет закономерное изменение параметров газа. За величину, определяющую закономерность энергетического взаимодействия в газовом процессе, принимают отношение изменения внутренней энергии газа к количеству подведенной к нему теплоты: α = du / δq . Если =const, то процесс будет политропным. 2. Какая величина характеризует закономерность изменения термических параметров в политропном процессе идеального газа? Для идеальных газов с постоянными изобарными и изохорными теплоемкостями закономерность процессов могут характеризовать следующие величины: α = (du / δq) = cvdT/cdT = cv /c =const или c =cv /α =const ,n = c-cp /c-cv = const или c = cv (n-k/n-1) ,где n – показатель политропы; с – теплоемкость процесса. 3. Какая величина характеризует закономерность политропы идеального газа в Т,s- диаграмме? Для политропного процесса идеального газа изменение энтропии определяется уравнением
Изображение политропы в Т,s- диаграмме ведется в соответствии с этим уравнением при фиксации начала отсчета энтропии. 4. Какие величины используются вместо коэффициента Пуассона для определения температуры второй точки по двум известным параметрам первой точки и давлению или объему второй точки в обратимых адиабатных процессах идеальных газов при учете влияния температуры на теплоемкости сv и сp ? В этих таблицах кроме u, h для идеальных газов приводятся значения относительных давлений o=р/po, объемов o=v/vo, которые используются только для адиабатных процессов при нахождении параметров второй точки процесса без использования коэффициента Пуассона по соотношениям p2/p1 = πо2/πо1 , или v2/v1 = θо2/ θо1. Также есть та часть удельной энтропии идеальных газов, которая зависит от температуры: So 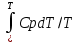 , где То=0 К . , где То=0 К .6.2. Контрольные вопросы 1. Может ли существовать насыщенный водяной пар с жидкой фазой воды в ненасыщенном состоянии, если да, то при каких условиях? Если число частиц, покидающих вещество за единицу времени больше числа частиц возвращающихся обратно за то же время, то пар называется ненасыщенным. То есть, когда пар ненасыщен, процесс испарения не останавливается, и масса вещества в жидком (или твердом) состоянии уменьшается, а объем ненасыщенного пара увеличивается. Динамическое равновесие при этом отсутствует. Насыщенный водяной пар с жидкой фазой воды может существовать в ненасыщенном состоянии, но при этом будет происходить процесс некомпенсированного перехода вещества из жидкой фазы в газообразную т.е. испарение. 2. Что означает понятие «сухой насыщенный пар»? Сухой насыщенный пар – это пар, не содержащий капель жидкости и имеющий температуру насыщение (t=t н ) при данном давлении. Состояние сухого насыщенного пара определяется только одним параметром – давлением или температурой. 3. Что означает понятие «жидкая фаза воды в состоянии насыщения»? Жидкая фаза воды при температуре кипения называется насыщенной жидкостью. |
