фенолоальдегидные смолы и пластмассы на их основе. Реферат кремнийорганические соединения. Кремнийорганические полимеры
 Скачать 188.33 Kb. Скачать 188.33 Kb.
|
|
Министерство науки и высшего образования Российской Федерации Федеральное государственное автономное образовательное учреждение высшего образования «Пермский национальный исследовательский политехнический университет» Аэрокосмический факультет Кафедра «Проектирование и производство энергетических конденсированных систем и изделий из них для ракетно-космической техники и энергетических установок» Направление(профиль) программы магистратуры:18.04.01-Химическая технология «Химическая технология энергетических конденсированных систем» РЕФЕРАТ на тему: «Кремнийорганические полимеры» Выполнил: студент гр. ТЭКС- 21-1моз Пищулева Наталья Федоровна (Фамилия, имя, отчество) ______________________________ (подпись) Проверил: Профессор, доктор технических наук Зиновьев Василий Михайлович (должность, Ф.И.О. руководителя от кафедры) __________ _________________________ (оценка) (подпись) _____________ (дата) Пермь 2022 Содержание Введение…………………………………………………………………………...3 1. Сырье для получения кремнийорганических полимеров………….………...4 2. Особенности получения и отверждения кремнийорганических полимеров……………………………………………………………………….....6 3. Производство полиорганосилоксанов с разветвленными и циклолинейными цепями ……………………………………………………….10 4. Свойства и применение полиорганосилоксанов……………………………11 Заключение……………………………………………………………………….21 Список использованных источников…………………………………………...23 ВВЕДЕНИЕ Кремнийорганические полимеры - высокомолекулярные соединения, содержащие атомы кремния, углерода и других элементов в элементарном звене макромолекулы. В зависимости от химического строения основной цепи кремнийорганические полимеры делят на три основные группы: 1) с неорганическими главными цепями макромолекул, которые состоят из чередующихся атомов кремния и других элементов (О, N, S, Al, Ti, В и др.), при этом углерод входит лишь в состав групп, обрамляющих главную цепь; 2) с органонеорганическими главными цепями макромолекул, которые состоят из чередующихся атомов кремния и углерода, а иногда и кислорода; 3) с органическими главными цепями макромолекул . Наиболее подробно изучены и широко применяются полиорганосилоксаны, а также полиметаллоорганосилоксаны и полиорганосилазаны. В 1937 г. советский академик К.А. Андрианов получил впервые в мире кремнийорганические полимеры – полиорганосилоксаны, которые относятся к классу элементорганических полимеров и являются среди них наиболее распространенными и ценными. Они принадлежат к группе полимеров с неорганическими главными цепями макромолекул, которые состоят из чередующихся атомов кремния и кислорода, а углерод входит лишь в состав групп, обрамляющих главную цепь: R R Si O Si O R R Многие особенности механических и физико-химических свойств этих полимеров связаны с высокой гибкостью их макромолекул и относительно малым межмолекулярным взаимодействием. Высокая гибкость силоксановой цепи утрачивается при переходе от линейной структуры к лестничной. Линейные и разветвленные полиорганосилоксаны с невысокой молярной массой — вязкие бесцветные жидкости. Высокомолекулярные линейные полиорганосилоксаны — эластомеры, а сшитые и разветвлённые — эластичные или хрупкие стеклообразные вещества. Полиорганосилоксаны характеризуются высокой термостойкостью, обусловленной высокой энергией связи Si—O, а также отличными диэлектрическими характеристиками [3]. Во многих странах и в России налажено производство кремнийорганических пластических масс (пресс-материалов, стеклопластиков, пенопластов и др.) Кремнийорганические соединения применяются в производстве каучуков и резин, лаков и эмалей, клеев, заливочных компаундов, смазочных веществ, пеногасящих и пропиточных средств, эмульгаторов и т.п. [1]. СЫРЬЕ ДЛЯ ПОЛУЧЕНИЯ КРЕМНИЙОРГАНИЧЕСКИХ ПОЛИМЕРОВ Кремний Si (silicium), химический элемент IVA подгруппы (C, Si, Ge, Sn и Pb) периодической системы элементов, неметалл. Кремний – темно-серое, блестящее кристаллическое вещество, хрупкое и очень твердое, кристаллизуется в решетке алмаза. Это типичный полупроводник. При высокой температуре кремний весьма реакционноспособен и взаимодействует с большинством элементов, образуя силициды. Кремний – второй по распространенности (после кислорода) элемент в земной коре, где он составляет более 25% (масс.). Встречается в природе в основном в виде песка, или кремнезема, который представляет собой диоксид кремния, и в виде силикатов (полевые шпаты M[AlSi3O8] (M = Na, K, Ba), каолинит Al4[Si4O10](OH)8, слюды). Кремний можно получить прокаливанием измельченного песка с алюминием или магнием; в последнем случае его отделяют от образующегося MgO растворением оксида магния в соляной кислоте. Технический кремний получают в больших количествах в электрических печах путем восстановления кремнезема углем или коксом. Высокочистый кремний получают выращиванием монокристалла из расплава полупроводникового кремния по методу Чохральского или методом бестигельной зонной плавки кремниевых стержней [4].
Алкил(арил)хлорсиланы представляют собой наиболее распространенный класс кремнииорганических соединений, пригодный для получения полимеров. Во всех химических реакциях принимает участие галоген, а органический радикал остается неизменным. Алкил(арил)хлорсиланы делятся на три группы: трифункциональные RSiCl3, дифункциональные R2SiCl2 и монофункциональные R3SiCl. Из них промышленное применение для синтеза кремнийорганических соединений нашли метил, этил- и фенилхлорсиланы. Синтез их осуществляется главным образом прямым взаимодействием при температурах 250-5000С алкил- или арилхлоридов в газовой фазе с кремнием в присутствии катализатора (меди):  2RCl + Si R2SiCl2 2RCl + Si R2SiCl2Одновременно образуются соединения типа RSiCl3, R3SiCl и различные побочные продукты. Разделяют их ректификацией. Карбофункциональные алкилхлорсиланы синтезируют по реакции гидросилирования – взаимодействия простейших кремнийорганических соединений, имеющих связь Si – Н, с непредельными органическими соединениями. Процесс проводят под давлением. Катализаторами реакции являются соединения платины и органические перекиси. Большинство алкил(арил)хлорсиланов представляет собой бесцветные жидкости с резким запахом, плотность которых составляет 850—1320 кг/м3, Ткип= 65 - 2200С. Они растворяются в эфирах, ароматических углеводородах и галогенуглеводородах. При взаимодействии со спиртами и фенолами образуют алкил(арил)алкокси- и соответсвующие арилоксисиланы; при действии атмосферной влаги гидролизуются с выделением хлористого водорода [2]. Замещенные эфиры ортокремневой кислоты представляют собой продукты, в которых наряду с органическими радикалами содержится одна, две или три алкоксигруппы. Различают три типа продуктов: трифункциоиальные RSi(OR')3, дифункциональные R2Si(OR')2 и монофункциональные R3SiOR'. Одним из основных методов получения замещенных эфиров является реакция этерификации алкил(арил)хлорсиланов спиртами:  RnSiCl4-n+ (4-n) R'OH RnSi (OR')4-n+ (4-n)HCl RnSiCl4-n+ (4-n) R'OH RnSi (OR')4-n+ (4-n)HClДля устранения побочных реакций процесс проводят в присутствии нейтрализующих веществ (третичных аминов, алкоголятов). Другим методом получения замещенных эфиров ортокремневой кислоты является обработка полных эфиров ортокремневой кислоты магнийорганическими соединениями (синтез по Гриньяру):  Si (OR)4 +RMgX RSi(OR)3 + ROMgX Si (OR)4 +RMgX RSi(OR)3 + ROMgXЗамещенные эфиры ортокремневой кислоты, в частности метил-, этил- и фенилэтоксисиланы, представляют собой бесцветные жидкости, плотность которых составляет 750—1010 кг/м3, Ткип= 150 - 2500С. Перегоняются при атмосферном давлении без разложения и хорошо растворяются в спиртах, эфирах, хлорированных и ароматических углеводородах. С водой они не смешиваются, но легко гидролизуются по эфирным связям. Конечным продуктом гидролиза являются полиорганосилоксаны. Свойства алкил(арил)хлорсиланов и замещенных эфиров ортокремневой кислоты приведены ниже [1]:
ОСОБЕННОСТИ ПОЛУЧЕНИЯ И ОТВЕРЖДЕНИЯ КРЕМНИЙОРГАНИЧЕСКИХ ПОЛИМЕРОВ Алкил(арил)хлорсиланы и замещенные эфиры ортокремневой кислоты при действии воды гидролизуются с образованием алкил(арил)силанолов, являющихся кремнийорганическими мономерами: R3SiCl + H2O R3SiOH + HCl R3SiOC2H5 + H2O R3SiOH + C2H5OH R2SiCl2 + 2H2O R2Si(OH)2 + 2HCl R2Si(OC2H5)2 + 2H2O R2Si(OH)2 + 2C2H5OH RSiCl3 + 3H2O RSi(OH)3 + 3HCl RSi(OC2H5)3 + 3H2O RSi(OH)3 + 3C2H5OH Силанолы сразу же претерпевают дальнейшие превращения (реакции поликонденсации) до образования силоксанов. Скорость реакции возрастает в присутствии кислоты и с повышением температуры. Состав и свойства образующихся продуктов зависят от количества воды и природы растворителя. Монофункциональные триалкил(триарил)гидроксисиланы в присутствии кислот превращаются в гексаалкил(гексаарил)дисилоксаны: 2R3SiOH R3Si O SiR3 + H2O Практическое значение монофункциональных соединений заключается в том, что их добавляют в небольших количествах к ди- и трифункциональным соединениям для получения полимеров определенного строения и состава (они замыкают цепи полиорганосилоксанов). Дифункциональные диалкил(диарил)дигидроксисиланы превращаются в полидиалкил(диарил)силоксаны линейного(I) и циклического(II) строения, при этом образуются смеси продуктов. 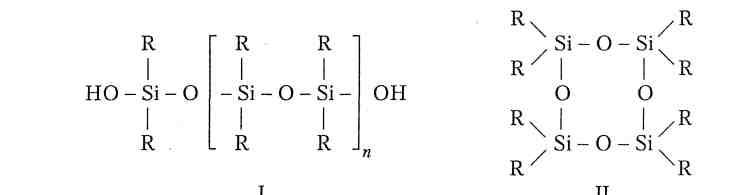 Наиболее устойчивыми являются соединения с восьмичленным циклом (тетрамеры). В случае совместной поликонденсации три- и дифункциональных соединений также образуются неплавкие и нерастворимые полиорганосилоксаны разветвленные полимеры (вид I):  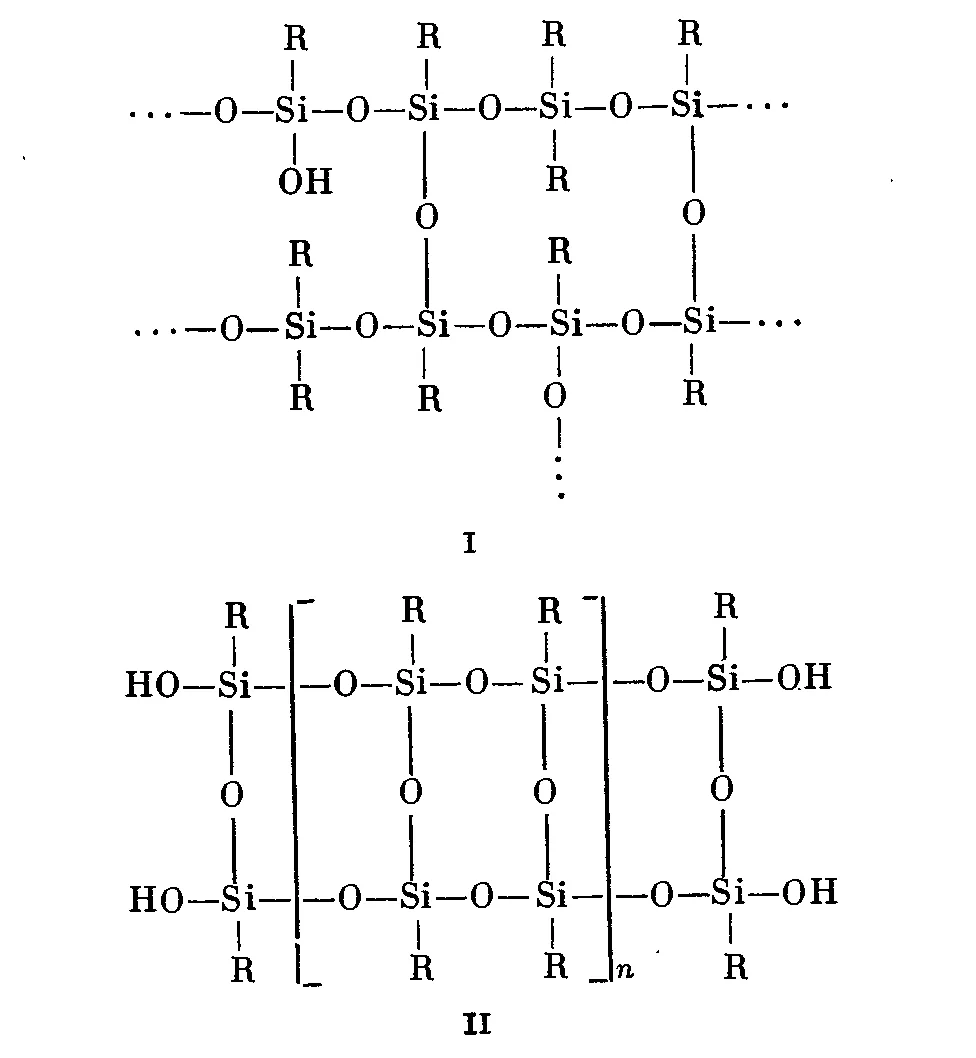 Трифункциональные алкил(арил)тригидроксисилаиы превращаются в неплавкие и нерастворимые продукты — лестничные полимеры, соответствующие эмпирической формуле (RSiO1,5 )n (вид II) Таким образом, условием гидролиза и поликонденсации алкил(арил)хлорсиланов и замещенных эфиров ортокремневой кислоты является наличие воды в реакционной смеси. При незначительном количестве воды происходит в основном образование линейных продуктов даже из трифункциональных соединений. Избыток же воды приводит к полному гидролизу. В кислой среде из дифункциоиальных продуктов кроме полимеров линейного строения, образуется до 40-45 % циклических олигомеров состава [R2Si = О]n, где п = 3-9, способных превращаться в полимеры по реакции полимеризации. Если в кислой среде гидролиз алкил(арил)хлорсиланов, а также полимеризация и поликонденсация промежуточных продуктов проходят мгновенно, то в нейтральной или слабокислой среде эти процессы протекают медленнее. Особенно это заметно в случае замещенных эфиров ортокремневой кислоты. Гидролиз и поликонденсация алкилзамещенных эфиров ортокремневой кислоты и алкил(арил)хлорсиланов при недостатке воды протекают по типу реакций ступенчатой конденсации. При гидролизе алкилтрихлорсиланов водой в присутствии растворителей (бензола, толуола и др.) образуются неплавкие и нерастворимые полимеры в виде аморфных осадков. В случае активных органических растворителей (спиртов, эфиров и др.), растворяющих как мономерные, так и полимерные продукты, реакция поликонденсации протекает в гомогенной среде и приводит к образованию линейных высокомолекулярных продуктов. При частичном гидролизе алкилтриэтоксисиланов водным раствором спирта (например, 90 %-ным) в отсутствие кислоты при 65-70 °С основным продуктом реакции является дисилоксан: RSi(OR')3 + H2O RSi(OR')2OH + R'OH 2RSi(OR')2OH RSi(OR')2OSiR(OR')2 При добавлении к реакционной смеси более 0,5 моль воды продолжается гидролиз и образуются линейные соединения формулы:   R RR O – Si OR' OR' n , где n = 2-7. Избыток воды способствует получению сложных полимеров пространственной структуры. Кремнийорганические полимеры (полиорганосилоксаны (ПОС)) могут быть линейными и пространственными (сшитыми, разветвленными, циклолинейными). На концах цепей полимеров находятся триалкил-(триарил)силоксановые группы. В общем виде структура кремнийорганических полимеров может быть представлена следующим образом: Линейные ПОС низкомолекулярные (олигоорганосилоксаны) (n = 3-700) и высокомолекулярные (n>700):    R RR3Si O Si OSiR3 R n Пространственные ПОС:     R R R3Si О Si О Si О SiR3 О n R m Низкомолекулярные ПОС представляют собой прозрачные вязкие жидкости, химически инертные, стойкие к окислению и нагреванию. Свойства их зависят от молекулярной массы и типа органического радикала, входящего в состав молекулы полимера. Получение жидких ПОС осуществляется гидролизом ди- и трифункциональных алкил(арил)хлорсиланов или алкилэтоксиланов. В основном получают циклические соединения, которые затем превращаются в линейные продукты нагреванием с активированной глиной при 90-1200С или добавлением концентрирванной серной кислоты в зависимости от природы используемых мономеров. Высокомолекулярные ПОС линейной структуры получают гидролизом и поликонденсацией дифункциональных соединений и каталитической полимеризацией органоциклосилоксанов. Присутствие монофункциональных соединений резко сокращает длину силоксановой цепи полимера. Высокомолекулярные соединения, полученнные из чистых исходных дифункциональных мономеров, представляют собой эластомеры. Наибольшее распространение в технике нашел полидиметилсилоксановый полимер, получаемый из смеси со средней функциональностью 2-2,02 (отношение CH3:Si=2-1,98). Первой стадией синтеза эластомеров является гидролиз водой диалкилдихлорсиланов. Процесс проводят при 200С в реакторе с обратным холодильником, мешалкой и рубашкой в течение 2-12 часов (в зависимости от состава исходного мономера). В результате реакции получают смесь линейных и циклических продуктов. На второй стадии проводят деполимеризацию линейных полимеров в присутствии едкого кали при 140-1600С и пониженном давлении 10-30 кПа. Продукт деполимеризации представляет собой смесь циклических диметилсилоксанов, содержащих тетрамер с примесью тримера и пентамера. На третьей стадии осуществляют полимеризацию смеси циклических продуктов в присутствии катализатора катионного типа, например, смеси сульфата алюминия, серной кислоты и диметилциклосилоксанов, при 80-1000С. Готовый полимер промывают водой температурой 500С и сушат при 800С.Таким путем получают эластомеры (каучуки) с молекулярной массой от 500 000 до 1 000 000 [1]. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
