КР титулка31. Курсовая работа предмет Химическая технология неорганических веществ
 Скачать 0.99 Mb. Скачать 0.99 Mb.
|
1 2 МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РЕСПУБЛИКИ КАЗАХСТАН МАНГИСТАУСКИЙ ЭНЕРГЕТИЧЕСКИЙ КОЛЛЕДЖ ИМЕНИ Н. БЕКБОСЫНОВА Специальность: 07110100 «Химическая технология и производство (по видам)» Квалификация: 4S071101102 «Техник -Технолог» КУРСОВАЯ РАБОТА Предмет: Химическая технология неорганических веществ__________________ Тема: Эффективность и обоснование выбора технологической схемы производства синтетического аммиака____________________________________ _______ Выполнил: Сагизбаев А.Н (оценка) (Ф.И.О.) Группа:___ХТП1/19_______ Проверил: Бекжанова А.У ⸏ ⸏ ⸏ ⸏ (Ф.И.О.) г. Актау 20 г. «УТВЕРЖДАЮ» заместитель руководителя по учебной работе «» 20 г ЗАДАНИЕ ДЛЯ КУРСОВОЙ РАБОТЫ Предмет Химическая технология неорганических веществ__________________ Курс 4 Группа ХТП 1/19 ГККП «Мангистауский энергетический колледж имени Н.Бекбосынова». (наименование учебного заведения) 07110100 «Химическая технология и производство (по видам)»______________________________________________________________ (специальность) Сагизбаев Алимжан Нуржанович Ф.И.О.) Тема и необходимые данные Эффективность и обоснование выбора технологической схемы производства среднего давления синтетического аммиака При выполнении курсовой работы, по теме, должны быть сданы: 1. Физико-химическая характеристика процесса: Методы производства 1.1 Физико-химическая характеристика сырья и готовой продукции 1.2 Физико-химические основы процесса (реакции получения) 2. Технологическая часть 2.1 Анализ существующих технологий производства синтетического аммиака 2.2 Обоснование выбора технологической схемы 2.3 Основное оборудование 2.4 Автоматизация производства 3 Расчетная часть 3.1 Материальный расчет (баланс) 3.2 Тепловой расчет 3.3 Конструктивный расчет 4 Охрана труда и окружающей среды 4.1 Требования безопасности к технологическому процессу производства синтетического аммиака 4.2 Об охране окружающей среды. Заключение содержит обзор по курсовой работе, подведение итогов -значение, эффективность метода. Использованная литература 2.Графическая часть Лист 1 ____________________________________________________________________ ____________________________________________________________________ Лист 2 Дата выдачи задания 202 ж. «___» __________ Срок окончания 202 ж. «___»__________ Руководитель курсовой работы Рассмотрено на предметно – цикловой комиссии. Протокол №___ «___»__________202 ж. Председатель комиссии__________ Содержание Введение……………..……………………………………………………………..5-6 1 Физико-технологическая часть 1.1 Физико-химические характеристики процесса……….……………………….7 1.2 Сырье для готовой продукции………………………………………………8-10 2 Технологическая часть 2.1 Основная технологическая часть…………………………..………………11-12 2.2Обзор различных технологических схем производства синтетического аммиака…..……………………………………………………13-20 2.3 Выбор схемы производства………………...………………………………21-22 3 Расчетная часть………………………………..………………………………22-27 3.1 Материальный рассчет……………………………………………………..24-26 3.2 Тепловой рассчет………………………………………………………………27 4.1 Охрана труда и окружающей среды……..………………………………...28-31 4.2 Вопросы безопасности при производстве синтетического аммиака………..32 Заключение…………………………………………….………………………...33-34 Список использованной литературы……………………...………………………35 Введение Одна из наиболее высокотехнологичных отраслей промышленности Казахстана – химическая. Она является важной сферой экономики республики. Продукция отрасли применяется при изготовлении разных потребительских товаров. Всего в химической отрасли Казахстана работают около 800 предприятий, основной объем производства обеспечивают 12 крупнейших заводов. Фундамент химической промышленности Республики Казахстан – богатые запасы фосфоритов в южной и западной части и различных видов солей на севере, развитая нефтегазовая промышленность и пр. На территории страны выявлено около 100 элементов таблицы Менделеева, а активно используются около 60 из них. Структурно химическую промышленность можно разделить агрохимию, нефтехимию и потребительскую химию. Аммиачные удобрения — азотные удобрения, содержащие азот в аммиачной (аммонийной) форме. К ним относятся нитрат аммония NH4NO3, сульфат аммония (NH4)2SO4, хлорид аммония NH4Cl, карбонат аммония (NH4)2CO3 и гидрокарбонат аммония NH4HCO3 , аммиак жидкий, аммиачная вода, сульфид аммония (NH4)2S, а также азотно-фосфорные удобрения (аммофос и диаммофос), азотно-калийные удобрения и др. Все аммиачные удобрения хорошо растворимы в воде, и их азот быстро усваивается растениями. Производство синтетического аммиака является важным процессом в химической промышленности. Это важнейший компонент в производстве удобрений и других химических продуктов. Процесс включает реакцию азота и водорода под высоким давлением и температурой с образованием аммиака. Производство синтетического аммиака было серьезной проблемой из-за сложности процесса. В этой статье мы обсудим физические и химические характеристики проекта, технологические аспекты производства синтетического аммиака, предполагаемые затраты и меры по охране окружающей среды, а также будущие направления исследований и разработок. Производство синтетического аммиака было впервые разработано Фрицем Габером и Карлом Бошем в начале 20 века. Их процесс, известный как процесс Габера-Боша, произвел революцию в производстве аммиака, позволив производить аммиак в больших масштабах. Процесс включает реакцию азота и водорода в присутствии катализатора при высоком давлении и температуре. Производство синтетического аммиака сыграло значительную роль в развитии сельского хозяйства и химической промышленности. Аммиак является важным соединением в химической промышленности из-за его универсальности и многочисленных применений. В основном он используется в качестве сырья для производства других химических веществ, включая удобрения, пластмассы, фармацевтические препараты и чистящие средства. Производство удобрений Большая часть аммиака используется в производстве удобрений, особенно удобрений на основе азота. Азот является важным питательным веществом для роста растений, а наличие азота в почве определяет урожайность сельскохозяйственных культур. Азотные удобрения, такие как мочевина, сульфат аммония и нитрат аммония, имеют решающее значение для обеспечения достаточного количества азота для роста сельскохозяйственных культур, особенно в районах, где почвенный азот ограничен. Производство пластмасс Аммиак используется в качестве сырья для производства различных пластмасс, включая нейлон, карбамидоформальдегидные смолы и меламиновые смолы. Нейлон - это синтетическое волокно, которое широко используется в одежде, коврах и других применениях. Карбамидоформальдегидные и меламиновые смолы используются в качестве клеев и покрытий в изделиях из дерева, слоистых материалах и покрытиях. Фармацевтическое производство Аммиак используется в производстве различных фармацевтических препаратов, включая антибиотики, противомалярийные препараты и гипотензивные препараты. Например, аммиак используется в качестве реагента при синтезе противомалярийного препарата хинолина. Чистящие средства Аммиак также используется в качестве чистящего средства из-за его щелочных свойств. Он особенно эффективен при расщеплении жиров и масел, что делает его полезным при уборке кухонь и других областей пищевой промышленности. Кроме того, аммиак используется в производстве моющих средств, особенно тех, которые предназначены для интенсивной уборки. В целом, важность аммиака в химической промышленности невозможно переоценить. Это универсальное и незаменимое соединение, которое используется в производстве многочисленных продуктов, на которые мы полагаемся в повседневной жизни. Важность эффективности и обоснования проектирования технологической схемы производства Эффективность и рациональность имеют решающее значение при разработке технологической схемы производства синтетического аммиака. Производственный процесс включает несколько стадий и требует значительного количества энергии и сырья. 1.1 Физико-химические характеристики процесса Области использования аммиака Аммиак – ключевой продукт для получения многочисленных азотсодержащих веществ, применяемых в промышленности, сельском хозяйстве и быту. На основе аммиака в настоящее время производятся практически все соединения азота, используемые в качестве целевых продуктов и полупродуктов неорганической и органической технологии Физические свойства азота и водорода играют решающую роль в производстве синтетического аммиака. Азот — это инертный газ, относительно нереакционноспособный, тогда как водород обладает высокой реакционной способностью. Химическая реакция между азотом и водородом требует высокой температуры и давления, что делает процесс энергоемким. Термодинамика процесса синтеза аммиака играет решающую роль в эффективности производства синтетического аммиака. Азот и водород являются газами при стандартной температуре и давлении. Азот представляет собой бесцветный газ без запаха и вкуса, который составляет около 78% атмосферы Земли. Водород также представляет собой бесцветный газ без запаха и вкуса и является самым распространенным элементом во Вселенной. Физические свойства азота и водорода важно учитывать при производстве синтетического аммиака. 1.2 Сырье для готовой продукции Сырьем в производстве аммиака является азотоводородная смесь (АВС) стехиометрического состава N2 : H2 = 1 : 3. Так как ресурсы атмосферного азота практически неисчерпаемы, сырьевая база аммиачного производства определяется вторым компонентом смеси – водородом, который может быть получен разделением обратного коксового газа, газификацией твердого топлива, конверсией природного газа. Структура сырьевой базы производства аммиака менялась, и сейчас свыше 90% аммиака вырабатывается на основе природного газа. Азотоводородная смесь независимо от метода ее получения содержит примеси веществ, некоторые из которых являются каталитическими ядами, вызывающими как обратимое (кислород, оксиды углерода, пары воды), так и необратимое (различные соединения серы и фосфора) отравление катализатора. С целью удаления этих веществ АВС подвергается предварительной очистке, методы и глубина которой зависят от их природы и содержания, то есть от способа производства АВС. Обычно АВС, получаемая конверсией природного газа, содержит оксид углерода (IV), метан, аргон, следы кислорода и до 0,4% об. оксида углерода (II). Для очистки АВС в промышленности используются методы абсорбции жидкими поглотителями (мокрый метод) и адсорбции твердыми поглотителями (сухой метод). При этом процесс очистки может производиться на различных стадиях производства: – исходного газа перед подачей его на конверсию; – конвертированного газа для удаления из него оксида углерода (IV); – азотоводородной смеси непосредственно перед синтезом аммиака (тонкая очистка АВС). Первые два процесса рассматриваются при описании соответствующих производств. 12 Тонкая очистка АВС достигается хемосорбцией примесей жидкими реагентами и окончательно каталитическим гидрированием их или промыванием АВС жидким азотом. Для удаления оксида углерода (IV) и сероводорода АВС промывают в башнях с насадкой щелочными реагентами, образующими с ними нестойкие термические соли: водным раствором этаноламина или горячим, активированным добавкой диэтаноламина, раствором карбоната калия. При этом протекают соответственно реакции: H2S + CH2OH–CH2NH2 [CH2OH–CH2NH3] +HS– – H, CO2 + K2CO3 + H2O 2KHCO3 – H. Оксид углерода (II) удаляют из АВС промывкой ее медно-аммиачным раствором ацетата меди CO + NH3 + [Cu(NH3)2] + Ац– [Cu(NH3)3CO]+Ац– – Н, где Ац = СН3СОО– Применяемые для хемосорбции абсорберы образуют с поглощаемыми из АВС нестойкие соединения. Поэтому при нагревании их растворов и снижении давления происходит десорбция растворенных примесей, что позволяет легко регенерировать абсорбент, возвратить его в процесс и обеспечить цикличность операции абсорбции.Более эффективным методом очистки АВС от оксида углерода (II) является применяемая в современных установках промывка АВС жидким азотом при –1900С, в процессе которой из нее удаляются, помимо оксида углерода (II), метан и аргон. Окончательная очистка АВС достигается каталитическим гидрированием примесей, получившим название метанирования, или предкатализа. Этот процесс проводится в специальных установках метнирования при температуре 250–3000С и давлении около 30 МПа на никель–алюминиевом катализаторе (Ni + Al2O3). При этом протекают экзотермические реакции восстановления кислородсодержащих примесей до метана, который не является ядом для железного катализатора, а вода конденсируется при охлаждении очищенного газа и удаляется из него: CO + 3H2 CH4 +H2O – H, CO2 + 4H2 CH4 + 2H2O – H, O2 + 2H2 2H2O – H. Если в предкатализе используется железный катализатор, то в процессе гидрирования также образуется некоторое количество аммиака, в этом случае предкатализ называется продуцирующим. Очищенная АВС, поступающая на синтез, содержит до 0,0025 об.долей аргона, 0,0075 об.долей метана и не более 0,00004 об.долей оксида углерода (II), являющегося наиболее сильным каталитическим ядом. Азот и водород являются двумя основными сырьевыми материалами, используемыми в производстве аммиака. Азот — бесцветный газ без запаха, который составляет около 78% атмосферы Земли. Он нетоксичен и негорюч, его температура кипения составляет -196°C. Водород представляет собой бесцветный газ без запаха, легко воспламеняющийся и взрывоопасный на воздухе. Он имеет температуру кипения -253°C и является самым распространенным элементом во Вселенной. И азот, и водород получают из природного газа в процессе, известном как паровая конверсия метана. Природный газ сначала преобразуется в синтетический газ, представляющий собой смесь монооксида углерода, водорода и диоксида углерода. Затем синтетический газ разделяется на составляющие его газы, при этом азот получается в результате разделения воздуха, а водород получается в результате паровой конверсии метана. Химические реакции при производстве синтетического аммиака Производство синтетического аммиака включает реакцию между азотом и водородом с образованием аммиака. Химическое уравнение реакции: N2 + 3H2 ⇌ 2NH3 Реакция экзотермическая, то есть выделяется тепло. Скорость реакции также низкая, и для протекания реакции требуются высокое давление и температура. Процесс Габера-Боша является наиболее широко используемым процессом для производства синтетического аммиака. Химические реакции, связанные с производством синтетического аммиака Производство синтетического аммиака включает следующие химические реакции: N2(г) + 3H2(г) ⇌ 2NH3(г) ΔH = -92,4 кДж/моль Эта реакция является экзотермической, а это означает, что она высвобождает энергию в виде тепла. Температура. Повышение температуры способствует увеличению скорости реакций и коэффициента диффузии аммиака в смеси и поэтому является наиболее эффективным средством увеличения скорости процесса, протекающего преимущественно в диффузионной области. Процесс Габера-Боша включает реакцию между азотом и водородом в присутствии катализатора с образованием аммиака. Реакция является экзотермической, и выделяемое при реакции тепло используется для поддержания температуры, необходимой для протекания реакции. Термодинамика реакции сложна, и на реакцию влияют давление, температура и присутствие катализатора. 2.1 Основная технологическая часть Основная стадия процесса синтеза аммиака из азотоводородной смеси описывается уравнением N2 + 3H2 = 2NH3. Так как преобладающим методом получения АВС является конверсия метана воздухом и водяным паром, химическая схема производства аммиака включает помимо этой реакции несколько реакций воздушной и паровой конверсии: CH4 + H2O = 3H2 + CO, CH4 + 0,5O2= 2H2+ CO 15 и последующего превращения оксида углерода (II) в оксид углерода (IV): CO + H2O = H2 + CO2. После удаления оксида углерода (IV) из газовой смеси и коррекции ее состава получают АВС с содержанием азота и водорода в отношении 1 : 3. Таким образом, современное производство аммиака состоит из двух стадий: приготовления АВС и превращения ее в аммиак, представляя единую энерготехнологическую схему, в которой сочетаются операции получения АВС, ее очистки и синтеза аммиака и эффективно используются тепловые эффекты всех стадий процесса, что позволяет в несколько раз снизить затраты электроэнергии. На рис. 1 приведена принципиальная схема производства аммиака, отвечающая рассмотренной выше химической схеме.  Рисунок 1 – Принципиальная схема производства аммиака: 1 – очистка природного газа от сернистых соединений; 2 – паровая конверсия метана; 3 – воздушная конверсия метана; 4 – конверсия оксида углерода (II); 5 – хемосорбци– онная очистка АВС; 6 – метанирование; 7 – синтез аммиака; 8 – абсорбция аммиака; 9 – сжатие аммиака Рисунок 1 – Принципиальная схема производства аммиака: 1 – очистка природного газа от сернистых соединений; 2 – паровая конверсия метана; 3 – воздушная конверсия метана; 4 – конверсия оксида углерода (II); 5 – хемосорбци– онная очистка АВС; 6 – метанирование; 7 – синтез аммиака; 8 – абсорбция аммиака; 9 – сжатие аммиакаПроизводство синтетического аммиака включает несколько технологических схем, каждая из которых имеет свои преимущества и недостатки. Блок-схема, выбранная для производства синтетического аммиака, зависит от нескольких факторов, включая желаемую производственную мощность, доступность сырья и экономическую целесообразность. Различные технологические схемы производства синтетического аммиака включают процесс Габера-Боша, процесс Келлога. Соображения по проектированию каждой блок-схемы различаются в зависимости от конкретного процесса. 2.2 Обзор различных технологических схем производства синтетического аммиака В зависимости от применяемого давления агрегаты синтеза аммиака делятся на три группы: работающие при среднем давлении 25—36 МПа, при высоких давлениях 45—100 МПа и при низких давлениях 10—20 МПа. В нашей стране работают и строятся преимущественно агрегаты среднего давления, эксплуатируется также несколько агрегатов под давлением 45 МПа. В мировой практике также наибольшее распространение получили агрегаты среднего давления. Независимо от применяемого давления в состав агрегата входит колонна синтеза, теплообменная и конденсационная аппаратура, сепараторы для выделения жидкого аммиака из азотоводородной смеси и циркуляционный компрессор (или инжектор) для возврата непрореагировавшей азотоводородной смеси в колонну синтеза. Основным аппаратом агрегата является колонна синтеза. Она имеет катализаторную коробку, в которой размещен катализатор, итеплообменник, где азотоводородная смесь нагревается до температуры синтеза аммиака за счет тепла газовой смеси, прошедшей катализатор. Во многих конструкциях в слое катализатора размещены теплообменные трубки. С их помощью отводится тепло реакции так, чтобы катализатор работал при температурах, близких к оптимальным. Наличие требуемой теплообменной поверхности обеспечивает работу колонны без подвода тепла извне, а лишь за счет рекуперации тепла реакции. В новейших конструкциях колонн синтеза тепло реакции используется более полно не только для подогрева азотоводородной смеси, но и для выработки пара или подогрева воды, подаваемой на выработку пара. Для разогрева катализатора и его восстановления при пуске колонны синтеза имеется внутренний электроподогреватель либо выносной газовый подогреватель. На современных установках для охлаждения азотоводородной смеси и конденсации аммиака применяется воздух и жидкий аммиак. На старых установках вместо воздуха используется вода. Для циркуляции азотоводородной смеси в агрегатах мощностью 1360 т/сут аммиака служит циркуляционное колесо, размещенное в корпусе центробежного компрессора азотоводородной смеси, создающее перепад давления, равный 3 МПа. На более мелких установках для этой цели установлены центробежные циркуляционные компрессоры, которые заменили работавшие ранее поршневые циркуляционные компрессоры. Последние загрязняли газ парами масла и для их обслуживания требовалось большое число эксплуатационного и ремонтного» персонала.  Агрегат с центробежным циркуляционным компрессором. Азотоводородная смесь, содержащая 86% N2+Н2), 3,5— 4% NH3 и 10—10,5% (СН4+Аr), под давлением 32 МПа поступает в колонну синтеза 2 (рис.1), где при объемной скорости 20000—25000 ч-1 и температуре 450—520 °С образуется аммиак. Из колонны синтеза при 160—170 °С выходит азотоводородная смесь, содержащая 73,5—74% (N2+Н2), 15—15,5% -NН3, 11—11,5% (СН4+Аr). Она охлаждается, проходя по трубкам водяного конденсатора 1, при этом часть образовавшегося аммиака конденсируется. Газ, охлажденный до 25—35 °С, проходит сепаратор 6, где сконденсировавшийся аммиак отделяют ют газа, дросселируют до 1,6 МПа и сливают в сборник жидкого аммиака 7, а из него направляют на склад аммиака. В результате дросселирования аммиака из него выделяют танковые газы, т. е. газы, растворившиеся в жидком аммиаке высокого давления. После сепаратора 6 газовая смесь направляется на дальнейшее охлаждение и конденсацию аммиака в конденсационную колонну 4. В верхней ее части расположен теплообменник, нижняя часть колонны является сепаратором. Проходя через теплообменник конденсационной колонны, а затем испаритель 5, газовая смесь охлаждается до (—5) — (10)°С кипящим в межтрубном пространстве аммиаком. Далее в сепарационной части колонны сконденсировавшийся аммиак отделяют от газов, дросселируют до 1,6 МПа и сливают в сборник 7, а затем передают на склад. В конденсационной колонне в слой жидкого аммиака вводят свежий газ, в котором помимо азота и водорода содержится около 1% (СН4+Аr), водяные пары и следы СО и С02. При барботировании через слой жидкого аммиака из свежего газа вымываются катализаторные яды — Н20 и С02, затем газ смешивается с основным потоком азотоводородной смеси, выходящей из испарителя, отдает свой холод в теплообменнике конденсационной колонны и поступает в циркуляционный компрессор 3 центробежного типа при температуре примерно 20—23 °С. Таким образом, теплообменник конденсационной колонны выполняет важную роль — рекуперирует холод циркуляционного газа и уменьшает расход жидкого аммиака на охлаждение газа в испарителе. Назначением циркуляционного компрессора является сжатие циркуляционного газа до 32 МПа и подача его в колонну синтеза, что замыкает цикл синтеза. С помощью компрессора компенсируется потеря напора, равная 2,5—3 МПа, при прохождении азотоводородной смеси через аппаратуру и коммуникации цикла синтеза. Центробежный циркуляционный компрессор (ЦЦК) приводится в движение электродвигателем с постоянным числом оборотов и имеет постоянную производительность. Поскольку газовая нагрузка на колонну синтеза меняется по мере старения катализатора и снижения его активности, предусмотрено регулирование потока газа, подаваемого в колонну синтеза. Избыточное количество газа, подаваемого ЦЦК, по байпасу поступает в межтрубное пространство теплообменника конденсационной колонны, проходит испаритель и трубное пространство конденсационной колонны и вновь проходит через ЦЦК. При циркуляции азотоводородной смеси часть ее на катализаторе превращается в аммиак; присутствующие в газе аргон и метан постепенно накапливаются в цикле синтеза аммиака. Во избежание накопленияинертных примесей небольшая часть азотоводородной смеси (продувочные газы), содержащая примерно 11 % аргона и метана, непрерывно выводится из цикла синтеза после сепаратора 6 и поступает на установку для поглощения содержащегося в смеси аммиака водой с получением аммиачной воды. Непоглощенные газы, содержащие водород, азот, метан и аргон, используются как горючие газы. Агрегат высокого давления с инжектором. На рис.2 показана схема агрегата мощностью 75 000 т/год аммиака, работающего под давлением 44 МПа. По этой схеме перерабатывается азотоводородная смесь (свежий газ), очищенная от катализаторных ядов промывкой жидким азотом. Содержание инертных газов в ней очень мало, поэтому постоянная продувка не требуется. В свежем газе отсутствуют водяные пары и диоксид углерода. Такой газ подается в цикл непосредственно перед колонной синтеза. Свежий газ из отделения компрессии под давлением 49 МПа поступает в инжектор 6, т. е. в газоструйный циркуляционный компрессор. Cвежий газ поступает в сопло инжектора 3, профиль и сечение которого выбирают таким образом, чтобы поток свежего газа выходил из сопла с очень большой скоростью. Циркуляционный газ под давлением 43 МПа входит в смесительную камеру инжектора, расположенную после сопла. За счет кинетической энергии струи свежего газа, вытекающей из сопла, циркуляционный газ засасывается потоком свежего газа и поступает в расширяющийся диффузор 1, где кинетическая энергия газового потока преобразуется в давление, равное 44 МПа. Затем газовая смесь подается в колонну синтеза 5 (см. рис. III.4), проходит теплообменник, нагреваясь в нем до 440—450 СС, и попадает в катализаторную коробку. Здесь на четырех полках размещены четыре слоя катализатора. После каждого из первых трех слоев катализатора расположены змеевики, по которым циркулирует бидистиллят (дважды дистиллированная вода) высокого давления. Бидистиллят нагревается за счет охлаждения азотоводородной смеси до 450—460 °С и отводит таким образом тепло реакции образования аммиака в каждом слое катализатора. Конвертированный газ проходит четвертый слой катализатора и поступает в теплообменник колонны синтеза, где охлаждается от 500—510 до 100—120°С и нагревает газ, направляемый на синтез аммиака. Газ, выходящий из колонны синтеза и содержащий 20—22% аммиака, охлаждается до 25—35 °С в вертикальном погружном водяном конденсаторе 7. Сконденсировавшийся аммиак выделяется в сепараторе 8. После сепаратора жидкий аммиак дросселируют до 1,8 МПа; его сливают в промежуточный сборник 9, а из него передают на склад для отгрузки потребителю. Циркуляционный газ из сепаратора, содержащий 6—8% аммиака, поступает в инжектор 6 и цикл синтеза замыкается. Бидистиллят, нагретый в змеевиках колонны синтеза, охлаждается до 260 °С в трубах котла 4. При этом питательная вода, додаваемая в межтрубное пространство котла, испаряется, образуя 7,75 т/ч насыщенного пара при давлении 3,2 МПа и температуре 237 °С. Следовательно, на 1 т аммиака получают 0,85 т насыщенного пара. Бидистиллят по выходе из парового котла засасывается циркуляционным насосом высокого давления 3 производительностью 40 м3/ч и подается вновь в змеевики колонны синтеза. Для восполнения потерь циркулирующего бидистиллята устанавливают насос высокого давления производительностью 80 л/ч. Для поддержания определенного давления циркулирующего бидистиллята и для подпитки системы установлен уравнительный сосуд 2, в верхнюю часть которого подводят свежий газ под давлением 49 МПа. К качеству бидистиллята (содержание солей) предъявляются жесткие требования (контроль осуществляется путем измерения омического сопротивления бидистиллята). Это необходимо для предотвращения забивки солями теплопередающих поверхностей змеевиков и парового котла. К особенностям этого агрегата, обусловленным применением высокого давления относятся: 1) высокая концентрация аммиака после колонны синтеза; 2) простота технологической схемы (отсутствие аммиачного охлаждения, так как весь аммиак конденсируется в водяном конденсаторе); 3) получение только жидкого аммиака, что облегчает его последующее использование и переработку в карбамид и азотную кислоту; 4) применение инжектора для циркуляции газа, что значительно проще; однако к. п. д. инжектора значительно ниже, чем. к. п. д. ЦЦК; 5) использование тепла синтеза аммиака для выработки насыщенного водяного пара (0,85 т/т аммиака, что эквивалентно получению 2300 МДж тепла); 6) компрессоры, сжимающие газ до 49 МПа, значительно сложнее компрессоров, сжимающих газ до 32 МПа, поэтому возрастает расход электроэнергии на сжатие азотоводородной смеси. В целом этот агрегат менее экономичен, чем агрегаты мощностью 1360 т/сут аммиака, поэтому он получил весьма ограниченное применение.  Рис.2 Схема агрегата высокого давления Агрегат мощностью 1360 т/сут аммиака. В настоящее время практически все вводимые в эксплуатацию агрегаты синтеза аммиака рассчитаны на мощность 1360 т/сут. Схема этого агрегата показана на рис. 3.  Рис. 3 Схема агрегата синтеза аммиака мощностью 1360 т/сут: 1— газовый подогреватель; 2 — колонна синтеза; 3 — подогреватель воды; 4 — выносной теплообменник; 5 — воздушный холодильник; 6 — сепаратор; 7 — циркуляционное колесо компрессора; 8 — конденсационная колонна; 9 — испаритель; 10 — сборник жидкого аммиака; Р1 Р2, Р2/, Р3, Р4, P5— регуляторы температур; Р6, Р7, Р8, Р9, Р10 — регуляторы уровня; Р11 — регулятор давления. Циркуляционный газ входит во внутренний теплообменник колонны синтеза 2, где нагревается до температуры начала реакции синтеза аммиака и проходит слои катализатора, в результате чего концентрация аммиака в газе повышается до 15—17%- Затем конвертированный газ охлаждается в теплообменнике до 330 °С и в подогревателе воды 3 до 215 °С. В аппарате 3 большая часть тепла синтеза аммиака расходуется на нагревание воды высокого давления от 102 до 310 СС. Эта вода испаряется в котлах конверсии метана и СО с образованием пара давлением 10,5 МПа. Далее конвертированный газ охлаждается в выносном теплообменнике 4 до 65—75 °С и в воздушном холодильнике 5 до 30—40 °С. Жидкий аммиак, сконденсировавшийся при охлаждении, отделяется от газовой смеси в сепараторе 6. После 'сепаратора конвертированный газ сжимается от 28,5 до 31,5 МПа в циркуляционном колесе компрессора азотоводородной смеси 7, с помощью которой компенсируются потери давления в агрегате синтеза. Дальнейшее охлаждение газа и конденсация аммиака происходят в теплообменнике конденсационной колонны S и в испарителе 9 (в последнем газ охлаждается до —4°С за счет кипения жидкого аммиака). Сконденсировавшийся аммиак отделяется от газовой смеси в сепарационной части конденсационной колонны, сюда же поступает свежий газ, который барботирует через слой жидкого аммиака, поглощающий водяные пары и следы С02. Циркуляционный газ, выйдя из конденсационной колонны, поступает в выносной теплообменник 4, где нагревается до 185—190 °С за счет тепла конвертированного газа, проходящего по трубному пространству. Затем подогретый газ поступает в колонну синтеза и цикл синтеза замыкается. Для разогрева и восстановления катализатора в колонне синтеза установлен газовый подогреватель 1. Циркулирующая в нем азотоводородная смесь постепенно нагревается до требуемой температуры, проходя по змеевикам подогревателя, которые обогреваются горячими дымовыми газами, получаемыми путем сжигания горючих газов в горелках. Жидкий аммиак из сепаратора 6 и конденсационной колонны 8 проходит фильтры жидкого аммиака (на схеме не показаны), где из него выделяется катализаторная пыль, унесенная конвертированным газом из слоя катализатора. Затем аммиак дросселируют до 4 МПа и отводят в сборники 10, а далее на склад. После сепаратора 6 непрерывно выводятся продувочные газы, содержащие 8—9% аммиака. В танковых газах из сборников 10 содержание аммиака близко к 20%. Количество продувочных и танковых газов относительно велико, поэтому в состав агрегата включена установка выделения аммиака. Танковые газы поступают в испаритель 3, где охлаждаются до —20°С; сконденсированный аммиак отделяется от газов в сепараторе 4 и передается на склад. Танковые газы, практически свободные от аммиака, используются как горючий газ. Газы постоянной продувки поступают в межтрубное пространство конденсационной колонны 1 продувочных газов, охлаждаются и затем в испарителе 2 дополнительно охлаждаются до —27 °С аммиаком, кипящим в межтрубном пространстве испарителя при —30 °С. Охлажденный газ вновь возвращают в конденсационную колонну для отделения сконденсировавшегося аммиака и для охлаждения в теплообменнике аппарата 1 поступающих продувочных газов. После установки улавливания аммиака продувочные газы содержат 1% NH3. Затем они дросселируются с 28,5 до 1 МПа и используются вместе с танковыми газами в горелках трубчатой печи. Каждая блок-схема имеет свои уникальные особенности проектирования. Процесс Габера-Боша требует высокого давления и температуры, а также использования катализатора. В процессе Келлог используется реактор с псевдоожиженным слоем, а в процессе используется трубчатый реактор. В процессе КБР используется реактор с псевдоожиженным слоем и установка вторичного риформинга. Каждая блок-схема имеет свой набор преимуществ и недостатков. Процесс Габера-Боша является наиболее широко используемым процессом и имеет высокую производительность. Процесс Келлога имеет более низкую производительность, но более энергоэффективен. Процесс Уде имеет высокую производительность, но менее энергоэффективен. Процесс с средним давлением более энергоэффективен и имеет более высокую производительность, чем процесс Келлога. 2.2 Выбор схемы производства Определяющим параметром в производстве аммиака из азотоводородной смеси является давление синтеза. В зависимости от применяемого давления все системы производства синтетического аммиака делятся на: системы низкого давления (10–15 МПа), системы среднего давления (25–60 МПа), системы высокого давления (60–100 МПа). Методом математического моделирования было найдено, что экономически наиболее выгодным является проведение процесса при среднем давлении. На стадиях компрессии газа, синтеза аммиака и конденсации его из АВС капитальные и энергоматериальные затраты с повышением давления снижаются до определенного предела. Оптимальным давлением является давление 32 МПа. Дальнейшее повышение давления не приводит к существенному снижению затрат, но усложняет технологическую схему производства. В системе среднего давления обеспечивается достаточно высокая скорость процесса, простота выделения аммиака из газовой смеси, возможность одновременного получения жидкого и газообразного продуктов. Вследствие этого в мировой и отечественной практике распространены установки среднего давления. На рис.1 приведена технологическая схема современного производства аммиака, при среднем давлении производительность 1360 т/сутки. Режим ее работы характеризуется следующими параметрами: 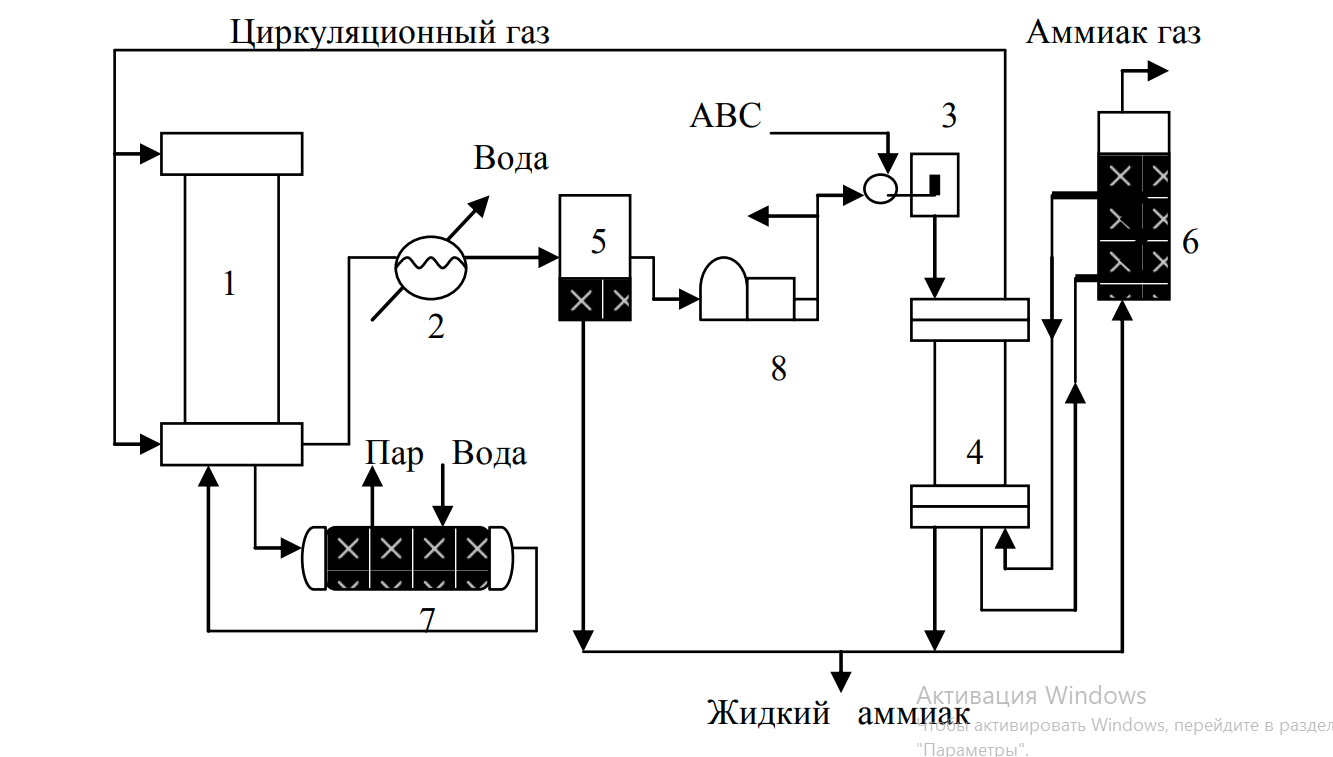 Жидкий аммиак Рисунок 1. – Технологическая схема производства аммиака: 1 – колонна синтеза; 2 – водяной конденсатор; 3 – смеситель (инжектор) свежей АВС и циркуляционного газа; 4 – конденсационная колонна,; 5 – газоотделитель; 6 – испаритель жидкого аммиака; 7 – выносной теплообменник (котел–утилизатор); 8 – трубоциркуля– ционный компрессор температура контактирования 450–5500С; давление 32 МПа; объемная скорость газовой смеси 4 104 нм 3 /м3 ч; состав азотоводородной смеси стехометрический. Смесь свежей АВС и циркуляционного газа под давлением подается из смесителя 3 в конденсационную колонну 4, где из циркуляционного газа конденсируется часть аммиака, откуда поступает в колонну синтеза 1. Выходящий 25 из колонны газ, содержащий до 0,2 об.дол.аммиака (2) направляется в водяной холодильник–конденсатор 2 и затем в газоотделитель 5, где из него отделяется жидкий аммиак. Оставшийся газ после компрессора 8 смешивается со свежей АВС и направляется сначала в конденсационную колонну 4, а затем в испаритель жидкого аммиака 6, где при охлаждении до –200С также конденсируется большая часть аммиака. Затем циркуляционный газ, содержащий около 0,03 об.дол.аммиака, поступает в колонну синтеза 1. В испарителе 6 одновременно с охлаждением циркуляционного газа и конденсацией содержащегося в нем аммиака происходит испарение жидкого аммиака с образованием товарного газообразного продукта. Основной аппарат технологической схемы – колонна синтеза, представляющая собой реактор РИВ–Н. Колонна состоит из корпуса и насадки различного устройства, включающей катализаторную коробку с размещенной в ней контактной массой, и систему теплообменных труб. Для процесса синтеза аммиака существенное значение имеет оптимальный температурный режим. Для обеспечения максимальной скорости синтеза процесс следует начинать при высокой температуре и по мере увеличения степени превращения понижать ее в соответствии с линией оптимальных температур (ЛОТ), как это показано на рис. Регулирование температуры и обеспечение автотермичности процесса обеспечиваются с помощью теплообменников, расположенных в слое контактной массы и дополнительно подачей части холодной АВС в контактную массу, минуя теплообменник. С учетом последовательного изменения температуры при прохождении реакционной смеси и продуктов реакции через теплообменные устройства, катализаторную коробку и 26 котел–утилизатор температурный режим работы колонны синтеза может быть представлен графиком. Для защиты корпуса колонны от действия высоких температур, способствующих диффузии водорода в сталь и ее разрушению, холодная АВС, поступающая в колонну, прежде чем пройти в катализаторную коробку проходит сначала по кольцевому пространству между корпусом и насадкой, непрерывно омывая стенки колонны и охлаждая их. – Изменение температуры в катализаторной коробке. График изменения температур в колонне синтеза В промышленности выпускаются два сорта (первый и второй) жидкого аммиака и водный раствор его (аммиачная вода). Согласно с ГОСТом 6221–75 аммиак первого сорта должен содержать не менее 99,9% и второго сорта не менее 27 99,6% NH3. Аммиак 1–го сорта применяется в качестве хладоагента в холодильных машинах и минерального удобрения, 2–го сорта – используется в производстве азотной кислоты. 3. Расчетная часть Производство синтетического аммиака требует использования сырья, такого как азот, водород и природный газ. Потребность в энергии для производства синтетического аммиака также значительна. Производство синтетического аммиака включает в себя реакцию газов азота и водорода при высоком давлении и температуре. В процессе обычно используется технология , для которой требуется следующее сырье: Азот: Газообразный азот поступает из воздуха, который в основном состоит из азота (около 78% по объему). Водород: газообразный водород может быть получен из различных видов сырья, таких как природный газ, уголь или вода, путем электролиза. Стехиометрическое уравнение для синтеза аммиака имеет вид: N2 + 3H2 --> 2NH3 Из этого уравнения мы можем определить стехиометрические соотношения азота и водорода, необходимые для получения определенного количества аммиака. Например, для производства одной тонны аммиака нам потребуется: 3,18 тонны водорода 0,54 тонны азота Энергозатраты на производство синтетического аммиака значительны. Процесс является очень экзотермическим, выделяя большое количество тепла. Однако реакция также требует значительных затрат энергии для преодоления энергетического барьера активации и продвижения реакции вперед. Потребности в энергии для процесса Haber-Bosch обычно составляют от 25 до 35 ГДж / т производимого аммиака. В заключение, чтобы оценить потребности в сырье и энергии для производства синтетического аммиака, нам необходимо учитывать следующие факторы: Азотное и водородное сырье Стехиометрические соотношения азота и водорода, необходимые для получения аммиака 3.1 Материальный рассчет Для расчета эффективности и выбора оптимальной технологической схемы производства синтетического аммиака необходимо учитывать следующие факторы: Сырье и ресурсы: синтез аммиака осуществляется из водорода и азота, поэтому необходимо обеспечить постоянный и стабильный доступ к этим сырьевым материалам. Кроме того, производство аммиака требует больших объемов энергии, поэтому необходимо обеспечить доступ к надежным источникам энергии. Технология производства: наиболее распространенной технологией производства синтетического аммиака является процесс Хабера-Боша. Однако существуют и другие технологии, которые могут быть более эффективными с точки зрения затрат на производство и экологических факторов. Например, технология производства аммиака из возобновляемых источников энергии, таких как ветроэнергия или солнечная энергия. Объем производства: объем производства синтетического аммиака должен быть определен на основе потребностей рынка и доступных ресурсов. При этом необходимо учитывать экономическую целесообразность производства на данном объеме. Экологические факторы: производство синтетического аммиака является значительным источником выбросов углекислого газа, который является основным газом, способствующим изменению климата. Поэтому при выборе технологии производства и объема производства необходимо учитывать возможность снижения выбросов и внедрения более экологически чистых технологий. Для материального расчета и обоснования выбора оптимальной технологической схемы производства синтетического аммиака необходимо провести следующие этапы: Определение потребностей рынка и доступных ресурсов: необходимо провести анализ потребностей рынка в синтетическом аммиаке и определить доступные ресурсы для производства, такие как доступность сырья, источники энергии, наличие инфраструктуры и т.д. Эта информация поможет определить возможный объем производства и выбор оптимальной технологической схемы. Выбор технологической схемы: на основе анализа доступных технологий производства синтетического аммиака, необходимо выбрать оптимальную технологическую схему с учетом затрат на производство, энергоэффективности и экологических факторов. Расчет стоимости производства: на основе выбранной технологической схемы необходимо провести расчет затрат на производство синтетического аммиака, включая затраты на сырье, энергию, технологическое оборудование, персонал и т.д. Это поможет определить экономическую целесообразность производства на заданном объеме и выбрать оптимальный объем производства. Оценка экологических факторов: необходимо оценить экологические факторы производства синтетического аммиака, включая выбросы углекислого газа и других вредных веществ, а также возможности их снижения. Это поможет выбрать технологическую схему и объем производства, которые будут наиболее экологически чистыми и соответствующими мировым требованиям по защите окружающей среды. Сравнение и выбор оптимального варианта: на основе проведенных расчетов необходимо сравнить различные варианты производства синтетического аммиака и выбрать оптимальный, который будет наиболее эффективным с точки зрения затрат, энергоэффективности, экологической чистоты и соответствия потребностям рынка. Таким образом, материальный расчет и обоснование выбора технологической схемы производства синтетического аммиака является сложным и многопроцессным процессом, который требует учета многих факторов и проведения глубокого анализа. Совершенствование промышленного производства аммиака идет по следующим основным направлениям: – кооперация производства аммиака с производствами основного органического синтеза на базе использования природного газа и газов нефтепереработки; – создание агрегатов большой (до 3000 т/сутки) единичной мощности; – применение колонн синтеза с кипящим слоем катализатора; – разработка новых катализаторов, устойчивых к ядам с низкой (3000С) температурой зажигания, позволяющих вести процесс синтеза без снижения выхода аммиака при низких (10 МПа) давлениях Существует несколько способов снижения расхода энергии и сырья при производстве синтетического аммиака. К ним относятся использование более эффективных технологических схем производства, использование альтернативного сырья и использование возобновляемых источников энергии. 3.2 Тепловой рассчет Рассмотрено и описано основное технологическое оборудование и технологический процесс производства аммиака. Очищенный природный газ с давлением 25 атмосфер поступает в компрессор синтез газа. Газ сжимается и направляется в подогреватели. Затем поступает в реактор гидрирования сероорганических соединений. Адсорбируется до H2 S. Газ нагревается в трубчатой печи и переходит в шахтный конвертор. В паровой котел подается вода за счет применения электронасоса. Из данного резервуара вода по специальным отводным трубам стекает в коллектор. В конверторе находится СО и имеется абсорбер СО2 . Для связывания диоксида углерода и влаги в линию газа перед холодильником насосами впрыскивается жидкий аммиак. Затем газ поступает в воздушный холодильник, в котором он охлаждается и потом направляется в конденсационную колонну. В теплообменнике газ нагревается и переходит в сепаратор, в котором производится отделение сконденсировавшейся жидкости из охлажденного газа. Произвели практический расчет материального баланса производства по следующим исходным данным: состав газа поступающего в колонну: массовая доля NH3 – 3,8 %, H2 – 61,95 %, N2 – 20,65 %, CH4 – 9,7 %, Ar – 3,9 %, давление в колонне – 25 атмосфер, температура – 500ºС, степень использования – 0,9. Зная состав циркуляционного газа на входе, рассчитали содержание компонентов смеси. Для расчета содержания компонентов смеси воспользовались формулой: где n – количество циркуляционного газа; ω(NH3 ) – массовая доля аммиака. Количество сконденсировавшегося аммиака рассчитали по уравнению: где Nам 2 – количество аммиака после колонны; ∑ni – сумма количеств веществ смеси после колонны; Δnж – количество сконденсировавшегося NH3 при первой конденсации. 4.1 Охрана труда и окружающей среды Производство синтетического аммиака связано со значительными соображениями безопасности, и должны быть приняты строгие меры безопасности для обеспечения безопасности рабочих. Кроме того, меры по охране окружающей среды необходимы для снижения воздействия производства синтетического аммиака на окружающую среду. Труд играет решающую роль в производстве синтетического аммиака, и роль труда в производственном процессе должна быть адекватно рассмотрена. 4.2 Вопросы безопасности при производстве синтетического аммиака Производство синтетического аммиака связано с работой с высокореакционными и потенциально опасными материалами. Следовательно, соображения безопасности имеют решающее значение для обеспечения защиты рабочих и окружающей среды. Синтез аммиака требует использования оборудования высокого давления и высокотемпературных условий реакции, которые представляют значительную угрозу безопасности. Кроме того, реагенты и продукты легковоспламеняющиеся и токсичные, что увеличивает риск несчастных случаев. Во время производственного процесса необходимо принять несколько мер безопасности, чтобы свести к минимуму риски. Во-первых, необходимо строгое соблюдение стандартных рабочих процедур (СРП), и все рабочие должны быть обучены обращению с опасными материалами, аварийным процедурам и использованию средств индивидуальной защиты (СИЗ). Использование СИЗ, таких как респираторы, защитные очки и перчатки, может защитить рабочих от воздействия токсичных веществ и предотвратить несчастные случаи. Еще одной важной мерой безопасности является регулярный осмотр и техническое обслуживание оборудования для обеспечения его правильной и безопасной работы. Отказы или неисправности оборудования могут привести к опасным ситуациям, представляющим опасность для рабочих и окружающей среды. Надлежащий мониторинг оборудования и плановое техническое обслуживание могут помочь выявить потенциальные проблемы и предотвратить несчастные случаи. В дополнение к безопасности работников, защита окружающей среды также имеет большое значение в производстве синтетического аммиака. Производственный процесс создает несколько опасностей для окружающей среды, включая загрязнение воздуха и воды, а также выброс парниковых газов. Процесс Габера-Боша является энергоемким, а сжигание ископаемого топлива для получения энергии вносит значительный вклад в выбросы углерода. Меры по охране окружающей среды должны быть реализованы для минимизации воздействия производства синтетического аммиака на окружающую среду. Один из подходов заключается в снижении потребления энергии за счет использования более энергоэффективных методов производства или альтернативных источников энергии, таких как возобновляемые источники энергии. Технологии улавливания и хранения углерода также можно использовать для улавливания и хранения выбросов углерода в процессе производства. Схема производственного процесса играет решающую роль в минимизации воздействия производства синтетического аммиака на окружающую среду. Блок-схема должна быть разработана таким образом, чтобы свести к минимуму выброс загрязняющих веществ и снизить потребление энергии. Несколько конструктивных соображений могут помочь свести к минимуму воздействие производства синтетического аммиака на окружающую среду. Во-первых, использование энергоэффективных технологий позволяет снизить потребление энергии и выбросы углерода. Во-вторых, внедрение процедур обращения с отходами может помочь свести к минимуму выброс загрязняющих веществ в окружающую среду. Наконец, использование технологий УХУ может улавливать и хранить выбросы углерода, снижая их воздействие на окружающую среду. Производство синтетического аммиака требует квалифицированной рабочей силы, которая может эксплуатировать и обслуживать машины и оборудование, задействованные в процессе. Рабочая сила отвечает за эффективную работу завода, обеспечение бесперебойной работы процесса и решение любых проблем, которые могут возникнуть во время производства. Успех производства синтетического аммиака во многом зависит от навыков и знаний рабочей силы. Процесс Габера-Боша представляет собой сложный химический процесс, для которого требуются опытные и квалифицированные операторы, обладающие знаниями в области химических реакций, термодинамики и управления процессом. Операторы несут ответственность за мониторинг параметров процесса, включая температуру, давление и скорость потока, чтобы гарантировать, что процесс работает в безопасных и эффективных пределах. Они также должны быть в состоянии устранять любые проблемы, возникающие в процессе производства, такие как неисправности оборудования или изменения качества сырья. В дополнение к квалифицированным операторам для производства синтетического аммиака также требуется вспомогательный персонал, такой как техники по техническому обслуживанию, инженеры и административный персонал. Специалисты по техническому обслуживанию несут ответственность за поддержание машин и оборудования в хорошем рабочем состоянии, выполнение планового технического обслуживания и ремонта по мере необходимости. Инженеры участвуют в проектировании и разработке нового оборудования и процессов, а также совершенствуют существующие. Административный персонал занимается такими задачами, как ведение учета, планирование и заказ расходных материалов. Производительность труда является существенным фактором эффективности производства синтетического аммиака. Операторы должны уметь работать быстро и точно, чтобы поддерживать высокий уровень производительности. Эффективные программы обучения и обучения могут способствовать развитию навыков и знаний рабочей силы, повышению производительности труда и обеспечению безопасной и эффективной работы предприятия. Помимо производительности, безопасность труда также является важной проблемой при производстве синтетического аммиака. Химический процесс связан с обращением с опасными материалами и использованием оборудования высокого давления, что может представлять значительный риск для здоровья и безопасности рабочих. Руководство завода должно внедрить эффективную политику и процедуры безопасности, предоставить соответствующие средства индивидуальной защиты и обучить персонал безопасным методам работы. Труд играет решающую роль в производстве синтетического аммиака. Рабочие должны быть должным образом обучены и оснащены для безопасной работы с опасными материалами и сложным оборудованием. Обучение и обучение рабочих должны быть постоянными, и все работники должны быть ознакомлены с протоколами и процедурами безопасности. В дополнение к техническим навыкам работники должны обладать сильными навыками решения проблем и критического мышления для выявления и решения потенциальных проблем. Эффективная коммуникация между работниками и руководством также имеет решающее значение для обеспечения своевременного решения проблем безопасности. Технологическая часть Обзор различных технологических схем производства синтетического аммиака Существует несколько различных технологических схем, которые можно использовать для производства синтетического аммиака. Наиболее широко используемой схемой является процесс Габера-Боша, который включает реакцию между азотом и водородом в присутствии катализатор. Производство синтетического аммиака требует использования сырья, такого как азот, водород и природный газ. Потребность в энергии для производства синтетического аммиака также значительна. Производство синтетического аммиака включает в себя реакцию газов азота и водорода при высоком давлении и температуре. В процессе обычно используется технология , для которой требуется следующее сырье: Азот: Газообразный азот поступает из воздуха, который в основном состоит из азота (около 78% по объему). Водород: газообразный водород может быть получен из различных видов сырья, таких как природный газ, уголь или вода, путем электролиза. Стехиометрическое уравнение для синтеза аммиака имеет вид: N2 + 3H2 --> 2NH3 Из этого уравнения мы можем определить стехиометрические соотношения азота и водорода, необходимые для получения определенного количества аммиака. Например, для производства одной тонны аммиака нам потребуется: 3,18 тонны водорода 0,54 тонны азота Энергозатраты на производство синтетического аммиака значительны. Процесс является очень экзотермическим, выделяя большое количество тепла. Однако реакция также требует значительных затрат энергии для преодоления энергетического барьера активации и продвижения реакции вперед. Потребности в энергии для процесса Haber-Bosch обычно составляют от 25 до 35 ГДж / т производимого аммиака. 1 2 |
