Выбрать конструкцию и рассчитать аппарат для охлаждения и конденсации газового потока состава 25 H2O; 70 этилового спирта, 5. курсовой проект конденсатора. Курсовой проект по пахт разработка конструкции и расчет теплообменного аппарата для охлаждения и конденсации газового потока состава 25 H
 Скачать 6.33 Mb. Скачать 6.33 Mb.
|
1 Аналитический обзор рассматриваемого процессаПоверхностная конденсация осуществляется в теплообменниках – поверхностных конденсаторах. В общем случае в поверхностных конденсатор поступает перегретых пар. Очень часто охлаждающим агентом является вода. Введем обозначения: D – количество поступающего в конденсатор пара, кг/ч; Н – энтальпия поступающего пара, кДж/кг; tп – температура поступающего перегретого пара, °С; tнас – температура насыщения (конденсации) пара, °С; tж температура конденсата на выходе из аппарата, °С; сп – теплоемкость перегретого пара, кДж/(кг·°С); сж – теплоемкость конденсата, кДж/(кг·°C); r – теплота конденсации пара (теплота испарения жидкости), кДж/кг; W – количество воды, поступающей на охлаждение, кг/ч; св – теплоемкость воды, кДж/(кг.°C); tв.н – начальная температура воды, tв.к – конечная температура воды, °С; Qп – потери тепла в окружающую среду, кДж/ч. При принятых обозначениях энтальпию поступающего перегретого пара можно выразить соотношением H= сп (tн–tнас)+ r+ сж tнас И представить тепловой баланс процесса равенством DH+W св tв.н=D сж tж+ W св tв.к+ Qп Из которого определяют расход охлаждающей воды:  По условиям теплообмена охлаждающая поверхность конденсатора делится на три зоны: охлаждения перегретого пара, конденсации и охлаждения конденсата. Первой из них соответствуют наихудшие условия теплообмена, второй – наилучшие. В результате этого поверхности охлаждения приходится находить для каждой зоны в отдельности. Для определения их необходимо вычисление количеств тепла, передаваемого через поверхность охлаждения в каждой зоне, и промежуточных температур охлаждающей воды tв1 и tв2 (рисунок 1). 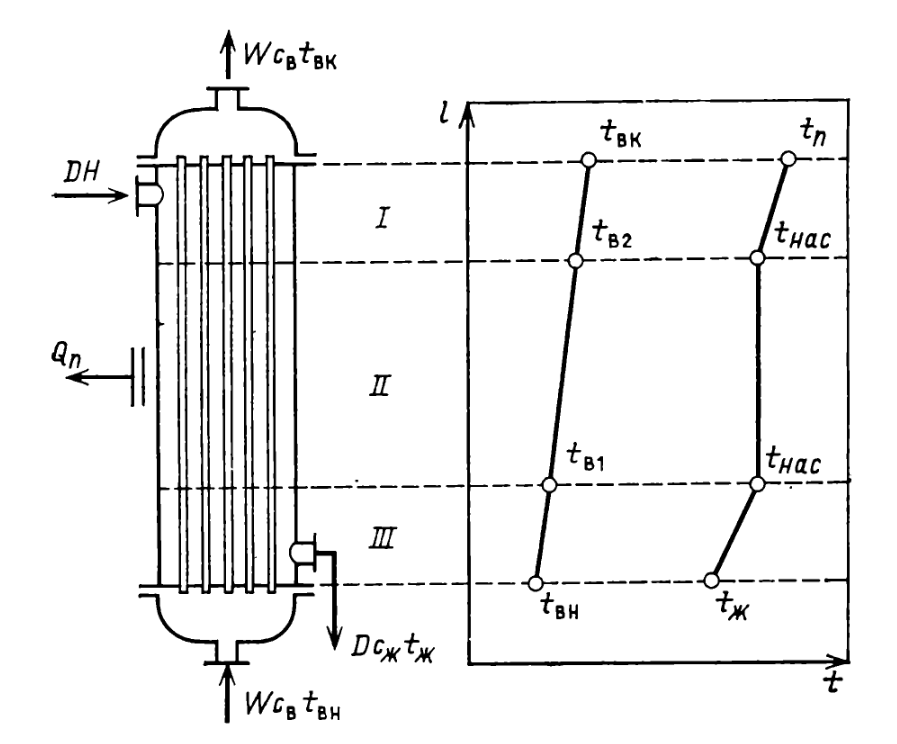 Рисунок 1 – К тепловому балансу процесса конденсации: Ⅰ - зона охлаждения перегретого пара; Ⅱ - зона конденсации; Ⅲ - зона охлаждения конденсата. Количество тепла, передаваемого через поверхность охлаждения в каждой из зон, находят из следующих равенств: для зоны охлаждения перегретого пара  Для зоны конденсации 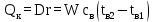 Для зоны охлаждения конденсата  Промежуточные температуры охлаждающей воды:   Значение требуемой поверхности теплообмена определяют по уравнению теплопередачи:
где F – площадь поверхности теплообмена, м2; K – коэффициент теплопередачи, Вт/(м2  час); час);Q – тепловой поток в аппарате, Вт/ч; 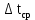 – средняя разность температур между теплоносителями, К. – средняя разность температур между теплоносителями, К. – температурный напор. – температурный напор.Для расчёта поверхности теплообмена удобнее всего принять, что аппарат работает в режиме идеального вытеснения, и разделить поверхности теплообмена на две части: зону конденсации и зону охлаждения конденсата [1]. Теория процессаКонденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость. В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, т. е. когда скорости процессов испарения и конденсации одинаковы. Такую систему называют двухфазной. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным. Число молекул, вылетающих с единицы площади поверхности жидкости за одну секунду, зависит от температуры жидкости. Число молекул, возвращающихся из пара в жидкость, зависит от концентрации молекул пара и от средней скорости их теплового движения, которая определяется температурой пара. Отсюда следует, что для данного вещества концентрация молекул пара при равновесии жидкости и ее пара определяется их равновесной температурой. Установление динамического равновесия между процессами испарения и конденсации при повышении температуры происходит при более высоких концентрациях молекул пара. Так как давление газа (пара) определяется его концентрацией и температурой, то можно сделать вывод: давление насыщенного пара p0 данного вещества зависит только от его температуры и не зависит от объема. Поэтому изотермы реальных газов на плоскости (p, V) содержат горизонтальные участки, соответствующие двухфазной системе (рисунок 2). 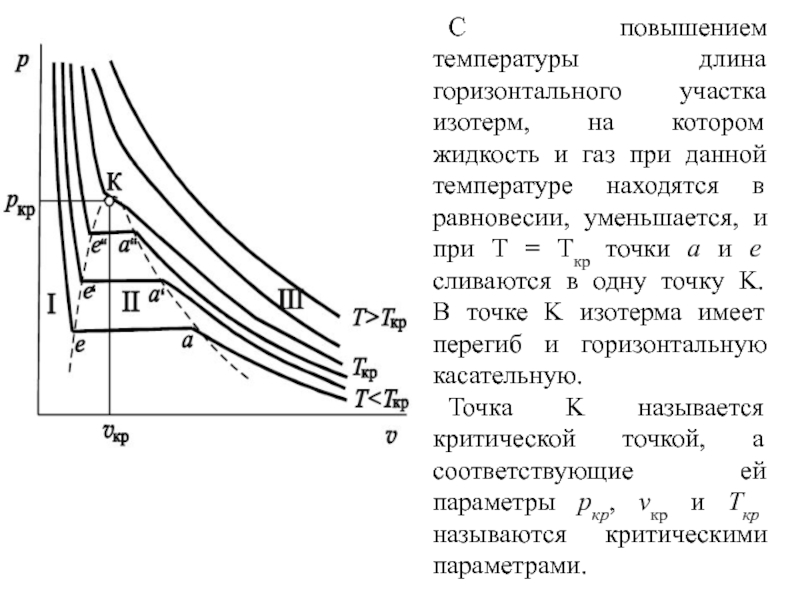 Область I – жидкость, область II – двухфазная система «жидкость + насыщенный пар», область III – газообразное вещество. K – критическая точка Рисунок 2 - Изотермы реального газа. [3] Теплоотдача при конденсации насыщенных паров. Этот вид теплоотдачи, а также теплоотдача при кипении жидкостей протекают при изменении агрегатного состояния теплоносителей. Особенность этих процессов состоит прежде всего в том, что тепло подводится или отводится при постоянной температуре. Теплоотдача при конденсации насыщенных паров представляет собой сложное явление одновременного переноса теплоты (определяемое теплотой парообразования) и массы (определяемой количеством сконденсированного пара). Конденсация насыщенного пара на охлаждаемой поверхности приводит к значительной интенсификации теплообмена по сравнению, например, с теплообменом от газа к стенке. При этом механизм конвекции совершенно иной. Молекулы пара не только переносятся к охлаждаемой стенке вихрями турбулентного потока, но и создают еще и собственное поступательное движение к стенке, так как в непосредственном соседстве с ней происходят конденсация пара и резкое уменьшение его объема. Образовавшийся конденсат стекает по стенке, а к стенке подходит свежий пар. Чем холоднее стенка, тем интенсивнее идут конденсация и движение молекул пара к стенке. Перенос теплоты и основной массы пара к стенке идет настолько быстро, что степень турбулизации потока не оказывает существенного влияния на процесс и часто может не учитываться в расчетах. На хорошо смачиваемых поверхностях капли конденсата, сливаясь друг с другом, образуют жидкую пленку, которая под действием силы тяжести стекает вниз. Такую конденсацию пара называют пленочной. На несмачиваемой или плохо смачиваемой поверхности капли конденсата быстро стекают («скатываются») по поверхности стенки, не образуя пленки. Такой вид конденсации называют капельной. Капельная конденсация на практике реализуется редко, несмотря на то что коэффициенты теплоотдачи в этом случае в несколько раз выше коэффициентов теплоотдачи при пленочной конденсации. Последнее объясняется тем, что и при пленочной конденсации коэффициенты теплоотдачи достаточно высоки, и поэтому стадия переноса теплоты при пленочной конденсации обычно не является лимитирующей в общем процессе теплопереноса. При пленочной конденсации на стенке вследствие разности температур образуется пленка конденсата, которая постепенно увеличивается по мере стекания. При этом увеличивается и термическое сопротивление пленки.[6] Основные физические свойства компонентов газового потока. Основные физические свойства этилового спирта при стандартных условиях: бесцветная летучая жидкость; имеет резкий запах и жгучий вкус; смешивается в произвольных отношениях с бензолом, водой, глицерином, ацетоном, метанолом; горюч, легче воды. Плотность этилового спирта 789,45 кг/м3 при 20 °C; 715,7 кг/м3 при 100 ºС, плотность паров 2,043 кг/м3 (0 ºС, 0,101 Мпа), 4,86 кг/м3 при 110 ºС. Температура кипения 78,39 °С. Стандартная мольная теплоёмкость Cp=1,197 Дж/моль·K (г) (при 298 К). Теплота испарения составляет 43250 кДж/моль при 20℃, 38938 кДж/моль при 77,4℃. Энтальпия кипения ΔHкип=839,3 кДж/моль. Этиловый спирт легко воспламеняется и в пожарном отношении очень опасен. Теплоёмкость пара этилового спирта при постоянном давлении равняется при температуре 108-220 ºС 1,897 кДж/(кг·К), при 350 ºС равна 2,562 кДж/(кг·К).[4]. Основные физические свойств воды при стандартных условиях: бесцветная летучая жидкость, не имеет вкуса и запаха, плотность 999,841 кг/м3 при 0℃; 999,8 кг/м3 при 8℃; 0,959 г/мл при 100 ℃. Плотность насыщенного пара при 100 ℃ составляет 0,598 кг/м3. Удельная теплоёмкость при 15℃ равна 4,1868·103Дж/(кг∙К). Температура кипения при 760 мм.рт.ст. и 100 ℃. Удельная теплота парообразования воды при атмосферном давлении и 100 °С 2250,8 кДж/(кг ∙ К). Теплопроводность водяного пара при атмосферном давлении и 100 °С равна 0,02 ккал/м ∙ ч ∙ °С. [5]. |

