работа по фито. Лекция 6 общие пути биологического окисления
 Скачать 2.87 Mb. Скачать 2.87 Mb.
|
|
Лекция № 6 ОБЩИЕ ПУТИ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ Метаболизм представляет собой высоко координированную и целенаправленную клеточную активность, обеспеченную участием многих взаимосвязанных ферментативных систем. Он выполняет три специализированные функции: 1. Энергетическая – снабжение клетки химической энергией, 2. Пластическая – синтез макромолекул как строительных блоков, 3. Специфическая – синтез и распад биомолекул, необходимых для выполнения специфических клеточных функций. АНАБОЛИЗМ Анаболизм – это биосинтез белков, полисахаридов, липидов, нуклеиновых кислот и других макромолекул из малых молекул-предшественников. Поскольку он сопровождается усложнением структуры, то требует затрат энергии. Источником такой энергии является энергия АТФ. 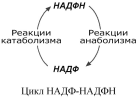 Также для биосинтеза некоторых веществ (жирные кислоты, холестерол) требуются богатые энергией атомы водорода – их источником является НАДФН. Молекулы НАДФН образуются в реакциях окисления глюкозо-6-фосфата ( см "Пентозофосфатный путь окисления глюкозы") и оксалоацетата (см "Биосинтез жирных кислот"). В реакциях анаболизма НАДФН передает свои атомы водорода на синтетические реакции и окисляется до НАДФ. Так формируется НАДФ-НАДФН-цикл. КАТАБОЛИЗМ Катаболизм – расщепление и окисление сложных органических молекул до более простых конечных продуктов. Оно сопровождается высвобождением энергии, заключенной в сложной структуре веществ. Большая часть высвобожденной энергии рассеивается в виде тепла. Меньшая часть этой энергии "перехватывается" коферментами окислительных реакций НАД и ФАД, некоторая часть сразу используется для синтеза АТФ. Следует заметить, что атомы водорода, высвобождаемые в реакциях окисления веществ, могут использоваться клеткой только по двум направлениям: 1) на анаболические реакции в составе НАДФН. 2) на образование АТФ в составе НАДН и ФАДН2 в дыхательной цепи митохондрий (см ниже). Весь катаболизм подразделяется на три этапа: I этап Происходит в кишечнике (переваривание пищи) или в лизосомах при расщеплении уже ненужных молекул. При этом освобождается около 1% энергии, заключенной в молекуле. Она рассеивается в виде тепла. II этап Вещества, образованные при внутриклеточном гидролизе или проникающие в клетку из крови, обычно превращаются в пировиноградную кислоту, ацетильную группу (в составе ацетил-SКоА), и в некоторые другие мелкие органические молекулы. Локализация второго этапа – цитозоль и митохондрии. Часть энергии рассеивается в виде тепла и примерно 13% энергии вещества усваивается, т.е. запасается в виде макроэргических связей АТФ. III этап Все реакции этого этапа идут в митохондриях. Ацетил-SКоА включается в реакции цикла трикарбоновых кислот и окисляется до углекислого газа. Выделенные атомы водорода соединяются с НАД и ФАД и восстанавливают их. После этого НАДН и ФАДН2 переносят водород в цепь дыхательных ферментов, расположенную на внутренней мембране митохондрий. Здесь в результате процесса под названием "окислительное фосфорилирование" образуется вода и главный продукт биологического окисления – АТФ. Часть выделенной на этом этапе энергии молекулы рассеивается в виде тепла и около 46% энергии исходного вещества усваивается, т.е. запасается в связях АТФ и ГТФ. 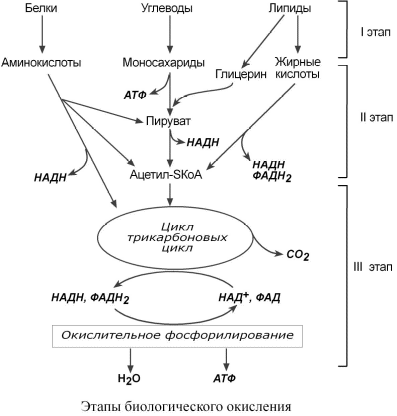 На втором этапе выделяется около 30% энергии, заключенной в молекуле. При этом запасается около 13% от всей энергии вещества (или примерно 43% от выделенной на этом этапе энергии). В третьем этапе выделяется до 70% всей энергии вещества. Из этого количества усваивается почти две трети (66%), что составляет около 46% от общей. Таким образом, из 100% молекулярной энергии клетка запасает больше половины – 59%. Ни один современный двигатель не имеет такого высокого КПД! 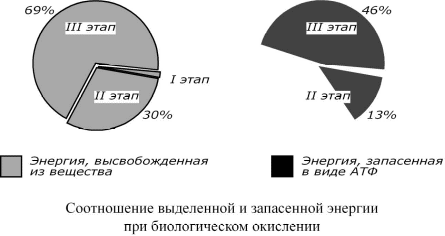 Энергия, высвобождаемая в реакциях катаболизма, запасается в виде связей, называемых макроэргическими. Основной и универсальной молекулой, запасающей энергию, является АТФ. 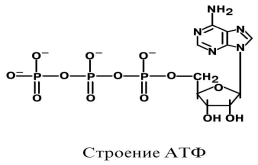 Все молекулы АТФ в организме непрерывно участвуют в каких-либо реакциях, постоянно расщепляются до АДФ и вновь регенерируют. Существует три основных способа использования АТФ, которые вкупе с процессом образования АТФ получили название АТФ- цикл. 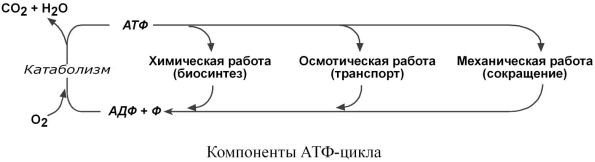 ОСНОВНЫЕ ИСТОЧНИКИ ЭНЕРГИИ В КЛЕТКЕ В клетке существуют четыре основных процесса, обеспечивающих высвобождение энергии из химических связей при окислении веществ и ее запасание: 1. Гликолиз (2 этап) – окисление молекулы глюкозы до двух молекул пировиноградной кислоты, при этом образуется 2 молекулы АТФ и НАДН. Далее пировиноградная кислота в аэробных условиях превращается в ацетил-SКоА, в анаэробных условиях – в молочную кислоту. 2. β-Окисление жирных кислот (2 этап) – окисление жирных кислот до ацетил-SКоА, здесь образуются молекулы НАДН и ФАДН2. Молекул АТФ "в чистом виде" не образуется. 3. Цикл трикарбоновых кислот (ЦТК, 3 этап) – окисление ацетильной группы (в составе ацетил-SКоА) или иных кетокислот до углекислого газа. Реакции полного цикла сопровождаются образованием 1 молекулы ГТФ (что эквивалентно одной АТФ), 3 молекул НАДН и 1 молекулы ФАДН2. 4. Окислительное фосфорилирование (3 этап) – окисляются НАДН и ФАДН2, полученные в реакциях катаболизма глюкозы и жирных кислот. При этом ферменты внутренней мембраны митохондрий обеспечивают образование основного количества клеточного АТФ из АДФ (фосфорилирование). Основным способом получения АТФ в клетке является окислительное фосфорилирование. Однако также есть другой способ фосфорилирования АДФ до АТФ – субстратное фосфорилирование. Этот способ связан с передачей макроэргического фосфата или энергии макроэргической связи какого-либо вещества (субстрата) на АДФ. К таким веществам относятся метаболиты гликолиза (1,3-дифосфоглицериновая кислота, фосфоенолпируват), цикла трикарбоновых кислот (сукцинил-SКоА) и креатинфосфат. Энергия гидролиза их макроэргической связи выше, чем в АТФ (7,3 ккал/моль), и роль этих веществ сводится к использованию для фосфорилирования АДФ. ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРОВИНОГРАДНОЙ КИСЛОТЫ Пировиноградная кислота (ПВК, пируват) является продуктом окисления глюкозы и некоторых аминокислот. Ее судьба различна в зависимости от доступности кислорода в клетке. В анаэробных условиях она восстанавливается до молочной кислоты. В аэробных условиях происходит ее окислительное декарбоксилирование до уксусной кислоты, переносчиком которой служит коэнзим А. 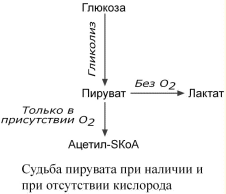 Суммарное уравнение реакции отражает декарбоксилирование пирувата, восстановление НАД до НАДН и образование ацетил-SKoA. 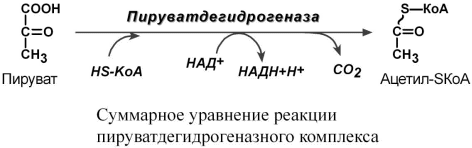 Превращение состоит из пяти последовательных реакций, осуществляется мультиферментным комплексом, прикрепленным к внутренней митохондриальной мембране со стороны матрикса. В составе комплекса насчитывают 3 фермента и 5 коферментов: Пируватдегидрогеназа (Е1, ПВК-дегидрогеназа), ее коферментом является тиаминдифосфат, катализирует 1-ю реакцию. Дигидролипоат-ацетилтрансфераза (Е2), ее коферментом является липоевая кислота, катализирует 2-ю и 3-ю реакции. Дигидролипоат-дегидрогеназа (Е3), кофермент – ФАД, катализирует 4-ю и 5-ю реакции. Помимо указанных коферментов, которые прочно связаны с соответствующими ферментами, в работе комплекса принимают участие коэнзим А и НАД. Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется пируватдегидрогеназой, Е1), окислению пирувата до ацетила и переносу ацетила на коэнзим А (катализируется дигидролипоамид-ацетилтрансферазой, Е2).  Оставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окисленное состояние (катализируются дигидролипоат-дегидрогеназой, Е3). При этом образуется НАДН. 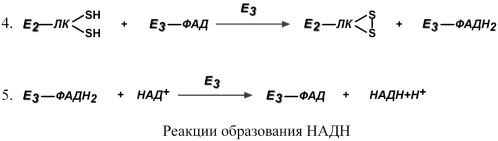 РЕГУЛЯЦИЯ ПИРУВАТДЕГИДРОГЕНАЗНОГО КОМПЛЕКСА В пируватдегидрогеназном комплексе имеются еще 2 вспомогательных фермента – киназа и фосфатаза, участвующие регуляции активности пируватдегидрогеназы (Е1) путем фосфорилирования и дефосфорилирования. 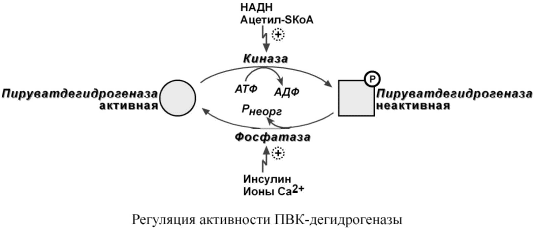 Киназа активируется при избытке АТФ и продуктов реакции – НАДН и ацетил-SКоА. При этом она фосфорилирует пируватдегидрогеназу, инактивируя ее. Фосфатаза, активируясь ионами кальция или инсулином, отщепляет фосфат и активирует пируватдегидрогеназу. Таким образом, в состоянии покоя при достаточном количестве АТФ пируватдегидрогеназа неактивна, окисление глюкозы прекращается, и она может использоваться на какиелибо синтетические процессы. Как только клетка начинает работать, уровень АТФ и НАДН резко снижается, киназная реакция останавливается, и в результате дефосфорилирования фермент активируется – начинается окисление глюкозы. В головном мозге доля пирувата, поступающая на ПВК-дегидрогеназу, составляет 80-90%, в отличие от печени, где эта доля соответствует 15-20%. В печени ПВК в основном используется для синтеза оксалоацетата. Этим объясняется высокая чувствительность нервной ткани к дефициту тиамина. ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ Образующийся в ПВК-дегидрогеназной реакции ацетил-SКоА далее вступает в цикл трикарбоновых кислот (ЦТК, цикл лимонной кислоты, цикл Кребса). В первой реакции цикла связываются ацетил и оксалоацетат (щавелевоуксусная кислота) с образованием цитрата (лимонной кислоты), далее происходит изомеризация лимонной кислоты до изоцитрата и две реакции дегидрирования с выделением СО2 и восстановлением НАД. В пятой реакции образуется ГТФ, это реакция субстратного фосфорилирования. Последние три реакции представляет собой дегидрирование, гидратацию и новое дегидрирование субстратов. В итоге после восьми реакций цикла вновь образуется оксалоацетат. Функции ЦТК: 1. Энергетическая – заключается в синтезе одной молекулы ГТФ (эквивалентна АТФ) и в генерации атомов водорода для работы дыхательной цепи (см ниже), а именно трех молекул НАДН и одной молекулы ФАДН2; 2. Анаболическая – в ЦТК образуется - предшественник гема – сукцинил-SКоА, - кетокислоты, способные превращаться в аминокислоты – α-кетоглутарат для глутаминовой кислоты, оксалоацетат для аспарагиновой, - лимонная кислота, используемая для синтеза жирных кислот (при определенных условиях), - оксалоацетат, используемый для синтеза глюкозы (при определенных условиях). Цикл Кребса протекает в матриксе митохондрий и включает 8 реакций. Он представляет собой последовательные реакции связывания ацетила и щавелевоуксусной кислоты (оксалоацетата) с образованием лимонной кислоты, ее изомеризации и последующие реакции окисления с сопутствующим выделением СО2. После восьми реакций цикла вновь образуется оксалоацетат.  РЕГУЛЯЦИЯ ЦТК 1. Главным и основным регулятором ЦТК является оксалоацетат, а точнее его доступность. Наличие оксалоацетата вовлекает в ЦТК ацетил-SКоА и запускает процесс. Обычно в клетке имеется баланс между образованием ацетил-SКоА (из глюкозы, жирных кислот или аминокислот) и количеством оксалоацетата. Источником оксалоацетата является синтез из пирувата (анаплеротическая или пополняющая реакция), поступление из фруктовых кислот самого ЦТК (яблочной, лимонной), образование из аспарагиновой кислоты. 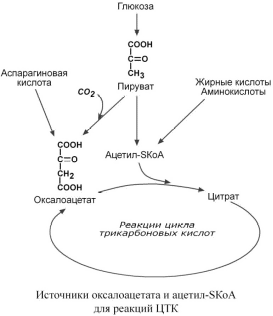  Понимание такого способа регуляции позволяет понять причину синтеза кетоновых тел и кетоацидоза при декомпенсации сахарного диабета I типа и при голодании. При указанных нарушениях в печени активирован процесс глюконеогенеза, т.е. образования глюкозы из оксалоацетата и других метаболитов, что влечет за собой снижение количества оксалоацетата. Одновременная активация окисления жирных кислот и накопление ацетил-SКоА запускает резервный путь утилизации ацетильной группы – синтез кетоновых тел. В организме при этом развивается закисление крови (кетоацидоз) с характерной клинической картиной: слабость, головная боль, сонливость, снижение мышечного тонуса, температуры тела и артериального давления. 2. Также некоторые ферменты ЦТК являются чувствительными к аллостерической регуляции метаболитами.  ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ Окислительное фосфорилирование – основная часть биологического окисления или тканевого дыхания, т.е. процессов, идущих в организме с участием кислорода. КРАТКАЯ ХАРАКТЕРИСТИКА Окислительное фосфорилирование – это многоэтапный процесс, происходящий во внутренней мембране митохондрий и заключающийся в окислении восстановленных эквивалентов (НАДН и ФАДН2) и сопровождающийся синтезом АТФ. Впервые механизм окислительного фосфорилирования был предложен Питером Митчеллом в 1961г. Согласно этой гипотезе перенос электронов, происходящий на внутренней митохондриальной мембране, вызывает выкачивание ионов Н+ из матрикса митохондрий в межмембранное пространство. Это создает градиент концентрации ионов Н+ между цитозолем и замкнутым внутримитохондриальным пространством. Ионы водорода в норме способны возвращаться в матрикс митохондрий только одним способом – через специальный фермент, образующий АТФ – АТФ-синтазу. Внутренняя митохондриальная мембрана содержит ряд мультиферментных комплексов, включающих множество ферментов. Эти ферменты называют дыхательными ферментами, а последовательность их расположения в мембране – дыхательной цепью. ПРИНЦИП РАБОТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ В целом работа дыхательной цепи заключается в следующем: 1. Образующиеся в реакциях катаболизма НАДН и ФАДН2 передают атомы водорода (т.е. протоны водорода и электроны) на ферменты дыхательной цепи. 2. Электроны движутся по дыхательной цепи и теряют энергию. 3. Эта энергия используется на выкачивание протонов Н+ из матрикса в межмембранное пространство. 4. В конце дыхательной цепи электроны попадают на кислород и восстанавливают его до воды. 5. Протоны Н+ стремятся обратно в матрикс и проходят через АТФ-синтазу. 6. При этом они теряют энергию, которая используется для синтеза АТФ. 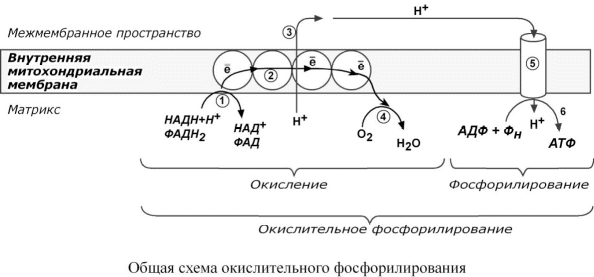 ФЕРМЕНТНЫЕ КОМПЛЕКСЫ ДЫХАТЕЛЬНОЙ ЦЕПИ Всего цепь переноса электронов включает в себя около 40 разнообразных белков. Все они организованы в 4 больших мембраносвязанных мульферментных комплекса. 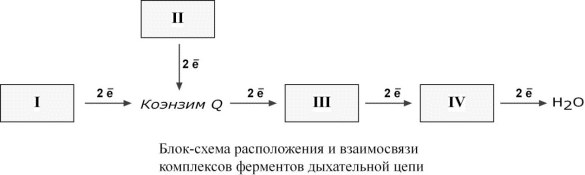 I КОМПЛЕКС, НАДН-KOQ-ОКСИДОРЕДУКТАЗА I комплекс носит общее название НАДН-дегидрогеназа, содержит ФМН, белковые молекулы, из них 6 железосерных белков. Функция 1. Принимает электроны от НАДН и передает их на коэнзим Q (убихинон). 2. Переносит 4 иона Н+ на наружную поверхность внутренней митохондриальной мембраны. Железосерные белки (FeS-белки) – это белки содержащие атомы железа, связанные с атомами серы. Атомы железа соединены с атомами серы и с серой остатков цистеина, образуя железо-серный центр. II КОМПЛЕКС II комплекс – как таковой не существует, его выделение условно, он включает в себя ФАД-зависимые ферменты, расположенные на внутренней мембране – например, ацилSКоА-дегидрогеназа (окисление жирных кислот), сукцинатдегидрогеназа (цикл трикарбоновых кислот), митохондриальная глицерол-3-фосфат-дегидрогеназа (челночный механизм переноса атомов водорода). Функция 1. Восстановление ФАД в окислительно-восстановительных реакциях. 2. Обеспечение передачи электронов от ФАДН2 на железосерные белки внутренней мембра- ны митохондрий. Далее эти электроны попадают на коэнзим Q. Общие пути биологического окисления 90 III КОМПЛЕКС. КОQ-ЦИТОХРОМ С – ОКСИДОРЕДУКТАЗА III комплекс – комплекс цитохромов b-c1, кроме цитохромов в нем имеются 2 железо- серных белка. Функция 1. Принимает электроны от коэнзима Q и передает их на цитохром с. 2. Переносит 2 иона Н+ на наружную поверхность внутренней митохондриальной мембраны. IV КОМПЛЕКС, ЦИТОХРОМ С – КИСЛОРОД-ОКСИДОРЕДУКТАЗА IV комплекс – цитохромы аа3 или цитохромоксидаза, содержит 2 иона меди. Функция 1. Принимает электроны от цитохрома с и передает их на кислород с образованием воды. 2. Переносит 4 иона Н+ на наружную поверхность внутренней митохондриальной мембраны. V КОМПЛЕКС V комплекс – это фермент АТФ-синтаза, состоящий из множества белковых цепей, подразделенных на две большие группы: Одна группа формирует субъединицу Fо (произносится со звуком "о", а не "ноль" т.к олигомицин-чувствительная) – ее функция каналообразующая, по ней выкачанные наружу протоны водорода устремляются в матрикс. Другая группа образует субъединицу F1 – ее функция каталитическая, именно она, используя энергию протонов, синтезирует АТФ. Для синтеза 1 молекулы АТФ необходимо прохождение приблизительно 3-х ионов Н+, еще один протон требуется для переноса через мембрану неорганического фосфата, АТФ и АДФ. Таким образом, для получения АТФ из АДФ в целом требуется 4 иона H+. РАБОТА КОМПЛЕКСОВ ДЫХАТЕЛЬНОЙ ЦЕПИ На основании вышеизложенного построена схема окислительного фосфорилирования: 1. Ферменты дыхательной цепи расположены в строго определенной последовательности: каждый последующий белок обладает большим сродством к электронам, чем предыдущий (он более электроположителен, т.е. обладает более положительным окислительно-восстановительным потенциалом). Это обеспечивает однонаправленное движение электронов. Способность окислительно-восстановительной пары обратимо отдавать электрон выражают окислительно-восстановительным потенциалом Е0'. В биохимии принято пользоваться понятием восстановительный потенциал. Чем более отрицательной величиной выражается восстановительный потенциал системы, тем выше ее способность отдавать электроны. При сравнении восстановительного потенциала пары НАДН / НАД = -0,32 В и пары Н2О / 1/2О2 = +0,82 В видно, что электроны будут переходить к воде. В действительности между названными донором и акцептором электронов имеется много промежуточных соединений. 2. Все атомы водорода, отщепленные дегидрогеназами от субстратов в аэробных условиях, достигают внутренней мембраны митохондрий в составе НАДН или ФАДН2. 3. Здесь атомы водорода (от НАДН и ФАДН2) передают свои электроны в дыхательную ферментативную цепь, по которой электроны движутся (50-200 шт/сек) к своему конечному акцептору – кислороду. В результате образуется вода. 4. Поступающие в дыхательную цепь электроны богаты свободной энергией. По мере их продвижения по цепи они теряют энергию. Эта энергия используется I, III, IV комплексами дыхательных ферментов для перемещения ионов водорода через мембрану в межмембранное пространство. Как известно из физики, энергией называется способность тела совершать работу. При перемещении электрического заряда энергия электронов убывает и частично превращается в теплоту. Другая часть энергии затрачивается на выкачивание водорода из матрикса в межмембранное пространство и создание градиента. 5. Перенос ионов водорода через мембрану (выкачивание) происходит не случайно, а в строго определенных участках мембраны. Эти участки называются участки сопряжения (или, не совсем точно, пункты фосфорилирования). Они представлены I, III, IV комплексами дыхательных ферментов. В результате работы этих комплексов формируется градиент ионов водорода между внутренней и наружной поверхностями внутренней митохондриальной мембраны. Такой градиент обладает потенциальной энергией. Градиент получил название электрохимический или протонный градиент (Δμ, "дельта мю"). Он имеет две составляющие – электрическую (ΔΨ, "дельта пси") и концентрационную (ΔрН): Δμ = ΔΨ+ ΔрН 6. Протоны теряют свою энергию, проходя через АТФ-синтазу. Часть этой энергии тратится на синтез АТФ. Так же как в случае с электронами, энергия ионов водорода (протонного градиента) не расходуется попусту. Двигаясь по электрохимическому градиенту, ионы водорода выделяют энергию, часть которой используется на синтез АТФ. РЕГУЛЯЦИЯ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Работа дыхательных ферментов регулируется с помощью эффекта, который получил название дыхательный контроль. Дыхательный контроль – это прямое влияние электрохимического градиента на скорость движения электронов по дыхательной цепи (величину дыхания). В свою очередь, величина градиента напрямую зависит от соотношения АТФ и АДФ, количественная сумма которых в клетке постоянна ([АТФ] + [АДФ] = const). Возрастание протонного градиента возникает при исчерпании запасов АДФ и накоплении АТФ, т.е. когда АТФ-синтаза лишена своего субстрата и ионы Н+ не проникают в матрикс митохондрии. При этом ингибирующее влияние градиента усиливается и продвижение электронов по цепи замедляется. Ферментные комплексы остаются в восстановленном состоянии. Следствием является уменьшение окисления НАДН и ФАДН2 на I и II комплексах и замедление катаболизма в клетке. 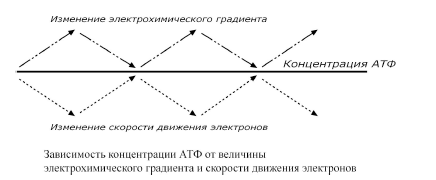 Снижение протонного градиента возникает, например, при интенсивной работе мышечной или иной клетки, когда количество АТФ в ней начинает уменьшаться. В этом случае АТФ-синтаза начинает работать, ионы Н+ через нее устремляются в матрикс, и величина электрохимического градиента снижается. В результате повышается выкачивание ионов Н+ ферментами дыхательной цепи в межмембранное пространство. Ферментные комплексы I и II усиливают окисление НАДН и ФАДН2 (как источников электронов) и снимается ингибирующее влияние НАДН на цикл лимонной кислоты и пируватдегидрогеназный комплекс активируются реакции катаболизма углеводов и жиров. Таким образом, количество АТФ остается на постоянном уровне. РАЗОБЩИТЕЛИ Разобщители – это вещества, которые снижают величину электрохимического градиента, что приводит к увеличению скорости движения электронов по ферментам дыхательной цепи. В результате этого уменьшается синтез АТФ и возрастает катаболизм. Так как электрохимический градиент состоит из двух компонентов (электрического и химического), то существуют два принципиальных способа его уменьшить – нивелировать разность зарядов или разность концентрации ионов водорода. К разобщителям в первую очередь относят "протонофоры" – вещества, переносящие ионы водорода. При этом уменьшаются оба компонента электрохимического градиента (pH и заряд). Классическим протонофором является динитрофенол, жирорастворимое соединение, присоединяющие ионы водорода на внешней поверхности внутренней митохондриальной мембраны и отдающие их на внутренней поверхности. Протонофоры одновременно снижают электрическую и химическую составляющую протонного градиента, энергия которого рассеивается в виде тепла.  Физиологическим протонофором является белок "термогенин", в изобилии имеющийся в клетках бурой жировой ткани (до 15% от всех белков митохондрий). Существенным отличием бурой жировой ткани от белой является большое количество митохондрий, которые придают клеткам буро-красный цвет. При охлаждении организма эти клетки получают сигналы по симпатическим нервам, и в них активируется расщепление жира – липолиз. Окисление жиров приводит к получению НАДН и ФАДН2, активизации работы дыхательной цепи и возрастанию электрохимического градиента. Однако АТФ-синтазы в мембранах митохондрий этих клеток мало, зато много термогенина. Благодаря ему, большая часть энергии ионов водорода рассеивается в виде тепла, обеспечивая поддержание температуры тела при охлаждении. Бурая жировая ткань широко представлена в верхней части спины у животных, впадающих в зимний сон (медведи), у детенышей животных и человеческих младенцев. Отдельные скопления бурых жировых клеток есть и у взрослого человека, они расположены в верхней части спины, между лопаток, под мышками, по ходу крупных кровеносных сосудов. 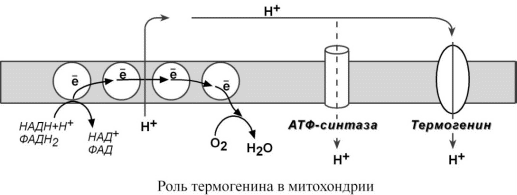 Кроме динитрофенола и термогенина протонофорами, к примеру, являются салицилаты, жирные кислоты и трийодтиронин. ИНГИБИТОРЫ ФЕРМЕНТОВ ДЫХАТЕЛЬНОЙ ЦЕПИ Ряд веществ может ингибировать ферменты дыхательной цепи и блокировать движение электронов от НАДН и ФАДН2 на кислород. 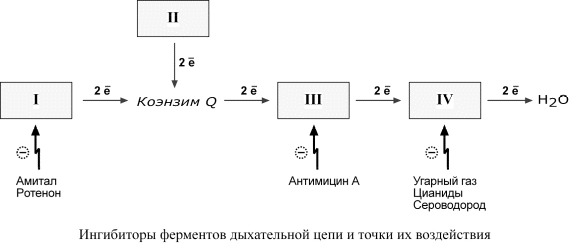 Выделяют три основных группы ингибиторов: - действующие на I комплекс, например, амитал (успокаивающее и снотворное средство), ротенон (пестицид широкого спектра), - действующие на III комплекс, например, антимицин А (антигрибковый пестицид), - действующие на IV комплекс, например, сероводород (H2S), угарный газ (СО), циа- ниды (-CN). КОЭФФИЦИЕНТ Р/О Энергетическую ценность и выгодность окисления вещества можно подсчитать. Количество запасенной энергии при окислении того или иного соединения характеризует количество АТФ, а эффективность использования энергии вещества и ее захвата – коэффициент P/O. Коэффициент Р/О – это отношение количества неорганического фосфата, включенного в молекулу АТФ АТФ-синтазой к количеству атомов кислорода, включенного в молекулу Н2О, при переносе одной пары электронов по дыхательной цепи. В настоящее время имеется две точки зрения на эффективность окисления веществ. По первой версии, в реакциях с участием НАД-зависимых дегидрогеназ соотношение P/O соответствует 3,0, по более современным данным этот коэффициент для НАДН равен 2,5. Аналогично для ФАД-зависимых дегидрогеназ коэффициент P/O либо принимается 2,0, либо по современным данным равен 1,5. Для расчета Р/О при окислении какой-либо молекулы необходимо знать: - восстановленный эквивалент (молекула НАДН или ФАДН2) передает в цепь переноса электронов по 2 электрона. - для восстановления кислорода в воду необходима 1 пара электронов, - при прохождении пары электронов через всю дыхательную цепь (т.е. через I, III, IV комплексы) выкачивается столько ионов Н+, сколько необходимо для синтеза 2,5 молей АТФ. - при прохождении пары электронов только через III и IV комплексы дыхательных ферментов ионов Н+ выкачивается столько, сколько необходимо для синтеза 1,5 молей АТФ. Далее при расчетах энергетической ценности окисления веществ будет использоваться величина P/O для НАДН равная 2,5, для ФАДН2 равная 1,5. ГИПОЭНЕРГЕТИЧЕСКИЕ СОСТОЯНИЯ Причинами гипоэнергетических состояний может быть следующее: - гиповитаминозы экзогенные и/или эндогенные – снижается скорость и эффективность окислительных реакций. Возникает обычно при нехватке витаминов группы В – В1, В2, никотиновой кислоты, В6, пантотеновой кислоты и аскорбиновой кислоты. - дефицит белка в пище – снижается синтез всех ферментов и ферментов катаболизма, в частности. - снижение потребления углеводов и липидов как основных источников энергии. - дефицит кислорода – отсутствие акцептора для электронов вызывает "переполнение" дыхательных ферментов, повышение электрохимического градиента, накопление НАДН и ФАДН2 в клетке и прекращение катаболизма. - дефицит железа – компонента цитохромов, миоглобина и гемоглобина, и меди – компонента цитохромоксидазы. ИСПОЛЬЗОВАНИЕ АТФ И ЕГО ПРЕДШЕСТВЕННИКОВ В МЕДИЦИНЕ 1. Внутримышечные инъекции раствора АТФ используют при мышечной дистрофии и атрофии, спазме периферических сосудов (болезнь Рейно, облитерирующий тромбоангиит), для стимулирования родовой деятельности. 2. Фосфаден – лекарственное название АМФ. Особенностью препарата является его сосудорасширяющий эффект и способность улучшать периферическое кровообращение. Фосфаден применяют при свинцовом отравлении, острой перемежающейся порфирии, сосудистых нарушениях и ишемической болезни сердца, болезнях печени. 3. Рибоксин или Инозин является непосредственным предшественником АТФ. Инозин способен проникать в клетки и повышать их энергетический баланс. Имеются данные о способности препарата повышать активность ферментов ЦТК, стимулировать синтез нуклеотидов и улучшать коронарное кровообращение. |
