Местные и общие реакции организма на повреждение
 Скачать 451.5 Kb. Скачать 451.5 Kb.
|
|
85 совокупности называемые антиоксидантами (табл. 10). 3.1.8. Стабильность липидного слоя мембран и явление электрического пробоя Стабильность липидного слоя и электрический пробой мембраны. В отличие от белков и нуклеиновых кислот, которые в клетке собираются каждый по своему чертежу сложнейшими молекулярными роботами, липидный слой мембраны обладает способностью собираться сам по себе из молекул фосфолипидов и холестерина, если только они содержатся в водном растворе в достаточной концентрации. Это связано с особым свойством молекул липидов, входящих в состав мембран, которое принято называть ам-фифильностью, т. е. сродством одновременно к воде (гидрофильность) и к неводным средам, таким как растительное масло или жидкий парафин (гидрофобность). Молекула фосфолипида (основной липид клеточной и внутриклеточных мембран) имеет форму сплющенного цилиндра (рис. 13, А), один (меньший) конец которого хорошо растворяется в воде («полярная голова»), а другой - в воде не растворяется («жирный хвост») (рис. 13, Б). В водной среде такие молекулы самособираются в липидный бислой (рис. 13, В), который сам на себя замыкается, образуя везикулы - липосомы (рис. 13, Г). Под влиянием тепловых движений молекул в липидном слое могут образоваться дефекты, которые приводят к образованию заполненных водой трещин и щелей (назовем их «порами»). Через такие дефекты могут проходить водорастворимые молекулы и ионы. Однако их появление крайне невыгодно с энергетической точки зрения, поскольку при этом граница раздела липид - вода сильно увеличивается, а это требует затраты работы на преодоление силы поверхностного натяжения. С ростом радиуса поры энергия системы растет пропорционально радиусу в соответствии с уравнением: АЕ = nrlo, где г - радиус поры; Z ■ толщина мембраны; а -энергия образования границы раздела площадью 1м2 (в системе СИ). При наличии мембранного потенциала (т. е. разности потенциалов между водными фазами 86 по сторонам мембраны), который обозначается как фт, энергия образования поры снижается. Как показывает теория, в этом случае энергия системы изменяется с ростом поры по уравнению: АЕ = nrlo ■ кг2еоФ*т (s„ - ej/ 21, где е0 - диэлектрическая постоянная, ец , ет- диэлектрическая проницаемость для воды и липидного слоя мембран соответственно; <р/( - мембранный потенциал. Изменение энергии поры с ростом ее радиуса при трех разных мембранных потенциалах показано на рис. 14, В. Видно, что с ростом радиуса энергия системы сначала растет, а затем начинает уменьшаться. Это означает, что после преодоления некоторого энергетического барьера рост поры будет происходить самопроизвольно, пока мембрана вообще не разрушится. Величина барьера снижается при увеличении мемб-  «Полярная голова»  Липидный бислой  «Жирный хвост» г Липосома Рис. 13. Самосборка фосфолипидов в бислой Часть I. ОБЩАЯ НОЗОЛОГИЯ рвнного потенциала. При небольших потенциалах, существующих в живой клетке (70 мВ на щдаоплазматической мембране и 175 мВ на внутренней мембране митохондрий), этого не проис-ходит, потому что барьер достаточно высок. С ростом потенциала может наступить момент, когда в мембране начнут формироваться и расти ■оры и она будет разрушена. Такое явление ноет название электрического пробоя мембраны.  О Образование водной поры Поверхность поры равна 2кН 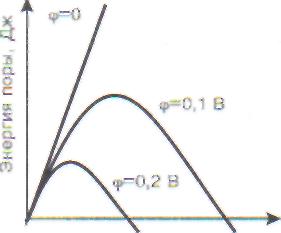 < с о I- Радиус поры, мкм 0 40 80 120 _ Рис. 14. Электрический пробой мембран: А - появление в липидном бислое мембраны поры, заполненной водой; В - размер внутренней поверхности поры пропорционален ее радиусу; В - энергия мембраны с порой в зависимости от ее радиуса. Величина потенциального барьера при росте поры уменьшается при увеличении потенциала на мембране; Г - возрастание тока в зависимости от потенциала пробоя Величина потенциала, при котором начинается электрический пробой, называется потенциалом пробоя и обычно обозначается как U* или ф*. Величина потенциала пробоя, несколько различающаяся для мембран с разным составом белков и липидов, может служить количественной мерой электрической стабильности мембраны. Чем стабильнее мембрана, тем выше потенциал, который ее «пробивает» (т. е. ф*) . Электрическая прочность различных мембранных структур. Явление электрического пробоя мембран изучалось многими авторами на искусственных мембранах и отдельных клетках. Мембраны обладают определенным сопротивлением R электрическому току I, которое при небольшой разности потенциалов ф между двумя сторонами мембраны является постоянной величиной. Иными словами, для мембраны соблюдается закон Ома: I=Ф/Л. Это означает, что зависимость между напряжением на мембране ф и током через мембрану I - линейная. Однако такая зависимость сохраняется при сравнительно небольших величинах ф: обычно не выше 200-300 мВ. При определенной разности потенциалов на мембране (потенциале пробоя ф*) происходит резкое возрастание тока (рис. 14, Г). При постоянном мембранном потенциале, если он превышает критическое значение, ток самопроизвольно нарастает во времени до полного разрушения мембраны. На рис. 14 представлены результаты опыта на бислойных липидных мембранах. Аналогичные опыты были проведены на везикулярных мембранных структурах: фосфолипидных везикулах - липосомах, изолированных митохондриях и эритроцитах. В случае липосом и эритроцитов потенциал на мембране создавался за счет разности концентраций проникающих ионов по сторонам мембраны, в случае митохондрий - за счет энергии окисления субстратов. Измерение мембранного потенциала осуществлялось различными способами, например в случае митохондрий, - с помощью потенциалчувствительного флуоресцентного зонда. Явление пробоя мембран наблюдалось во всех случаях. В табл. 11 приведены величины потенциалов пробоя мембран всех этих объектов. Разумеется, потенциал пробоя во всех случаях выше потенциала, существующего на мембранах в живой клетке: иначе Глава 3 / МЕСТНЫЕ И ОБЩИЕ РЕАКЦИИ ОРГАНИЗМА НА ПОВРЕЖДЕНИЕ 87 Таблица 11 Электрические потенциалы (мВ) на мембранах клеток и потенциалы пробоя модельных и биологических мембран (A3. Путвинский, Т.В. Пучкова, ОМ. Париев, Ю.А. Владимиров)
все мембраны пробились бы своим собственным потенциалом и клетка не могла бы существовать. Однако запас электрической прочности невелик: всего 20-30 мВ. Это означает, что при снижении прочности мембраны может произойти ее «самопробой». Электрический пробой как универсальный механизм нарушения барьерной функции мембран. Чрезвычайно важно, что электрическая прочность мембран, мерой которой служит потенциал пробоя, снижается под действием повреждающих факторов. Как уже говорилось, основными причинами нарушения барьерных свойств мембран при патологии являются: пе-рекисное окисление липидов, действие мембранных фосфолипаз, механическое растяжение мембран или адсорбция на них некоторых белков. Изучение влияния этих действующих факторов на электрическую прочность мембран показало, что все они снижают потенциал пробоя мембран (рис. 15). При повреждении мембранных структур происходит снижение потенциала пробоя <р* и может сложиться ситуация <р* < ф, когда мембрана будет «пробиваться» собственным мембранным потенциалом. К чему это приводит в условиях живой клетки? Предположим, клетку облучают ультрафиолетовыми лучами, под влиянием которых в липидных мембранах активируется пе-рекисное окисление. В неповрежденных митохондриях потенциал на мембране равен 175 мВ, а потенциал пробоя составляет около 200 мВ (см. табл. 11). В процессе активации перекисного окисления липидов потенциал пробоя начинает постепенно снижаться, и как только он достигает значения 175 мВ, мембрана митохондрий «пробивается» собственным мембранным потенциалом. То же происходит и при активации фосфолипаз: снижение потенциала пробоя до величины, равной существующему на мембране потенциалу, приводит к электрическому пробою мембраны и потере ею барьерных свойств. В условиях эксперимента на эритроцитах и митохондриях было показано, что осмотическое растяжение мембраны и добавление чужеродных белков, так же как и действие перекисного окисления и фос-фолипазы, снижают потенциал пробоя мембран настолько, что они начинают «пробиваться» собственным мембранным потенциалом. Естествен вопрос, почему такие, казалось бы, разные воздействия, как перекисное окисление липидов, ферментативный гидролиз фосфолипид-ных молекул, механическое растяжение мембраны или адсорбция полиэлектролитов, приво- Рис. 15. Снижение электрической прочности БЛМ при действии ультрафиолетового излучения (УФ), фосфо-липазы А2, пептидов, при растяжении мембраны, вызванном разностью гидростатического давления (ДР) Часть I. ОБЩАЯ НОЗОЛОГИЯ дят к одному и тому же результату - снижению электрической прочности (т.е. уменьшению величины потенциала пробоя) мембраны? Теория электрического пробоя дает четкий ответ на этот вопрос. Самопроизвольному росту пор, случайно зародившихся в липидном бислое, препятствуют силы поверхностного натяжения на границе раздела фаз: липидный слой мембраны - окружающий водный раствор. Нужно приложить довольно большую разность потенциалов к мембране, чтобы преодолеть эти силы и вызвать рост поры. Все вещества, снижающие поверхностное натяжение (детергенты), облегчают самопроизвольный рост пор и снижают величину потенциала пробоя. И продукты перекисного окисления липидов, и продукты гидролиза фосфоли-пидов фосфолипазами (лизолецитины), и многие белки снижают поверхностное натяжение на границе раздела фаз и таким образом уменьшают электрическую прочность мембраны. Механическое растяжение мембраны действует сходно, так как противодействует силам поверхностного натяжения. Таким образом, электрический пробой мембран оказывается универсальным механизмом нарушения барьерной функции мембран при патологии. Мембранные системы защиты от электрического пробоя. Известны два фактора, с помощью которых живые клетки повышают электрическую стабильность своих мембранных структур: асимметричный поверхностный потенциал и холестерин. Поверхностный потенциал возникает на мембране в случае появления на поверхности ли-пидного слоя заряженных химических группировок, например таких, как карбоксил или фосфат. Непосредственно на липидный бислой действует потенциал, равный разности величины мембранного потенциала (т.е. потенциала между водными средами, омывающими мембрану) и поверхностного потенциала (рис. 16). За счет неодинаковой плотности зарядов на поверхностях мембраны реальная разность потенциалов, приложенная к липидному бислою, может быть больше или меньше трансмембранной разности потенциалов. В большинстве биологических мембран заряды распределены между поверхностями таким образом, что разность потенциалов на липидном бислое меньше разности потенциалов между водными растворами, омывающими мем- брану. Это снижает вероятность пробоя мембраны разностью потенциалов, которая существует между водными фазами по сторонам мембран в живых клетках. Второй фактор, повышающий электрическую прочность мембран, - это холестерин. Было показано, что включение молекул холестерина в фосфолипидный бислой весьма заметно увеличивает электрическую прочность мембран, т. е. повышает потенциал пробоя (см. рис. 14, Г). Особенно заметно действие холестерина на поврежденные мембраны. Защитные свойства холестерина против электрического пробоя мембраны можно объяснить влиянием холестерина на вязкость липидного бислоя. Известно, что введение холестерина в фосфолипидный бислой может повысить вязкость последнего в 2-3 раза. Это приводит к замедлению образования и роста дефектов (пор) в липидном бислое мембран. Как уже говорилось, именно образование и увеличение дефектов в липидном бислое под действием приложенного электрического поля лежит в основе явления электрического пробоя. Нарушение структурных (матричных) свойств липидного бислоя. Наиболее изучены три характеристики липидного слоя мембран, от которых зависят его свойства как жидкой фазы (матрицы), обеспечивающей функционирование мембранных белков и рецепторов: поверхностный заряд, вязкость и площадь липидного слоя. Все эти характеристики исследуются с помощью флуоресцентных и спиновых зондов. 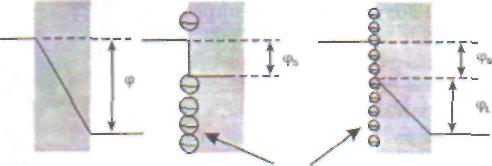 Группы,несущие заряд Рис. 16. Влияние поверхностного потенциала (фд) на разность потенциалов на липидном слое мембран (ф,) при одном и том же мембранном потенциале (ф) Перекисное окисление липидов и действие мембранных фосфолипаз приводят к накоплению в липидной фазе мембран полиненасыщенных жирных кислот, которые придают мембране при нейтральных рН отрицательный заряд. Увели- Глава 3 / МЕСТНЫЕ И ОБЩИЕ РЕАКЦИИ ОРГАНИЗМА НА ПОВРЕЖДЕНИЕ 89 чение отрицательных зарядов на поверхности мембраны облегчает связывание с мембраной ионов и белковых молекул, несущих положительные заряды, и, наоборот, уменьшает взаимодействие мембран с отрицательно заряженными молекулами или другими мембранами. Связывая больше ионов Са2*, мембраны с большим числом отрицательных зарядов на поверхности становятся более доступными для действия фос-фолипаз, но зато хуже связывают ионы Fe2+, которые ускоряют пероксидацию липидов. С другой стороны, при перекисном окислении липидов происходит увеличение вязкости липидного слоя мембран. Значительное увеличение вязкости имеет место также при увеличении содержания в мембранах холестерина. Возрастание вязкости приводит к торможению работы мембранных рецепторов, а также встроенных в мембраны ферментов, таких как Na" -K+ -АТФаза и Са2* - Mg^-АТФаза. В свою очередь, это изменяет ионный баланс клетки и может привести к нарушениям метаболизма. С помощью флуоресцентных зондов было показано, что при перекисном окислении происходит уменьшение площади поверхности липидного слоя мембран, а также площади, занимаемой фосфолипидами на поверхности липопроте-инов плазмы крови. Это связано с окислением части жирно-кислотных цепей фосфолипидов и выходом их в водную фазу. Одним из результатов такого явления оказывается увеличение относительной концентрации холестерина в липид-ном монослое на поверхности липопротеинов, подвергнутых перекисному окислению. Липопротеины низкой плотности (ЛПНП) в результате этого переносят еще больше холестерина в клеточные мембраны сосудистой стенки, чем нео-кисленные ЛПНП, и их атероген-ность возрастает. Липопротеины высокой плотности (ЛПВП), в норме акцептирующие холестерин с мембран клеток и обладающие ан-тиатерогенным действием, в результате перекисного окисления полностью теряют способность акцептировать холестерин. Возрастание ате-рогенных (холестерин-донорных) свойств ЛПНП и утрата антиатеро-генных (холестерин-акцепторных) свойств ЛПВП, несомненно, отно- сятся к числу причин того, почему перекисное окисление липидов в районе сосудистой стенки способствует развитию атеросклероза. 3.2. ОБЩИЕ РЕАКЦИИ ОРГАНИЗМА НА ПОВРЕЖДЕНИЕ Повреждение, вызываемое различными болезнетворными факторами, кроме местных изменений одновременно приводит к развитию общих реакций организма. Степень выраженности общих реакций неодинакова и имеет разное проявление. К этим реакциям относятся стресс, реакции «острой фазы», лихорадка, шок, кома и др. 3.2.1. Общий адаптационный синдром (стресс)  При действии на организм различных повреж дающих факторов в нем возникают двоякого рода изменения. С одной стороны, выявляется полом, повреждение, а с другой - как реакция на по вреждение - включаются защитно-компенсатор ные механизмы. Последняя группа механизмов всегда привлекала внимание исследователей. И.П. Павлов обозначил ее как «физиологическую меру» организма. В 1932 г. американский физи олог У. Кеннон сформулировал принцип гомео- стазиса, суть которого заключается в том, что организм непрерывно поддерживает постоянство внутренней среды и при действии повреждаю щих факторов, нарушающих это постоянство, включается сложная цепь различных компенса торно-приспособительных механизмов, направ ленных на его восстановление. Эти механизмы обычно стереотипны и включаются при действии различных повреждаю щих факторов. Следовательно, они по своему характеру неспецифичны. У. Кеннон подчеркнул значение симпа тического отдела нервной системы в этих реакциях, а Л. А. Орбели в 1935 г. сформулировал положение об адап тационно-трофической роли симпати ческой нервной системы. Было пока зано, что при повреждающих воздей ствиях именно через симпатическую нервную систему активируются выс шие отделы центральной нервной Г. Селье системы, идет мобилизация энерге- 90 |
