Местные и общие реакции организма на повреждение
 Скачать 451.5 Kb. Скачать 451.5 Kb.
|
Глава 3 / МЕСТНЫЕ И ОБЩИЕ РЕАКЦИИ ОРГАНИЗМА НА ПОВРЕЖДЕНИЕ> ONOOH (пероксинит-рит)рые синтетические соединения, например трет-бутилгидрокситолуол (ионол). Водорастворимые радикалы эффективно «перехватываются» аскорбиновой или мочевой кислотой. Для «улавливания» радикалов гидроксила (НО) используют маннитол или бензойную кислоту, а иногда -этанол. Однако далеко не всегда ловушки специфичны: многие из них реагируют не только с радикалами, но и с достаточно активными молекулами. Прямым методом изучения свободных радикалов можно считать метод электронного парамагнитного резонанса (ЭПР), позволяющий обнаруживать молекулярные частицы и ионы металлов, обладающие неспаренным электроном. По амплитуде и форме сигналов (спектров) ЭПР можно определять концентрацию частиц с не-спаренными электронами и судить об их строении. К эффективным методам изучения реакций, идущих с участием радикалов, можно отнести метод хемилюминесценции (ХЛ). В основе его лежит то обстоятельство, что при взаимодействии радикалов друг с другом выделяется много энергии, которая может испускаться в виде фотонов (квантов света). Интенсивность такого свечения (ХЛ) пропорциональна скорости реакций, в которой участвуют радикалы, и, следовательно, показывает изменение их концентрации в ходе изучаемого процесса. В биологических системах скорости образо- вания радикалов кислорода или липидных радикалов в мембранах не так уж велики, зато очень велики скорости исчезновения этих радикалов, поэтому концентрация радикалов в каждый данный момент времени (так называемая стационарная концентрация) обычно очень мала. Выход из положения заключается в использовании так называемых спиновых ловушек в методе ЭПР и активаторов свечения. В первом случае к изучаемому образцу (например, к суспензии клеток, гомогенату ткани или раствору, где протекают реакции с участием свободных радикалов) добавляют особые вещества - спиновые ловушки. Например, в качестве ловушки для радикалов гидроксила (ОН) используют фенил-бутилнитрон (ФБН). При взаимодействии ловушки с радикалом происходит присоединение радикала к ловушке с образованием нового, стабильного радикала, получившего название спинового аддукта (от английского слова add - добавлять, складывать). Сигналы ЭПР спиновых аддуктов разных радикалов слегка различаются по форме. Это позволяет идентифицировать радикалы, образующиеся в изучаемой системе. Для улавливания других радикалов (скажем, супероксида) используют другие ловушки. 3.1.7. Свободнорадикальное (перекисное) окисление липидов Все радикалы, образующиеся в организме человека, можно разделить на природные и чужеродные. В свою очередь природные радикалы можно разделить на первичные, вторичные и третичные (рис. 8). Первичные радикалы - те радикалы, образование которых осуществляется при участии определенных ферментных систем. Прежде всего к ним относятся радикалы (семихиноны), образующиеся в реакциях таких переносчиков электронов, как коэнзим Q (обозначим радикал как Q) и флавопротеины. Два других радикала - су- 80 Часть I. ОБЩАЯ НОЗОЛОГИЯ род и перекись водорода. Судьба последней может быть разной (рис. 10). В норме фагоциты используют перекись водорода для синтеза гипохлорита, выделяя специальный фермент - миелопероксидазу (МП). Миелопероксидаза катализирует реакцию миелопероксидаза Н202 + С1 ->• Н20 + СЮ (гипохлорит) Гипохлорит разрушает стенку бактериальной клетки и тем самым убивает бактерии. Перекись водорода диффундирует в клетки, но там разрушается в результате активности ферментов ка-талазы и глутатионпероксидазы (GSH-перокси-дазы), которые катализируют соответственно такие реакции: каталаза 2НЮ2 -» 2Н20 + 02 Н202 + 2GSH GSSG + 2H20 глутатионпероксидаза -> В присутствии ионов двухвалентного железа перекись водорода разлагается с образованием гидроксильного радикала (НО): Н202 + Fe2+ -» Fe3+ + НО + НО Эта реакция (известная как реакция Фентон) приводит к тяжелым последствиям для окружающих клеток. Радикал гидроксила чрезвычайно активен химически и разрушает почти любую встретившуюся ему молекулу. Действуя на SH-группы, гистидиновые и другие аминокислотные остатки белков, НО' вызывает денатурацию последних и инактивирует ферменты. В нуклеиновых кислотах НО' разрушает углеводные мостики между нуклеотидами и таким об- разом разрывает цепи ДНК и РНК, в результате чего происходят мутации и гибель клеток. Внедряясь в липидный слой клеточных мембран, гидроксильный радикал запускает (инициирует) реакции цепного окисления липидов, что приводит к повреждению мембран, нарушению их функций и гибели клеток. Гидроксильный радикал образуется не только в реакции Фентон, но и при взаимодействии ионов железа (Fe2+) с гипохлоритом (реакция Осипова): СЮ + Fe2+ + Н+ -» Fe3+ + С1 + НО Супероксидный радикал (00 )и продукты его метаболизма (Н202, НО', СЮ) называют активными формами кислорода. Окись азота. К числу радикалов, синтезируемых клетками, относится монооксид азота 'NO, называемый также нитроксидом. Нитроксид образуется клетками стенок кровеносных сосудов (эндотелия); эта реакция катализируется гемсо-держащим ферментом N0 -синтазой. N0 играет ключевую роль в регуляции тонуса сосудов и кровяного давления: его недостаток приводит к гипертензии, избыток - к гипотензии. Нарушение метаболизма фактора расслабления вызывает заболевания, связанные с изменением кровяного давления. ' N0 выделяется также клетками-фагоцитами и вместе с супероксид-радикалами используется для борьбы с микробами (преимущественно грибковой природы). Полагают, что цитотоксическое действие N0 обусловлено его реакцией с супероксидом N = О + 00 + Н+ 82 Часть I. ОБЩАЯ НОЗОЛОГИЯ 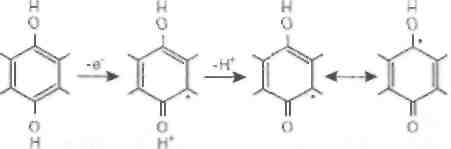 убихинона (QH , гидрохинон-форма): Пероксинитрит, образующийся в этой реакции, может разлагаться с образованием 'ОН: О = N - О - ОН -> О = N - О + ОН (радикал гидроксила) Образование пероксинитрита и радикала гидроксила приводит к повреждению клеток. По-видимому, одна из функций супероксиддисму-тазы состоит в предотвращении образования пероксинитрита за счет удаления супероксида из зоны образования окиси азота. Радикал коэнзима Q. Биологическое окисление субстратов клеточного дыхания, таких как глюкоза, пировиноградная и янтарная кислоты и другие, осуществляется, как известно, в два этапа. На первом этапе в цикле трикарбоновых кислот происходит последовательный отрыв атомов водорода от субстрата и образование восстановленных форм пиридиннуклеотидов НАДН и НАДФН. На втором этапе электроны от НАДН и НАДФН переносятся по так называемой дыхательной цепи на кислород. В состав дыхательной цепи входят флавопротеиды, комплексы негемового железа, убихинон и гемопротеиды (цитохромы a, b и с и цитохромоксидаза). Схема дыхательной цепи дана на рис. 11. сн, В 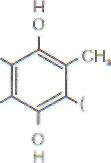 ажным звеном цепи переноса электронов служит убихинон (коэнзим Q) : ажным звеном цепи переноса электронов служит убихинон (коэнзим Q) :н,С-0 СН,-СН=С=СН,)„Н Н,С-0 радикал которого (семихинон, QH на рис. 11) образуется либо при одноэлектронном окислении гидрохинон катион-радикал нейтральный гидрохинона радикал (семихинон) либо при одноэлектронном восстановлении убихинона (Q на рис. 11): 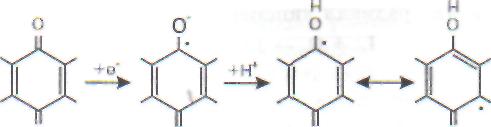
В норме этот радикал является рядовым участником процесса переноса электронов, но при нарушении работы дыхательной цепи он может стать источником других, менее безобидных радикалов, в первую очередь радикалов кислорода. Основные стадии цепного окисления. Реакция цепного окисления липидов играет исключительную роль в клеточной патологии. Она протекает в несколько стадий, которые получили название инициирование, продолжение, разветвление и обрыв цепи (см. схему 3). Инициирование цепной реакции начинается с того, что в липидный слой мембран или ли-попротеинов внедряется свободный радикал. митохондрий Глава 3 / МЕСТНЫЕ И ОБЩИЕ РЕАКЦИИ ОРГАНИЗМА НА ПОВРЕЖДЕНИЕ 83 Чаще всего это радикал гидроксила. Будучи небольшой по размеру незаряженной частицей, он способен проникать в толщу гидрофобного липидного слоя и вступать в химическое взаимодействие с полиненасыщенными жирными кислотами (которые принято обозначать как LH), входящими в состав биологических мембран и липопротеинов плазмы крови. При этом образуются липидные радикалы: НО + LH -> Н20 + L Липидный радикал (L) вступает в реакцию с растворенным в среде молекулярным кислородом, при этом образуется новый свободный радикал - радикал липоперекиси (LOO ): L + 02 -> LOO Этот радикал атакует одну из соседних молекул фосфолипида с образованием гидроперекиси липида LOOH и нового радикала L': LOO-+ LH -> LOOH + L- Чередование двух последних реакций как раз и представляет собой цепную реакцию перекис-ного окисления липидов (см. схему 3). Существенное ускорение пероксидации липидов наблюдается в присутствии небольших количеств ионов двухвалентного железа. В этом случае происходит разветвление цепей в результате взаимодействия Fe2i с гидроперекисями липидов: Fe2+ + LOOH -> Fe3+ + НО + LO Образующиеся радикалы LO' инициируют новые цепи окисления липидов (см. схему 3): LO + LH -> LOH + L ;L + 02-> LOO -> и т.д. В биологических мембранах цепи могут состоять из десятка и более звеньев. Но в конце концов цепь обрывается в результате взаимодействия свободных радикалов с антиоксидантами (InH), ионами металлов переменной валентности (например, теми же Fe2T) или друг с другом: LOO + Fe2+ + Н+ -> LOOH + Fe3+ LOO + InH -> In ■+ LOOH LOO' + LOO' -> молекулярные продукты Последняя реакция особенно интересна, поскольку она сопровождается свечением (хеми-люминесценцией). Интенсивность этой хемилю-минесценции очень мала, поэтому ее иногда называют «сверхслабым свечением». Интенсивность свечения пропорциональна квадрату концентрации свободных радикалов в мембранах, а Схема 3 Цепная реакция перекисного окисления липидов скорость перекисного окисления прямо пропорциональна концентрации тех же радикалов. Поэтому интенсивность «сверхслабого» свечения однозначно отражает скорость липидной пероксидации в изучаемом биологическом материале и измерение хемилюминесценции довольно часто используется при изучении перекисного окисления липидов в различных объектах. 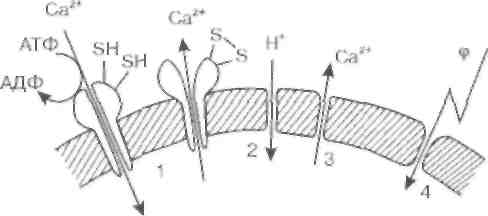 Рис. 12. Повреждающее действие перекисного окисления липидов на биологические мембраны Повреждающее действие пероксидации липидов. На рис.12 показаны основные мишени перекисного окисления липидов в мембранных структурах клеток. Повреждаются либо белковые структуры, либо липидный бислой в целом. В последнее время ученые уделяют все большее внимание взаимодействию мембран с нуклеиновыми кислотами в ядре и митохондриях. По-видимому, одним из результатов пероксидации 84 Часть I. ОБЩАЯ НОЗОЛОГИЯ Наиболее известные антиоксиданты Таблица 10
липидов может стать повреждение этих молекул со всеми вытекающими последствиями. Наиболее чувствительны к переписному окислению липидов сульфгидрильные, или тиоловые, группы (- SH) мембранных белков: ферментов, ионных каналов и насосов. В ходе окисления тиоловых групп образуются радикалы (- S), которые затем либо взаимодействуют друг с другом с образованием дисульфидов (- SS-), либо связываются с кислородом с образованием сульфитов и сульфатов (- S03 и - S04). Большую роль в патологии клетки играет также повреждение ионтранспортирующих ферментов (например, Ca2t , М£2+-АТФазы), в активный центр которых входят тиоловые группы (рис. 12-1). Инактивация Са2+-АТФазы приводит к замедлению откачивания из клетки ионов кальция и ускорению их «протечки» в клетку (где их концентрация меньше). Это вызывает рост уровня ионов кальция в цитоплазме и повреждение клеточных структур. Окисление тиоловых групп мембранных белков приводит к появлению дефектов в мембранах клеток и митохондрий. Под действием электрического поля через такие дефекты в клетки входят ионы натрия, а в митохондрии - ионы калия. В результате происходит увеличение осмотического давления внутри клеток и митохондрий и их набухание. Это приводит к еще большему повреждению мембранных структур. Еще одним интересным примером может служить окисление белков и последующее образо- вание белковых агрегатов в хрусталике глаза, вызванное пероксидацией липидов. Процесс приводит к помутнению хрусталика и может считаться одной из причин развития старческой и других видов катаракты у человека. Наряду с белками и нуклеиновыми кислотами мишенью повреждающего действия перекисного окисления служит сам липидный бислой. Было показано, что продукты перекисного окисления липидов делают липидную фазу мембран проницаемой для ионов водорода и кальция (рис. 12-2; 12-3). Это приводит к тому, что в митохондриях окисление и фосфорилирование разобщаются и клетка оказывается в условиях энергетического голода. Одновременно из митохондрий в цитоплазму выходят ионы кальция, которые повреждают клеточные структуры (см. выше). Но, быть может, самый важный результат пероксидации - это уменьшение электрической стабильности липидного слоя, которое приводит к электрическому пробою мембраны собственным мембранным потенциалом (рис. 12-4). Электрический пробой вызывает полную потерю мембраной ее барьерных функций. Клеточные системы защиты от повреждения свободными радикалами. Свободные радикалы преследовали живую материю с первых же моментов ее появления на Земле, и неудивительно, что в ходе эволюции клетки и организм в целом выработали нечто подобное глубокоэше-лонированной обороне, которая включает в себя ферменты и низкомолекулярные соединения, в |
