химия. Методические указания и контрольные задания для студентов заочников инженернотехнических (нехимических)
 Скачать 2.15 Mb. Скачать 2.15 Mb.
|
|
(Р – растворимое вещество; М – малорастворимое вещество; Н – практически нерастворимое вещество; прочерк означает, что вещество не существует или разлагается водой) Ряд стандартных электродных потенциалов металлов
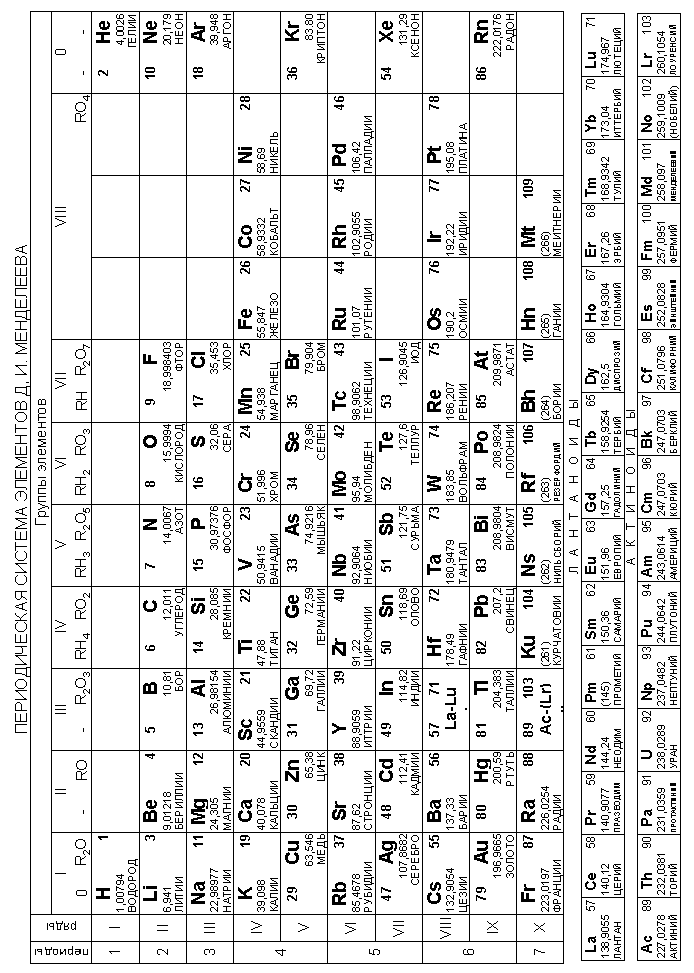 Оглавление ВВЕДЕНИЕ 3 КОНТРОЛЬНЫЕ ЗАДАНИЯ 5 КОНТРОЛЬНОЕ ЗАДАНИЕ 1 5 Моль. Эквиваленты и молярные массы эквивалентов простых и сложных веществ. Закон эквивалентов 5 Строение атома 9 Периодическая система элементов Д. И. Менделеева 13 Химическая связь и строение молекул. Конденсированное состояние вещества 16 Энергетика химических процессов (термохимические расчеты) 21 Химическое сродство 24 Химическая кинетика и равновесие 29 Способы выражения концентрации растворов 35 Свойства растворов 39 Ионно-молекулярные (ионные) реакции обмена 43 Гидролиз солей 47 КОНТРОЛЬНОЕ ЗАДАНИЕ 2 50 Окислительно-восстановительные реакции 50 Электродные потенциалы и электродвижущие силы 57 Электролиз 62 Коррозия металлов 66 Комплексные соединения 71 s-элементы 76 Жесткость воды и методы ее устранения 85 Примеры решения задач 85 р-элементы (...ns2np1–6) 88 d-элементы (...(n – l)d1-10ns0-2) 95 Органические соединения. Полимеры 104 ПРИЛОЖЕНИЕ 114 Растворимость солей и оснований в воде 116 Оглавление 119 |
