Фенолы. Мы с Вами изучили одноатомные и многоатомные спирты
 Скачать 115 Kb. Скачать 115 Kb.
|
|
Фенолы Мы с Вами изучили одноатомные и многоатомные спирты. Сегодня мы познакомимся с веществами, которые тоже содержат данную функциональную группу. Это фенолы. Цели урока: мы изучим на примере первого представителя данного класса состав и строение фенолов, их свойства и познакомимся с применением соединений данного класса. Формула первого представителя данного класса: С6Н5ОН. Называется вещество фенол. Другое его название – карболовая кислота. Посмотрите на структурные формулы: фенола и других представителей данного класса.  Вы видите, что помимо гидроксильной группы в состав фенолов входит бензольное или ароматическое кольцо, но ни к спиртам, ни к аренам их не относят. Это отдельный класс органических соединений. Определение фенолов. Соединения, в которых ароматический радикал фенил С6Н5- непосредственно связан с гидроксильной группой - ОН выделяют в отдельный класс органических соединений, называемый фенолами. Строение молекулы фенола. Группа С6Н5- , называемая фенил радикал, обладает свойством притягивать к себе электроны кислородного атома группы –ОН, а значит химическая связь между кислородом и водородом становится более полярной, а атом водорода более подвижный. Это усиливает кислотные свойства фенола. Но в свою очередь гидроксильная группа –ОН тоже влияет на бензольное кольцо. Это связано со смещением электронной плотности внутри бензольного кольца. В результате этого химическая связь между С – Н в положениях 2,4 и 6 ослабляется, т.е. атомы водорода в этих положениях становятся более подвижными для реакций замещения, пртекающих по бензольному кольцу.
Физические свойства фенола Фенол – это бесцветное кристаллическое вещество. При окислении на воздухе кристаллы приобретают розоватый оттенок. Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к образованию водородных связей  Это объясняет, почему у фенола довольно высокие температуры плавления (+43) и кипения (+182). Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде:  Способность растворяться в воде уменьшается с увеличением углеводородного радикала и от многоатомных гидроксисоединений к одноатомным. Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Растворимость фенола в воде ограничена. Фенол хорошо растворяется в горячей воде. Кроме того, фенол – это ядовитое вещество. При попадании кристалликов фенола на кожу, вызывает сильный химический ожог. Химические свойства фенола 1) Рассмотрим реакции фенола по ОН- группе:  Кислотные свойства у фенола выражены сильнее, чем у спирта С2Н5ОН. Фенол – слабая кислота (карболовая). 2) Реакции фенола по бензольному кольцу:  Какой вывод о взаимном влиянии атомов в молекуле фенола можно сделать? Фенильная группа C6H5 – и гидроксил –ОН взаимно влияют друг на друга. 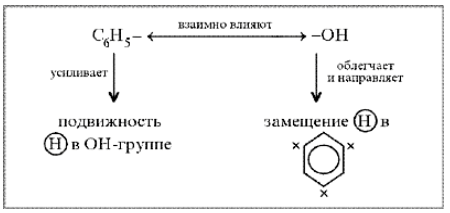 3) Качественная реакция на фенол. С6Н5ОН + FeCl3 —> фиолетовое окрашивание Получение фенола. Способы получения фенолов. Фенолы выделяют из каменноугольной смолы, а также из продуктов пиролиза бурых углей и древесины (деготь). Промышленный способ получения самого фенола С6Н5ОН основан на окислении ароматического углеводорода кумола (изопропилбензол) кислородом воздуха с последующим разложением получающейся гидроперекиси, разбавленной H2SO4 . Реакция проходит с высоким выходом и привлекательна тем, что позволяет получить сразу два технически ценных продукта – фенол и ацетон. Другой способ – каталитический гидролиз галогензамещенных бензолов.  Физиологическое действие фенола и его применение Фенол - ядовит!!! При попадании на кожу вызывает ожоги, при этом он всасывается через кожу и вызывает отравление. Раствор фенола используют в качестве дезинфицирующего средства (карболовая кислота). Двухатомные фенолы – пирокатехин, резорцин, а также гидрохинон (пара-дигидроксибензол) применяют как антисептики (антибактериальные обеззараживающие вещества), вводят в состав дубителей для кожи и меха, как стабилизаторы смазочных масел и резины, а также для обработки фотоматериалов и как реагенты в аналитической химии. В виде отдельных соединений фенолы используются ограниченно, зато их различные производные применяют широко. Фенолы служат исходными соединениями для получения разнообразных полимерных продуктов – фенолоальдегидных смол, полиамидов, полиэпоксидов.Например: текстолита ( подшипники), карболита (Эл. розетки, вилки), стеклотекстолит, волокнит( электроизоляционные материалы, детали радиоаппаратуры, облицовочные материалы, для получения красителей, лаков, эмалей. На основе фенолов получают многочисленные лекарственные препараты, например, аспирин, салол, фенолфталеин, кроме того, парфюмерные продукты, пластификаторы для полимеров и средства защиты растений. Биологическая роль соединений фенола:
|

