патфиз. Нарушения водного обмена. Нарушения водного обмена
 Скачать 0.93 Mb. Скачать 0.93 Mb.
|
|
§ общем или белковом голодании, § нарушении полостного и/или мембранного пищеварения (например, при резекции фрагментов кишечника, дисбактериозе, синдромах мальабсорбции). ‡ Снижении синтеза альбуминов в печени (например, при воздействии на неё гепатотропных ядов, выраженном циррозе). ‡ Избыточной потере белка организмом (например, с мочой при нефротическом синдроме, с плазмой крови при обширных ожогах; с калом при расстройстве пищеварения в желудке и кишечнике). † Повышающие онкотическое давление интерстициальной жидкости. Эти причины имеют в основном регионарное значение и вызывают или потенцируют развитие местных отёков. Гиперонкия интерстициальной жидкости является результатом: ‡ Избыточного транспорта белков плазмы крови в межклеточное пространство. Обычно это обусловлено повышением проницаемости стенок микрососудов при: § развитии воспаления или местных аллергических реакций (под влиянием медиаторов воспаления и аллергии, например, кининов, гистамина, серотонина); § действии некоторых химических веществ (например, хлора, фосгена, люизита); § попадании в ткань ядов насекомых и пресмыкающихся; § воздействии ядов микробов (например, возбудителей дифтерии или сибирской язвы). ‡ Выхода в межклеточную жидкость белков клеток при их повреждении или разрушении (например, в очаге воспаления, при ишемии, аллергической реакции). ‡ Увеличения гидрофильности белковых мицелл интерстициальной жидкости. Это может быть при: § накоплении в интерстиции избытка некоторых ионов (например, H+, K+, Na+), § дефиците в межклеточном пространстве ионов Ca2+, § избытке БАВ (например, гистамина и серотонина), § дефицита йодсодержащих тиреоидных гормонов. • Механизм реализации онкотического фактора (рис. 11–10) заключается в уменьшении эффективной онкотической всасывающей силы (как следствие гипопротеинемии и/или гиперонкии ткани). В результате возрастает объём фильтрации воды из микрососудов в интерстициальную жидкость по градиенту онкотического давления и уменьшается резорбция жидкости из межклеточного пространства в посткапиллярах и венулах. 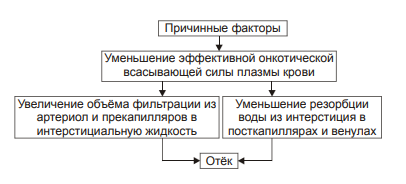 Рис. 11–10. Механизм реализации онкотического фактора развития отёка. Осмотический фактор Осмотический фактор развития отёка заключается либо в повышении осмоляльности интерстициальной жидкости, либо в снижении осмоляльности плазмы крови, либо в сочетании того и другого. 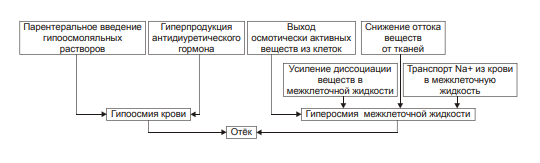 Причины включения осмотического фактора отёка. † Факторы, снижающие осмотическое давление крови. ‡ Парентеральное введение больших объёмов растворов, содержащих соли в недостаточном количестве. В реальной клинической практике это встречается чрезвычайно редко (являясь следствием врачебной ошибки, например, при проведении мероприятий по устранению гипогидратации организма или отклонений показателей КЩР). Даже в этих случаях избыточная жидкость быстро выводится почками при условии нормальной их экскреторной функции. ‡ Гиперпродукция АДГ. Может наблюдаться при повышении внутричерепного давления, повреждении структур гипоталамуса (особенно нейронов его супраоптических ядер), после энцефалитов. Повышение в связи с этим продукции АДГ в гипоталамусе и его уровня в крови стимулирует избыточную реабсорбцию воды в почках. Однако, и в данном случае, как правило, в почках повышена и реабсорбция Na+, что препятствует развитию гипоосмии крови. † Факторы, повышающие осмоляльность интерстициальной жидкости. ‡ Выход из повреждённых или разрушенных клеток осмотически высокоактивных веществ (например, ионов Na+, K+, Ca2+, глюкозы, МК, азотистых соединений). ‡ Повышение диссоциации в интерстициальной жидкости солей и органических соединений (например, в условиях гипоксии или ацидоза). ‡ Снижение оттока осмотически активных веществ (ионов, органических и неорганических соединений) от тканей в результате расстройств микроциркуляции. ‡ Транспорт Na+ из плазмы крови в интерстициальную жидкость. Это может наблюдаться, например, при гиперальдостеронизме. • Механизм реализации осмотического фактора развития отёка (рис. 11–12) заключается в избыточном транспорте воды из клеток и сосудов микроциркуляторного русла в межклеточную жидкость по градиенту осмотического давления (более высокого в интерстиции). Данный механизм включается как компонент патогенеза при сердечном, почечном (нефритическом), печёночном и других отёках. 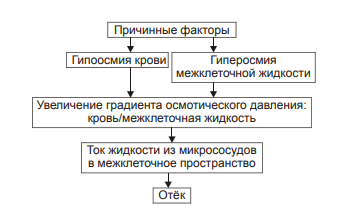 Механизм осмотического фактора отёка. Мембраногенный фактор Мембраногенный фактор характеризуется существенным повышением проницаемости стенок сосудов микроциркуляторного русла для воды, мелко‑ и крупномолекулярных веществ (наибольшее значение среди последних имеют белки). • Причины повышения проницаемости стенок микрососудов перечислены на рис. 11–13. 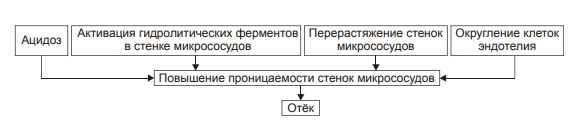 Причины включения мембраногенного фактора развития отёка. † Ацидоз. В условиях ацидоза возрастает неферментный («кислотный») гидролиз основного вещества базальной мембраны сосудистой стенки. Это и приводит к её разрыхлению и как следствие — возрастанию проницаемости. † Повышение активности гидролитических ферментов в стенке микрососудов и/или прилегающих к ним тканях. Это интенсифицирует процесс ферментативного гидролиза гликозаминогликанов, а также волокнистых структур сосудистой стенки. Такая картина наблюдается при выраженной гипоксии, ацидозе, при воздействии так называемых лабилизаторов лизосом (например, лизофосфолипидов, продуктов липопероксидации, протеолитических ферментов). † Перерастяжение стенок микрососудов. Это наблюдается при: ‡ Развитии артериальной гиперемии нейромиопаралитического типа (т.е. в условиях длительного снижения нейрогенного и мышечного тонуса артериол и прекапилляров). ‡ Венозной гиперемии и лимфостазе. • Механизмы реализации мембраногенного фактора развития отёка (рис. 11–14). 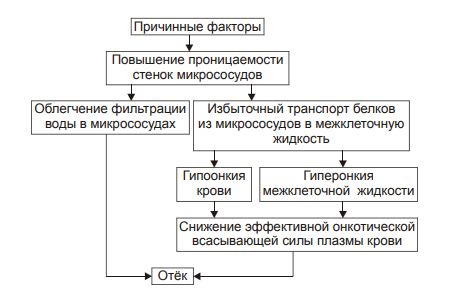 Механизм реализации мембраногенного фактора развития отёка. † Облегчение фильтрации воды. В связи с этим увеличивается выход жидкости из крови и лимфы в интерстициальное пространство. Однако, этот механизм может быть сбалансирован повышением реабсорбции воды в венозном отделе капилляров в связи с истончением их стенок. † Увеличение выхода молекул белка из микрососудов в межклеточную жидкость. Это ведёт к снижению онкотического давления плазмы крови и лимфы и одновременно к развитию гиперонкии межклеточной жидкости. В условиях повышенной проницаемости стенок микрососудов жидкость из них интенсивно поступает в межклеточное пространство по градиенту онкотического давления. Именно такой механизм (помимо других) лежит в основе развития отёка тканей при их воспалении, местных аллергических реакциях, укусах насекомых и змей, действии некоторых отравляющих веществ, чистого кислорода, особенно при избыточном атмосферном давлении. Многофакторность В клинической практике, как правило, не встречаются отёки, развивающиеся на основе только одного из описанных выше патогенетических факторов (иначе говоря нет монопатогенетических отёков). В связи с этим в каждом конкретном случае при наличии отёка выделяют: 1) инициальный (стартовый, первичный) патогенетический фактор у данного пациента и 2) патогенетические факторы, включающиеся в процессе развития отёка вторично. Отёки при сердечной недостаточности Патогенез отёков при сердечной недостаточности представлен на рис. 11–15. 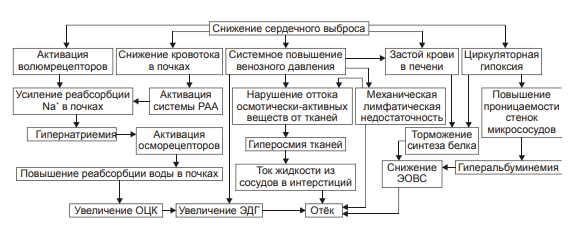 Патогенез отёка при сердечной недостаточности. РАА — система «ренин‑ангиотензин‑альдостерон»; ЭДГ — эффективное гидростатическое давление; ЭОВС — эффективная онкотическая всасывающая сила. • Причина: сердечная недостаточность (состояние, при котором сердце не обеспечивает потребности органов и тканей в кровоснабжении, адекватном их функции и уровню пластических процессов) . • Инициальный патогенетический фактор — гидродинамический. - Причины включения гидродинамического фактора ‡ Системное повышение венозного давления в связи со снижением сократительной функции сердца. ‡ Увеличение ОЦК. Это наблюдается при хронической сердечной недостаточности, закономерно сопровождающейся развитием циркуляторной гипоксии — при хронической гипоксии наблюдается эритроцитоз и, как следствие — увеличение ОЦК (подробнее см. в главе 15 «Гипоксия»). - Механизмы реализации ‡ Торможение резорбции жидкости из межклеточного пространства в венозной части капилляров. Это является результатом повышения в них венозного давления и, как следствие — эффективного гидростатического давления. ‡ Увеличение фильтрации жидкости в артериальной части капилляров. Последнее обусловлено повышением в артериальном участке микрососудистого русла эффективного гидродинамического давления в связи с возрастанием (за счёт эритроцитоза в условиях гипоксии) ОЦК. • Последовательность включения и значимость других патогенетических факторов отёка в каждом конкретном случае могут быть различными в зависимости от динамики расстройств кровообращения и их последствий. В любом случае патогенез сердечного отёка включает рассмотренные ниже звенья. - Активация барорецепторов в стенке кровеносных сосудов. ‡ Причина: уменьшение сердечного выброса и ОЦК. ‡ Механизм реализации: § сужение артериол коркового вещества почек, § увеличение тока крови в мозговом веществе почек, § усиление канальцевой реабсорбции ионов Na+, что приводит к гиперосмии крови; § активация осморецепторов, § усиление синтеза и высвобождения в кровь АДГ, § возрастание реабсорбции воды в почках, § увеличение эффективного гидродинамического давления, § активация фильтрации жидкости в артериальном регионе капилляра, сочетающуюся с торможением реабсорбции воды в венозном отделе микрососудов. Как первое, так и второе обусловливает развитие отёка. † Уменьшение объёма кровотока в сосудах почек. ‡ Причина: снижение величины сердечного выброса. ‡ Механизм реализации: § Активация системы «ренин‑ангиотензин‑альдостерон». § Усиление реабсорбции Na+ в канальцах почек. † Развитие механической лимфатической недостаточности. ‡ Причина: снижение сердечного выброса. ‡ Механизм реализации: § Нарушение оттока венозной крови от тканей к сердцу. § Системное увеличение венозного давления: как центрального, так и в периферических венозных сосудах. § Торможение оттока лимфы от тканей — развитие механической лимфатической недостаточности. § Увеличение объёма интерстициальной жидкости, т.е. — степени отёка. † Увеличение осмотического давления в тканях. ‡ Причины § Нарушение оттока осмотически активных веществ (ионов, неорганических и органических соединений) в результате венозного застоя (венозной гиперемии) и лимфатической недостаточности. § Увеличение концентрации метаболитов (например, молочной и пировиноградной кислот, пептидов, аминокислот) в связи с нарушением обмена веществ в условиях гипоксии. ‡ Механизм реализации: ток жидкости из микрососудов в интерстиций по градиенту осмотического давления. † Нарушение системного кровообращения с развитием циркуляторной гипоксии и ацидоза. ‡ Причина возникновения гипоксии и ацидоза: уменьшение сердечного выброса. ‡ Механизмы реализации: § Повышение проницаемости лизосом и высвобождение из них гидролитических ферментов. Ферменты гидролизуют основное вещество и волокна соединительной ткани в стенке сосудов. В связи с этим увеличивается их проницаемость для воды, что потенцирует развитие отёка. § Активация неферментного гидролиза компонентов базальной мембраны стенок микрососудов. Это также приводит к повышению их проницаемости. § Увеличение образования и активности БАВ, повышающих проницаемость стенок микрососудов (например, гистамина, серотонина, кининов, отдельных факторов комплемента). § Повышение выхода белка из крови в интерстициальное пространство. § Нарушение (в условиях недостаточности кровообращения) белоксинтетической функции печени, ведущее к гипоальбуминемии. § Снижение эффективной онкотической всасывающей силы. § Усиление тока воды из микрососудов в межклеточное пространство по возросшему градиенту онкотического давления. † Развитие застоя крови в сосудах печени и нарушение её кровоснабжения. ‡ Причина: уменьшение сердечного выброса. ‡ Механизмы реализации § Расстройства энергетического, субстратного и кислородного обеспечения процесса синтеза белка в гепатоцитах. § Развитие гипоальбуминемии, характерной для печёночной недостаточности. § Падение эффективной онкотической всасывающей силы. § Увеличение транспорта жидкости из микрососудов в интерстиций. Таким образом, развитие отёка при сердечной недостаточности является результатом сочетанного и взаимопотенцирующего действия всех патогенетических факторов: гидродинамического, осмотического, онкотического, мембраногенного и лимфогенного. Отёк лёгкого Как правило, отёк лёгких развивается весьма быстро. В связи с этим он чреват общей острой гипоксией и существенными расстройствами КЩР. Причины: • Сердечная недостаточность (левожелудочковая или общая) в результате: - инфаркта миокарда, - порока сердца (например, при недостаточности или стенозе аортального клапана, стенозе митрального клапана); - экссудативного перикардита (сопровождающегося сдавлением сердца), - гипертензивного криза, - аритмий (например, пароксизмальной желудочковой тахикардии). • Токсичные вещества, повышающие проницаемость стенок микрососудов лёгких (например, некоторые боевые отравляющие вещества типа фосгена, фосфорорганические соединения, угарный газ, чистый кислород под высоким давлением). 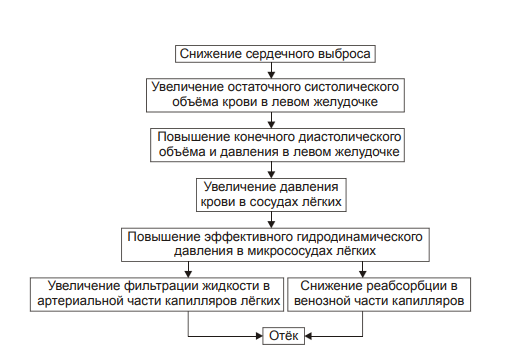 Патогенез отёка лёгких при сердечной недостаточности. Механизм развития. Инициальный и основной патогенетический фактор развития отека легких — гемодинамический: он заключается в снижением сократительной функции миокарда левого желудочка. • Увеличением остаточного систолического объёма крови в левом желудочке сердца. • Повышением конечного диастолического объёма и давления в левом желудочке сердца. • Увеличением давления крови в сосудах малого круга кровообращения выше 25–30 мм рт.ст. • Возрастанием эффективного гидродинамического давления. При превышении им эффективной онкотической всасывающей силы транссудат поступает в межклеточное пространство лёгких (развивается интерстициальный отёк). При накоплении в интерстиции большого количества отёчной жидкости она проникает между клетками эндотелия и эпителия альвеол, заполняя полости последних (развивается альвеолярный отёк). В связи с этим нарушается газообмен в лёгких, развиваются дыхательная гипоксия (усугубляющая имеющуюся циркуляторную) и ацидоз. Это требует уже при первых признаках отёка лёгких проведения неотложных врачебных мероприятий. † Отёк лёгких под воздействием токсичных веществ 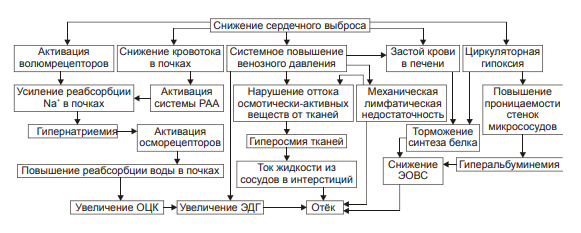 • Инициальный и основной патогенетический фактор — мембраногенный, что приводит к повышению проницаемости стенок микрососудов. Причины: - Токсичные веществ (например, боевые отравляющие типа фосгена). - Высокая концентрация кислорода, особенно под повышенным давлением. В эксперименте показано, что при рО2 дыхательной смеси выше 350 мм рт.ст. развивается отёк лёгких и кровоизлияния в них. Использование 100% кислорода при проведении ИВЛ приводит к развитию выраженного интерстициального и альвеолярного отёка, сочетающегося с признаками деструкции эндотелия и альвеолоцитов. В связи с этим в клинике для лечения гипоксических состояний применяют газовые смеси с 30–50% концентрацией кислорода. Этого достаточно для поддержания адекватного газообмена неповреждёнными лёгкими. • Факторы, ведущие к повышению проницаемости стенок сосудов при действии токсичных веществ: - Ацидоз, в условиях которого потенцируется неферментный гидролиз основного вещества базальной мембраны микрососудов. - Повышение активности гидролитических ферментов. - Образование «каналов» между округлившимися повреждёнными клетками эндотелия. Почечные отёки Различные формы патологии почек сопровождаются развитием более или менее выраженных общих отёков. Их инициальные патогенетические звенья различны при нефритах и нефрозах. Отёк при нефрозах Нефрозы — патология почек, как правило, первично невоспалительного генеза. Они характеризуются диффузной деструкцией паренхимы почек. Причины развития нефрозов: первичное повреждение почек (например, при фокальном гломерулосклерозе) и вторичная альтерация почечной ткани (например, при СД, иммунопатологических состояниях, амилоидозе, интоксикации некоторыми ЛС). • Инициальный патогенетический фактор отёка — онкотический. • Причины развития отёка |
