решение 1-5. КР 1. Воротынцев А.В.. Образовательного учреждения высшего образования национальный исследовательский технологический университет мис
 Скачать 115.03 Kb. Скачать 115.03 Kb.
|
|
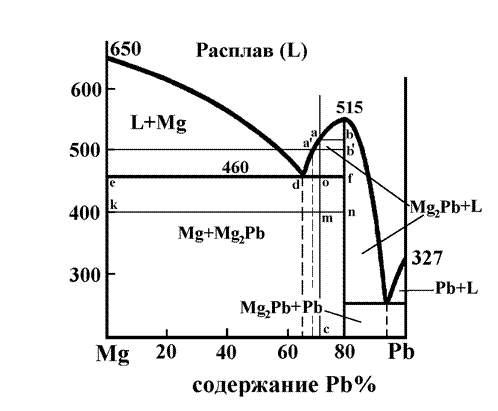 |
Рисунок 3.
На диаграмме состояния системы Mg-Pb существуют следующие фазы: жидкость (L), чистый магний (Mg), чистый свинец (Pb), химическое соединение (Mg2Pb).
При охлаждении в сплаве с 70 %Pb, 30 %Mg происходят фазовые преврашения, описанные ниже.
В точке а из жидкости начинают выделяться первые кристаллы химического соединения Mg2Pb. При последующем охлаждении количество твердого химического соединения увеличивается. При этом состав оставшейся жидкости изменяется по линии аd. При достижении температуры 460 оС оставшаяся жидкость кристаллизуется по эвтектическому механизму: L → Mg + Mg2Pb. Образуются твердый магний и химическое соединение.
При дальнейшем охлаждении количество и состав фаз не изменяется.
Химический состав фаз при температурах:
· 400 оС – твердый магний и химическое соединение Мg2Pb;
· 500 оС – жидкая фаза с составом а' и химическое соединение Мg2Pb;
· 650 оС – только расплав магния с содержанием свинца 30 %.
Количество фаз при температуре 400 оС определяется по правилу рычага:
· магния mn/kn= 10/80 = 12,5 %;
· химического соединения Мg2Pb km/kn = 70/80 = 87,5 %.
Задание 3.
Под действием каких напряжений возникает пластическая деформация? Как при этом изменяется структура и свойства металлов и сплавов?
Деформацией называется изменение формы и размеров тела под действием напряжений.
При пластическом деформировании одна часть кристалла перемещается по отношению к другой под действием касательных напряжений. При снятии нагрузок сдвиг остается, т.е. происходит пластическая деформация.
С увеличением степени деформации характеристики пластичности (относительное удлинение, относительное сужение) и вязкости (ударная вязкость) уменьшаются, а прочностные характеристики (предел упругости, предел текучести, предел прочности) и твердость увеличиваются. Также повышается электросопротивление, снижаются сопротивление коррозии, теплопроводность, магнитная проницаемость.
Совокупность явлений, связанных с изменением механических, физических и других свойств металлов в процессе пластической деформации называют деформационным упрочнением или наклепом.
Задание 4.
Вычертите диаграмму состояния «железо-карбид железа». Укажите структурные составляющие во всех областях диаграммы. Опишите превращения и постройте кривую нагревания в интервале температур от 0 до 1600°С (с применением правила фаз) для сплава, содержащего 0,1% С. Для заданного сплава определите при температуре 1500°С: процентное содержание углерода в фазах; количественное соотношение фаз.
Диаграмма железо - углерод должна распространяться от железа до углерода. Железо образует с углеродом химическое соединение: цементит (карбид железа). Каждое устойчивое химическое соединение можно рассматривать как компонент, а диаграмму - по частям. Так как на практике применяют металлические сплавы с содержанием углерода до, то рассматриваем часть диаграммы состояния от железа до химического соединения цементита, содержащего углерода.
Диаграмма состояния железо - цементит представлена на рисунке 4.
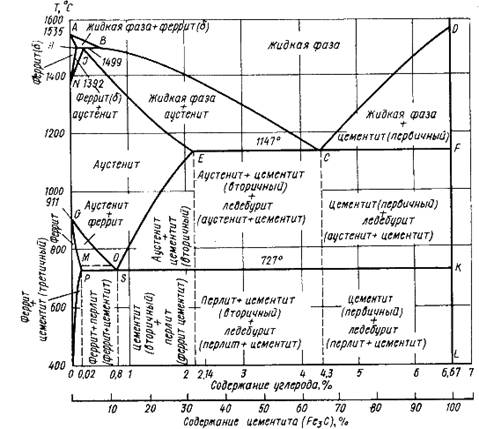
Рисунок 4. - Диаграмма состояния железо - цементит
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит.
1. Железо - переходный металл серебристо-светлого цвета. Имеет высокую температуру плавления - 1539o С 5o С.
В твердом состоянии железо может находиться в двух модификациях. Полиморфные превращения происходят при температурах 911o С и 1392o С. При температуре ниже 911o С существует с объемно-центрированной кубической решеткой. В интервале температур 911…1392o С устойчивым является с гранецентрированной кубической решеткой. Выше 1392o С железо имеет объемно-центрированную кубическую решетку и называется или высокотемпературное . Высокотемпературная модификация не представляет собой новой аллотропической формы. Критическую температуру 911o С превращения обозначают точкой , а температуру 1392o С превращения - точкой А4.
При температуре ниже 768o С железо ферромагнитно, а выше - парамагнитно. Точка Кюри железа 768o С обозначается А2.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (предел прочности - , предел текучести - ) и высокими характеристиками пластичности (относительное удлинение - , а относительное сужение - ). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна.
Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами - растворы замещения, с углеродом, азотом и водородом - растворы внедрения.
2. Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления - 3500 °С, плотность - 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления - 5000 °С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения - цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
3. Цементит (Fe3C) - химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода.
Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу.
Температура плавления цементита точно не установлена (1250, 1550o С). При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 217o С.
Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность. Такие свойства являются следствием сложного строения кристаллической решетки.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: азотом, кислородом; атомы железа - металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Цементит - соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
В системе железо - углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит.
1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
2. Феррит (Ф) (C) - твердый раствор внедрения углерода в -железо.
Феррит имеет переменную предельную растворимость углерода: минимальную - 0,006 % при комнатной температуре (точка Q), максимальную - 0,02 % при температуре 727o С ( точка P). Углерод располагается в дефектах решетки.
При температуре выше 1392o С существует высокотемпературный феррит () ( (C), с предельной растворимостью углерода 0,1 % при температуре 1499o С (точка J).
Свойства феррита близки к свойствам железа. Он мягок (твердость - 130 НВ, предел прочности - ) и пластичен (относительное удлинение - ), магнитен до 768o С.
3. Аустенит (А) (С) - твердый раствор внедрения углерода в железо.
Углерод занимает место в центре гранецентрированной кубической ячейки.
Аустенит имеет переменную предельную растворимость углерода: минимальную - 0,8 % при температуре 727o С (точка S), максимальную - 2,14 % при температуре 1147o С (точка Е).
Аустенит имеет твердость 200…250 НВ, пластичен (относительное удлинение - ), парамагнитен.
При растворении в аустените других элементов могут изменяться свойства и температурные границы существования.
4. Цементит - характеристика дана выше.
В железоуглеродистых сплавах присутствуют фазы: цементит первичный (ЦI), цементит вторичный (ЦII), цементит третичный (ЦIII). Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении - вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен. кристаллизация напряжение металл сплав
Процессы при структурообразовании железоуглеродистых сплавов
Линия АВСD - ликвидус системы. На участке АВ начинается кристаллизация феррита (), на участке ВС начинается кристаллизация аустенита, на участке СD - кристаллизация цементита первичного.
Линия AHJECF - линия солидус. На участке АН заканчивается кристаллизация феррита (). На линии HJB при постоянной температуре 1499°С идет перетектическое превращение, заключающееся в том, что жидкая фаза реагирует с ранее образовавшимися кристаллами феррита (), в результате чего образуется аустенит:
На участке JЕ заканчивается кристаллизация аустенита. На участке ECF при постоянной температуре 1147o С идет эвтектическое превращение, заключающееся в том, что жидкость, содержащая 4,3 % углерода превращается в эвтектическую смесь аустенита и цементита первичного:
Эвтектика системы железо - цементит называется ледебуритом (Л), по имени немецкого ученого Ледебура, содержит 4,3 % углерода.
При температуре ниже 727o С в состав ледебурита входят цементит первичный и перлит, его называют ледебурит превращенный (ЛП).
По линии HN начинается превращение феррита () в аустенит, обусловленное полиморфным превращением железа. По линии NJ превращение феррита () в аустенит заканчивается.
По линии GS превращение аустенита в феррит, обусловленное полиморфным превращением железа. По линии PG превращение аустенита в феррит заканчивается.
По линии ES начинается выделение цементита вторичного из аустенита, обусловленное снижением растворимости углерода в аустените при понижении температуры.
По линии МО при постоянной температуре 768o С имеют место магнитные превращения.
По линии PSK при постоянной температуре 727o С идет эвтектоидное превращение, заключающееся в том, что аустенит, содержащий 0,8 % углерода, превращается в эвтектоидную смесь феррита и цементита вторичного:
По механизму данное превращение похоже на эвтектическое, но протекает в твердом состоянии.
Эвтектоид системы железо - цементит называется перлитом (П), содержит 0,8 % углерода.
Название получил за то, что на полированном и протравленном шлифе наблюдается перламутровый блеск.
Перлит может существовать в зернистой и пластинчатой форме, в зависимости от условий образования.
По линии PQ начинается выделение цементита третичного из феррита, обусловленное снижением растворимости углерода в феррите при понижении температуры.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо - цементит, т.е. критические точки, имеют условные обозначения.
Обозначаются буквой А (от французского arret - остановка):
А1 - линия PSK (727°С) - превращение П А;
A2 - линия MO (768°С, т. Кюри) - магнитные превращения;
A3 - линия GOS ( переменная температура, зависящая от содержания углерода в сплаве) - превращение Ф А;
A4 - линия NJ (переменная температура, зависящая от содержания углерода в сплаве) - превращение ;
Acm - линия SE (переменная температура, зависящая от содержания углерода в сплаве) - начало выделения цементита вторичного (иногда обозначается A3).
Так как при нагреве и охлаждении превращения совершаются при различных температурах, чтобы отличить эти процессы вводятся дополнительные обозначения. При нагреве добавляют букву с, т.е. , при охлаждении - букву r, т.е. .
При температуре 1300оС для сплава, содержаещего 1,8% С количественное соотношение фаз - жидкая фаза+аустенит.
Задание 5.
В чем отличие обычной закалки от ступенчатой и изотермической? Каковы преимущества и недостатки каждого из этих видов закалки?
Конструкционные стали подвергают закалке и отпуску для повышения прочности и твердости, получения высокой пластичности, вязкости и высокой износостойкости, а инструментальные - для повышения твердости и износостойкости.
Верхний предел температур нагрева для заэвтектоидных сталей ограничивается, так как приводит к росту зерна, что снижает прочность и сопротивление хрупкому разрушению.
Основными параметрами являются температура нагрева и скорость охлаждения. Продолжительность нагрева зависит от нагревательного устройства, по опытным данным на 1 мм сечения затрачивается: в электрической печи - 1,5…2 мин.; в пламенной печи - 1 мин.; в соляной ванне - 0,5 мин.; в свинцовой ванне - 0,1…0,15 мин.
Способы закалки
В зависимости от формы изделия, марки стали и нужного комплекса свойств применяют различные способы охлаждения.(рис.5)
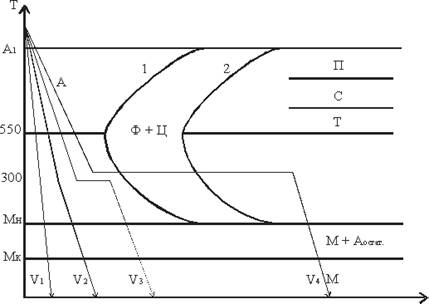
Рисунок 5 - Режимы закалки
1. Закалка в одном охладителе (V1).
Нагретую до нужной температуры деталь переносят в охладитель и полностью охлаждают. В качестве охлаждающей среды используют:
· воду - для крупных изделий из углеродистых сталей;
· масло - для небольших деталей простой формы из углеродистых сталей и изделий из легированных сталей.
Основной недостаток - значительные закалочные напряжения.
2. Закалка в двух сферах или прерывистая (V2).
Нагретое изделие предварительно охлаждают в более резком охладителе (вода) до температуры 300°C и затем переносят в более мягкий охладитель (масло).
Прерывистая закалка обеспечивает максимальное приближение к оптимальному режиму охлаждения.
Применяется в основном для закалки инструментов.
Недостаток: сложность определения момента переноса изделия из одной среды в другую.
3. Ступенчатая закалка (V3).
Нагретое до требуемой температуры изделие помещают в охлаждающую среду, температура которой на 30 - 50oС выше точки МН и выдерживают в течении времени, необходимого для выравнивания температуры по всему сечению. Время изотермической выдержки не превышает периода устойчивости аустенита при заданной температуре.
В качестве охлаждающей среды используют расплавленные соли или металлы. После изотермической выдержки деталь охлаждают с невысокой скоростью.
Способ используется для мелких и средних изделий.
4. Изотермическая закалка (V4).
Отличается от ступенчатой закалки продолжительностью выдержки при температуре выше МН, в области промежуточного превращения. Изотермическая выдержка обеспечивает полное превращение переохлажденного аустенита в бейнит.При промежуточном превращении легированных сталей кроме бейнита в структуре сохраняется аустенит остаточный. Образовавшаяся структура характеризуется сочетанием высокой прочности, пластичности и вязкости. Вместе с этим снижается деформация из-за закалочных напряжений, уменьшаются и фазовые напряжения.
В качестве охлаждающей среды используют расплавленные соли и щелочи.
Применяются для легированных сталей.
5. Закалка с самоотпуском.
Нагретые изделия помещают в охлаждающую среду и выдерживают до неполного охлаждения. После извлечения изделия, его поверхностные слои повторно нагреваются за счет внутренней теплоты до требуемой температуры, то есть осуществляется самоотпуск. Применяется для изделий, которые должны сочетать высокую твердость на поверхности и высокую вязкость в сердцевине (инструменты ударного действия: мототки, зубила).