Курсовой проект новенький. Окисление изопропилбензола
 Скачать 3.5 Mb. Скачать 3.5 Mb.
|
                                                                                                                                                                                                                        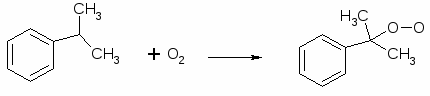   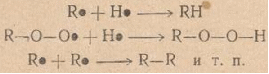 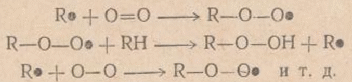      Министерство образования Российской федерации Министерство образования Российской федерацииГосударственное образовательное учреждение высшего профессионального образования «САМАРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» Кафедра общего органического и нефтехимического синтеза Курсовой проект на тему: «Окисление изопропилбензола» Выполнил студент 5 курса 2 группы (специальность 240401) Артюнина Е.С. _________________________ Научный руководитель Дружинина Ю. А. ____________________ Работа защищена апреля 2012г. Оценка___________________ САМАРА 2012 СОДЕРЖАНИЕ
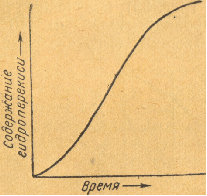
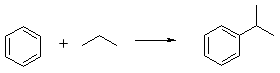
Введение Фенол и ацетон являются важнейшими крупнотоннажными продуктами промышленности органического и нефтехимического синтеза. Совместное их получение гораздо более экономичнее всех ранее реализованных методов, вследствие чего оно нашло широкое применение во всех промышленно развитых странах мира. Широкое распространение получил кумольный метод синтеза фенола совместно с ацетоном, основанный на окислении изопропилбензола в гидроперекись и последующем разложении гидроперекиси на фенол и ацетон. При этом образуется также небольшое количество побочных продуктов. Изопропилбензол, в свою очередь, получается алкилированием бензола пропиленом. Таким образом, исходным сырьем для получения фенола и ацетона по кумольному методу являются бензол и пропилен. Первое крупное производство фенола и ацетона кумольным методом было реализовано в 1949 году в Советском Союзе. В основу этого производства были положены исследования П.П Сергеева, Б.Д. Кружалова и Р.Ю. Удриса по окислению изопропил бензола в гидроперекись с последующим её разложением на фенол и ацетон[2]. Процесс производства фенола и ацетона кумольным методом складывается из следующих стадий: 1. Алкилирование бензола пропиленом. 2. Окисление изопропилбензола в гидроперекись. 3. Выделение гидроперекиси изопропилбензола. 4. Разложение технической гидроперекиси изопропилбензола серной кислотой. 5. Нейтрализация реакционной массы после разложения. 6. Ректификация реакционной массы после разложения и выделение товарных фенола и ацетона. Наиболее важной стадией кумольной технологии фенола является окисление кумола до его гидропероксида (ГПК), так как именно на этой стадии образуются основные и побочные продукты производства. Побочные продукты в дальнейших стадиях участвуют в разнообразных реакциях, тем самым усложняют производство. Промышленные методы получения изопропилбензола Изопропилбензол, или кумол, С6Н5СН (СН3)2 был впервые получен сухой перегонкой кальциевой соли или бариевой соли куминовой (n- изопропилбензойной) кислоты. Впоследствии его обнаружили в продуктах сухой перегонки каменного угля. Строение кумола установили Р.Фиттинг и его ученики, а классический синтез по Вюрцу-Фиттингу взаимодействием йодистого изопропилбензола, бромбензола и натрия провёл О.Якобисен. в 1895 году был осуществлён синтез изопропилбензола из бензола и пропилена при помощи безводного хлористого алюминия в жидкой фазе. Изопропилбензол в обычных условиях - бесцветная легкоподвижная жидкость с приятным запахом, при большом разведении, напоминающем запах древесины хвойных пород. Несмотря на то, что химические методы получения изопропилбензола разработаны давно, промышленное производство его впервые было начато лишь во время второй мировой войны в СССР и США. В то время изопропилбензол целиком использовался в качестве высокооктановой добавки к авиационным бензинам. В промышленности органического синтеза изопропилбензол стал применяться совсем недавно как исходный продукт для получения фенола и ацетона, а также в производстве а-метилстирола. Известны три метода получения изопропилбензола, имеющие промышленное значение: 1.Алкилирование бензола пропиленом в присутствии безводного хлористого алюминия (алкилирование по Фриделю-Крафтсу). 2.Алкилирование бензола пропиленом в паровой фазе с применением фосфорнокислотного катализатора. 3.Алкилирование бензола пропиленом в жидкой фазе в присутствии серной кислоты как катализатора. В России изопропилбензол производят главным образом алкилированиемпоФриделю-Крафтсу. В основе всех перечисленных методов получения кумола лежит реакция алкилирования бензола пропиленом, которая протекает по схеме: Физико-химические свойствагидропероксида изопропилбензола Гидроперекись изопропилбензола С6Н5(СН3)2-О-ОН представляет собой бесцветную маслянистую, немного вязкую жидкость с характерным запахом, напоминающим запах озона. При попадании на кожу вызывает ожоги, подобно концентрированным растворам Н2О2. В глубоком вакууме гидроперекись перегоняется без разложения. Перегонка при остаточном давлении выше 5 мм.рт. ст. сопровождается, по-видимому, уже незначительным разложением, о чём можно судить по бледной, зеленовато-жёлтой окраске дистиллята, отбираемого в этих условиях, в отличие от бесцветных дистиллятов, получаемых при большом разложении. Гидроперкись хорошо растворима в обычных органических растворителях (спирте, эфире, бензоле, ацетоне и др.) и сравнительно плохо - в воде. В обычных условиях гидроперекись является вполне стойким соединением; так, при хранении в течение длительного времени в стеклянной посуде на рассеянном свету(комнатная температура) она не разлагается. Опыты, проведённые П.Г.Сергеевым по хранению технической (87%-ной) гидроперекиси в таре из углеродистой стали показали, что состав гидроперекиси не изменился в течении четырёх лет. Гидроперекись как «детонатор» часто добавляют к дизельному топливу для повышения его цетанового числа. Гидроперкись не даёт окрашенных растворов с хромовой и титановой кислотами. Поэтому с помощью данных реактивов можно обнаружить присутствие перекиси водорода при наличии гидроперекиси изопропилбензола. При кипячении с водой гидроперекись частично перегоняется с водяным паром без изменения, остальное количество её распадается с образованием перекиси водорода и диметилфенилкарбинола. Гидроперекись изопропилбензола медленно реагирует при комнатной температуре с раствором 2,4-динитрофенилгидразина в соляной кислоте, причём выпадает коричневый осадок, состав которого не исследован. Это обстоятельство следует учитывать при попытках идентификации кетонов и альдегидов в виде гидразонов в присутствии гидроперекиси.[2] Гидроперекись является активным инициатором полимризации в водных эмульсиях таких соединений, как дивинил, стирол, а-метилстирол и т.п. Получение гидропероксида изопропилбензола Гидропероксиды – это первичные молекулярные продукты окисления углеводородов. Они относятся к числу довольно нестабильных соединений, превращающихся при окислении в другие продукты. Поэтому их концентрация в реакционной массе, особенно при каталитическом окислении или при повышенных температурах, невелика. Наиболее нестабильны первичные гидропероксиды и, наоборот, относительно стабильны третичные гидропероксиды, которым, собственно и является гидропероксид изопропилбензола. В основе современной теории окисления углеводородов ле жат представления, высказанные более 60 лет назад А. Н. Ба хом и, независимо от него, К. Энглером, согласно которымокисление углеводородов протекает через образование пере кисных соединений, являющихся первыми стабильными продук тами реакции. В настоящее время работами многих исследова телей на примере углеводородов самого различного строения по казано, что на начальных стадиях окисления гидроперекисиявляются практически единственными продуктами. Однакоперекисная теория Баха—Энглера, соответствующая уровнюзнаний конца XIX—начала XX столетия, естественно, не моглаобъяснить целый ряд особенностей процессов окисления. Наиболее полно механизм процессов окисления углеводо родов удалось раскрыть лишь благодаря появлению теориирадикально-цепных реакций, значительную роль в создании ко торой сыграли работы Н. А. Шилова и особенно Н. Н. Семено ва и его школы. Согласно этой теории, окисление углеводоро дов рассматривается как цепной процесс, происходящий приучастии свободных радикалов. Радикально-цепная теория осно вывается на следующих двух положениях классической химии: Свободный радикал (в противоположность валентнонасыщенной молекуле) является весьма активной частицей. Длявзаимодействия между свободными радикалами необходимасравнительно небольшая энергия активации (обычно не выше41 900 кдж/кмоль= 10 ккал/моль), в то время как для реакциймежду валентнонасыщенными молекулами эта величина состав ляет 167 500--418 700 кдж/кмоль=40—100 ккал/моль и более.Реакции свободных радикалов с молекулами также требуютменьшей энергии активации, чем реакции между самими моле кулами. Другими словами, свободный радикал, благодаря на личию свободной валентности, способен возбуждать молекулу,делать ее более активной. При взаимодействии свободных радикалов с молекуламисвободная валентность не исчезает. Среди продуктов такоговзаимодействия неизбежно будет находиться новый свободныйрадикал. Из этих двух положений следует, что если в какой-либореакционной системе появился свободный радикал, то он, легковзаимодействуя с одной из молекул окружающей его среды, об разует новый радикал, который опять вступает в реакцию собразованием радикала, и т. д. Таким образом, возникает реак ционная цепь, которая оборвется лишь в том случае, если исчез нет свободная валентность. Большой экспериментальный материал по окислению углеводородов, накопленный к настоящему времени, убедительнопоказывает, что начальная стадия процесса окисления — образование гидроперекиси — является радикально-цепной реак цией. Одно из доказательств этого — наличие индукционногопериода и ускоряющее действие на процесс, особенно в началь ный период, веществ, способных в условиях окисления разла гаться с образованием свободных радикалов (различные пере киси и гидроперекиси,азосоединения и др.). Ускоряющеевлияние перекисей на окисление углеводородов было показаноцелым рядом исследований. Цепной характер окисленияуглеводородов доказывается также тем, что небольшие при меси некоторых веществ (например, фенолов) способны резко замедлять процесс. Процесс окисления углеводородов, как и всякий цепной про цесс, включает в себя по крайней мере три реакции: зарожде ние (инициирование), рост и обрыв цепи.[1] Реакция зарождения цепи связана с разрывом С—Н-связи в валентнонасыщенной молекуле окисляемого углеводорода RH: Однако энергия разрыва связи С—Н обычно составляет 335000—418 700 кдж/кмоль (80—100 ккал/моль) и, следова тельно, в условиях жидкофазного окисления такой разрыв само произвольно не происходит. Он может наблюдаться при столк новении молекулы RH с какой-либо активной частицей А: или при поглощении кванта световой энергии в случае фото химического окисления: В настоящее время принято, что реакция зарождения цепи при окислении углеводородов кислородом протекает по схеме: которая является наиболее энергетически выгодной так как требует затраты энергии на 196 900 кдж/кмоль (47 ккал/моль) меньше, чем процесс образования радикалов Re путем распада молекулы по связи С—Н32. Рост цепи при наличии в системе радикалов происходит та ким образом: Возникает более или менее длинная реакционная цепь, в результате чего значительная часть молекул исходного угле водорода может превратиться в гидроперекись. Обрыв цепи происходит вследствие различных причин, основ ные из которых следующие: рекомбинация свободных радика лов, обрыв цепи на стенках реактора и взаимодействие свобод ных радикалов с примесями, являющимися ингибиторами. Рекомбинация может заключаться в следующих элементар ных актах: В некоторых условиях процесс рекомбинации можетпротекать в заметном объеме. Так, описано получение с выходомдо 38% соответствующих «димеров» (R—R) изопропилбензола,п-цимола и хлоризопропилбензола путем жидкофазного окисле ния этих углеводородов кислородом воздуха. Значительнораньше (в 1944 г.) П. Г. Сергеевым, Б. Д. Кружаловым иР. 10. Удрисом при изучении состава продуктов, образующихсяв результате окисления изопропилбензола, был выделен иидентифицирован 2,4-диметил-2,4:дифенилбутан, появление ко торого можно объяснить лишь димеризацией радикала R*.Однако следует отметить, что на первых стадиях процесса,когда концентрация свободных радикалов в системе незначи тельна, вероятность такого бимолекулярного столкновениярадикалов мала и рекомбинация не является главной причинойобрыва цепи. То же самое относится и к обрыву цепи за счетстолкновения свободных радикалов со стенками реактора. В от личие от процессов, протекающих в газовой фазе, где роль стен ки реактора гораздо больше, при жидкофазном процессе веро ятность такого столкновения мала, ввиду значительно меньшейскорости диффузии свободных радикалов к стенке через жид кость, чем через газ. Кроме того, любой свободный радикал,диффундируя через слой жидкости к стенке, неизбежно встре тит на своем пути громадное количество молекул и радикалов,способных реагировать с ним. Сказанное, разумеется, не отно сится к реакторам, имеющим развитую поверхность в виде на садки, или к реакторам пленочного типа. Главная роль в обрыве цепи при жидкофазном окисленииуглеводородов, по-видимому, принадлежит ингибиторам — ве ществам, способным тормозить цепные реакции. Механизм дей ствия ингибиторов и, в частности, антиокислителей (антиоксидантов), т. е. ингибиторов процессов окисления, в ряде случаевостается неясным. Тормозящее действие некоторых ингибито ров совершенно не связано с реакцией обрыва цепи, а может,например, заключаться в уменьшении скорости реакции зарож дения цепи. В данном случае речь идет лишь о тех ингибито рах, роль которых состоит в обрыве реакционной цепи. В зави симости от своего химического строения ингибиторы по-разномуобрывают цепь; здесь различают два случая:
Если вновь образованные свободные радикалы In* или RInH* и иR02lnH* будут менее активны, чем исходные радикалы R* иR02*, то произойдет ингибирование— торможение цепного про цесса окисления. Совершенно очевидно, что ингибиторы первого типа должныиметь более слабую связь In—Н, чем связь С—Н у окисляе мого углеводорода. К этой категории ингибиторов следует от нести, например, фенолы и нафтолы. Ко второму типу ингиби торов, по-видимому, относятся амины (главным образомароматические), способные присоединять радикалы R02*, и хиноны, способные к захвату радикалов R*. Окисление углеводородов относится к числу автокаталити ческих процессов, в связи с чем часто применяют термин «автоокислеиие» (аутооксидация). Процессы автокатализа являютсяцепными реакциями с вырожденным разветвлением, теория ко торых подробно разработана Н. Н. Семеновым. Самоускоре ние, или автокатализ, процессов окисления заключается в том,что первичный продукт окисления — гидроперекись обладаетспособностью в условиях окисления подвергаться частичномураспаду на свободные радикалы (вырожденное развет вление). Уже при небольших концентрациях гидроперекиси(10-4 моль/л) скорость реакции ее распада намного превы шает скорость реакции зарождения цепи путем разрыва связиС—Н в углеводороде. Поэтому основным источником свободныхрадикалов в системе является реакция вырожденного развет вления. |
