Описание получения сырья
 Скачать 0.8 Mb. Скачать 0.8 Mb.
|
|
Описание получения сырья Сырьем для получения гранулированной аммиачной селитры является азотная кислота массовой долей не менее (56÷57) % и газообразный аммиак. Для уменьшения слеживаемости аммиачной селитры в технологический цикл производства вводится магнезиальная добавка. Осветленный (30÷40) % раствор нитрата магния поступает из заводской сети в установленные на нулевой отметке три хранилища поз.Е-5, Е-6 и Е-7 вместимостью соответственно 40, 40 и 60м3. Готовится раствор нитрата магния в цехе МУиК №2 отделения магнезиальной добавки на специальной установке. Уровень нитрата магния в хранилищах контролируется в ЦПУ, имеется сигнализация минимального и максимального уровня. Из хранилищ раствор нитрата магния, пройдя фильтр поз.16, подается центробежным насосом поз.Н-4 через регулирующий клапан и ротаметр в смеситель, установленный на трубопроводе азотной кислоты перед каждым аппаратом ИТН. Количество нитрата магния, подаваемого в аппарат ИТН, регулируется автоматически клапанами и фиксируется ротаметрами по месту и на вторичных приборах в ЦПУ. В случае выхода из строя ротаметра или регулирующего клапана предусмотрена подача нитрата магния по байпасу. Азотная кислота, массовой долей не менее (56-57) %, подается центробежным насосом со склада отделения азотной кислоты цеха МУиК №1 в трубное пространство подогревателей азотной кислоты поз.2 на отм.+53м., где подогревается до температуры (5080) 0C за счет тепла конденсации сокового пара, поступающего из аппаратов ИТН поз.3 в межтрубное пространство подогревателей азотной кислоты. Избыточное давление азотной кислоты на отм.+53м должно поддерживаться на уровне (0,2-0,4) МПа. Температура азотной кислоты на выходе из подогревателей поз.2 поддерживается автоматически изменением уровня конденсата сокового пара в межтрубном пространстве. В случае выхода из строя подогревателей азотной кислоты поз.2(1÷4) предусматривается подача азотной кислоты в аппараты ИТН поз.3(1÷4) мимо подогревателей по байпасной линии. Газообразный аммиак из общезаводского коллектора под избыточным давлением (0,180,35) МПа поступает в сепаратор–испаритель поз.32, установленный на входе газообразного аммиака в отделение, а затем в трубную часть перегревателя аммиака поз.2а. Греющим агентом сепаратора–испарителя служит пар давлением (1,21,5) МПа. Греющим агентом перегревателя аммиака поз.2а служит паровой конденсат, поступающий из подогревателей воздуха поз.10,21, конденсат с упаковки, с зарядной станции, с установки обработки гранул аммиачной селитры антислеживателем и с сепаратора-испарителя поз.32. При возможных забросах жидкого аммиака, в межтрубное пространство перегревателей поз.2а в линию конденсата после поз.10,21 дополнительно подается пар под избыточным давлением (1,21,5) МПа. Паровой конденсат из перегревателей аммиака поз.2а разделяется на два потока. Один поток направляется в отделение азотной кислоты, другой – в сборник парового конденсата поз.4. Температура газообразного аммиака на выходе из перегревателей поз.2а регулируется вручную количеством парового конденсата, либо количеством греющего пара. Из перегревателей поз.2а газообразный аммиак с температурой не ниже +50C и с избыточным давлением не ниже 0,18 МПа, которое поддерживается автоматически, поступает в трубное пространство подогревателя поз.1, где подогревается до температуры (70-190)0C паровым конденсатом, поступающим в межтрубное пространство подогревателя из межтрубного пространства выпарного аппарата поз.5. Охлажденный в подогревателе аммиака поз.1 паровой конденсат направляется в промежуточную емкость конденсата поз.37, после промежуточной емкости поз.37 конденсат направляется в бак конденсата поз.17. Минеральные удобрения находят широкое применение, как в сельском хозяйстве, так и в различных областях промышленности. В отличие от мирового рынка, именно промышленное потребление азотных удобрений является основным на внутреннем рынке. Важнейшим видом минеральных удобрений являются азотные: аммиачная селитра, карбамид, сульфат аммония, водные растворы аммиака. Аммиачная селитра, или нитрат аммония, NH4NO3 – кристаллическое вещество белого цвета, содержащее 35% азота в аммонийной и нитратной формах, обе формы легко усваиваются растениями . Основными потребителями аммиачной селитры являются следующие отрасли: - сельское хозяйство; - производство сложных минеральных удобрений; - горнопромышленный комплекс (собственное производство ВВ); - угольная промышленность (собственное производство ВВ); - производство взрывчатых веществ; - строительная индустрия; Аммиачная селитра обладает потенциальной, или физиологической кислотностью. Эта кислотность возникает в почве, с одной стороны, в результате более быстрого потребления растениями ионов (NH4+) и соответственно накопления кислотного остатка (ионов NO3) в почве и, с другой стороны, в результате окисления аммиака в азотную кислоту нитрифицирующими микроорганизмами почвы. При длительном применении аммиачной селитры потенциальная кислотность этого удобрения может привести к изменениям химического состава почвы, что в ряде случаев служит причиной снижения урожайности Гранулированную аммиачную селитру применяют больших масштабах перед посевом и для всех видов подкормок. В меньших масштабах ее используют для производства взрывчатых веществ. Аммиачная селитра хорошо растворяется в воде и обладает большой гигроскопичностью (способность поглощать влагу из воздуха). Это является причинного того, что гранулы удобрения расплываются, теряют свою кристаллическую форму, происходит слеживание удобрений – сыпучий материал превращается в твердую монолитную массу. Нитрат аммония имеет ряд преимуществ перед другими азотными удобрениями, так как содержит 34 % азота и в этом отношение уступает лишь карбамиду. Кроме того аммиачная селитра содержит одновременно аммиачную и нитратную форму азота, которые используются растениями в разные периоды роста, что положительно складывается на увеличение урожайности почти всех сельскохозяйственных культур. Отрасли, использующие аммиачную селитру как сырье для производства взрывчатых веществ (ВВ) являются вторым по емкости сегментом ее потребления на внутреннем рынке после сельского хозяйства. Аммиачно- селитряные ВВ представляют собой большую группу взрывчатых веществ. Их принято относить к бризантным взрывчатым веществам пониженной мощности (в тротиловом эквиваленте на 25% слабее тротила). Однако это не вполне так. По бризантности аммиачно-селитряные ВВ. Важнейшими причинами слеживаемости являются: 1.Повышенное содержание влаги в готовом продукте; 2.Неоднородность и низкая механическая прочность частиц селитры; 3.Изменение кристаллических модификаций аммиачной селитры. Нитрат аммония – сильный окислитель. С растворами некоторых веществ он реагирует бурно, вплоть до взрыва (нитрит натрия).Малочувствителен к толчкам, трению, ударам, сохраняет устойчивость при попадание искр различной интенсивности. Он способен взрываться только под действием сильного детонатора или при термическом разложении. Селитра не является горючим продуктом. Горение поддерживает только оксид азота. Таким образом одним из условий производства аммиачной селитры является чистота ее исходных растворов и готового продукта. 2.Технология производства аммиачной селитры 2.1 Схема агрегата по производству аммиачной селитры АС–72 Принимаем схему производства аммиачной селитры АС-72 (см. рисунок 2.1). 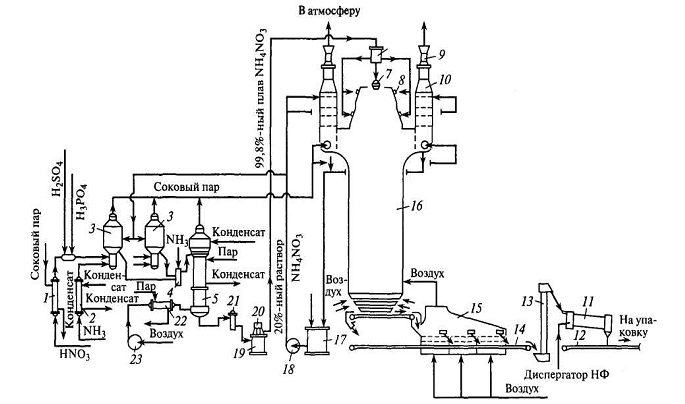 Рисунок (2.1) Схема агрегата по производству аммиачной селитры АС–72: 1 – подогреватель кислоты; 2 – подогреватель аммиака; 3 – аппараты ИТН; 4 – донейтрализаторы; 5 – выпарной аппарат; 6 – напорный ак; 7,8 - грануляторы; 9,23 – вентиляторы; 10 – промывной скруббер; 11 – барабан; 12,14 – транспорте-ры; 13 – элеватор; 15 – аппарат кипящего слоя; 16 – грануляционноая башня; 17 – сборник; 18,20 – насосы; 19 – бак для плава; 21 – фильтр для плава; 22 – подогреватель воздуха В современном крупнотоннажном агрегате по производству аммиачной селитры АС-72 мощностью 1360 т/сут. исходная 55 – 60 %-ная азотная кислота подогревается в подогревателе 1 до 70– 800 С соковым паром из аппарата ИТН 3 и подается на нейтрализацию. Перед аппаратами 3 к азотной кислоте добавляют фосфорную и серную кислоты в таких количествах, чтобы в готовом продукте со-держалась 0,3 – 0,5 % Р2О5 и 0,05 – 0,2 % сульфата аммония. В агрегате установлены два аппарата ИТН, работающие параллельно. Кроме азотной кислоты в них подают газообразный аммиак, предварительно нагревание а также частицы унесенной аммиачной селитры. Для очистки этих потоков в верхней части грануляционной башни расположены шесть параллельно работающих промывных скрубберов тарельчатого типа 10, орошаемых 20—30 %-ным раствором аммиачной селитры, которая подается насосом 18 из сборника 17. Часть этого раствора отводится в нейтрализатор ИТН промывки сокового пара, а затем подмешивается к раствору селитры, и, следовательно, используется для выработки продукции. Очищенный воздух отсасывается из грануляционной башни вентилятором 9 и выбрасывается в атмосферу. 2.2 Нейтрализация азотной кислоты аммиаком Процесс нейтрализации азотной кислоты аммиаком описывается NH3 + HNО3 = NH4NО3 + Q Эта реакция является практически необратимой и протекает с большой скоростью без образования побочных продуктов. В процессе нейтрализации выделяется большое количество тепла, определяемое тепловым эффектом реакции, концентрацией исходной азотной кислоты и температурой реагентов. Тепловой эффект реакции может быть рассчитан по теплотам образования веществ, участвующих в реакции, из простых веществ при температуре 18 °C и нормальном давлении [1]. В соответствии с известным законом Гесса, тепловой эффект реакции нейтрализации чистых веществ при стандартных условиях равен 144 936 Дж/моль (34624 кал/моль). Так как в реальном процессе в реакции участвует, в частности не 100%-ная азотная кислота, а ее 47 –60%-ные растворы, то тепловой эффект реакции. процесс нейтрализации, поэтому с точки зрения целесообразности снижения температуры в зоне реакции, что является полезным из-за изложенных выше соображений, целесообразно проводить процесс нейтрализации при низком давлении и даже под вакуумом. Наиболее широкое распространение получили установки, в которых процесс нейтрализации осуществляют под давлением, близким к атмосферному (избыточное давление сокового пара 5 – 20 кПа). Преимуществом нейтрализации под атмосферным давлением является простота схемы, возможность использования газообразного аммиака, который из цеха синтеза аммиака выдается под давлением, как правило, не выше 200–300 кПа, без его сжижения и повторного испарения. Эти преимущества особенно весомы при использовании азотной кислоты концентрацией не выше 50%, когда соковый пар при атмосферном давлении можно использовать для дополнительного упаривания под вакуумом растворов, полученных в нейтрализаторе, т. е. когда удается двукратно использовать тепло реакции нейтрализации. Проведение процесса нейтрализации с использованием вакуума имеет относительно ограниченное применение вследствие усложнения схемы стадии нейтрализации, а также невозможности полезного использования тепла сокового пара и, следовательно, снижения экономичности процесса. Такие схемы используются лишь в установках, где в качестве сырья применяют не чистый аммиак, в аммиак-содержащие газовые смеси, такие, как танковые и продувочные газы производства аммиака или газы дистилляции производства карбамида. Нейтрализация азотной кислоты аммиаком под повышенным давлением позволяет уменьшить габариты нейтрализаторов, промывателей сокового пара, а также получать соковый пар с более высоким потенциалом. Однако обычно эти преимущества не окупаются из-за необходимости применять жидкий аммиак вместо газообразного, повышения температуры в зоне нейтрализации, а также из-за усложнения схемы, и ограниченных возможностей использования сокового пара. 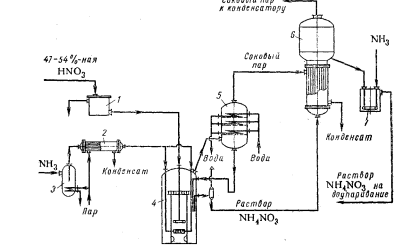 Рисунок 2.2 – Схема нейтрализации HNO3 под атмосферным давлением: 1– бак для азотной кислоты; 2 – подогреватель аммиака; 3 – сепаратор жидко-го аммиака; 4 – аппарат ИТН; 5 – ловушка-промыватель сокового пара; 6 – ваку-умный выпарной аппарат I степени; 7 – донейтрализатор. Азотная кислота концентрацией 47 –54% поступает в напорный бак 1, а затем через автоматический регулятор расхода в нейтрализатор – аппарат ИТН 4. Газообразный аммиак поступает из цеха синтеза аммиака под давлением 200 –300 кПа, проходит сепаратор 3 и подогреватель 2 для предотвращения попадания в нейтрализатор жидкого аммиака. Давление газообразного аммиака на входе в цех стабилизируется с помощью автоматического регулятора; расход аммиака в нейтрализатор автоматически регулируется по соотношению с азотной кислотой и корректируется по рН раствора на выходе из нейтрализатора. Нейтрализатор получил название аппарата ИТН (использование тепла нейтрализации) в отличие от ранее применявшимся нейтрализаторов, в которых тепло реакции отводилось водой без использования для упаривания растворов. Как правило, в выходящем растворе поддерживают небольшой избыток азотной кислоты (до 2–3 г/л), поскольку стабильно сохранять стехиометрическое соотношение HNO3 и NH3 на входе в ИТН практически невозможно. При избытке аммиака в выходящем растворе резко возрастает загрязнение им сокового пара; избыток азотной кислоты позволяет практически полностью поглотить аммиак. В этих схемах нейтрализация аммиака осуществляется в аппарате, работающем при атмосферном давлении, а испарение воды из раствора аммиачной селитры в вакуум-испарителе. При этом между нейтрализатором и вакуум-испарителем циркулирует большое количество раствора. Кратность циркуляции раствора рассчитывается таким образом, чтобы температура раствора в нейтрализаторе, нагревающегося за счет тепла реакции нейтрализации, была ниже температуры кипения раствора аммиачной селитры при атмосферном давлении, при котором ведется нейтрализация. Она обычно составляет 10–45 объемов на 1 объем продукционного раствора. Этим предотвращается кипение раствора в зоне реакции. Испарение воды осуществляется в вакуум-испарителе, где происходит вскипание раствора аммиачной селитры, перегретого по отношению к температуре кипения этого раствора при выбранном вакууме, который обычно достигает 80–87 кПа. Так как полезно использовать тепло сокового пара, удаляемого из раствора под вакуумом, невозможно, то в настоящее время при использовании чистого газообразного аммиака такие схемы нейтрализации не применяются. Однако при использовании аммиак-содержащих газовых смесей, например газов дистилляции из цехов карбамида или продувочных газов, такая схема рациональна по следующим причинам: соковый пар смешивается с инертными газами исходных газовых смесей и все равно не может быть использован; при применении вакуум-испарителя и снижении температуры в зоне реакции инертные газы после поглощения аммиака выбрасываются в атмосферу с меньшим содержанием вредных примесей; повышается степень поглощения аммиака. В отечественной промышленности такие схемы получения аммиачной селитры в настоящее время не применяются. Однако рядом зарубежных фирм эксплуатируются установки, в которых процесс нейтрализации осуществляют под давлением 350–600 кПа, в зависимости от концентрации азотной кислоты (49–57%). Чаще всего применяют 56 –57%-ную кислоту и нейтрализацию ведут под давлением 350 кПа. На рисунке 2.2 изображена принципиальная схема нейтрализации. 56%-ной азотной кислоты под давлением 350 кПа. также увеличивает безопасность процесса, однако приводит к значительному повышению содержания аммиака в соковом паре. Конденсат сокового пара из выпарного аппарата 5 дросселируется в сборник 10, в котором он вскипает. Растворенный аммиак удаляется с парами. Пар вторичного вскипания конденсируется в конденсаторе 11 и насосом 13 подается в нейтрализатор / с содержанием аммиака 10–12 г/л. Основное количество конденсата сокового пара содержит до 2 г/л аммиака. После нейтрализации азотной кислотой конденсат сокового пара с содержанием до 10 г/л NH4NО3 направляется на орошение абсорбционных колонн производства азотной кислоты. Расход аммиака на 1 т NH4NО3 в такой установке достигает 220 кг, т. е. значительно выше, чем на отечественных установках с нейтрализацией под атмосферным давлением в кислой среде. Этот процесс может быть усовершенствован. Например, соковый пар, выходящий из нейтрализатора, может быть подвергнут промывке в тарельчатом промывателе кислым раствором аммиачной селитры; соответственно будут снижены потери аммиака и загрязненность конденсата сокового пара. В этом процессе выгодно также вести предварительный подогрев азотной кислоты за счет тепла сокового пара из нейтрализатора. Такой прием позволяет использовать азотную кислоту более низкой концентрации с получением в конечном итоге (после выпаривания) раствора аммиачной селитры той же концентрации (95%). Описанная схема является схемой с двойным использованием тепла нейтрализации в случае применения азотной кислоты концентрацией 55 –57%, что, естественно, позволяет экономить свежий пар на стадии доупаривания растворов. |
