ЗАНЯТИЕ 5 Буферные растворы. Определение буферных систем и их классификация
 Скачать 228.5 Kb. Скачать 228.5 Kb.
|
Вычисление рН и рОН буферных систем. Уравнение Гендерсона-ГассельбахаКаждая из буферных систем характеризуется определенной присущей ей концентрацией ионов Н+ (активной кислотностью), которую система и стремится сохранить на неизменном уровне при добавлении к ней сильной кислоты либо щелочи. Установим на примере ацетатного буфера факторы, влияющие на величину активной кислотности. В растворе данной буферной системы происходят следующие реакции электролитической диссоциации: CH3COOH CH3COO– + H+ CH3COONa → CH3COO– + Na+ (Гидролиз соли, т.е. взаимодействие ацетат-ионов с Н2О CH3COO– + HOH CH3COOH + OH– учитывать не будем.) Таким образом, ионы Н+ образуются только за счет диссоциации некоторого числа молекул уксусной кислоты. Этот процесс является обратимым и количественно характеризуется константой кислотности Kа: 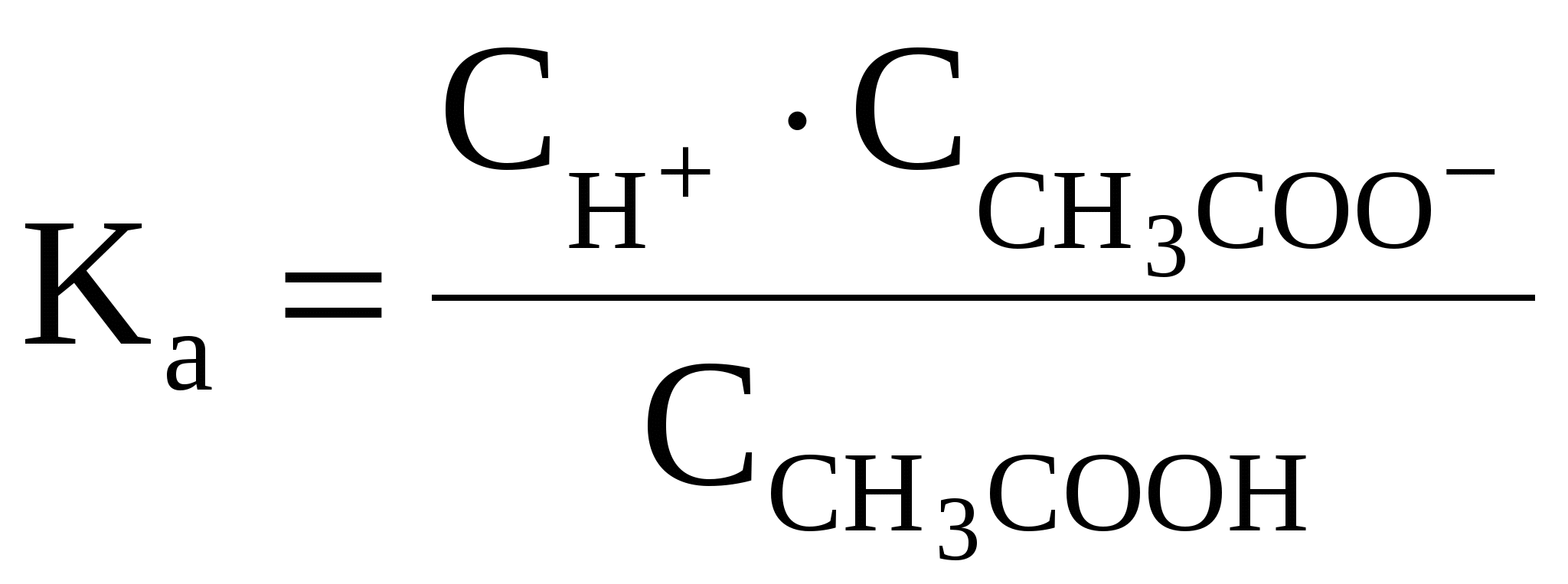 где Из данного уравнения можно выразить 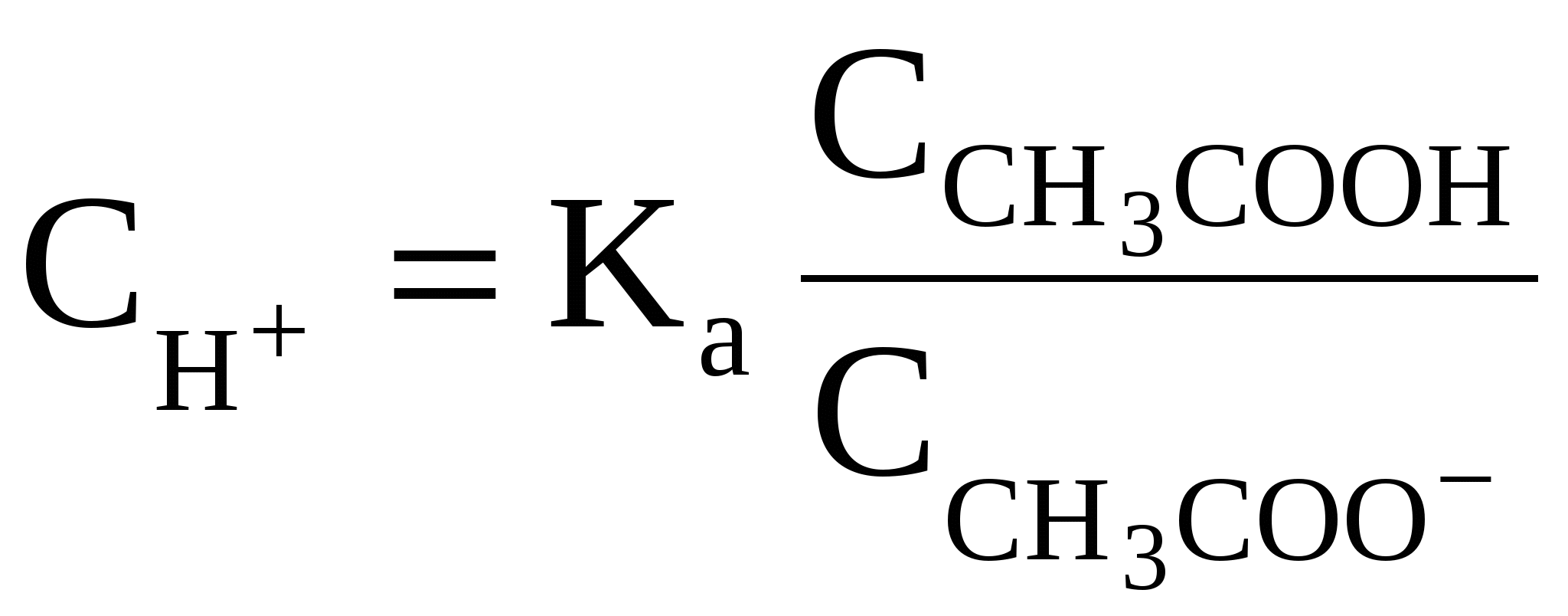 Кроме уксусной кислоты в растворе присутствует ее соль CH3COONa. Она является сильным электролитом и полностью распадается на ионы. В результате этого концентрация анионов СН3СОО– резко возрастает и согласно принципа Ле-Шателье равновесие реакции диссоциации уксусной кислоты смещается влево, т.е. в сторону образования ее молекул. Причем диссоциация уксусной кислоты в присутствии собственной соли может быть настолько подавленной, что равновесную концентрацию ее нераспавшихся молекул в растворе можно считать равной концентрации СН3СООН, а равновесную концентрацию ацетат-ионов – исходной концентрации соли. В связи с этим выражение, по которому рассчитывается концентрация ионов Н+, можно записать иначе: где Скислоты и Ссоли – исходные концентрации компонентов буферной системы. Прологорифмируем полученное уравнение (с учетом того, что логарифм произведения равен сумме логарифмов сомножителей): и умножим обе его части на –1: Как было показано нами ранее В связи с этим запишем уравнение для расчета концентрации ионов Н+ в окончательном виде: Данное выражение называется иначе уравнением Гендерсона-Гассельбаха. Его можно использовать для вычисления рН любой кислотной буферной системы. Например, для фосфатного буфера уравнение Гендерсона-Гассельбаха запишется следующим образом: 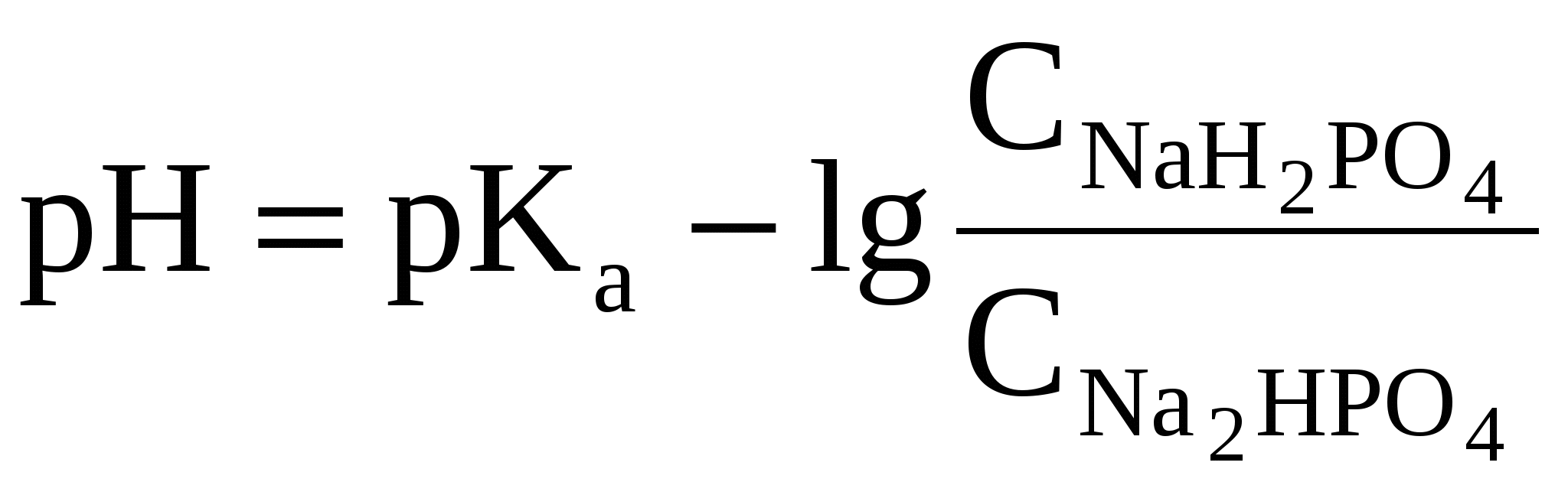 (в данной системе роль слабой кислоты играет анион Н2РО4–, то В водных растворах рН и рОН являются сопряженными величинами. Их сумма всегда равна 14, т.е.: рН + рОН = 14 Зная концентрацию ионов Н+ или рН можно вычислить концентрацию гидроксильных ионов или рОН. Уравнения Гендерсона-Гассельбаха для расчета рОН и рН в оснóвных буферных системах выглядят следующим образом: где pKb = –lg Kb (основания), Соснования и Ссоли – исходные молярные концентрации компонентов данных буферных систем, т.е. слабого основания и его соли с сильной кислотой. Из приведенных выше уравнений следует, что рН и рОН буферной системы зависит от константы кислотности или основности слабого электролита, входящего в ее состав и от соотношения концентраций компонентов буфера. Значение рК для слабого электролита является величиной постоянной, не зависит от концентрации этого электролита в растворе и приводится в соответствующих справочниках. Зная его можно с помощью уравнения Гендерсона-Гассельбаха рассчитать рН буферного раствора, если известен его количественный состав или, наоборот, определить состав раствора (исходные концентрации его компонентов), который будет обеспечивать заданное значение рН. На практике обычно пользуются готовыми таблицами, в которых указано, в каком соотношении должны быть взяты компоненты для получения буферного раствора с желаемым значением рН. Если концентрации веществ в буферной системе одинаковые, т.е. Скислоты = Ссоли или Соснования = Ссоли, то рН = рKa (для кислотной буферной системы) pOH = pKb (для оснóвной буферной системы) Изменяя концентрацию какого-либо компонента можно сместить значение рН в ту или иную сторону для достижения нужной величины. В буферных системах, используемых на практике, концентрации компонентов не отличаются друг от друга более чем в 10 раз, т.е. их рН не отклоняется больше чем на единицу от величины рK своего слабого электролита. Таким образом, область практических значений рН буферных систем (область буферирования) лежит в интервале pK ± 1. Если концентрации компонентов буферного раствора различаются более чем в 10 раз, то такой раствор обладает слабым буферным действием и может удерживать неизменным содержание ионов Н+ только при добавлении очень малых количеств сильной кислоты либо щелочи. Это делает неудобным его использование в практических целях. При разбавлении концентрации обоих компонентов буферных растворов уменьшаются в одинаковое число раз, поэтому их соотношение остается неизменным. Следовательно по уравнению Гендерсона-Гассельбаха величина рН буферного раствора при этом тоже не должна изменяться. При разбавлении в 10-20 раз экспериментальные измерения рН хорошо согласуются с теоретическими расчетами. Однако при большем разбавлении наблюдается небольшое увеличение рН раствора, которое связано с возрастанием степени диссоциации слабого электролита и увеличением константы его диссоциации. Уравнение Гендерсона-Гассельбаха является приближенным и его не рекомендуется использовать в следующих случаях: 1) если кислота либо основание буферной системы не является достаточно слабым электролитом (например, для кислоты pKa < 3). Тогда нельзя пренебрегать их диссоциацией в присутствии собственной соли; 2) если кислота либо основание буферной системы являются, наоборот, слишком слабыми электролитами (например, для кислоты pKa > 11). Тогда нельзя пренебрегать гидролизом их солей. |
