Особенности химического состава клетки и химического взаимодействия
1. Электронная структура атома?
Основными характеристиками атома, которые определяют его поведение в химических реакциях и при образовании простых веществ, является строение внешнего электронного слоя и энергия электронов относительно положительно заряженного ядра. Обе характеристики подлежат периодической зависимости от порядкового номера элемента, который всегда указывается в периодической таблице элементов.
Согласно современным квантово-механическими представлениями конфигурация электронной оболочки определяется зарядом ядра атома и положением элемента в периодической системе. Как уже установлено, электроны с одинаковым значением главного квантового числа образуют квантовые уровни, емкость которых увеличивается по мере удаления от ядра. Квантовые уровне, в свою очередь, построенные из подуровней, объединяющих электроны с одинаковым значением орбитального квантового числа. А подуровни состоят из орбиталей, на каждой из которых может находиться не более двух электронов. Распределение электронов в атоме выражают с помощью электронной формулы (условного записи распределения электронов в атоме с помощью квантовых чисел) и электронно-графической схемы ‒ квантовых ячеек, в которых клеточка символизирует орбиталь, а стрелка ‒ электрон.
В электронных формулах цифрами указывают номер энергетического уровня, латинскими буквами ‒ энергетические подуровни, а цифрами вверху справа ‒ количество электронов на подуровне. Например, условная запись 5d4 означает, что на d-подуровне пятого энергетического уровня размещаются четыре электрона.
2. Чем обусловлена стабильность и нестабильность атомов?
Изотопы ‒ это атомы одного и того же элемента, которые имеют разные атомные структуры. Изотопы одного и того же элемента имеют один и тот же атомный номер, поскольку они представляют собой разные формы одного и того же элемента. Они отличаются друг от друга количеством нейтронов, которые они имеют в своих ядрах. Атомная масса элемента определяется суммой числа протонов и числа электронов. Поэтому атомные массы изотопов отличаются друг от друга. Изотопы можно разделить в основном на две группы как стабильные изотопы и нестабильные изотопы. Основное различие между стабильными и нестабильными изотопами состоит в том, что стабильные изотопы имеют стабильные ядра, тогда как нестабильные изотопы имеют нестабильные ядра.
Стабильные изотопы ‒ это атомы, имеющие стабильные ядра. Они нерадиоактивны из-за стабильности их ядер. Поэтому стабильные ядра не испускают излучение. Конкретный элемент может иметь более одного стабильного изотопа. Для некоторых элементов, таких как уран, все изотопы нестабильны. Двумя основными фактами, определяющими стабильность ядер, являются отношение протонов к нейтронам и сумма протонов и нейтронов.
Нестабильные изотопы ‒ это атомы, которые имеют нестабильные ядра. Это радиоактивные изотопы. Поэтому их также называют радиоактивные изотопы, Некоторые элементы, такие как уран, имеют только радиоактивные изотопы. Другие элементы имеют как стабильные, так и нестабильные изотопы. Нестабильный элемент может быть нестабильным по нескольким причинам. Наличие большого количества нейтронов по сравнению с числом протонов является одной из таких причин. В этом типе изотопов радиоактивный распад происходит, чтобы получить устойчивое состояние. Здесь нейтроны превращаются в протоны и электроны.
3. Типы связей в живых системах, как они возникают?
Живые организмы определенным образом связаны друг с другом. Различают следующие типы связей между видами: трофические, топические, форические, фабрические.
Трофические связи возникают между видами, когда один вид питается другим: живыми особями, мертвыми остатками, продуктами жизнедеятельности. Трофическая связь может быть прямой и косвенной. Прямая связь проявляется при непосредственном поедании одними особями других живых особей и их трупов. Косвенная связь возникает при конкуренции разных видов за один пищевой ресурс.
Топические связи проявляются в изменении одним видом условий обитания другого вида. Например, под хвойным лесом, как правило, отсутствует травянистый покров.
Форические связи возникают, когда один вид участвует в распространении другого вида (перенос животными семян, спор, пыльцы растений, мелких особей).
Фабрические связи заключаются в том, что один вид использует для своих сооружений продукты выделения, мертвые остатки или даже живых особей другого вида. Например, птицы при постройке гнёзд используют ветки деревьев, траву, пух и перья других птиц.
Протокооперации – взаимовыгодное, но не обязательное сосуществование организмов, пользу из которого извлекают все участники. Например, раки-отшельники и актинии. На раковине рака может поселяться коралловый полип актиния, который имеет стрекательные клетки, выделяющие яд. Актиния защищает рака от хищных рыб, а рак-отшельник, перемещаясь, способствует распространению актиний и увеличению их кормового пространства.
Мутуализм – взаимовыгодное сожительство, когда либо один из партнеров, либо оба не могут существовать без сожителя. Например, травоядные копытные и целлюлозоразрушающие бактерии.
Комменсализм – взаимоотношения, при которых один из партнеров получает пользу от сожительства, а другому присутствие первого безразлично. Различают две формы комменсализма: синойкия (квартиранство) и трофобиоз (нахлебничество).
Конкуренция – взаимоотношения, при которых организмы соперничают друг с другом за одни и те же ресурсы внешней среды при недостатке последних. Организмы могут конкурировать за пищевые ресурсы, полового партнера, убежище, свет.
Паразитизм – взаимоотношения, при которых паразит не убивает своего хозяина, а длительное время использует его как среду обитания и источник пищи. К паразитам относятся: вирусы, патогенные бактерии, грибы, простейшие, паразитические черви. Различают облигатных и факультативных паразитов. Облигатные паразиты ведут исключительно паразитический образ жизни и вне организма хозяина либо погибают, либо находятся в неактивном состоянии (вирусы). Факультативные – ведут паразитический образ жизни, но в случае необходимости могут нормально жить во внешней среде, вне организма хозяина (патогенные грибы, бактерии).
Хищничество – взаимоотношения, при которых один из участников умерщвляет другого и использует его в качестве пищи. Частным случаем хищничества является каннибализм (крысы, бурые медведи).
Аменсализм – взаимоотношения, при которых один организм воздействует на другой и подавляет его жизнедеятельность, а сам не испытывает никаких отрицательных влияний со стороны подавляемого.
Нейтрализм – сожительство двух видов на одной территории, не имеющее для них ни положительных, ни отрицательных последствий.
4. Слабые взаимодействия в органических соединениях, где и когда они появляются?
Слабые взаимодействия, например водородные связи, между химическим группами остова во многих белках приводят к образованию в них регулярных участков, представляющих собой спирали или слоистые структуры. Однако уникальная пространственная структура образуется с участием и ряда других слабых взаимодействий между боковыми радикалами. Большое их число (несмотря на слабость) обусловливает то, что белковая молекула может обладать стабильной пространственной конфигурацией.
Среди 20 видов боковых радикалов имеются заряженные (положительно или отрицательно), гидрофобные, гидрофильные, содержащие циклические группы и др. Их сближение характеризуется целым спектром слабых взаимодействий: ионных, ион-дипольных, диполь-дипольных (разнообразных вандерваальсовских – совокупность ориентационных, индукционных и дисперсионных сил), гидрофобных и др. Энергия U слабых взаимодействий в разной степени n зависит от расстояния r между взаимодействующими элементами:
U 1/rn.
5. Почему углерод важный элемент биологических систем?
Важность углерода в живых существах это основано на факте, что это химический элемент, на котором основано существование жизни. Его способность образовывать полимеры делает его идеальным элементом для объединения в молекулы, которые генерируют жизнь.
Углерод является ключевым химическим элементом для жизни и природных процессов, происходящих на земле. Это шестой самый распространенный элемент во вселенной, участвующий в формированиях и астрономических реакциях.
Углерод является легким элементом, и его присутствие в живых существах является фундаментальным, так как он используется и управляется энзимами органических систем.
Человеческое тело состоит из 18% углерода, и было подсчитано, что вся органическая жизнь на Земле имеет в качестве основы наличие углерода.
Некоторые теории предполагают, что если в другой части Вселенной есть жизнь, то в ее составе также присутствует большое количество углерода.
Углерод является фундаментальным элементом для формирования таких компонентов, как белки и углеводы, а также для физиологического функционирования живого организма.
Несмотря на то, что он является природным элементом, углерод также присутствует в реакциях и химических вмешательствах, которые совершил человек, обеспечивая новые преимущества.
Поскольку живые существа являются результатом ряда химических реакций в определенный момент времени, и, как уже упоминалось, углерод играет фундаментальную роль в этих реакциях, было бы невозможно представить жизнь без присутствия этого элемента.
Универсальность углерода позволила ему присутствовать в клеточных и микроорганических процессах, которые вызывают жизненно важные компоненты организма: жиры, белки, липиды, которые помогают формированию неврологических систем, и нуклеиновые кислоты, которые хранят ДНК (генетический код каждого человека).
Углерод, в форме углекислого газа, представляет собой газ, присутствующий на атмосферном уровне, естественно. Двуокись углерода препятствует выходу внутренней температуры земли, а ее постоянное присутствие позволяет ее поглощению другими существами выполнять свои циклы питания.
Порядок питания в экосистемах тесно связан с переносом углерода между живыми существами, которые участвуют в этих взаимодействиях. Например, животные обычно получают углерод от первичных производителей и передают его всем, кто находится выше в цепи.
В конце концов углерод возвращается в атмосферу в виде диоксида углерода, где он участвует в каком-то другом органическом процессе.
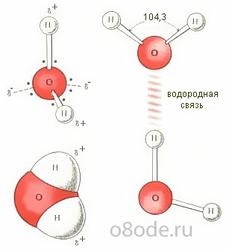
6. Структура молекулы воды.
Молекула воды представляет собой маленький диполь, содержащий положительный и отрицательный заряды на полюсах. Так как масса и заряд ядра кислорода больше, чем у ядер водорода, то электронное облако стягивается в сторону кислородного ядра. При этом ядра водорода «оголяются». Таким образом, электронное облако имеет неоднородную плотность. Около ядер водорода имеется недостаток электронной плотности, а на противоположной стороне молекулы, около ядра кислорода, наблюдается избыток электронной плотности. Именно такая структура и определяет полярность молекулы воды. Если соединить прямыми линиями эпицентры положительных и отрицательных зарядов получится объемная геометрическая фигура ‒ правильный тетраэдр.

Благодаря наличию водородных связей каждая молекула воды образует водородную связь с 4-мя соседними молекулами, образуя ажурный сетчатый каркас в молекуле льда. Однако, в жидком состоянии вода – неупорядоченная жидкость; эти водородные связи ‒ спонтанные, короткоживущие, быстро рвутся и образуются вновь. Всё это приводит к неоднородности в структуре воды.
То, что вода неоднородна по своему составу, было установлено давно. С давних пор известно, что лёд плавает на поверхности воды, то есть плотность кристаллического льда меньше, чем плотность жидкости.
Водородная связь ‒ это взаимодействие атома водорода с более электроотрицательным атомом, имеющее частично донорно-акцепторный, частично электростатический характер. Любая химическая связь характеризуется энергией ее образования.
Необычная структура воды обусловливает ее уникальные физико-химические свойства. Все биохимические процессы в организме протекают в водной среде. Вещества, находящиеся в водном растворе, имеют водную оболочку, которая образуется в результате взаимодействия полярных молекул воды с заряженными группами макромолекул или ионов. Чем больше такая оболочка, тем лучше растворимо вещество.
7. Физико-химические свойства воды в связи с ее ролью в биологических системах.
Физико-химические свойства воды определяют ее биологические функции:
• Вода является прекрасным растворителем.
• Вода выполняет функцию регулятора теплового баланса организма, так как ее теплоемкость значительно превышает теплоемкость любого биологического вещества. Поэтому вода может долго сохранять тепло при изменении температуры окружающей среды и переносить его на расстояние.
• Вода способствует сохранению внутриклеточного давления и формы клеток (тургор).
• В определенных биохимических процессах вода выступает в качестве субстрата.
Содержание воды в организме человека зависит от возраста: чем моложе человек, тем выше содержание воды. У новорожденных вода составляет 75% от массы тела, у детей от 1 года до 10 лет ‒ 60-65%, а у людей старше 50 лет ‒ 50-55%. Внутри клеток содержится 2/3 общего количества воды, внеклеточная вода составляет 1/3. Необходимое содержание воды в организме человека поддерживается за счет поступления ее извне (примерно 2 л в сутки); около 0,3 л в сутки образуется в процессе распада веществ внутри организма. Нарушение водного баланса в клетках организма приводит к тяжелым последствиям вплоть до гибели клеток. Функции клеток зависят от общего количества внутриклеточной и внеклеточной воды, от водного окружения макромолекул и субклеточных структур. Резкое изменение содержания воды в организме приводит к патологии.
|
 Скачать 42 Kb.
Скачать 42 Kb.