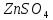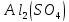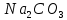отче5(Гидролиз). Ознакомиться с процессом гидролиза солей и его следствиями, научиться составлять уравнения гидролиза
 Скачать 22.77 Kb. Скачать 22.77 Kb.
|
|
Цель работы: ознакомиться с процессом гидролиза солей и его следствиями, научиться составлять уравнения гидролиза. Общие сведения:Гидролизом называют процесс химического взаимодействия солей с водой. Продуктами гидролиза являются малодиссоциированные соединения в растворе, иногда – осадки или газы. Соответственно соли, образованные сильной кислотой и сильным основанием, не гидролизуются. К ним относятся, например, хлориды, нитраты и сульфаты щелочных металлов, стронция и бария. Различают три типа гидролизующихся солей: Гидролиз соли, образованной сильным основанием и слабой кислотой. Гидролизуется анион слабой кислоты: А + Н2О = НА + ОН, в растворе появляются ионы ОН, поэтому среда – щелочная, рН > 7. Например, Na2CO3 образован сильным основанием NaOH и слабой угольной кислотой H2CO3. Диссоциация карбоната натрия описывается уравнением: 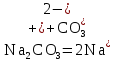 . .С водой взаимодействует карбонат-ион по реакции: 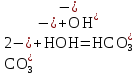 . .Распределяя катионы натрия по образующимся в ходе гидролиза анионам, получим молекулярное уравнение гидролиза: Na2CO3 + H2O = NaHCO3 + NaOH. Гидролиз соли, образованной слабым основанием и сильной кислотой. Гидролизуется катион слабого основания: М+ + Н2О МОН + Н+, в растворе появляются ионы Н+, поэтому среда кислая, рН < 7. Например, FeSO4 образован слабым основанием Fe(OH)2 и сильной кислотой H2SO4. Сульфат железа (II) диссоциирует по реакции: 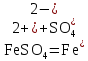 . . С водой реагирует остаток слабого основания – катион Fe2+: Fe2+ + HOH FeOH+ + H+. Так как в ходе гидролиза образуются ионы H+, то среда в растворе FeSO4 будет кислой. Молекулярное уравнение гидролиза: 2FeSO4 + 2H2O = (FeOH)2SO4 + H2SO4. Степень гидролиза солей этих двух групп невелика, не превышает нескольких процентов. Поэтому гидролиз многозарядных ионов протекает не далее первой ступени, то есть ограничивается взаимодействием иона только с одной молекулой воды. Гидролиз соли, образованной двумя слабыми электролитами. Гидролиз протекает как по катиону, так и по аниону: М+ + А + Н2О = МОН + НА. Например, ацетат натрия CH3COONa образован слабым основанием NH4OH и слабой кислотой CH3COOH, соответственно с водой взаимодействует и катион аммония и ацетат-ион: 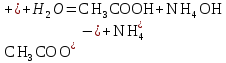 Молекулярная форма реакции: CH3COONH4 + H2O = CH3COOH + NH4OH Образующиеся слабые кислота и основание диссоциируют в разной степени, поэтому среда в растворе зависит от их относительной силы. Если кислота сильнее, то ее константа диссоциации больше и среда слабокислая. Если сильнее основание, то среда слабощелочная. Степень гидролиза соли, образованной слабой кислотой и слабым основанием многократно выше, чем у солей первых двух групп, гидролизующихся только по одному иону. Если продуктами гидролиза являются труднорастворимые соединения или газы, то гидролиз протекает полностью. Пример необратимого, полного гидролиза: Al2S3 + 6H2O = 2Al(OH)3 + 3H2S. Степень гидролиза солей зависит от ряда факторов, определяемых принципом Ле-Шателье. Чем слабее кислота или основание, образующиеся в результате гидролиза, тем выше глубина протекания процесса. С увеличением количества воды, то есть с разбавлением раствора, степень гидролиза возрастает. Поскольку гидролиз всегда протекает с поглощением тепла, является эндотермической реакцией, степень гидролиза повышается при нагревании раствора. Гидролиз солей первой группы может быть подавлен добавлением кислоты, а во второй группе солей – добавлением щелочи. При смешивании растворов солей первой и второй групп происходит взаимное усиление гидролиза. Опыт 1: «Гидролиз солей»
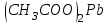 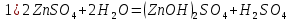 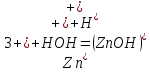 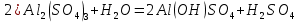 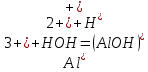 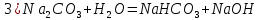 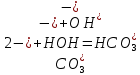 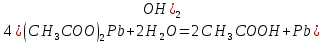 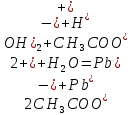 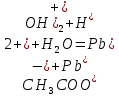 Опыт 3B: «Факторы, влияющие на степень гидролиза солей» 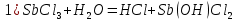 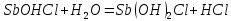 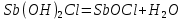 (Трехступенчатый гидролиз хлорида сурьмы до образования осадка SbOCl) 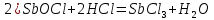 (Наблюдаем растворение осадка хлорида оксосурьмы) Опыт 4: «Растворение металлов в продуктах гидролиза солей» 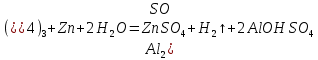 Наблюдается неполное растворение цинка и выделение водорода Опыт 5 (А, Б): «Взаимное усиление гидролиза при взаимодействии растворов двух солей» 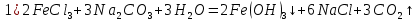 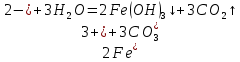 (выпадение бурого осадка и выделение бесцветного газа)  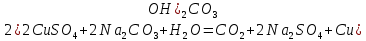 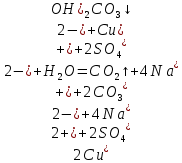 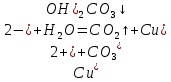 (выпадение голубого осадка) (выпадение голубого осадка)Вывод: В процессе работы мы на практике ознакомились с процессом гидролиза и его следствиями и научились составлять уравнения гидролиза. |