Полиэфиры. Эпоксидные полимеры. Получение, строение, свойства и важнейшие линии применения.. Полиэфиры. Полиэфиры. Эпоксидные полимеры. Получение, строение, свойства и важнейшие линии применения
 Скачать 238.5 Kb. Скачать 238.5 Kb.
|
|
Министерство образования и науки Российской Федерации Государственное образовательное учреждение высшего профессионального образования «Хакасский государственный университет им. Н.Ф. Катанова» Институт естественных наук и математики Специальность «050101» - Химия с дополнительной специальностью «050102» - Биология Полиэфиры. Эпоксидные полимеры. Получение, строение, свойства и важнейшие линии применения. Выполнил: Студент 5 курса группы Х- 51 Иншакова Н.Н. Проверила: Мухина Е.С. Полиэфиры (полиэстеры) — высокомолекулярные соединения, получаемые поликонденсацией многоосновных кислот или их альдегидов с многоатомными спиртами. Известны: природные (янтарь, пленки и лаки, образующиеся при высыхании льняного, тунгового и других растительных масел, молекулы полиэфиров фосфорной кислоты входящие в состав ДНК, ответственных за передачу наследственной информации и синтез белков и др.) искусственные (глифталевые смолы, полиэтилентерефталат, полиэфирмалеинаты и полиэфиракрилаты и др.) Полиэфирное волокно — синтетическое волокно, формируемое из расплава полиэтилентерефталата или его производных. «+» - незначительная сминаемость, отличная свето- и атмосферостойкость, высокая прочность, хорошая стойкость к истиранию и к органическим растворителям; «-» - трудность крашения, сильная электризуемость, жесткость (устраняется химическим модифицированием). Полиэфиры могут быть как пластиками, так и волокнами. Простые полиэфиры. HO—[—R—O—] n—H, где R — углеводородный радикал различного строения, содержащий не менее двух атомов углерода, получают полимеризацией циклических окисей (например, пропилена окиси, этилена окиси) или поликонденсацией гликолей. Сложные полиэфиры линейной структуры. Н-[-ОАО-СО-А' -СО-] n-OH, где А — углеводородный радикал, А' — остаток органической или неорганической кислоты, получают поликонденсацией либо гликолей с двухосновными кислотами или их ангидридами, либо оксикислот. При использовании многоатомных спиртов получают разветвленные (например, алкидные смолы) или сшитые полиэфиры. Применяется: в производстве различных тканей, искусственного меха, канатов, для армирования шин. Основные торговые названия: лавсан, терилен, дакрон, тетерон, элана, тергаль, тесил. Классификация волокон от вида: штапельные (волокна конечной штапельной длины, как правило не более 40—45 мм (волокна хлопковой штапельной диаграммы), используемые в текстильной промышленности для выработки пряжи; филаментные (комплексные нити, непрерывные волокна) — представляют собой нити, состоящие из отдельных бесконечных полиэфирых нитей малой линейной плотности (десятые доли текса и ниже): характеризуются линейной плотностью (как правило — тексом — весом в граммах одного километра нити), филаментарностью — количеством элементарных нитей, из которых оно состоит, титром — средней линейной плотностью одного филамента; текстурированные — как правило, филаментные волокна, подвергнутые специальному извитию филаментов, для придания объема или соединения (компактирования) филаментов вместе и т. п.; мононити; объемные нити (BCF). В настоящее время в мировой текстильной промышленности полиэфирные волокна занимают доминирующую позицию среди волокон искусственного происхождения. Как правило, формование полиэфирных волокон происходит методом экструзии (продавливания через фильтры) из расплава полимера (полиэтилентерефталат) и воздушного охлаждения. Затем волокна подвергаются вытяжке для достижения необходимой штапельной линейной плотности и прочности. Для получения штапельных (дискретных) волокон осуществляется штапелирование волокнистого жгута путем резки или разрыва. Свойства полиэфиров: Очень разнообразны и зависят от химического состава, структуры, молекулярной массы и наличия функциональных групп (—ОН и —СООН). Как правило, простые полиэфиры эластичнее сложных. Полиэфиры могут вступать в химическую реакцию по концевым функциональным группам с увеличением молекулярной массы; ненасыщенные полиэфиры способны «сшиваться» с образованием трёхмерных структур. Сложные полиэфиры гидролизуются под действием кислот и щелочей, простые полиэфиры значительно устойчивее к гидролизу. Применение полиэфиры определяется их свойствами. Ненасыщенные полиэфиры невысокой молекулярной массы (олигоэфиры) применяют в качестве компонентов клеев, лакокрасочных материалов, для пропитки и т.п. Полиэфиры высокой молекулярной массы используют в производстве пластмасс (например, Поликарбонаты), плёнок и полиэфирных волокон (См. Полиэфирные волокна). Методы синтеза полиэфиров сложных. 1) Полиэтерификация (поликонденсация, приводящая к образованию в макромолекулах сложноэфирных связей): а) равновесная (полиэфиры сложные получают взаимодействием гидроксикарбоновых, дикарбоновых кислот или их циклических ангидридов с гликолями, а также сложных эфиров дикарбоновых кислот или самих кислот соотв. с диолами или их ацилпроизводными), в промышленности процесс проводят в расплаве в присутствии катализатора, на заключительной стадии - понижении давления и температуры 250-300 °С; б) неравновесная (взаимодействие дигалогенангидридов и др. активных производных дикарбоновых кислот с диолами), реакцию проводят при 150-250 °С (высокотемпературная поликонденсация в растворе) или при 20-100 °С в присутствии третичных аминов, щелочей или карбонатов щелочных металлов (акцепторно - каталитическая поликонденсация в растворе, межфазная, эмульсионная). 2) Неравновесная поликонденсация солей дикарбоновых кислот с алкиленгалогенидами. 3) Миграционнаяполимеризация кетенов с диолами: 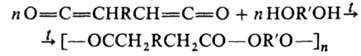 4) Полимеризация и сополимеризация циклических соединений, например 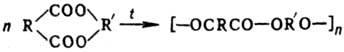 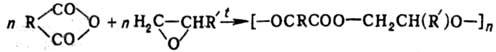 Из полиэфиров сложных наибольшее применение находят полиэтилентерефталат, полибутилентерефталат, алкидные смолы, поликарбонаты, полиарилаты, полиалкиленгликолъмалеинаты и полиалкиленгликолъфумараты, олигоэфиракрилаты (см. Олигомеры акриловые). Из полиэфиров сложных получают пленки, волокна, лакокрасочные материалы, орг. стекла, композиционные материалы. Низкомолекулярные сложные полиэфиры используют в производстве полиэфир - уретанов (см. Полиуретаны) и как пластификаторы. Для получения высокопрочных изделий используют термотропные жидкокристаллические полиэфиры сложные. Полиэтилентерефталат (ПЭТФ, ПЭТ). 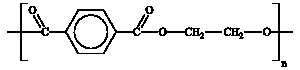 Применение: термопластичные материалы, волокна Мономеры: этиленгликоль и диметилтерефталат Полимеризация: переэтерификация (transesterification) Морфология: высокая степень кристалличности Температура плавления: 265oC Температура стеклования: 74oC (то есть температура, при которой ПЭТ становится мягким) 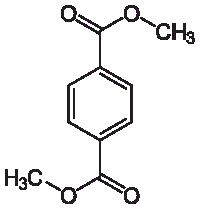 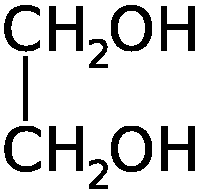 Этиленгликоль Диметилтерефталат 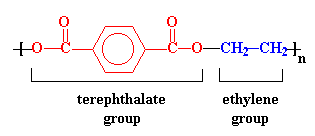 Термопластик, наиболее распространённый представитель класса полиэфиров, известен под разными фирменными названиями. Продукт поликонденсации этиленгликоля с терефталевой кислотой (или её диметиловым эфиром). Эфирные группы в цепочке полиэфира полярны, причем входящий в состав карбонильной группы атом кислорода несет на себе частичный отрицательный заряд, а связанный с ним карбонильный атом углерода обладает частичным положительным зарядом. Положительные и отрицательные заряды различных эфирных групп притягиваются друг к другу. Это позволяет эфирным группам соседних цепочек выстраиваться, образуя при этом кристаллическую структуру. Вот почему полиэфиры могут образовывать прочные волокна. Физические свойства: Твёрдое, бесцветное, прозрачное вещество в аморфном состоянии и белое, непрозрачное в кристаллическом состоянии. Переходит в прозрачное состояние при нагреве до температуры стеклования и остаётся в нём при резком охлаждении и быстром проходе через т. н. «зону кристаллизации». Одним из важных параметров ПЭТ является характеристическая вязкость определяемая длиной молекулы полимера. С увеличением присущей вязкости скорость кристаллизации снижается. Прочен, износостоек, хороший диэлектрик. Применение: В России полиэтилентерефталат используют главным образом для изготовления заготовок (преформ) различного вида, из которых затем изготавливаются (выдуваются после нагрева) пластиковые контейнеры различного вида и назначения (в первую очередь, пластиковые бутылки). В меньшей степени применяется для переработки в волокна, плёнки, а также литьём в различные изделия. В мире ситуация обратная: большая часть ПЭТФ идет на производство нитей и волокон. Многообразно применение заготовок и ПЭТФ в машиностроении, химической промышленности, пищевом оборудовании, транспортных и конвейерных технологиях, медицинской промышленности, приборостроении и бытовой технике. Для обеспечения лучших механических, физических, электрических свойств ПЭТФ наполняется различными добавками (стекловолокно, дисульфид молибдена, фторопласт). ПЭТФ относится к группе алифатически - ароматических полиэфиров, которые используются для производства волокон, пищевых плёнок и пластиков, представляющих одно из важнейших направлений в полимерной индустрии и смежных отраслях. самое массовое из всех видов химических волокон для бытовых целей (одежда) и техники; ёмкости для жидких продуктов питания, особенно ёмкости (бутылки) для различных напитков; основной материал для армирования автомобильных шин, транспортерных лент, шлангов высоко давления и других резинотехнических изделий; чрезвычайно важный современный материал для носителей информации — основа всех современных фото-, кино- и рентгеновских плёнок; основа носителей информации в компьютерной технике, основа магнитных лент для аудио-, видео- и другой записывающей техники; пластик для ответственных видов изделий в различных отраслях машиностроения, электро- и радиотехнике. В частности данный материал широко используется при производстве инфракрасной нагревательной пленки для электрических теплых полов; листовой материал, прозрачный для солнечных лучей (в том числе и УФ) и устойчивый к воздействиям окружающей среды, используемый в сельском хозяйстве и строительстве. «-» - Существенными недостатками ПЭТ-тары являются её относительно низкие барьерные свойства. Она пропускает в бутылку ультрафиолетовые лучи и кислород, а наружу — углекислоту, что ухудшает качество и сокращает срок хранения продукта. Это связано с тем, что высокомолекулярная структура ПЭТ не является препятствием для газов, имеющих небольшие размеры молекул относительно цепочек полимера. Названия: В СССР полиэтилентерефталат и получаемое из него волокно называли лавсаном, в честь места разработки — ЛАборатории Высокомолекулярных Соединений Академии Наук. Аналогичные волоконные материалы, изготавливаемые в других странах, получили другие названия: терилен (Великобритания), дакрон (США), тергал (Франция), тревира (ФРГ), теторон (Япония), полиэстер, мелинекс, милар (майлар), Tecapet («Текапэт») и Tecadur («Текадур») (Германия) и т. д. Пластики на основе полиэтилентерефталата называются ПЭТФ (в российской традиции) либо PET/ПЭТ (в англоязычных странах). В настоящее время в русском языке употребляются оба сокращения, однако когда речь идет о полимере, чаще используется название ПЭТФ, а когда об изделиях из него — ПЭТ. Получение: Пищевой ПЭТФ получают сополимеризацией терефталевой кислоты, этиленгликоля и небольшого количества по объёму изофталевой кислоты. Процесс его получения состоит из двух стадий: этерификации терефталевой и изофталевой кислот этиленгликолем поликонденсации в присутствии катализатора — триоксида сурьмы. Также существует технология получения полиэтилентерефталата из диметилтерефталата. В настоящее время более 90% производимого ПЭТФ изготавливается на основе очищенной терефталевой кислоты. полиэтиленнафталат (ПЭН). 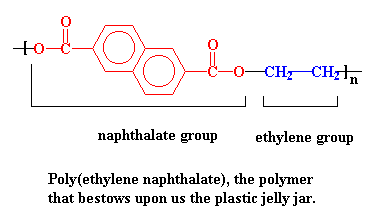 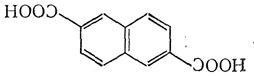 Нафталиндикарбоновая кислота ПЭН обладает более высокой температурой стеклования, чем ПЭТ. Получение: Н 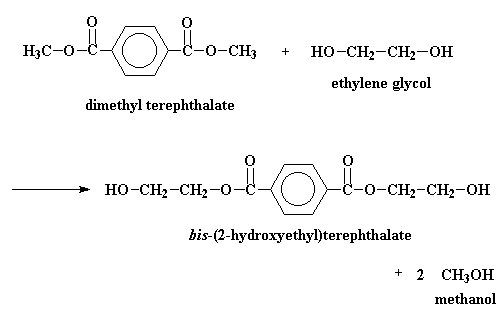 а заводах по изготовлению полиэфира начинают с соединения диметилтерефталата с этиленгликолем посредством реакции называемой переэтерификация. В результате образуется ди-(2-гидроксиэтил)терефталат и метанол. Нагреем взаимодействующие вещества до 210 oC - метанол вскипит и испарится. а заводах по изготовлению полиэфира начинают с соединения диметилтерефталата с этиленгликолем посредством реакции называемой переэтерификация. В результате образуется ди-(2-гидроксиэтил)терефталат и метанол. Нагреем взаимодействующие вещества до 210 oC - метанол вскипит и испарится.Потом ди-(2-гидроксиэтил)терефталат нагревается до 270 oC, и вступает в реакцию с образованием полиэтилентерефталата и этиленгликоля в качестве побочного продукта. 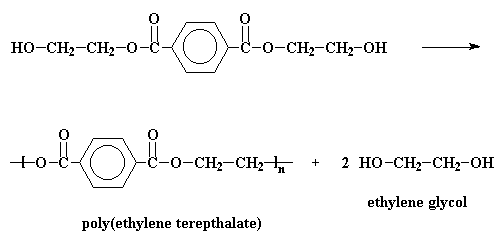 Эти два вещества - этиленгликоль и диметилтерефталат совместить, то происходит переэтерификация. 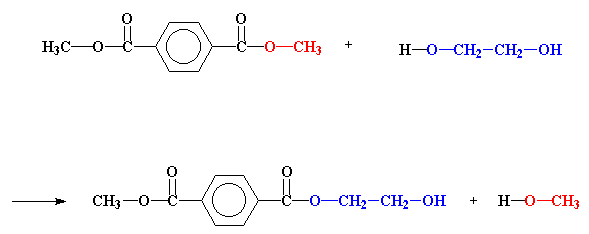 Атом углерода, входящий в состав карбонильной группы отдает электроны атому кислорода, который более электроотрицателен. В результате этого атом углерода приобретет частичный положительный заряд. Он может быть весьма легко атакован парой электронов у атома кислорода в составе молекулы этиленгликоля. 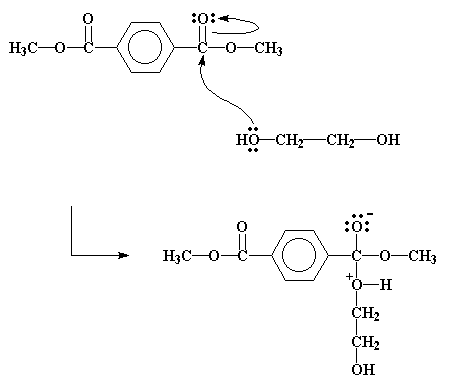 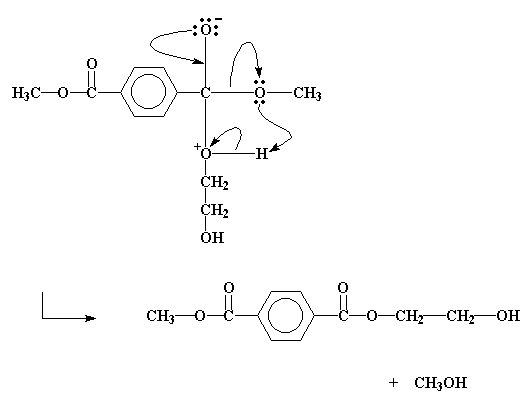 Точно такая же реакция произойдет и на другом конце молекулы терефталата, в результате чего мы получим ди-(2-гидроксиэтил)терефталат. 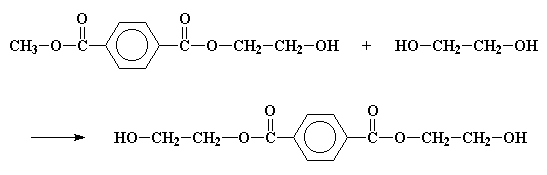 Эта молекула является одновременно и спиртом, и сложным эфиром. Поэтому она может осуществить реакцию переэтерификации сама с собой, как показано на рисунке внизу. 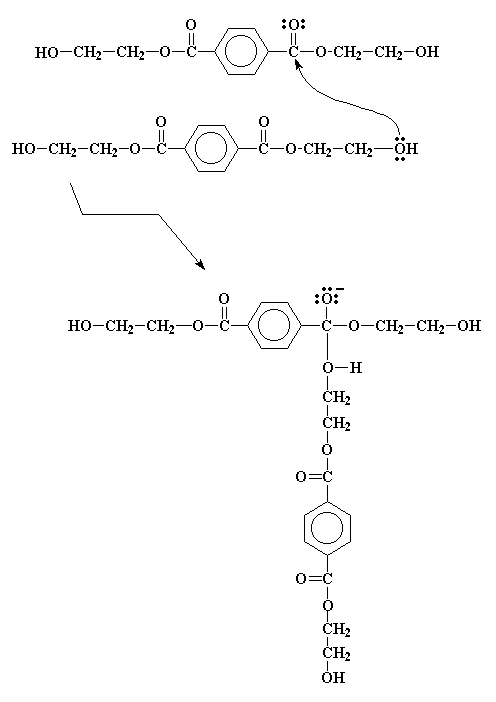 Она образует промежуточный продукт, похожий на тот, что мы видели раньше, в нем происходит похожая перестройка электронов, в результате чего мы получаем продукт: 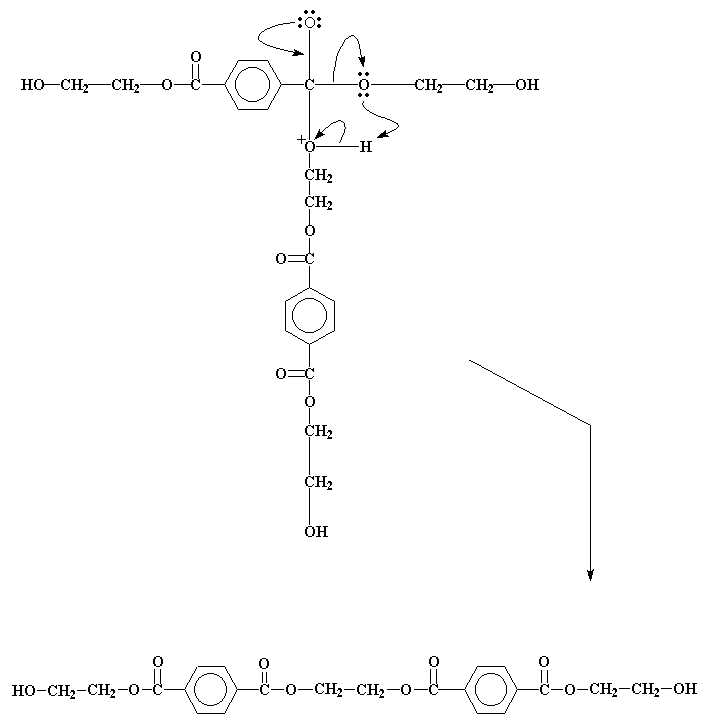 Этот продукт может снова вступить в реакцию, точно так же, как раньше это сделал ди-(2-гидроксиэтил)терефталат. По мере того, как это происходит, молекулы становятся все больше и больше. 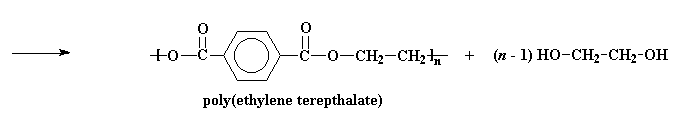 Эпоксидные полимеры Эпоксидные полимеры получили свое название по эпоксидным группам входящим в молекулу полимера. Простейшее эпоксидное соединение — окись этилена — обладает большой реакционной способностью. Полифункциональные эпоксидные соединения стали известны сравнительно недавно. Промышленное производство эпоксидных полимеров стало возможным лишь после освоения метода синтеза эпихлоргидрипа, являющегося наиболее простым эпоксидным соединением с дополнительной реакциошюспособной группой в молекуле. Отличная адгезия ко многим материалам, хорошие диэлектрические свойства, небольшая усадка при отверждении, высокая химическая стойкость способствовали широкому внедрению эпоксидных полимеров в различные области науки и техники. Сырье Эпоксидные полимеры, содержащие две и более эпоксидные группы, получают как отверждением олигомеров, образующихся при взаимодействии эпихлоргидрина с веществами, имеющими две и более групп с подвижными атомами водорода (полнепиртами, полиаминами, фенолами), так и обработкой надкислотами (надуксусной, надбензойной) низкомолекулярных веществ, полимеров и сополимеров бутадиена с двойными связями, В основном эпоксидные олигомеры, выпускаемые промышленностью, получают в результате взаимодействия эпихлоргидрина и 4,4-диоксидифенилпропана. Синтез эпихлоргидрина из пропилена проводят путем его хлорирования в проточном реакторе при Бремени контакта в несколько секунд пли при 500°С и давлении 18 МП а до аллилхлорида. Затем при взаимодействии с хлороватистой кислотой получают дихлоргидрил глицерина, который под действием щелочи превращается в эпихлоргидрин. Эпихлоргидрин — бесцветная прозрачная жидкость, нерастворимая в поде, по растворимая в бензоле, толуоле, ацетоне, спирте и т. д. Температура кипения +118°С; плотность при 20°С — И 75—1185 кг/м3, показатель преломления n.20D= 1,4382. Технический эпихлоргидрин должен соответствовать требованиям и нормам, указанным в ГОСТ 12844—74. Прямым эпоксидированием дициклопеитадиена надуксусной кислотой получают диоксид дициклопентадиена ДДЦПД, а также циклоалифатические эпоксидные олигомеры. Путем прямого эпоксидирования получают также полиэпоксидные олигомеры — эпоксидированный дивинил, эпок-сидированный дивниилстирол и др. Образование эпоксидной группы из хлоргидриновой представляет эндотермический процесс, требующий 117,7 кДж/моль. Так: как некоторое количество тепла возникает в результате растворения и нейтрализации хлористого водорода, то в итоге реакция образования эпоксидных полимеров мало экзотермича — она сопровождается выделением только 17,5 кДж/моль тепла. Эпоксидные олигомеры в неотвержденном состоянии представляют длинные полиэфирные цепи, в которых свободные гидроксильные группы находятся на значительном расстоянии друг от друга, а на концах имеются эпоксидные группы. Молекулярная масса неотвержденных эпоксидных олигомеров составляет 370—380. В настоящее время нашей промышленностью производятся низкомолекулярные (молекулярная масса 370—600), среднемолекулярные (600—1500) и высокомолекулярные (1500—3800) диановые эпоксидные олигомеры, алифатические эпоксидные олигомеры с низкой вязкостью, азот- и галогеносодержащие, эпоксиноволочные и другие олигомеры. Получение диановых эпоксидных олигомеров Низкомолекулярные диановые эпоксидные олигомеры изготовляют из эпихлоргидрина (2 моля) и диоксидифенилпропана (1 моль) в присутствии едкого натра в виде 15%-ного раствора (2 моля). Полученный олигомер отмывают от хлористого натрия и продуктов побочных реакций смесью толуола (200 мае. ч.) и воды (325 мае. ч.) при 60—70°С. После расслоения нижний прозрачный водосолевой слой сливают в систему очистки сточных вод. Промежуточный слой представляет собой водотолуольную эмульсию олигомера и побочных продуктов. Для выделения олигомера промежуточный слой сливают в отстойно-промывную колонну. Олигомер экстрагируют толуолом, который подают в нижнюю часть колонны. В верхнюю часть колонны заливают воду. После отстаивания то-луольный раствор олигомера из колонны пропускают через фильтры в приемник, а затем на вторую промывку в реактор, где находится основное количество толуольного раствора олигомера. При наличии хлора в толуольном растворе олигомера производят дегидрохлорирование (омыление). Для этого олигомер обрабатывают водным раствором щелочи при перемешивании в течение 1 ч при 80—90°С. После отстаивания водно-солевой слой сливают в. систему очистки сточных вод, а промежуточный слой — в отстойно-промывную колонку. Литература: Бениг Г. В. Ненасыщенные полиэфиры. Строение и свойства, пер с англ., М., 1968; Жидкокристаллический порядок в полимерах, пер. с англ., М., 1981; Энтелис С. Г , Евреинов В В , Кузаев А И., Реакционноспособные олигомеры, М., 1985 http://www.xumuk.ru/encyklopedia/2/3621.html http://www.xumuk.ru/bse/2177.html http://dic.academic.ru/dic.nsf/enc_chemistry/3676/ПОЛИЭФИРЫ Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988. http://dic.academic.ru/dic.nsf/bse/122170/Полиэфиры Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978. http://ru.wikipedia.org/wiki/Полиэфир http://www.pslc.ws/russian/petg.htm http://ru.wikipedia.org/wiki/Полиэтилентерефталат http://www.bibliotekar.ru/spravochnik-52/18.htm http://www.polimerportal.ru/index.php/2009/09/epoksidnye-polimery-2/ |
