Биочип Шафиев. Пористый кремний как материал биочипа
 Скачать 6.11 Mb. Скачать 6.11 Mb.
|
|
Государственное бюджетное образовательное учреждение средняя общеобразовательная школа № 2 г. Сызрани Тема «Пористый кремний как материал биочипа» (Научная работа по (физике)) Выполнил: Шафиев, Рамиль, 11 класс, ГБОУ СОШ № 2 Проверил: Гундерина, Светлана, Юрьевна, учитель физики, ГБОУ СОШ № 2 г. Сызрань 2018 г Содержание Введение. …………………………………………………………………………3 1.Монокристаллический кремний ………………………………………………4 1.2. Использование монокристаллов кремния………………………………4 1.2.1 Формирование слоев пористого кремния……………………………..6 1.3. Виды, свойства и функции биочипов…………………………………….8 1.4 Анализ биочипов…………………………………………………………...9 2.Основная часть. 2.1 Биологический родственник электронных чипов. …………………….10 2.2. Будущее российских биочипов …………………………………….......11 2.3. Геношарики ……………………………………………………………...13 2.4 Нанороботы или наноботы …………………………………………………14 2.5 Эксперимент……………………………………………………………….17 Заключение……………………………………………………………………....22Список использованной литературы…………………………………………...23 Введение Сегодня для исследования ДНК, белков; выявления онкологических заболеваний, туберкулёза и других болезней, которые можно выявить на нано уровне, используют биочипы. По точности анализа они опередили старые методы, но кроме этого так же выигрывают в затрате времени и стоимости исследования. Биочипы имеют большой потенциал, поэтому меня заинтересовала эта тема. Пористый кремний является перспективным мате- риалом микро-, нано- и оптоэлектроники. Его свойства на протяжении последнего десятилетия активно исследуются более чем в 40 странах мира, а объем научных публикаций достигает 500 статей в год. На крупных международных конференциях обсуждаются и уникальные свойства этого материала, и возможности его применения в приборах различного назначения. В работе обобщены наиболее важные сведения по технологии изготовления слоев пористого кремния, изучению их электрофизических характеристик, процессов фото- и электролюминесценции, а также по их возможному применению. Целью работы является получение ответов на следующие принципиальные вопросы: каков механизм формирования пористого кремния, и что обеспечивает его наноразмерную структуру; как обеспечить переход от "принципиальной" к реальной совместимости технологии пористого кремния со стандартной кремниевой технологией; Для достижения данной цели необходимо решить следующие задачи: 1. Провести анализ известных закономерностей физических и химических процессов. Исходя из результатов анализа, провести экспериментальные и теоретические исследования кинетики и других особенностей процесса формирования этого материала. 2. Установить физико-химические закономерности процесса формирования наноразмерной структуры 1. Монокристаллический кремний 1.2. Использование монокристаллов кремния Широкое использование монокристаллов кремния в устройствах электроники стало настолько привычным, что мало задается вопросом, почему именно кремнию из всех полупроводников отдается предпочтение при создании электронных приборов. Ведущее положение кремния связано с широким набором положительных свойств, многих из которых нет у других полупроводниковых материалов. Кремний как химический элемент широко распространен в природе, и его содержание в земной коре составляет 29,5%. Он технологичен, инертен в обычных условиях, выдерживает высокие температуры, сопровождающие процесс изготовления приборов и интегральных схем. Для создания диэлектрических слоев нет необходимости специально искать диэлектрические материалы – собственный окисел SiO2 , формируемый на кремнии при высоких температурах в окислительной среде, прекрасно выполняет изолирующие и маскирующие функции. В кристаллической решетке атомы кремния занимают только 25% объема, в результате чего материал имеет малую плотность (2,32 г/см3, для Ge 5,35 г/см3) и допускает сильное легирование элементами III и V групп. Каждый введенный в кристалл кремния атом III или V группы добавляет один носитель заряда с положительным знаком (дырку) или один электрон соответственно. Концентрация носителей заряда в результате этого может изменяться в широких пределах – от 1010 до 1021 см−3. Высокие значения коэффициентов диффузии легирующих элементов в кремнии позволяют формировать локальные области микронных и субмикронных размеров с дырочным (p-Si) или электронным (n-Si) типом проводимости, совокупность которых и составляет основу любой интегральной схемы или полупроводникового прибора. Производство кремниевых монокристаллов превышает 3000 тонн в год. Однако монокристаллический кремний имеет и недостатки. Один из них связан с относительно невысокой подвижностью носителей заряда (для электронов 1500 см2/(В ⋅ с), дырок 600 см2/(В ⋅ с)), что ограничивает быстродействие приборов. Для этих целей применяют другой полупроводник – арсенид галлия GaAs, у которого подвижность электронов при комнатной темпера- туре 8500 см2/(В ⋅ с), а при температуре кипения жидкого азота (77 К) 250 000 см2/(В ⋅ с). Результатом этого стало появление нового технологического направления, получившего название арсенид-галлиевой микроэлектроники. Другой недостаток монокристаллического кремния заключается в том, что его нельзя использовать для создания светоизлучающих приборов. Светоизлучающие структуры широкого спектрального диапазона изготавливают на основе других полупроводников (GaAs, GaP, GaN, ZnS, ZnSe и др.), однако решение этой задачи в перспективе все же возможно в рамках кремниевой технологии. В настоящее время существуют два подхода к этой проблеме. Один из них состоит в легировании кремния редкоземельными элементами (Er, Eu, Gd), в результате чего такой модифицированный кремний обладает излучающими свойствами в инфракрасном диапазоне. Другой подход заключается в формировании на поверхности или в объеме диэлектрических материалов (например, SiO2) кремниевых кристаллов нанометровых размеров (1 нм = 1 ⋅ 10−9 м). Среди таких технологических приемов наиболее доступным и дешевым является создание нанокристаллов посредством вытравливания в монокристаллах кремния мельчайших пустот, в результате чего оставшиеся области кремния могут иметь размеры в несколько нанометров. Монокристаллический кремний, пронизанный сетью пор (пустот), получил название пористого кремния. Такой материал не только обладает светоизлучающими, но и другими уникальными свойствами. Кремний существует в нескольких структурных модификациях. Все эти материалы имеют различные физические свойства, разные области применения, хорошо совместимы и, взаимно дополняя друг друга, обеспечивают широкие возможности кремниевой технологии. 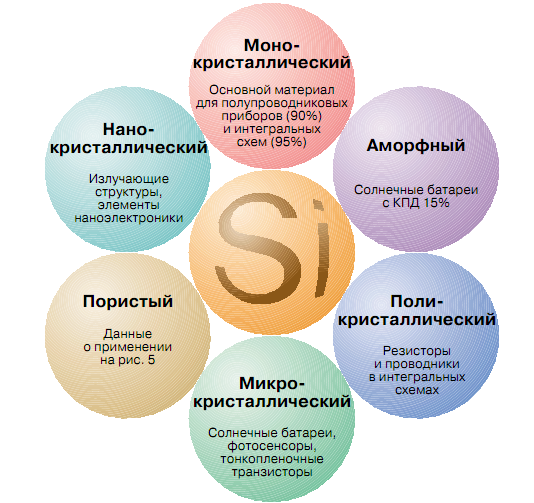 1.2.1 Формирование слоев пористого кремния Пористый кремний получается при анодной электрохимической обработке монокристаллического кремния в растворах на основе плавиковой кислоты HF. Кремниевая пластина в таких экспериментах является анодом, а катодом служит платиновый электрод. Впервые пористый кремний был получен в середине 1950-х годов в ходе исследований процесса электрохимической полировки поверхности кремния в водных растворах HF. Такая операция необходима для придания рабочей поверхности идеально гладкого, зеркального состояния. В ходе травления было обнаружено, что при определенных режимах (низкой плотности анодного тока и высокой концентрации HF в электролите) вместо процесса электрополировки наблюдалось образование окрашенных пленок на поверхности кремния. Было установлено, что цветные слои имеют в своем объеме сеть мельчайших пор. Формирование пор начинается на поверхности пластины, с течением времени анодной обработки концы пор все дальше продвигаются в глубь кристалла. В результате этого толщина пленок пористого кремния в зависимости от времени травления может изменяться от нескольких микрон(1 мкм = 10−6 м) до сотен микрон. Пористый кремний в зависимости от условий травления обладает широким интервалом величин удельного сопротивления (10−2–1011 Ом ⋅ см), диэлектрической проницаемости (1,75–12) и показателя преломления (1,2–3,5). Это означает, что пористый кремний может быть использован как в качестве полупроводниковых, так и диэлектрических слоев в приборах и интегральных схемах. Оказалось, что в рамках одного процесса травления варьированием режимов (плотностью тока анодирования, освещенностью) можно получать многослойные структуры, когда каждый слой обладает заданной пористостью и геометрией пор. Такая технология содержит в себе большие потенциальные возможности для разработки различных устройств. Большие перспективы пористый кремний имеет для создания датчиков влажности, газовых, химических и биологических сенсоров. Принцип действия таких датчиков основан на влиянии внешних молекул на электронное состояние поверхности. В случае пористого кремния за счет высокой удельной поверхности это влияние становится более эффективным и сенсоры обладают высокой чувствительностью. Обычно такие датчики фиксируют изменение емкостных, проводящих, люминесцентных свойств пористого кремния при наличии в контролируемой среде заданных молекул и химических соединений. Интересным представляется применение пористого кремния в качестве рабочего элемента биохимических и биологических сенсоров. Это стало особенно актуальным после того, как было показано, что пористый кремний является биосовместимым материалом. Биоматериалы по своим свойствам подразделяются на биоинертные, биоактивные и биорезорбируемые. Оказалось, что в зависимости от величины пористости пористый кремний может быть отнесен к любому из этих классов, что открывает большие перспективы в создании биомедицинских приборов. Эти работы проводились под руководством академика Андрея Дарьевича Мирзабекова (1937-2003), в то время он возглавлял Институт молекулярной биологии им. В.А. Энгельгардта РАН (ИМБ РАН) и заведовал лабораторией биочипов в этом институте. Во времена реализации проекта «Геном человека» А.Д. Мирзабеков в течение нескольких лет был вицепрезидентом Международной организации по изучению генома человека (HUGO). В середине 90-х годов, когда финансирование отечественной науки практически прекратилось, его пригласили работать в Argonne National Laboratory (Аргоннская национальная лаборатория, Чикаго, США). Он согласился работать только при условии создания совместной исследовательской группы, включающей американских ученых и российских специалистов из ИМБ. В течение 5-6 лет совместных исследований, которые контролировал Департамент энергетики США, в свое время курировавший разработку атомной бомбы, и которые обошлись Правительству США в несколько миллионов долларов, были разработаны биочипы, базовый пакет патентов на которые принадлежал России. 1.3. Виды, свойства и функции биочипов. Выпускаемые многочисленными фирмами биочипы отличаются друг от друга по методике изготовления, виду подложки и зонда, методу регистрации результата взаимодействия реагента с исследуемым образцом. Для считывания результатов реакции используются флуоресцентные сигнализаторы, лазеры и оптические сканеры. В настоящее время производство биочипов полностью автоматизировано, используются роботы, применяемые в микроэлектронике для создания микросхем. ДНК чипы. Используются для идентификации генов и их мутаций, связанных с различными заболеваниями; наблюдения за активностью генов; диагностики инфекционных заболеваний и определения наиболее эффективного метода антибиотикотерапии; скрининга микроорганизмов. Белковые чипы. Используются для обнаружения белковых маркеров, характерных для различных заболеваний и разных стадий их развития; оценки потенциальной эффективности и токсичности препаратов в доклинических испытаниях; измерения различи в синтезе белков различными типами клеток и клетками, находящимися на разных стадиях развития, а также здоровыми и патологически измененными клетками; изучения взаимосвязи между структурой и функциями белков; оценки различий в экспрессии белков с целью выявления мишеней для новых лекарственных препаратов; изучения взаимодействий между белками и другими молекулами. Клеточные чипы. Позволяют избежать проблемы нестабильности белков в белковых чипах и проводить более точный анализ взаимодействий белков внутри клетки. Тканевые чипы. Позволяют проводить анализ тысяч образцов тканей на одном предметном стекле. Используются для определения содержания белков в здоровых и патологически измененных тканях и оценки потенциальных мишеней для лекарственных препаратов. 1.4 Анализ биочипов Регистрация происходящих на биочипах процессов осуществляется с помощью флюоресцентных, а также в некоторых случаях хемилюминис-центных и масспектрометрических методов. Для количественного флюоресцентного анализа нами были разработаны совместно с РНЦ "Государственный оптический институт им. С.И. Вавилова" флюоресцентные широкопольные высоко-апертурные микроскопы, снабженные ПЗС-камерой и компьютером. Прибор позволяет проводить в реакционной камере количественный анализ в реальном времени сразу всех элементов биочипа в автоматическом режиме, одновременно при четырех длинах волн, при заданной или меняющейся температуре. Более 20 таких достаточно дорогих исследовательских анализаторов биочипов поставлены в лаборатории России и США. Для клиник нами разработан более простой и дешевый лазерный анализатор. Он позволяет проводить количественную регистрацию флюоресценции одновременно со всего биочипа с помощью более простой ПЗС-камеры и обрабатывать результаты на прилагаемом портативном компьютере с помощью специально созданных программ. Хемилюминисцентные методы, хотя и уступают по чувствительности люминесцентным, позволяют значительно упростить и удешевить регистрирующую аппаратуру. Кроме того, разработан специальный метод прямого анализа соединений непосредственно в гелевых элементах с помощью MALDI-TOF масс-спектрометрии. Этот важный в протеомике метод позволяет проводить дополнительную идентификацию взаимодействующих с биочипами соединений по их массе. 2.1 Биологический родственник электронных чипов Прообразом современных "живых чипов" послужил саузерн-блот, изготовленный в 1975 году Эдом Саузерном. Он использовал меченую нуклеиновую кислоту для определения специфической последовательности среди фрагментов ДНК, зафиксированных на твердой подложке. Биочип представляет из себя матрицу - крохотную пластинку со стороной 5-10 миллиметров, на которую можно нанести до нескольких тысяч различных микротестов. Профессионалы называют этот носитель "платформой". Чаще всего используют стеклянные или пластиковые платформы, на которые наносятся биологические макромолекулы (ДНК, белки, ферменты), способные избирательно связывать вещества, содержащиеся в анализируемом растворе. В зависимости от того, какие макромолекулы используются, выделяют различные виды биочипов, ориентированные на разные цели. Основная доля производимых в настоящее время биочипов приходится на ДНК-чипы (94 процента), то есть матрицы, несущие молекулы ДНК. Оставшиеся 6 процентов составляют белковые чипы. Биологические микрочипы во многом схожи с электронными - и те, и другие собирают и обрабатывают огромное количество информации на малой поверхности. И те, и другие состоят из огромного количества идентичных миниатюрных элементов, размещенных рядом друг с другом, - правда, ячейки биочипа по полупроводниковым меркам просто огромны - 100х100х20 микрометров. При этом действие электронного, компьютерного чипа основано на ответе "да-нет", а биологический чип позволяет выбрать из миллионов или миллиардов возможностей единственно верную. Компьютерный чип производит миллионы математических операций в секунду, но и на биочипе за пару секунд проходят тысячи биохимических реакций. Как работает биочип? Генетический код человека хранится в виде двойной спирали ДНК, образованной двумя полимерными цепями. Каждая из этих цепей представляет собой длинную последовательность, образованную из четырех нуклеотидов: аденина, гуанина, тимина и цитозина. При этом последовательность одной цепи однозначно определяет последовательность другой, поскольку нуклеиновые кислоты, расположенные на одинаковых позициях в разных цепях, являются комплементарными. То есть если на сто тридцатой позиции в одной цепи находится аденин, то на той же позиции во второй цепи должен находится тимин, а если на двадцатой позиции во второй цепи стоит цитозин, то с полной уверенностью можно утверждать, что в первой цепи на двадцатом месте стоит гуанин. Когда две цепи объединяются в спираль, между комплементарными нуклеиновыми основаниями образуются водородные связи, которые и удерживают цепи вместе. Именно на способности комплементарных оснований образовывать химические связи основан принцип действия биологических чипов. В ходе реакции происходит взаимодействие комплементарных цепей ДНК: одна из них (ДНК-проба) с известной последовательностью нуклеотидов зафиксирована на подложке (пластине), а другая одноцепочечная ДНК-мишень (зонд), меченная флуоресцентной меткой, вносится в ДНК-чип. Разработанный в России биочип - это стеклянная пластинка, на которую нанесены десятки едва видимых глазом полусферических гидрогелевых ячеек, диаметром менее 100 микрон каждая и содержащих известные вещества-маркеры. При взаимодействии биочипа с исследуемым образцом, предварительно обработанным светящимся (флуоресцентным) красителем, в соответствующих ячейках происходит химическая реакция, и тогда эти ячейки начинают светиться - тем сильнее, чем интенсивнее процесс. По сути, именно в выявлении и сопоставлении наиболее ярко светящихся ячеек и заключается работа прибора-анализатора биочипов. Таким образом, определяются различные характеристики образца - например, присутствие в организме тех или иных возбудителей инфекций или, скажем, наличие в геноме каких-либо измененных генов. Особенность российских биочипов в том, что их ячейки заполнены гелем трехмерной структуры. Такие гели удерживают большее количество пробы, нежели двумерные, и потому чувствительность отечественных биочипов выше, а, следовательно, ниже требования к регистрирующей аппаратуре. Немаловажно и то, что реакции в объемном геле протекают так же, как и в жидкостях - а значит, как и в живом организме. Это позволяет получить результат, максимально приближенный к реальности. На Западе исследователи пошли по другому пути, и разработали для создания ДНК-чипов процесс фотолитографии, аналогичный процессу производства кремниевых процессоров. Например, Affimetrix (США) создал GeneChip-технологию, основанную на высокоплотных чипах, содержащих ДНК-последовательности, и предназначенную для анализа генетической информации человека. Правда, хотя такие чипы обладают гораздо большей емкостью, стоят они значительно дороже, что пока позволяет использовать их исключительно в крупных исследовательских центрах или в коммерческих клиниках. Другим методом конструирования биочипов является использование "технологии струйного принтера" для нанесения необходимого нуклеотида в строго определенное место матрицы. Он менее дорог, но при этом не позволяет достичь высокой скорости синтеза. 2.2 Будущее российских биочипов Сейчас число размещаемых на российском биочипе ячеек достигает уже нескольких тысяч, а это соответствует тысячам пробирок с тысячами проводимых в них анализов. Такие биочипы представляют собой целые экспресс-лаборатории, которые дают возможность сэкономить массу времени как врачам, так и пациентам. Чаще используются куда более дешевые биочипы с гораздо меньшим числом ячеек. Например, один-единственный простой чип может выявить все известные на сегодняшний день формы возбудителя туберкулеза, а также определить, каким именно антибиотиком нужно лечить конкретную форму. И определяется это не за несколько недель, как традиционным способом, а всего в течение несколько суток. При помощи белковых чипов, несущих молекулы, "чувствительные" к различным низкомолекулярным соединениям, уже в самое ближайшее время можно будет определить наличие широкого спектра лекарственных веществ, гормонов, наркотиков, ядов, пестицидов практически в любом анализируемом материале - будь то кровь, вода, пища или образец почвы. Не составит проблемы и выявление штаммов вирусов иммунодефицита (ВИЧ) и гепатита. Пока же в России основная масса разработок в этой области сосредоточена на создании биочипов для выявления урогенитальных инфекций, поскольку это наиболее востребованная тема. Например, потребность в биочипах только для столицы может составить не менее 1 миллиона штук в год. На Западе и в России сейчас сформировалось два разных направления и два разных стандарта по созданию и применению биочипов. Российские биочипы дешевле, а западные объемнее. При этом в России биочипами занимаются пока преимущественно исследовательские лаборатории, а на Западе - это, в первую очередь, военные исследования и коммерческое производство чипов для диагностики. Остается надеяться, что хотя бы в области биочипостроения Россия не даст себя обогнать, как это случилось с электронными чипами. 2.3 Геношарики Австралийские ученые объявили об изобретении "геношариков" (geneballs), которые могут анализировать генетическую информацию человека и определять его предрасположенность к тем или иным заболеваниям. Аспирант одного из университетов разработал кварцевые шарики диаметром не более одной десятой толщины человеческого волоса. Поверхность шарика испещрена каналами толщиной 10 нанометров, которые как губка могут впитывать флюоресцентную краску. Вся система работает по принципу знакомого всем по магазинам штрих-кода - повеpхность "геношарика" покрыта специфической ДНК, каждый ген которой обладает уникальным цветом. ДНК, находящаяся на "геношарике", настроена на один определенный ген, с которым она и соединяется в образце исследуемой крови. Ничего сенсационного в "геношариках" нет, просто разработано еще одно устройство из достаточно большого уже семейства биочипов. Геношарики могут анализировать генетическую информацию человека и определять его предрасположенность к тем или иным заболеваниям. Повеpхность геношарика покрыта специфической ДНК, каждый ген которой обладает уникальным цветом. ДНК, находящаяся на геношарике, настроена на один определенный ген, с которым она и соединяется в образце исследуемой крови. 2.4 Нанороботы или наноботы Нанороботы и наноботы управляемые устройства, размер которых сопоставим с размерами молекул (в некоторых случаях допускается до микронных размеров),составленные из наноразмерных компонентов и обладающие функциями движения, обработки и передачи информации, а также исполнения программ. Нанороботостроение - мультидисциплинарная область, в которой сосредоточены совместные усилия физиков, химиков, биологов, программистов, инженеров и других специалистов для получения положительных результатов. 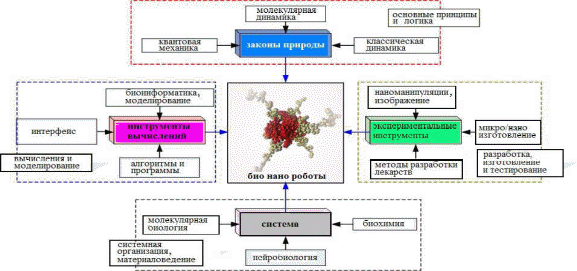 2.5 Жесткие диски будущего Технологический процесс производства головок чтения/записи очень напоминает процесс производства процессоров для ПК. Первоначально кремниевые 6-дюймовые пластины (wafer) подвергаются окислению чистым кислородом для создания тончайшей защитной пленки диоксида кремния. Пластины помещают в камеру, где при высокой температуре и давлении происходит диффузия кислорода в поверхностные слои пластины, приводящая к окислению кремния и образованию поверхностной пленки диоксида кремния. Диоксид кремния является очень хорошим изолятором и выполняет функцию защитной пленки при дальнейшей обработке кристалла кремния. После того как кремниевая подложка покроется защитной пленкой диоксида кремния, необходимо удалить эту пленку с тех мест, которые будут подвергаться дальнейшей обработке. Удаление пленки осуществляется посредством травления, а для того, чтобы защитить от травления остальные области, на поверхность пластины наносится слой так называемого фоторезиста. Термином «фоторезист» обозначают светочувствительные и устойчивые к воздействию агрессивных факторов составы. Основное назначение фоторезистов — создание защитного рельефа нужной конфигурации. После нанесения и сушки слоя фоторезиста наступает этап формирования необходимого защитного рельефа. Рельеф образуется в результате того, что под действием ультрафиолетового излучения, попадающего на определенные участки слоя фоторезиста, последний изменяет свои свойства растворимости (например, освещенные участки перестают растворяться в растворителе, удаляющем участки слоя, которые не подверглись освещению, или, наоборот, растворяются освещенные участки). Для засветки нужных участков слоя фоторезиста используется специальный шаблон-маска. Ультрафиолетовое излучение, проходя сквозь такой шаблон, засвечивает только нужные участки поверхности слоя фоторезиста. После облучения фоторезист подвергается проявлению, в результате которого удаляются ненужные участки слоя. Д  иск состоит из трех слоев: основного, сделанного из пластмассы (поликарбоната); отражающего - из алюминия (иногда даже серебра и золота) и защитного - из прозрачного лака полиакрилата. Основной слой несет полезную информацию, закодированную в выжженных в нем лазером микроскопических углублениях - питах (от англ. pit - ямка). Чередование ямок и ровных участков, располагающихся, как в грампластинке, по спирали от периферии к центру, это и есть цифровая запись чрезвычайно высокой плотности. иск состоит из трех слоев: основного, сделанного из пластмассы (поликарбоната); отражающего - из алюминия (иногда даже серебра и золота) и защитного - из прозрачного лака полиакрилата. Основной слой несет полезную информацию, закодированную в выжженных в нем лазером микроскопических углублениях - питах (от англ. pit - ямка). Чередование ямок и ровных участков, располагающихся, как в грампластинке, по спирали от периферии к центру, это и есть цифровая запись чрезвычайно высокой плотности. Первые CD-диски и записывались подобно грампластинкам: один раз и навсегда. Они называются CD-R (Recordable). Однако очень скоро появились диски для многократной перезаписи - CD-RW (ReWritable). Технология изготовления последних несколько иная. Информация записывается не на слой пластмассы, а на пленку из специального металлического сплава, меняющего свои свойства под воздействием лазерного нагрева и образующего чередование темных и светлых участков. Такие диски можно перезаписывать до 1000 раз без потери качества записи! CD несли 700 мегабайт информации, и на фоне объемов памяти тогдашних персональных компьютеров это выглядело потрясающе. Понятно, что для цифрового способа записи нет разницы в том, что именно записывать - компьютерную программу, музыку или видеоряд. Пятидюймовая пластинка вмещала головоломные компьютерные игры, библиотеки из 10 тысяч наименований книг! А вот записать кинофильм на CD не получалось - места маловато. В 1995 году усилия по созданию следующего поколения компакт-дисков объединили десять лидеров компьютерной индустрии: "Хитачи", "Мацушиба", "Мицубиси", "Тошиба", "Сони", "Томсон", "ДжиВиСи", "Филипс", "Тайм Уорнер" и "Пайонир". Результатом стало появление нового диска - DVD. Интересно, что вначале эта аббревиатура расшифровывалась как Digital Video Disc, то есть цифровой видеодиск. Прошел год, пока создатели осознали возможности своего творения, явно не ограничивающиеся сферой киноиндустрии. К тому времени сокращение DVD стало привычным, но расшифровывали его теперь иначе: Digital Versative Disc - цифровой многофункциональный диск. DVD-диски научились делать: а) двусторонними, б) двухслойными, в)двусторонними и двухслойными одновременно, увеличив полный объем памяти одного диска до 17 гигабайт. В сущности, процесс массового производства дисков очень напоминает изготовление обычных грампластинок. Вначале записывающий аудио- или видеоинформацию лазер выжигает в эталонном мастер-диске из очень чистого нейтрального стекла, покрытого пластиком, спираль ямочек-питов. Затем с мастер-диска отливают металлический негатив - матрицу, с помощью которой штампуют из пластмассы тираж. Впрочем, слово "штампуют" не вполне точное. На самом деле на специальном оборудовании протекает сложный и весьма тонкий процесс литья под давлением. После этого каждый диск с обратной стороны покрывают отражающим лазерный луч слоем металла, который, в свою очередь, защищается слоем лака. Эксперимент Цель: определить период лазерного компакт-диска, используя его в качестве отражательной дифракционной решётки. Оборудование: штатив, лазерная указка, кронштейн, лапки-2 шт., компакт-диск, экран. Теоретические сведения Лазерный диск благодаря информационным бороздкам, нанесённым на его поверхность, может служить отличной дифракционной решёткой, действующей в отражённом свете. На поверхности CD очень легко наблюдать дифракционный спектр, так как плотность записи информации на нём (количество дорожек на единицу длины) достаточно велика. Д 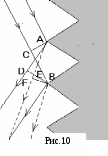 ля объяснения образования видимых цветных полос спектра можно воспользоваться рисунком 10. ля объяснения образования видимых цветных полос спектра можно воспользоваться рисунком 10. Почти параллельные лучи, падающие от источника света на небольшой участок диска, отражается от соседних выпуклостей между бороздками в точках А и В. Лучи, отражённые под углом, равному углу падения, имеют в точках В и D для любой длины волны одинаковые фазы, и образуют на сетчатке глаза наблюдателя изображение источника света в виде белой линии. В самом деле, если через точку А провести волновую поверхность перпендикулярно падающим лучам, а через точку В – поверхность, перпендикулярную отражённым лучам, то расстояние АD, и СВ, пройденные каждым из лучей от одной поверхности к другой, равны между собой. Следовательно, на сетчатке глаза, где они соберутся, будут складываться колебания с одинаковыми фазами. Лучи, отражённые под иным углом, имеют некоторую разность хода ЕF. Действительно, точки В и D, как было показано, находятся в одинаковых фазах. В той же фазе находиться и точка Е, т.к. точки D и Е принадлежат одной волновой поверхности. Если отрезок ЕF равен не чётному числу полуволн, соответствующих, например, зелёному свету, то эти волны гасятся и наблюдатель воспринимает свет, цвет которого определяется суммой цветов оставшейся части спектра (смешение красного и фиолетового цветов дают пурпур). Рядом на сетчатке глаза располагается полоса другого цвета, т.к. разность хода лучей, образующих её, иная и погашенным оказывается свет с другой длиной волны. При освещении диска монохроматическим светом наблюдается аналогичное явление, только спектр состоит из тёмных и светлых полос. Используя явление разложения в спектр монохроматического света лазерным диском, можно найти расстояние между его дорожками (период) с помощью лазера, руководствуясь следующими соображениями. Свет, проходя через диск или отражаясь от него, испытывает дифракцию. В результате, кроме прошедшего луча (нулевой порядок дифракции), возникают лучи, отклонённые на определённые углы. Расстояние между дорожками d можно найти, зная длину волны λ излучения лазера, расстояние D между светлыми точками на экране от лучей нулевого и первого порядка дифракции и расстояние от плоскости диска до плоскости экрана L: d = *(L/D) (2) Формула получается следующим образом: Условие появления дифрагировавшего луча первого порядка заключается в том, чтобы на каждом периоде решётки «набегала» длина волны света. В результате угол отклонения такого луча: = λ/d (3) Расстояние на экране между максимумами нулевого и первого порядка дифракции: D = L (4) Комбинируя (3) и (4), получим (2). Порядок выполнения работы Р  еализация эксперимента осуществлялась с помощью установки, изображённой на фотографии. еализация эксперимента осуществлялась с помощью установки, изображённой на фотографии. Основными её элементами являются: кронштейн, в лапке которого зажат компакт-диск (CD); 2- штатив, в лапке которого зажата лазерная указка; 3- экран (в качестве его удобнее использовать стену). Достижение поставленной цели требует выполнения следующей последовательности действий. собрать установку; осветив пучком лазерной указки cd, добиться расположения максимумов 1-го порядка дифракционной картины на экране на максимальном расстоянии друг от друга, а также их симметричности; измерить расстояние от диска до экрана с помощью рулетки; измерить расстояние между максимумами 1-го порядка; зафиксировать результаты; провести математическую обработку данных. Полученные результаты Выполнив эксперимент, мы получили в ходе его данные, представленные ниже. Расстояние от диска до экрана L= 50,0 cм; Расстояние между максимумами 1-го порядка l1= 100,0 cм; Расстояние от центрального максимума до максимумов 1-го порядка а равно половине величины l1, т.е. а= 50,0 см. Используя эти данные, рассчитаем период диска d по формуле (1): 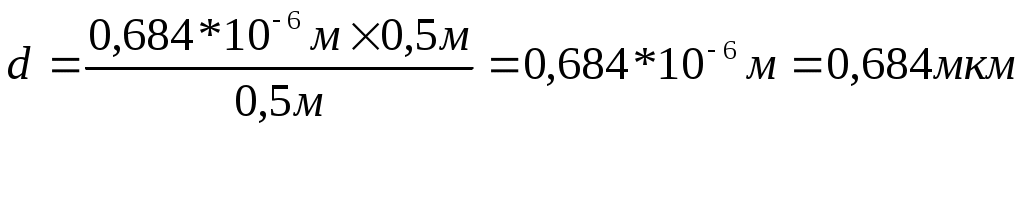 Расчёт погрешности результата Величина L измерялась рулеткой, инструментальная погрешность которой составляет 0,2 мм, а погрешность отсчёта 0,5 мм. Тогда Δ Погрешность определения длины волны λ была определена нами во втором эксперименте : Δλ=0,04 мкм. Погрешность величины а будет равна половине погрешности величины L. А эта погрешность складывается из погрешности отсчёта рулетки и инструментальной её погрешности. Кроме того, в определении положения центров дифракционных максимумов мы могли допустить ошибку в 0,5 мм (эта погрешность оценивается приблизительно и она может быть отнесена к разряду методических, причина её возникновения обусловлена диффузностью объекта измерения). Таким образом, величина погрешности величины а cоставит Δ Используя эти данные, рассчитаем результирующую погрешность Δd уже использованным методом. Результат определения погрешности в среде табличного процессора Excel представлен на рисунке. Результирующая погрешность Δd = 0,0041мкм. По правилам округления погрешностей оставляем одну значащую цифру (т.к. первая цифра – 4). Т.е. Δd=0,004 мкм. В 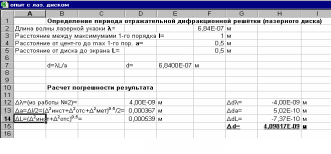 ывод: окончательно можем записать полученный в ходе эксперимента результат в виде: расстояние между бороздками компакт-диска d = ( 0,684 ± 0,004) мкм. ывод: окончательно можем записать полученный в ходе эксперимента результат в виде: расстояние между бороздками компакт-диска d = ( 0,684 ± 0,004) мкм.Заключение Для решения многих практических задач нет необходимости использовать идеальные, бездефектные, сверхчистые монокристаллы. Здесь на помощь могут прийти дешевые материалы с управляемой структурой, примером чего являются пористый кремний и другие пористые полупроводниковые материалы (GaAs, SiC, SiGe, GaP, InP). В последнее время были предложены новые области применения пористого кремния: создание акустических излучателей широкого диапазона, использование пористых слоев для отделения и перенесения монокристаллических кремниевых пленок на другие подложки и т.д. Это свидетельствует о том, что наука о пористом кремнии продолжает активно развиваться. ЛИТЕРАТУРА 1. Лысов Ю., Флорентьев В., Хорлин А. и др. Определение нуклеотидной последовательности ДНК гибридизацией с олигонуклеотидами. Новый метод // Докл. Акад. наук СССР. 1988. Т. 303. С. 1508-151 1. 2. Барский В., Колчинский А., Лысов Ю., Мирзабеков А. Биологические микрочипы, содержащие иммобилизованные в гидрогеле нуклеиновые кислоты, белки и другие соединения: свойства и приложения в геномике // Мол. биол., 2002. Т. 36. С. 563-584. 3. Рубина А., Паньков С., Иванов С. и др. Белковые микрочипы // Докл. Акад. наук. 2001. № 5. С. 419-422. 4. Фесенко Д., Наседкина Т., Мирзабеков А. Бактериальный микрочип: принцип работы на примере обнаружения антибиотиков // Докл. Акад. наук, 2001. Т. 381. № 6. С. 831-833. |
