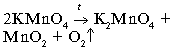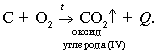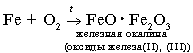Получение и свойства кислорода. Практическая работа №3. «Получение и свойства кислорода».. Практическая работа 3. Получение и свойства кислорода. Цель работы
 Скачать 76.09 Kb. Скачать 76.09 Kb.
|
|
Дата:19.11.21г. Практическая работа №3. «Получение и свойства кислорода». Цель работы: Получить кислород (методом вытеснения воздуха) и изучить его свойства. Приборы и оборудование: KMnO4 – перманганат калия KMnO4 (марганцовка), С – древесный уголь, известковая вода, пробка с газоотводной трубкой, лучинка, спиртовка, спички, колба, вата, пробирка, штатив лабораторный с лапкой или пробиркодержатель, халат химический, перчатки. Правила техники безопасности.
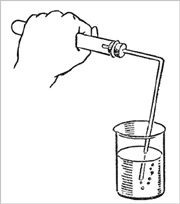
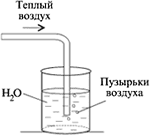
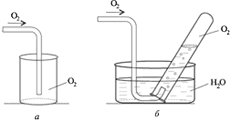
Работа со спиртовкой: Не переносите горящую спиртовку с места на место. Гасите спиртовку только с помощью колпачка. При нагревании не забудьте прогреть пробирку. Для этого пробирку, закрепленную в лапке штатива, медленно проведите сквозь пламя от донышка до отверстия и обратно. Эту операцию повторите несколько раз: чтобы стекло равномерно прогрелось. Признаком прогрева стекла можно считать исчезновение запотевания на стенках пробирки. Дно пробирки должно находиться в верхней части пламени. Дно пробирки не должно касаться фитиля. Работа со стеклом: Помните, что горячее стекло по внешнему виду не отличается от холодного. Не прикасайтесь к горячей пробирке. Закрепляя пробирку в лапке штатива, не закручивайте сильно винт. При нагревании стекло расширяется и пробирка может треснуть 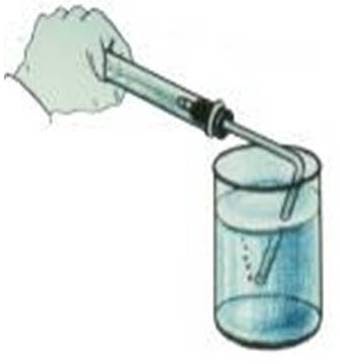 Проверка прибора на герметичность: Закройте пробирку пробкой с газоотводной трубкой, опустите конец трубки в стакан с водой. Плотно обхватите ладонью пробирку и внимательно следите за появлением пузырьков воздуха. ВЫПОЛНЕНИЕ РАБОТЫ Один опыт я ставлю выше, чем тысячу мнений, рожденных только воображением. М.В.Ломоносов Получение кислорода методом вытеснения воздуха (10 мин) 1. Перманганат калия (КMnO4) поместите в сухую пробирку. У отверстия пробирки положите рыхлый комочек ваты. 2. Закройте пробирку пробкой с газоотводной трубкой, проверьте на герметичность (рис. 1).
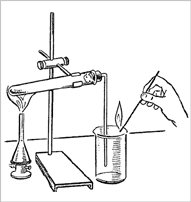
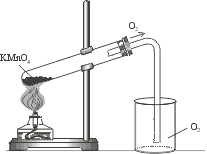
(Пояснения учителя, как проверить прибор на герметичность.) Укрепите прибор в лапке штатива. 3. Газоотводную трубку опустите в стакан, не касаясь дна, на расстоянии 2–3 мм (рис. 2).
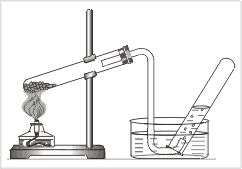
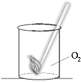
4. Подогрейте вещество в пробирке. (Помните правила техники безопасности.) 5. Проверьте наличие газа тлеющей лучинкой (угольком). Что наблюдаете? Почему кислород можно собирать методом вытеснения воздуха? 6. Соберите полученный кислород в две колбы для проведения следующих опытов. Колбы закройте пробками. 7. Оформите отчет, пользуясь табл. 1, которую разместите на развороте тетради. Получение кислорода методом вытеснения воды (10 мин) 1. Пробирку заполните водой. Закройте пробирку большим пальцем и переверните ее вверх дном. В таком положении опустите руку с пробиркой в кристаллизатор с водой. Подведите к концу газоотводной трубки пробирку, не вынимая ее из воды (рис. 3).
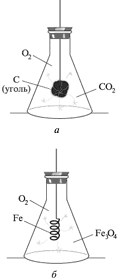
2. Когда кислород вытеснит воду из пробирки, закройте ее большим пальцем и выньте из воды. Почему кислород можно собирать способом вытеснения воды? Внимание! Выньте газоотводную трубку из кристаллизатора, не прекращая нагревать пробирку с КMnО4. Если этого не сделать, то воду перебросит в горячую пробирку. Почему? 2. Обнаружение кислорода Кислород поддерживает горение - это свойство кислорода используется для его обнаружения 3.Горение угля в кислороде Кислород активно взаимодействует со многими веществами. Посмотрим, как реагирует кислород с углем. Для этого раскалим кусочек угля на пламени спиртовки. На воздухе уголь едва тлеет, потому что кислорода в атмосфере около двадцати процентов по объему. В колбе с кислородом уголь раскаляется. Горение углерода становится интенсивным. При сгорании углерода образуется углекислый газ: С+О2= СО2 Добавим в колбу с газом известковую воду – она мутнеет. Известковая вода обнаруживает углекислый газ. Вспомните, как разжигают гаснущий костер. Дуют на угли или интенсивно обмахивают их для того, чтобы увеличить подачу кислорода в зону горения. Оформите отчет о работе в табл. 1.
Сделайте письменный общий вывод о проделанной работе (5 мин). Выводы: кислород в лаборатории можно получить разложением _________. Кислород собирают методом _______. В результате горения простых веществ в кислороде образуются _________. Выводы: кислород в лаборатории можно получить разложением _________. Кислород собирают методом _______. В результате горения простых веществ в кислороде образуются _________. Выводы: кислород в лаборатории можно получить разложением _________. Кислород собирают методом _______. В результате горения простых веществ в кислороде образуются _________. Приведите рабочее место в порядок (3 мин): разберите прибор, расставьте посуду и принадлежности на свои места. Сдайте тетради на проверку. |