практикум строев. Практикум по биологической химии, изданный в 1986 году, подвергся существенной переработке, а также дополнен новыми лабораторными работами в разделах белки, липиды,
 Скачать 1.74 Mb. Скачать 1.74 Mb.
|
ОБМЕН АЗОТСОДЕРЖАЩИХ НЕБЕЛКОВЫХ ВЕЩЕСТВОсновную часть азотсодержащих небелковых соединений составляют нуклеиновые кислоты, нуклеотиды, порфирины и ряд других веществ, которые образуются в процессе их обмена. В широком смысле к азотсодержащим небелковым компонентам относят пептиды, аминокислоты и некоторые продукты обмена последних. Однако исследование пептидов и аминокислот более информативно для состояния белково-аминокислотного обмена, а некоторые продукты их метаболизма, определяемые в клинике (так называемый остаточный азот, мочевина и др.), характеризуют в целом состояние азотистого обмена. 1. Исследование общих продуктов азотистого обмена Некоторые продукты обмена азотистых соединений являются общими как для белковых, так и небелковых веществ. В клинико-биохимических лабораториях с целью диагностики нарушений обмена азотсодержащих соединений чаще всего определяют такие показатели, как остаточный азот, мочевину, аммиак. Остаточный азот – это азот небелковых соединений, остающихся в экстракте после полного осаждения белков крови. В состав остаточного азота входит азот мочевины, пептидов, аминокислот, аммиака, креатина, креатинина, индикана, билирубина и других азотсодержащих низкомолекулярных веществ. Работа 60. Количественное определение остаточного азота в крови фотоколориметрическим методом Реактивы. Реактив Несслера*; трихлоруксусная кислота, 10%-ный раствор; серная кислота, конц.; пероксид водорода, 30%-ный раствор; гидроксид натрия, 0,4 М раствор. Оборудование. Штатив с пробирками; пипетки вместимостью 1, 5 и 10 мл; глазные пипетки; центрифуга с центрифужными весами; песчаная баня; ФЭК. Материал. Кровь, взятая из пальца. Метод основан на способности аммиака, образующегося в результате минерализации безбелковых азотсодержащих соединений крови, давать с реактивом Несслера соединение желтого цвета, интенсивность которого пропорциональна концентрации остаточного азота. Ход определения. В центрифужную пробирку наливают 0,5 мл дистиллированной воды, берут из пальца обследуемого микропипеткой 0,2 мл крови и вносят ее в пробирку, несколько раз промывая микропипетку содержимым. В пробу добавляют 1,3 мл раствора трихлоруксусной кислоты, содержимое перемешивают стеклянной палочкой и оставляют осаждаться белки в течение 20 мин, затем центрифугируют 10 мин при 3000 об/мин и сливают в чистую пробирку надосадочную жидкость. Отбирают 1 мл безбелкового центрифугата в другую пробирку, приливают к нему 3 капли концентрированной серной кислоты и 2 капли раствора пероксида водорода. Ставят пробирки примерно на 30 мин в песчаную баню для минерализации содержимого (до полного просветления раствора). После охлаждения пробирки до комнатной температуры в нее вносят 10 мл дистиллированной воды, тщательно снимают со стенок минерализат стеклянной палочкой и перемешивают. Приливают в пробирку по 0,5 мл раствора гидроксида натрия и реактива Несслера. После появления желтого окрашивания фотометрируют опытную пробу против контрольной (10 мл дистиллированной воды и 0,5 мл реактива Несслера) на ФЭКе при 610-650 нм (красный светофильтр) в кювете с толщиной слоя 2 см. Расчет производят по формуле m2∙5000 х = ————— , 1∙1000 где х – концентрация остаточного азота в крови, г/л; m – содержание азота в пробе, найденное по калибровочному графику (рис.10), мг; 5000 – коэффициент пересчета на 1 л крови; 2 – объем уксусного экстракта, мл; 1 – объем безбелкового центрифугата, взятого на анализ, мл. 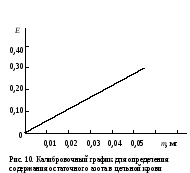 После упрощения формула приобретает следующий вид: х = m10. Оформление работы. По экстинкции рассчитать содержание азота в крови, сравнить его с нормой и сделать вывод о возможных отклонениях. Практическое значение работы. За норму принимается содержание остаточного азота в крови в пределах 0,2-0,4 г/л. Повышение остаточного азота в крови – азотемия – бывает абсолютная и относительная. Абсолютная вызывается задержкой азотистых шлаков или повышенном образованием их в организме; относительная наблюдается при обезвоживании организма (неукротимая рвота, усиленное потоотделение и др.). Различают почечную и внепочечную азотемию. Первая наблюдается при нарушении выделительной способности почек (острые и хронические нефриты), причем степень азотемии соответствует тяжести патологического процесса. Внепочечная является следствием повышенного распада белков в организме при лихорадочных состояниях, ожогах, диабете, тяжелых поражениях печени и т.д. Работа 61. Количественное определение мочевины в сыворотке крови и моче Реактивы. Цветной реактив*; мочевина, стандартный раствор 1 г/л, или 16,65 ммоль/л; набор «Уреатест». Оборудование. Штатив с пробирками; пипетки вместимостью 0,1, 2 и 5 мл; алюминиевая фольга; водяная баня; ФЭК. Материал.
а. Определение содержания мочевины в сыворотке крови. Метод основан на способности мочевины в присутствии тиосемикарбазида и солей железа в сильнокислой среде образовывать с диацетилмонооксимом соединение красного цвета, интенсивность окраски которого пропорциональна содержанию мочевины в исследуемой жидкости. Ход определения. В опытную пробирку отмеривают 0,1 мл разведенной в 10 раз сыворотки крови, в стандартную – такой же объем стандартного раствора мочевины и в контрольную – 0,1 мл дистиллированной воды. Добавляют во все пробирки по 2 мл цветного реактива и тщательно перемешивают их содержимое встряхиванием. Все пробирки закрывают крышечкой из алюминиевой фольги и нагревают в кипящей водяной бане в течение 10 мин (точно!). Затем охлаждают их под струей холодной воды. Измеряют экстинкцию стандартной и опытной проб против контрольной на ФЭКе при 540-560 нм (светофильтр зеленый) в кювете с толщиной слоя 0,5 см. Примечание. Окраска неустойчива, поэтому измерение необходимо провести в течение 15 мин. Расчет. Содержание мочевины х (ммоль/л) в сыворотке крови рассчитывают по формуле Еоп16,65∙10 х = ————— , Ест где Еоп – экстинкция опытной пробы против контрольной; Ест – экстинкция стандартной пробы против контрольной; 16,65 – концентрация мочевины в стандартной пробе, ммоль; Азот мочевины (в ммоль/л) рассчитывают, разделив полученное значение содержания мочевины в сыворотке на 2,14 (число, выражающее отношение молекулярной массы азота мочевины к массе всей молекулы мочевины). б. Определение содержания мочевины в моче. Принцип метода тот же, что и в предыдущей работе. Ход определения. Для анализа используют 0,1 мл разведенной мочи и 0,1 мл стандартного раствора мочевины и обрабатывают эти пробы так же, как и сыворотку крови. Расчет проводят по формуле ЕопV25∙1,665 х = ————— , Ест0,1∙1000 где х – количество мочевины, ммоль/сут; V – объем суточной мочи; 1,665 – содержание мочевины в 0,1 мл стандартной пробы, мкмоль; Еоп – экстинкция опыта; Ест – экстинкция стандарта; 0,1 – объем мочи, взятый на исследование, мл; 1000 – коэффициент пересчета мкмоль в ммоль. в. Определение содержания мочевины в сыворотке крови экспресс-методом с помощью набора «Уреатест». Метод основан на способности уреазы разлагать мочевину с образованием аммиака, который окрашивает полоску реактивной хроматографической бумаги в голубой цвет. Высота окрашенной зоны пропорциональна концентрации мочевины, которую рассчитывают по калибровочному графику. Ход определения. Сыворотку крови разводят водой в отношении 1:1. На пропитанный ферментом конец бумажной полоски в 3 мм от красной парафиновой полосы наносят специальной пипеткой 0,03 мл разведенной сыворотки крови. Полоску тотчас помещают в чистую сухую пробирку, герметически закрывают ее пробкой и ставят в термостат при 37˚С. Через 20 минут полоску извлекают, измеряют высоту окрашенной в голубой цвет зоны. Расчет. По калибровочному графику, входящему в набор «Уреатест», находят концентрацию мочевины в сыворотке крови. Оформление работы. Сделать расчет содержания мочевины и азота мочевины в исследуемой сыворотке и моче. В выводе отметить возможные изменения в азотном обмене. Практическое значение работы. В норме содержание мочевины в сыворотке крови человека составляет 3,0-7,0 ммоль/л, а азота мочевины – 1,2-3,7 ммоль/л. Содержание мочевины в сыворотке крови значительно колеблется в зависимости от приема белков с пищей. Повышение уровня мочевины в крови (азотемия) отмечается при заболеваниях почек (когда нарушена их выделительная функция), при усиленном распаде белков, избыточном белковом питании, а также в случае обезвоживания организма (в данном случае имеет место относительная, а не абсолютная форма азотемии). Снижение уровня мочевины в крови и выделения ее с мочой (в сутки в норме выделяется 333-582,8 ммоль/сут) наблюдается при заболевании печени (паренхиматозная желтуха, дистрофия печени, цирроз), что связано с нарушением мочевинообразовательной функции. Работа 62. Количественное определение креатина и креатинина по методу Брауна Реактивы. Пикриновая кислота, насыщенный раствор*; соляная кислота, 0,1 моль/л; основной калибровочный раствор креатинина*; 12,5% раствор едкого натрия. Оборудование. Штатив с пробирками; пипетки на 0,2; 1,0; 2,0 и 5,0 мл; ФЭК; водяная баня. Материал. Исследуемая моча. Принцип метода. Основан на способности креатинина в щелочной среде с пикриновой кислотой образовывать комплекс оранжевого цвета, интенсивность которого пропорциональна концентрации креатинина. Определение креатина проводится после перевода его в креатинин при нагревании мочи в солянокислой среде. Ход определения. В три меченные обычные пробирки внести по 0,2 мл концентрированной соляной кислоты (осторожно, только пипеткой с резиновой грушей!). В 1-ю и 2-ю пробирки добавить по 0,2 мл исследуемой мочи, предварительно разведенной в 5 раз: 1 пробирка служит для определения креатинина, 2 – креатина, 3 – контрольная. Вторую пробирку нагреть в течение 5 минут на бурно кипящей водяной бане, после чего охладить под струей водопроводной воды. Во все пробирки внести дистиллированную воду в следующих количествах: первая пробирка – 2,0 мл, вторая – 2,0 мл, третья – 2,2 мл и в каждую добавить по 0,6 мл насыщенного раствора пикриновой кислоты и по 1,0 мл 12,5% раствора гидроксида натрия, тщательно перемешивают. Оставляют стоять на 10 минут при комнатной температуре, после чего во все три пробирки добавляют по 6,0 мл дистиллированной воды. Оптическую плотность исследуемых растворов определяли на ФЭКе с длиной волны 507 нм в кювете на 10 м против контрольной пробы (третья пробирка). Количество определялось по калибровочному графику. Расчет. Находят содержание свободного креатинина в первой пробирке по калибровочному графику, а затем, используя нижеприведенную формулу, проводят расчет: a∙5∙1000∙5 х = ——————— , 1000∙1000 где х – количество креатинина в г на 1 л мочи; а – количество креатинина в мкг в 0,2 мл разведенной мочи, взятой для анализа; 5 – разведение мочи; 5 – для перевода количества креатинина с 0,2 мл мочи на 1 мл; 1000 – перерасчет на 1 л, числитель; 1000 – для перевода мкг в мг, знаменатель; 1000 – для перевода мг креатинина в г, знаменатель. Расчет креатина – вторая пробирка содержит сумму свободного креатинина и креатинина, переведенного из креатина при нагревании в солянокислой среде. Из количества креатинина, полученного при определении суммы креатин-креатинин, вычитают количество параллельно исследуемого свободного креатинина и полученную разность умножают на 1,16 – коэффициент перевода креатинина в креатин. Построение калибровочного графика: из рабочего калибровочного раствора креатинина готовят разведение, как указано ниже:
|
