Концентрация. приготовление раствора и определение его концентрации
 Скачать 46.26 Kb. Скачать 46.26 Kb.
|
|
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ  МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ федеральное государственное бюджетное образовательное учреждение высшего образования «САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСТИТЕТ» Кафедра общей химии ЛАБОРАТОРНАЯ РАБОТА № 4 По предмету: ХИМИЯ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ Тема: «ПРИГОТОВЛЕНИЕ РАСТВОРА И ОПРЕДЕЛЕНИЕ ЕГО КОНЦЕНТРАЦИИ»
Санкт-Петербург 2022 Цель работы: Ознакомиться с методами приготовления растворов заданной концентрации и анализом раствора при помощи титрования. Ход работы 1. В 3 конические колбы пипеткой Мора отобрали аликвотные объемы приготовленного раствора 5 мл, добавили немного дистиллированной воды (до толщины слоя жидкости около 5 мм) и 2−3 капли индикатора – фенолфталеина. 2. Бюретку на 25 мл наполнили титрованным раствором едкого натра. Кончик бюретки был заполнен раствором, а уровень жидкости доведен точно до нулевого деления. Затем медленно, по каплям, добавляли раствор щелочи из бюретки к аликвоте кислоты, непрерывно перемешивая раствор в конической колбе. 3. Определили эквивалентные точки: 2,4; 2,4; 2,45. 4. Титрование повторили 3 раза, измеренные эквивалентные объемы щелочи усреднили и получили: Протокол лабораторной работы 1. Заданная преподавателем концентрация соляной кислоты 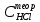 = 0,1 моль/л = 0,1 моль/л 2. Расчет объема соляной кислоты, необходимого для приготовления 100 мл раствора кислоты заданной концентрации: 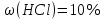 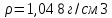 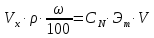 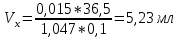 3. Объем аликвоты соляной кислоты, взятый для титрования, Va = 5 мл. 4. Концентрация раствора щелочи 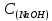 = 0,2 моль/л. = 0,2 моль/л.5. Объем щелочи, пошедший на титрование пробы соляной кислоты: 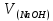 1 = 2,45 мл; 1 = 2,45 мл;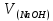 2 = 2,4 мл; 2 = 2,4 мл;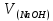 3 = 2,4 мл; 3 = 2,4 мл;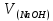 ср = 2,4 мл. ср = 2,4 мл.Обработка результатов эксперимента Вычисление концентрации полученного раствора: 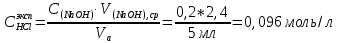 Вычисление погрешности: 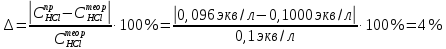 Вывод: в ходе лабораторной работы были получены навыки приготовления раствора заданной концентрации и анализа раствора при помощи титрования. При приготовлении раствора погрешность составила |Δ| = 4%, такая погрешность может быть связана с невысокой точностью бюретки, и с тем, что в процессе реакции капли растворов кислоты и щелочи оставались на стенках сосудов. |
