Программа промежуточной аттестации составлена в соответствии с рабочей программой профессионального модуля пм. 02 Изготовление лекарственных форм и проведение обязательных видов внутриаптечного контроля
 Скачать 401.17 Kb. Скачать 401.17 Kb.
|
|
Спиртовые жидкости добавляют в микстуры: А- В порядке возрастания крепости этанола Б- В порядке уменьшения крепости этанола В- В любом порядке В микстурах путем смешивания с равным количеством готового раствора добавляют: А- Настойку пустырника Б- Настойку мяты В- Настойку валерианы Г- Настойку ландыша В микстурах во флакон к приготовленному раствору без предварительного смешивания добавляют: А- Грудной эликсир Б- Нашатырно-анисовые капли В- Настойку мяты перечной Г- Настойку пустырника Рассчитать количество воды очищенной по рецепту: Возьми: Цинка оксида 5,0 Талька 5,0 Воды очищенной до 100 мл Смешай. Дай. Обозначь. А- 100 мл Б- 95 мл В- 90 мл Г- 110 мл Количество жидкости, добавляемое для диспергирования веществ: Возьми: Цинка оксида 5,0 Талька 5,0 Воды очищенной до 100 мл Смешай. Дай. Обозначь. А- 100 мл Б- 10 мл В- 5 мл Г- 50 мл Срок хранения суспензий согласно пр. МЗ РФ №751н: А- 10 суток Б- 3 суток В- 1 сутки Г- 2 суток При отсутствии указаний о количестве лекарственного растительного сырья (при отсутствии дополнительных указаний) настои и отвары готовят в соотношении: А- 1:10 Б- 1:400 В- 1:20 Г- 1:30 При изготовлении водных извлечений из ЛРС содержащего сильно действующие и ядовитые вещества, при отсутствии дополнительных указаний следует брать: А- 1:10 Б- 1:20 В- 1:30 Г- 1:400 При отсутствии указаний в рецепте о количестве лекарственного растительного сырья корня алтея, водное извлечение готовят в соотношении: А- 1:10 Б- 1:20 В- 1:30 Г- 1:400 Для приготовления настоев и отваров воду берут с учетом: А-Коэффициента водопоглощения Б- Коэффициента увеличения объема В- Обратного коэффициента замещения Рассчитать количество лекарственного растительного сырья по рецепту: Возьми: Извлечения листьев мяты 150 мл Дай. Обозначь. А- 15,0 Б- 5,0 В- 0,37 Г- 30,0 Определить режим настаивания извлечения по рецепту: Возьми: Извлечения листьев мяты 150 мл Дай. Обозначь. А- Настаивание 10 мин, охлаждение 30 мин. Б- Настаивание 30 мин, охлаждение 10 мин. В- Настаивание 30 мин, без охлаждения Г- Настаивание 15 мин, охлаждение 45 мин. Рассчитать количество лекарственного растительного сырья по рецепту: Возьми: Извлечения листьев толокнянки 100,0 Дай. Обозначь. А- 1,0 Б- 10,0 В- 3,33 Г- 0,25 Определить режим настаивания извлечения по рецепту: Возьми: Извлечения листьев толокнянки 100,0 Дай. Обозначь. А- Настаивание 10 мин, охлаждение 30 мин. Б- Настаивание 30 мин, охлаждение 10 мин. В- Настаивание 30 мин, без охлаждения Г- Настаивание 15 мин, охлаждение 45 мин. Рассчитать количество очищенной воды для настаивания по рецепту: Возьми: Извлечения корневищ с корнями валерианы 150 мл Дай. Обозначь: По столовой ложке 3 раза в день. КВП=2,9 А- 193,5 мл Б- 164,5 мл В- 151,08 мл Рассчитать количество очищенной воды для настаивания по рецепту: Возьми: Настоя листьев шалфея 100 мл Дай. Обозначь. КВП= 3,3 А- 100,8 мл Б- 110,9 мл В- 133 мл Определить режим извлечения по рецепту: Возьми: Извлечения листьев шалфея 100 мл Дай. Обозначь. А- Настаивание 10 мин, охлаждение 30 мин. Б- Настаивание 15 мин, охлаждение 45 мин. В- Настаивание 30 мин, охлаждение 10 мин. Г- Настаивание 30 мин, охлаждение 0 мин. Рассчитать количество очищенной воды для настаивания по рецепту: Возьми: Настоя травы зверобоя 200 мл Дай. Обозначь. КВП= 1,6 А- 232 мл Б- 200,8 мл В- 210,6 мл Рассчитать количество лекарственного растительного сырья по рецепту: Возьми: Извлечения корневищ змеевика 180 мл Дай. Обозначь. А- 18,0 Б- 9,0 В- 6,0 Г- 0,45 При отсутствии указаний в рецепте о количестве лекарственного растительного сырья травы горицвета, водное извлечение готовят в соотношении: А- 1:10 Б- 1:20 В- 1:30 Г- 1:400 При отсутствии указаний в рецепте о количестве лекарственного растительного сырья травы термопсиса, водное извлечение готовят в соотношении: А- 1:400 Б- 1:30 В- 1:20 Г- 1:10 При отсутствии указаний в рецепте о количестве лекарственного растительного сырья корневищ с корнями валерианы, водное извлечение готовят в соотношении: А- 1:10 Б- 1:20 В- 1:30 Г- 1:400 При изготовлении настоя и отвара с использованием сухого экстракта-концентрата 1:1, последний берут в количестве: А- Равном количеству лекарственного растительного сырья Б- В 2 раза больше по отношению к лекарственному растительному сырью В- В 2 раза меньше по отношению к лекарственному растительному сырью При изготовлении водного извлечения с использованием жидкого экстракта-концентрата 1:2, последний берут в количестве: А- Равном количеству лекарственного растительного сырья Б- В 2 раза больше по отношению к лекарственному растительному сырью В- В 2 раза меньше по отношению к лекарственному растительному сырью 145. Если настои и отвары готовят из лекарственного сырья: А- То можно использовать концентрированные растворы солей Б- То концентрированные растворы солей использовать нельзя Лекарственное растительное сырье с меньшей биологической активностью или меньшим содержанием алкалоидов: А- Использовать нельзя Б- Использовать можно Определить режим приготовления настоя с пометкой cito!: А- Настаивание 15 мин, охлаждение 45 мин. Б- Настаивание 25 мин, охлаждение искусственное В- Настаивание 25 мин, не охлаждают Г- Настаивание 30 мин, охлаждение 10 мин. Определить режим приготовления 1 л настоя листьев мяты: А- Настаивание 15 мин, охлаждение 45 мин. Б- Настаивание 25 мин, охлаждение искусственное В- Настаивание 25 мин, охлаждение 55 мин. Г- Настаивание 30 мин, охлаждение 10 мин. Если настои и отвары готовят с использованием экстрактовконцентратов: А- Можно использовать концентрированные растворы солей Б- Нельзя использовать концентрированные растворы солей 150. Срок хранения водных извлечений согласно пр. МЗ РФ №751н: А- 1 сутки Б- 2 суток В- 3 суток Г- 10 суток МДК 02.02 «Контроль качества лекарственных средств» Латинское название кальция хлорида А. Calcii chloratum Б. Calcium chloridum В. Kalii chloridum Г. Calcii chloridum Латинское название магния сульфата. А. Magnesii sulfas Б. Magnesii sulfatum В. Magnesii sulfatis Г. Magnium sulfaticum Латинское название цинка сульфата. А. Zinci sulfuricum Б. Cinci sulfas В. Zinci sulfas Г. Zincum sulfatum Латинское название натрия тиосульфата. А. Natrium thiosulfas Б. Natrii thiosulfas В. Natrii thiosulfatis Г. Natrii thiosulfatum Латинское название серебра нитрата. А. Argentum nitris Б. Argenti nitras В. Argenti nitris Г. Argenti nitratum Латинское название натрия гидрокарбоната. А. Natrium hydrocarbonas Б. Natrii hydrocarbonas В. Natrium hydrocarbonici Г. Natrium hydrocarbonatum Лекарственное средство, соответствующее названию "соль горькая" или "английская" А. цинка сульфат Б. натрия хлорид В. кальция хлорид Г. магния сульфат Формула магния сульфата А. магния сульфат с пятью молекулами воды Б. магния сульфат с семью молекулами воды В. магния сульфат с двумя молекулами воды Г. магния сульфат с шестью молекулами воды Лекарственное средство, для какого характерны свойства: Бесцветные призматические кристаллы, выветривающиеся на воздухе, горько-соленого вкуса. Водные растворы нейтральной реакции. Легко растворим в воде, легче в кипящей, не растворим в спирте А. цинка сульфат Б. серебра нитрат В. магния сульфат Г. натрия хлорид Лекарственное средство, для какого характерны свойства: Бесцветные кристаллы без запаха, горько-соленого вкуса. Очень гигроскопичен, на воздухе расплывается. Очень легко растворим в воде, легко в спирте. Водные растворы нейтральной реакции. А. цинка сульфат Б. кальция хлорид В. магния сульфат Г. борная кислота Лекарственное средство, для какого характерны свойства: Бесцветные прозрачные кристаллы или мелкокристаллический порошок, без запаха. На воздухе выветривается. Очень легко растворим в воде, не растворим в спирте, медленно в глицерине. Водные растворы кислой реакции. А. магния сульфат Б. серебра нитрат В. цинка сульфат Г. натрия тетраборат Лекарственное средство, для какого характерны свойства: Белый кристаллический порошок солено-щелочного вкуса. Устойчив в сухом воздухе, медленно разлагается во влажном. Растворим в воде, не растворим в спирте. Водные растворы имеют слабо-щелочную реакцию. А. магния сульфат Б. серебра нитрат В. натрия гидрокарбонат Г. калия хлорид Лекарственное средство, для какого характерны свойства: Бесцветные прозрачные кристаллы в виде белых или цилиндрических палочек без запаха. Под действием света темнеет. Очень легко растворим в воде, трудно в спирте. Водные растворы нейтральной реакции. А. кальция хлорид Б. серебра нитрат В. магния сульфат Г. натрия бромид Реактивы, доказывающие подлинность кальция хлорида натрия гидроксид А. 2,3,4 аммония оксалат Б. 1,2,3 серебра нитрат В. 2,3 натрия гидрофосфат Г. 3,5 гексацианоферрат III калия Реактивы, доказывающие подлинность цинка сульфата серебра нитрат А. 1,2,4,5 гексацианоферрат II калия Б. 2,3,4,5 гексацианоферрат III калия В. 2,4,5 бария хлорид Г. 4,5,6 натрия сульфид аммония оксалат Реактивы, доказывающие подлинность магния сульфата. аммония оксалат А. 1,3,5,6 натрия гидрофосфат Б. 2,3,5,7 бария хлорид В. 2,3,6,7 серебра нитрат Г. 3,5,6,7 аммония гидроксид натрия гидроксид аммония хлорид Реактивы, доказывающие подлинность катиона натрия в гидрокарбонате натрия кислота виннокаменная А. 1,3,5 цинкуранилацетат Б. 2,3,4 натрия ацетат В. 2,4 кислота пикриновая Г. 2,3 этанол Реактивы, доказывающие подлинность гидрокарбонат-иона в гидрокарбонате натрия серебра нитрат А. 2,3,4 кислота хлороводородная Б. 3,5,6 натрия гидрофосфат В. 2,4,6
С раствором хлороводородной кислоты определяют подлинность лекарственного средства А. серебра нитрат Б. магния сульфат В. кальция хлорид Г. спиртовой раствор йода Цвет осадка, образующегося при взаимодействии нитрата серебра с калия йодидом А. белый Б. желтый В. кирпично-красный Г. зеленовато-голубой Реакция с раствором дифениламина характерна для лекарственного средства А. натрия гидрокарбонат Б. магния сульфат В. серебра нитрат Г. натрия тетраборат С раствором гексацианоферрата II калия определяют подлинность лекарственного средства А. серебра нитрат Б. магния сульфат В. цинка сульфат Г. натрия бромид Цвет осадка гексацианоферрата II калия цинка А. белый Б. желтый В. кирпично-красный Г. черный Цвет осадка, образующегося при взаимодействии цинка сульфата с сульфидом натрия А. желтый Б. черный В. белый В. кирпично-красный Катион, окрашивающий пламя спиртовки в кирпично-красный цвет А. цинка Б. натрия В. кальция Г. калия Цвет осадка бария сульфата А. белый Б. желтый В. светло-желтый Г. черный Реакция с серебра нитратом характерна для: А. магния сульфата Б. натрия гидрокарбоната В. кальция хлорида Г. раствора пероксида водорода Цвет осадка хлорида серебра А. белый Б. желтоватый В. желтый Г. кирпично-красный Реакцию с раствором формальдегида в присутствии раствора аммиака выполняют для доказательства подлинности: А. калия йодида Б. серебра нитрата В. натрия гидрокарбоната Г. натрия тетраборат Цвет осадка магния аммония фосфата А. черный Б. белый В. кирпично-красный Г. зеленый В желтый цвет окрашивают пламя горелки: А. катионы натрия Б. катионы калия В. катионы кальция Г. катионы меди При смачивании куркумовой бумажки раствором натрия тетрабората, раствором хлороводородной кислоты образуется: А. розовое окрашивание Б. грязно - зелёное окрашивание В. малиновое окрашивание Г. сине-фиолетовое окрашивание Название реактива: K4[Fe(CN)6] А. гексацианоферрат III калия Б. гексацианоферрат II калия В. гексанитрокобальтат III калия Г. гексагидроксостибиат V калия Качественная реакция на катион магния выполняется с добавлением реактивов серебра нитрата А. 1,2,3 натрия гидрофосфата Б. 2,3,4,5 гексацианоферрата II калия В. 2,4,6 аммония хлорида Г. 2,4,5 аммония оксалата аммония гидроксида Раствор цинка сульфата имеет pH-среды: А. > 7 Б. < 7 В. = 7 Слабощелочную реакцию среды имеют растворы: А. магния сульфата Б. цинка сульфата В. натрия гидрокарбоната Г. борная кислота При взаимодействии натрия гидрокарбоната с хлороводородной кислотой образуется: А. белый осадок Б. неприятный запах В. пузырьки газа Г. желтый осадок и характерный запах Реакция на гидрокарбонат-ион с насыщенным раствором магния сульфата выполняется на холоду при нагревании при комнатной температуре При количественном определении серебра нитрата применяют индикатор: А. калия хромат Б. эозинат натрия В. железоаммониевые квасцы Г. бромфеноловый синий Количественное определение серебра нитрата проводят методом аргентометрии по: А. Фаянсу Б. Фольгарду В. Мору Г. Кольтгофу Серебра нитрат количественно определяют методом: А. комплексонометрии Б. алкалиметрии В. аргентометрии Г. йодометрии Конец титрования в методе аргентометрии по Фольгарду определяют по образованию А. белого осадка Б. кроваво-красного окрашивания В. розовато-желтого окрашивания Г. фиолетового осадка Количественное определение серебра нитрата проводят в среде: А. разведенной уксусной кислоты Б. аммиачно-буферного раствора В. разведенной азотной кислоты Г. разведенной серной кислоты Метод количественного определения натрия гидрокарбоната А. комплексонометрии Б. ацидиметрии В. аргентометрии Г. йодометрии Наиболее экономичный метод количественного определения 50% раствора кальция хлорида А. аргентометрия Б. рефрактометрия В. нейтрализация Г. алкалиметрия Метод количественного определения цинка сульфата А. нейтрализация Б. аргентометрия В. комплексонометрия Г. ацидиметрия Наиболее экономичный метод количественного определения 25% раствора магния сульфата для инъекций А. нейтрализация Б. рефрактометрия В. аргентометрия Г. йодометрия Метод количественного определения кислоты борной А. нейтрализация, прямое титрование Б. нейтрализация, обратное титрование В. аргентометрия Г. комплексонометрия Лекарственные средства, количественно определяемые методом комплексонометрии натрия гидрокарбонат А. 1,2,4,5 магния сульфат Б. 2,4,5 серебра нитрат В. 4,5,6 кальция хлорид Г. 1,4,5 цинка сульфат калия бромид Количественное определение кальция хлорида проводят в среде: А. разведенной уксусной кислоты Б. аммиачно-буферного раствора В. разведенной азотной кислоты Г. разведенной серной кислоты Индикатор метода комплексонометрии. А. метиловый оранжевый Б. хромовый темно-синий В. метиленовый синий Г. фенолфталеин Точку эквивалентности в методе комплексонометрии определяют по: А. красно-фиолетовому окрашиванию Б. сине-фиолетовому окрашиванию В. обесцвечиванию Г. розовому окрашиванию Индикатор с помощью которого количественно определяют натрия гидрокарбонат. фенолфталеин метиловый-оранжевый эозинат натрия Г. хромат калия Конец титрования при проведении количественного определения натрия гидрокарбоната определяют: А. по обесцвечиванию раствора Б. по розовато-оранжевому окрашиванию В. по розовому осадку Г. по сине-фиолетовому окрашиванию Лекарственное средство, количественно определяемое по данной методике: Т.н. растворяют в воде, прибавляют индикатор метиловый оранжевый, титруют 0,1 моль/л раствором хлороводородной кислоты до розовато-желтого окрашивания. А. калия йодид Б. натрия гидрокарбонат В. серебра нитрат Г. кальция хлорид Лекарственное средство, количественно определяемое по данной методике: Т.н. растворяют в воде, прибавляют индикатор хромат калия, титруют 0,1 н растворам нитрата серебра до красно - бурого окрашивания. А. натрия гидрокарбонат Б. натрия хлорид В. магния сульфат Г. натрия тетраборат Лекарственное средство, при количественном определении которого добавляют глицерин. А. кислота борная Б. серебра нитрат В. натрия гидрокарбонат Г. цинка сульфат Лекарственные средства, количественное определение которых проводят методом нейтрализации. серебра нитрат А. 1,2 натрия гидрокарбонат Б. 2,3 50% раствор кальция хлорида В. 2,5 25% раствор магния сульфата Г. 2,6 кислота хлороводородная цинка сульфат Молярная масса эквивалента калия йодида А. М 1/z= М.м. Б. М 1/z = М.м./2 В. М 1/z = 2М.м. Г. М 1/z = М.м./4 Лекарственное средство, количественно определяемое по следующей методике: Т.н. растворяют в воде, добавляют аммиачно-буферный раствор, индикатор хромовый темно-синий и титруют 0,05 моль/л раствором трилона Б до сине-фиолетового окрашивания А. магния сульфат Б. серебра нитрат В. калия хлорид Г. барная кислота Индикаторы метода комплексонометрии: хромовый темно-синий А. 1,2,3 метиленовый синий Б. 1,3,4 эрихром черный Т В. 1,2,3,4 ксиленовый оранжевый Г. 3,4,5 метиловый оранжевый фенолфталеин Молярная масса эквивалента натрия гидрокарбоната А. М 1/z = М.м. Б. М 1/z = 2М.м. В. М 1/z = М.м./2 Г. М 1/z = М.м./4 Уравнение реакции, лежащее в основе количественного определения кальция хлорида А. CaCl2 + Na2H2Tr = CaNa2Tr + 2HCl Б. CaCl2 + H2Ind = CaInd + 2HCl CaInd + Na2H2Tr = Na2CaTr + H2Ind В. CaCl2 + (NH4)2C2O4 = CaC2O4 + 2 NH4Cl Уравнение реакции, в котором допущена ошибка А. ZnSO4 + Na2S = ZnS + Na2SO4 Б. 3ZnSO4 + 2K4[Fe(CN)6] = K2Zn3[Fe(CN)6] + 3K2SO4 Уравнение реакции, в котором допущена ошибка А. KCl + Na3[Co(NO2)6] = KNa[Co(NO2)6] + NaCl Б. 2KCl + Na3[Co(NO2)6] = K2Na[Co(NO2)6] + 2NaCl Уравнение реакции, в котором допущена ошибка А. AgNO3 + NaCl = AgCl + NaNO3 2AgNO3 + K2CrO4 = Ag2CrO4 + 2KNO3 Б. AgNO3 + NaCl = AgCl + NaNO3 AgNO3 + K2CrO4 = Ag2CrO4 + KNO3 Методом аргентометрии по Фольгарду количественно определяют: магния сульфат серебра нитрат натрия гидрокарбонат Г. цинка сульфат Кальция хлорид количественно определяют методом: А. аргентометрии по Мору Б. аргентометрии по Фаянсу В. комплексонометрии Г. алкалиметрии Сделайте заключение о качестве лекарственной формы состава: Натрия бромида 2,0 Кальция хлорида 3,0 Воды очищенной 200 мл если содержание кальция хлорида оказалось 2,97.
Сделайте заключение о качестве лекарственной форме состава: Натрия бромида 2,0 Кальция хлорида 3,0 Воды очищенной 200 мл если содержание кальция хлорида оказалось 2,97. А. удовлетворяет приказу МЗ РФ от 26.10.15 г. № 751н Б. не удовлетворяет приказу МЗ РФ от 26.10.15 г. № 751н Рассчитайте допустимый интервал отклонений для 50% концентрированного раствора кальция хлорида А. 49,5 - 50,5 Б. 49,0 - 51,0 В. 45,0 – 55,0 Г. 48,5 – 51,5 Сделайте заключение о качестве 50% концентрированного раствора кальция хлорида, если содержание оказалось 49,3%. А. удовлетворяет приказу МЗ РФ от 26.10.15 г. № 751н Б. не удовлетворяет приказу МЗ РФ от 26.10.15 г. № 751н Рассчитайте допустимые интервалы отклонений борной кислоты по химическому контролю для лекарственной формы состава: Раствора борной кислоты 2% - 10 мл Цинка сульфата 0,03 А. 0,18 - 0,22 Б. 0,16 - 0,24 В. 0,19 – 0,21 Г. 0,175 – 0, 225 Рассчитайте допустимые интервалы отклонений цинка сульфата по химическому контролю для лекарственной формы состава: Раствора борной кислоты 2% - 10 мл Цинка сульфата 0,03 А. 0,0255 - 0,0345 Б. 0,024 - 0,0306 В. 0,026 – 0,034 Г. 0,027 – 0,033 Нормы отклонений для 10% концентрированного раствора кальция хлорида по приказу МЗ РФ от 26.10.15 г. № 751н А. +-2% Б. +-1% В. +-3% Г. +- 0,5% Нормы отклонений для 5% концентрированного раствора натрия гидрокарбоната по приказу МЗ РФ от 26.10.15 г. № 751н А. +-1% Б. +-2% В. +- 0,5% Г. +- 3% Нормы отклонений для 25% концентрированного раствора магния сульфата по приказу МЗ РФ от 26.10.15 г. № 751н А. +-1% Б. +-2% В. +- 0,5% Г. +- 3% Интервалы отклонений для химического контроля лекарственной формы состава: Раствора нитрата серебра 1% - 20 мл А. 0,18 - 0,22 Б. 0,16 - 0,24 В. 0,17 – 0,23 Г. 0,175 – 0,225 Виды внутриаптечного контроля, обязательные для лекарственной формы состава: Раствора цинка сульфата 0,25% - 100 мл (внутриаптечная заготовка) письменный А. 1,3,5,6 опросный Б. 1,3,4,5,6,7 органолептический В. 1,3,6,7 физический Г. 1,2,3,4,6 качественный количественный контроль при отпуске Виды внутриаптечного контроля обязательны при заполнении штангласа цинка сульфата: письменный А. 3,5 опросный Б. 1,2,3,4 органолептический В. 1,3,4,7 физический Г. 1,3,7 качественный количественный контроль при отпуске Виды внутриаптечного контроля обязательные для 50% концентрированного раствора кальция хлорида: письменный А. 1,3,5,6 опросный Б. 1,2,3,5,6 органолептический В. 1,3,4,5,7 физический Г. 1,3,7 качественный количественный контроль при отпуске Виды внутриаптечного контроля обязательны для лекарственной формы состава: Раствора кальция хлорида 5% - 100 мл (ребенку 20 дней) № 5 письменный А. 1,2,3,4,5,6,7 опросный Б. 1,3,4,5,6,7 органолептический В. 1,3,5,6,7 физический Г. 1,3,7 качественный количественный контроль при отпуске Виды внутриаптечного контроля, обязательные для лекарственной формы состава: Раствора магния сульфата 20% - 20 мл для инъекций № 10 письменный А. 1,2,3,4,5,6,7 опросный Б. 1,3,4,5,6,7 органолептический В. 1,3,5,6,7 физический Г. 1,3,7 качественный количественный контроль при отпуске Виды внутриаптечного контроля, обязательные для лекарственной формы состава:
качественный количественный контроль при отпуске Виды внутриаптечного контроля, обязательные для 20% концентрированного раствора магния сульфата: письменный А. 1,2,3,4,5,6 опросный Б. 1,3,4,6,7 органолептический В. 1,3,5,6 физический Г. 1,3,7 качественный количественный контроль при отпуске Лекарственное средство, обладающее антисептическим действием А. магния сульфат Б. натрия гидрокарбонат В. раствор пероксида водорода Г. натрия бромид Лекарственные средства, обладающие антисептическим действием: натрия гидрокарбонат А. 1,2,3 магния сульфат Б. 3,4 цинка сульфат В. 2,3 раствор пероксида водорода Г. 2,3,4 Лекарственное средство, обладающее вяжущим, антисептическим действием А. кальция хлорид Б. натрия гидрокарбонат В. цинка сульфат Г. натрия хлорид Применение кальция хлорида: антисептическое А. 1,2,3 2. противоаллергическое Б. 2,3 кровоостанавливающее В. 2,3,5 прижигающее Г. 1,3,4 Применение магния сульфата: слабительное А. 1,2,3 противоаллергическое Б. 1,3,4 успокаивающее ЦНС В. 1,3,5 антисептическое Г. 1,2,4,5 спазмолитическое Лекарственное средство, обладающее вяжущим, противовоспалительным, бактерицидным, антисептическим действием А. кальция хлорид Б. серебра нитрат В. натрия гидрокарбонат Г. калия бромид Лекарственное средство, применяющееся при хроническом гастрите и язвенной болезни желудка А. цинка сульфат Б. натрия гидрокарбонат В. серебра нитрат Г. раствор пероксида водорода Лекарственное средство, применяющееся как отхаркивающее А. магния сульфат Б. натрия гидрокарбонат В. кальция хлорид Г. раствор кислоты хлористоводородной 1% Лекарственное средство, чернеющее при неправильном хранении А. кальция хлорид Б. серебра нитрат В. натрия гидрокарбонат Г. натрия хлорид Лекарственное средство, хранящееся в хорошо укупоренных склянках, залитых парафином или мастикой? А. цинка сульфат Б. кальция хлорид В. магния сульфат Г. натрия тетраборат Лекарственное средство, выветривающееся при неправильном хранении А. цинка сульфат Б. кальция хлорид В. серебра нитрат Г. калия йодид Лекарственные средства, хранящиеся в хорошо укупоренных банках оранжевого стекла, в защищенном от света месте магния сульфат А. 1,2 серебра нитрат Б. 2,3 цинка сульфат В. 2,4 калия йодид Г. 5,6 кальция хлорид натрия гидрокарбонат Приказ МЗ РФ, согласно требованиям которого хранятся лекарственные средства А. Приказ МЗ РФ от 26.10.15 г. № 751н Б. Приказ МЗ РФ от 23.08.10 г. № 706н В. Приказ МЗ РФ от 14.01.19 г. № 4н Г. Приказ МЗ РФ от 21.10.97 г. № 309 Формула расчета массовой доли для жидких лекарственных форм, прямое титрование. А. W=T*V*K*Vл.ф./а Б. W=T*(V1-V2)*Vл.ф./а В. W=T*V*K*100%/а Г. W =(n-no)/F Формула расчета массовой доли для жидких лекарственных форм, обратное титрование А. W=T*V*K*Vл.ф./а Б. W=T*(V1*K-V2*K)*Vл.ф./а В. W=T*V*K*100%/а Г. W =(n-no)/F Формула расчета, применяемая в методе рефрактометрии. А. W =(n-no)/F Б. W =T*V*K*100%/а В. W=T*V*K*Vл.ф./а Г. W=T*(V1-V2)*Vл.ф./а При рефрактометрическом определении концентрация раствора кальция хлорида, если n=1,3558, F= 0,00114 равна А. 20% Б. 20,5% В. 19,9% Г. 20,15% При рефрактометрическом определении концентрация раствора кальция хлорида, если n=1,3446, F= 0,00119 равна А. 9,75% Б. 10,5% В. 9,9% Г. 10,15% При рефрактометрическом определении концентрация раствора кальция хлорида, если n=1,3489, F= 0,00117 равна А. 10% Б. 13,59% В. 9,85% Г. 10,85% При рефрактометрическом определении концентрация раствора кальция хлорида, если n=1,339, F= 0,00117 равна А. 5,13% Б. 5% В. 4,95% Г. 5,2% При рефрактометрическом определении концентрация раствора кальция хлорида, если n=1,3870, F= 0,00108 равна А. 50,5% Б. 50% В. 49,6% Г. 50,35% При рефрактометрическом определении концентрация раствора магния сульфата, если n=1,3511, F= 0,00090 равна А. 21% Б. 20,1% В. 19,88% Г. 20,3% 110.Функциональные группы в приведенной формуле: 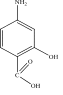 А. Первичная ароматическая аминогруппа, фенольный гидроксил, карбоксильная группа. Б. Первичная ароматическая аминогруппа, спиртовый гидроксил, карбоксильная группа. В. Первичная ароматическая аминогруппа, фенольный гидроксил, сложноэфирная группа. Г. Первичная ароматическая аминогруппа, спиртовый гидроксил, сложноэфирная группа. 111.Функциональные группы в приведенной формуле: 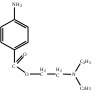 А. Первичная ароматическая аминогруппа, сложноэфирная группа, диэтиламиногруппа. Б. Первичная ароматическая аминогруппа, амидная, сложноэфирная группа . В. Вторичная аминогруппа, третичный атом азота, сложноэфирная группа. Г. Первичная ароматическая аминогруппа, имидная группа, сложноэфирная группа. 112.Функциональные группы в формуле: 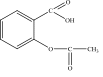

114.Функциональные группы в приведенной формуле: CH3 - CH - COOH │ OH
5. Сложноэфирная группа. 6. Амидная группа. 115.Функциональные группы в приведенной формуле: 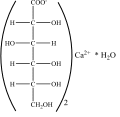 1. Первичная ароматическая аминогруппа А. верно 2,4 2. Спиртовой гидроксил. Б. верно 1,5 3. Фенольный гидроксил. В. верно 3,4 4. Карбоксильная группа. Г. верно 1,3,4 5. Сложноэфирная группа. 116.Функциональные группы в приведенной формуле: 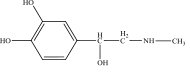 Первичная ароматическая аминогруппа. А. верно 2,3,6 Спиртовой гидроксил. Б. верно 1,5 Фенольный гидроксил. В. верно 3,6 4. Карбоксильная группа. Г. верно 1,3,4 5. Сложноэфирная группа. 6. Вторичная аминогруппа. 117.Функциональные группы в приведенной формуле: 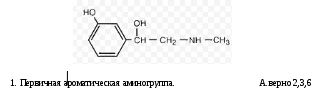 Спиртовой гидроксил. Б. верно 1,5 Фенольный гидроксил. В. верно 3,6 4. Карбоксильная группа. Г. верно 1,3,4 Сложно-эфирная группа. Вторичная аминогруппа. 118.При изготовлении концентратов до 20% допустимая норма отклонений в (%): А. +-1%. Б. +-2%. В. +-3%. Г. +-4%. Допустимые отклонения по приказу МЗ РФ от 26.10.15г. № 751н для концентрированных растворов кальция хлорида 1:2: А. +-0,5%. Б. +-5%. В. +-3%. Г. +-1%. Допустимые отклонения по приказу МЗ РФ от 26.10.15г. № 751н для концентрированных растворов натрия бромида 1:5: А. +-3%. Б. +-2%. В. +-1%. Г. +-4%. Допустимые отклонения по приказу МЗ РФ от 26.10.15г. № 751н для концентрированных растворов кофеин-бензоата натрия 1:10: А. +-5%. Б. +-0,5%. В. +-1%. Г. +-2%. Допустимые отклонения по приказу МЗ РФ от 26.10.15г. № 751н для концентрированных растворов магния сульфата 1:5: А. +-3%. Б. +-2%. В. +-1%. Г. +-4%. Обязательные виды внутриаптечного контроля для лекарственной формы состава: Возьми: Раствора атропина сульфата 1% - 10 мл Дай таких доз №10 Глазные капли А. Письменный, органолептический, контроль при отпуске. Б. Письменный, органолептический, полный химический, контроль при отпуске. В. Письменный, органолептический, полный химический, физический, контроль при отпуске. Г. Письменный, опросный, физический, полный химический. Обязательные виды внутриаптечного контроля для лекарственной формы состава: Возьми: Раствора кислоты хлористоводородной 2% - 100 мл Выдай. Обозначь: По 1 дес. ложке 3 раза в день А. Письменный, органолептический, контроль при отпуске. Б. Письменный, органолептический, полный химический, контроль при отпуске В. Письменный, органолептический, полный химический, физический, контроль при отпуске. Г. В. Письменный, опросный, органолептический, полный химический. 125.Обязательные виды внутриаптечного контроля для лекарственной формы состава: Возьми: Раствора бендазола гидрохлорида 1% - 5 мл Дай таких доз №10 Простерилизуй! А. Письменный, органолептический, контроль при отпуске. Б. Письменный, органолептический, полный химический, контроль при отпуске. В. Письменный, органолептический, полный химический, физический, контроль при отпуске. Г. Письменный, опросный, физический, полный химический. Тип реакции взаимодействия лекарственного вещества, имеющего в структуре первичную ароматическую аминогруппу, с нитритом натрия в кислой среде: А. Окисление. Б. Осаждение. В. Диазотирование. Г. Электрофильное замещение. При выполнении реакции образования азокрасителя используют реактивы: Нитрат серебра, формалин, аммиак. Нитрит натрия, азотную кислоту, щелочной раствор B-нафтола. Нитрат натрия, хлороводородную кислоту, щелочной раствор B-нафтола. Нитрит натрия, кислоту хлороводородную, щелочной раствор B-нафтола. Глютаминовая, аминокапроновая, бензойная, салициловая кислоты содержат функциональную группу: А. Альдегидную. Б. Аминогруппу. В. Карбоксильную. Г. Сложноэфирную. Фенольный гидроксил открывают реактивом: А. Раствора бария хлорида. Б. Раствора меди II сульфата. В. Раствора серебра нитрата. Г. Раствора железа III хлорида. Для количественного анализа лекарственных средств, имеющих в молекуле первичную ароматическую аминогруппу, может быть использован метод: А. Комплексонометрии. Б. Аргентометрии. В. Нитритометрии. Г. Кислотно-основного титрования. Реакция, которая используется при доказательстве подлинности спиртов: А. "Серебряного зеркала". Б. Образования азокрасителя. В. Этерификации. Г. Гидролиза. Реакция, которая используется при доказательстве подлинности альдегидов: А. Гидролиза. Б. Этерификации. В. Образования азокрасителя. Г. "Серебряного зеркала". Реактив, который можно использовать для доказательства наличия в органических лекарственных средствах спиртового гидроксила: А. Кислота уксусная. Б. Раствор хлорида железа III. В. Аммиачный раствор оксида серебра. Г. Реактив Несслера. Реактив, который можно использовать для доказательства наличия в органических лекарственных средствах альдегидной группы: Раствор гидроксида диаминсеребра I. Раствор хлорида железа III. Раствор меди сульфата. Кислота уксусная. Спирт этиловый обнаруживают реакцией: А. С аммиачным раствором оксида серебра. Б. С реактивом Несслера. В. Образования йодоформа. Г. Образования ауринового красителя. Метенамин определяют по реакции: А. С серной кислотой и раствором гидроксида натрия при нагревании. Б. С реактивом Фелинга. В. С раствором сульфата меди. Г. С раствором хлорида бария. Метенамин в лекарственных формах количественно определяют методом: А. Алкалиметрии. Б. Ацидиметрии (прямое титрование). В. Ацидиметрии (обратное титрование). Г. Йодометрии. Наиболее рациональный метод количественного определения ингредиента в лекарственной форме: Возьми: Раствора метенамина 40% - 10 мл. Дай таких доз № 10 в ампулах А. Комплексонометрия. Б. Йодометрия. В. Рефрактометрия. Г. Аргентометрия. В результате взаимодействия декстрозы с реактивом Фелинга при нагревании образуется: А. Красное окрашивание. Б. Осадок кирпично-красного цвета. В. Осадок белого цвета. Г. Сине-фиолетовое окрашивание. Реакция определения подлинности декстрозы выполняется с реактивом: А. Раствором оксалата аммония. Б. Бромной водой. В. Концентрированной серной кислотой. Г. Реактивом Фелинга. В реакцию с раствором гидроксида диаминсеребра I вступает лекарственное средство: Спирт этиловый. Метенамин. Глюкоза. Кальция хлорид. При взаимодействии кальция глюконата с хлоридом железа III образуется окрашивание: А. Оранжевое. Б. Светло-зеленое. В. Красное. Г. Фиолетовое. При определении подлинности дифенгидрамина гидрохлорида используют реакцию: А. Образования азокрасителя. Б. "Серебряного зеркала". В. С реактивом Несслера. Г. Образования оксониевой соли. Реакция кислоты аскорбиновой с раствором серебра нитрата протекает за счет: А. Спиртового гидроксила. Б. Ендиольной группы. В. Карбонильной группы. Г. Карбоксильной группы С раствором оксалата аммония образует белый осадок лекарственное вещество: А. Прокаина гидрохлорид. Б. Аскорбиновая кислота. В. Кальция глюконат. Г. Салициловая кислота. Методом комплексонометрии определяют количественное содержание: А. Формалина. Б. Метенамина. В. Кальция глюконата. Г. Аскорбиновой кислоты. Химические свойства, которые лежат в основе количественного определения глютаминовой кислоты: А. Восстановительные. Б. Окислительные. В. Кислотные. Г. Способность вступать в реакцию замещения на галогены. Методом йодометрии (прямое титрование) определяют количественное содержание в лекарственных формах: А. Глютаминовой кислоты. Б. Аскорбиновой кислоты. В. Кальция глюконата. Г. Метенамина С раствором нитрата серебра серый осадок образует: А. Аскорбиновая кислота Б. Дифенгидрамина гидрохлорид В. Формалин Г. Кальция глюконат В результате взаимодействия димедрола с концентрированной серной кислотой образуется: А. Синее окрашивание. Б. Зеленое окрашивание. В. Желтое окрашивание, переходящее в кирпично-красное. Г. Пурпурно-красное окрашивание. |
