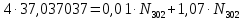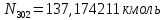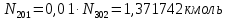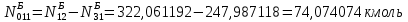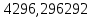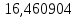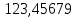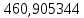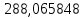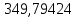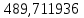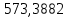Курсовая работа Производство дивинила. ДИВИНИЛ 3 вариант. Производство дивинила
 Скачать 487.42 Kb. Скачать 487.42 Kb.
|
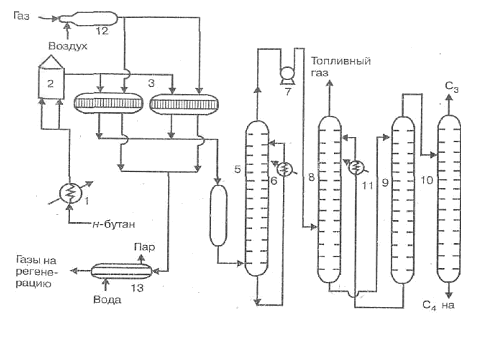
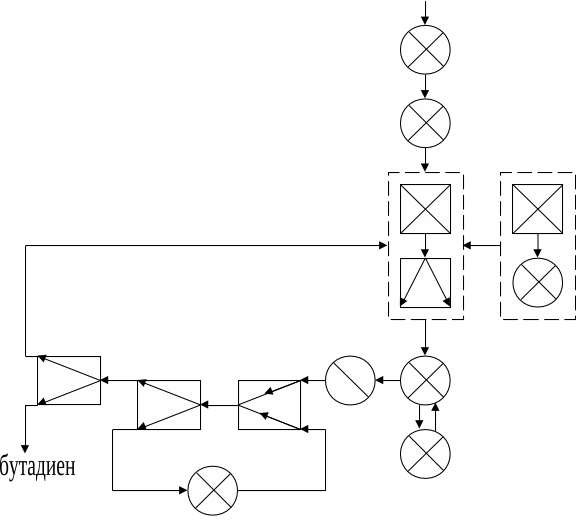
60% бутана и 40% бутиленов, следовательно Описание технологической схемы подогрев Функциональная схема Операторная схема Структурная схема блок смешения; 2- дегидрирование; 3- разделение Расчет материального баланса ХТС Данные для расчета
Составление уравнений 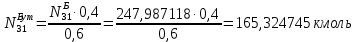 Рассчитываем количество газов после выделения углеводородов С4: Водород: 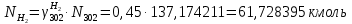 Метан: 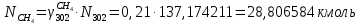 Этен:  Этан: 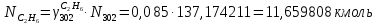 Пропен: 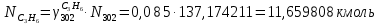 Пропан: 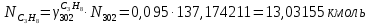 Рассчитываем массы веществ: Исходный н-бутан: 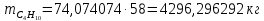 Рециркулирующие газы: 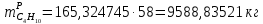 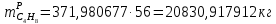 Масса углерода:  Масса газов: 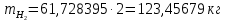 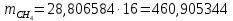 кг кг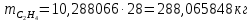 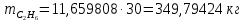 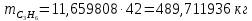 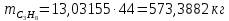 Результаты занесем в таблицу 5. Таблица 5. Материальный баланс химико-технологической системы «Производство дивинила» на 1500 кг дивинила
Поточная диаграмма:    сырье сырье  Подготовка сырья    Синтез отходы    Разделение отходы     рецикл рецикл продукт Расчет технологических показателей Стехиометрический расходный коэффициент по сырью: 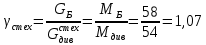 Практический расходный коэффициент по сырью: 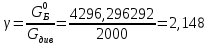 Выход целевого продукта: 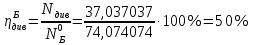 Степень превращения: Будет равна 100%, так как бутан из схемы не выходит 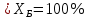 Селективность: 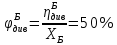 Вывод В настоящее время в промышленности для производства бутадиена используются двух- и одностадийное дегидрирование бутана. Процесс получения бутадиена из этилового спирта является старым, по технико-экономическим показателям, значительно уступающим дегидрированию бутана и выделению бутадиена из пиролизных фракций. Объем производства бутадиена из этилового спирта все время сокращается, в то же время увеличивается выделение бутадиена из пиролизной фракции. Двухстадийным методом бутадиен получается с меньшим количеством примесей и выход бутадиена выше, чем в одностадийном методе получения. Список используемой литературы 1. Аверко-Антонович Л.А. Химия и технология синтетического каучука. - М.: Химия, Колос, 2008. - 357 с. 2. Еремина Е. А. и др. Справочник по химии/ Еремина Е. А., Еремин В. В., Кузьменко Н. Е. — М.: Дрофа, 1996. — 208 с. 3. Кононова Г.Н., Сафонов В.В., Егорова Е.В. Расчет материального баланса химико-технологических систем интегральным методом. — М.:ИПЦ МИТХТ им. М.В. Ломоносова, 2007. —30 с. 4. Мухленов И. П. Основы химической технологии: учебник для студентов ВУЗов / Мухленов И. П., Горштейн А. Е., Тумаркина Е. С., Тамбовцева В. А. под ред Мухленова И. П. — 3-е изд. перераб. и доп. — М.: Высш. школа, 1983. ,-335 с. 5. Оганесян. Э. Т. Руководство по химии: справ. пособие. — М.: Высш. школа, 1987. — 399 с. 6. Сборник заданий и методических указаний по расчету материального баланса химико-технологических производств. Учебно-методическое пособие./Авт.: Брук Л.Г., Егорова Е.Г., Кононова Г.Н., Сафонов В.В., Смирнова С.Н., Чабан Н.Г., Шварц А.Л. Под ред. Брука Л.Г., Кононовой Г.Н., Сафонова В.В. Изд. 3-е, перераб. — М.: ИПЦ МИТХТ им. М.В. Ломоносова, 2008. — 72 с. 7. Соколов Р. С. Химическая технология: учебное пособие для студентов ВУЗов: в 2 томах: Гуманит. Изд. центр ВЛАДОС, 2003.т.2. — 368 с. 8. План развития газо- и нефтехимии России на период до 2030 года, Москва, 2012. 153 с. 9. Краткий справочник физико-химических величин. Издание девятое/ Под ред. А.А. Равделя и А.М. Пономаревой. – СПб.: Специальная Литература, 1998. –232с.: ил. 10. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии. – Л.: Химия, 1987. – 576 с. 11. Варгафтик Н.Б. Справочник по физическим свойствам газов и жидкостей. – М.: Физматгиз, 1963, 108 с. 12. Стэлл Таблицы упругости паров индивидуальных углеводородов, 1949. 13. Айнштейн В.Г., Захаров М.К., Носов Г.А. и др. Общий курс процессов и аппаратов химической технологии. – М.: Логос – Высшая школа, 2002. – 1758 с. 14. Дытнерский Ю.И. Основные процессы и аппараты химической технологии. Пособие по проектированию. М., Химия, 1991. 15. Лащинский А.А., Толчинский А.Р. Основы конструирования и расчета химической аппаратуры. М., Машиностроение, 1970. Приложение. 16. Стандартные кожухотрубные теплообменные аппараты общего назначения. Каталог. М., ЦИНТИХИМНЕФТЕМАШ, 1988. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||





























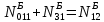
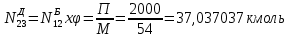
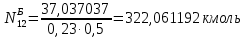
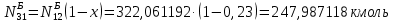
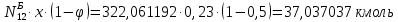
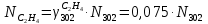
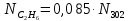
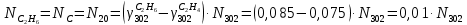
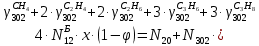 )
)