АНАЛИЗ СУЩЕСТВУЮЩИХ МЕТОДОВ ПРОТИВОКОРРОЗИОННОЙ ЗАЩИТЫ МЕТАЛЛОВ И СПЛАВОВ. Противокоррозионной защиты металлов и сплавов
 Скачать 270.61 Kb. Скачать 270.61 Kb.
|
|
УДК АНАЛИЗ СУЩЕСТВУЮЩИХ МЕТОДОВ ПРОТИВОКОРРОЗИОННОЙ ЗАЩИТЫ МЕТАЛЛОВ И СПЛАВОВ Артём Агасиев, Новочеркасский инженерно-мелиоративный институт им. А. К. Корутнова, Новочеркасск В настоящее время коррозия металлов является одной из важнейших научных и экономических проблем. Поиском новых, более надежных способов защиты от коррозии заняты многие ученые в разных странах мира. Применение высокоэффективных методов противокоррозионной защиты не только позволит защитить окружающую среду, сэкономить природные ресурсы, увеличить эксплуатационный период, уменьшить себестоимость и повысить рентабельность оборудования, но и предотвратить техногенные аварии. Экономические убытки от коррозии металлов огромны. По данным ученых [1] около 10% ежегодной добычи металла расходуется на покрытие безвозвратных потерь вследствие коррозионных процессов. Различают два вида потерь: прямые и косвенные. Прямые – это безвозвратные потери металла, стоимость замены оборудования, металлоконструкций, расходы на противокоррозионную защиту. Косвенные – простой оборудования, снижение мощности, снижение качества продукции, расход металла на утолщение стенок и т.п. Каждый год в производство вводятся постоянно нарастающие объемы металлоизделий и соответственно растут ежегодные убытки, исчисляемые миллионами тонн прокорродировавшего металла и огромными денежными затратами на борьбу с коррозией. Все вышесказанное определяет актуальность исследований в этой области науки. Коррозия металлов – это процесс разрушения металлов вследствие химического или электрохимического взаимодействия их с коррозионной средой. При этом металл переходит в окисленное (ионное) состояние и теряет присущие ему свойства. По механизму коррозионного процесса различают два основных типа коррозии: химическую и электрохимическую (рис. 1) [2]. Газовая коррозия происходит при отсутствии конденсации влаги на поверхности. На практике такой вид коррозии встречается при эксплуатации металлов при повышенных температурах. Атмосферная коррозия относится к наиболее распространенному виду электрохимической коррозии, так как большинство металлических конструкций эксплуатируются в атмосферных условиях. Коррозия, протекающая в условиях любого влажного газа, также может быть отнесена к атмосферной коррозии. Жидкостная коррозия в зависимости от жидкой среды бывает кислотная, щелочная, солевая, морская и речная. По условиям воздействия жидкости на поверхность металла эти виды коррозии получают добавочные характеристики: с полным и переменным погружением, капельная, струйная. Кроме того по характеру разрушения различают коррозию равномерную и неравномерную. Выполнено под руководством Скляренко Е.О. 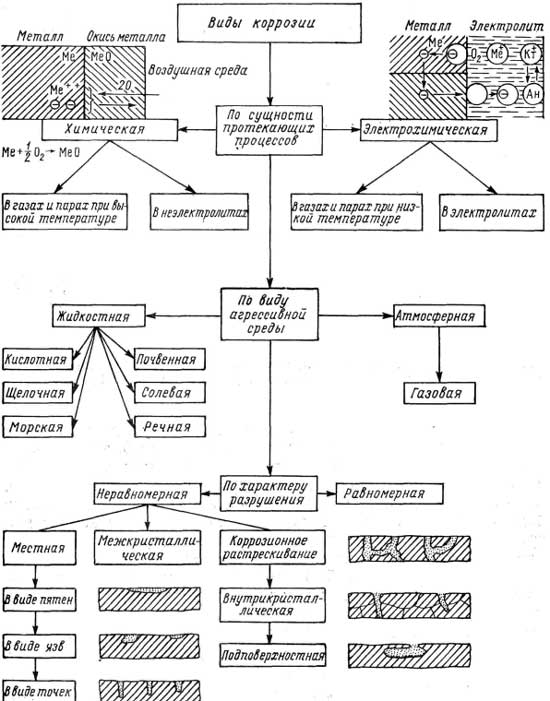 Рисунок 1 - Классификация типов коррозии [2]. На скорость коррозии влияет состав металлов, их механическая и термическая обработка, состояние поверхности, а также среда, температура и характер нагрузки. С повышением температуры скорость коррозионных процессов возрастает. Полированные поверхности окисляются медленнее, так как оксиды равномерны по толщине и поэтому более прочно сцеплены с поверхностью металла. В настоящее время известно более тридцати пяти факторов, влияющих на скорость атмосферной коррозии, основными из которых являются: степень увлажнения металла, состояние поверхности конструкции (пористость, загрязненность), химический состав атмосферы (наличие гигроскопичных и агрессивных продуктов). Основные методы защиты металлов от коррозии можно сгруппировать по следующим направлениям: изоляция металла от коррозионной среды, электрохимические методы защиты (протекторная защита, электрозащита), изменение свойств коррозионной среды и получение коррозионностойких сплавов.  Рисунок 2 - Основные методы защиты от коррозии. [3] Для того чтобы антикоррозионная защита эффективно выполняла свои функции, она должна удовлетворять целому ряду требований: - низкая влаго- и кислородопроницаемость; - высокие механические характеристики; - высокая и стабильная во времени адгезия покрытия к стали; - стойкость к катодному отслаиванию; - хорошие диэлектрические характеристики; - устойчивость покрытия к тепловому старению.  Рисунок 3 - Структура использования основных методов защиты от коррозии [4]. Рассмотрим, в чём заключаются наиболее распространённые методы противокоррозионной защиты металлов и сплавов, применяемые сегодня, насколько они эффективны и какие имеют недостатки. Легирование металлов – эффективный (хотя и дорогой) метод повышения коррозионной стойкости металлов. При легировании в состав сплава вводят компоненты, вызывающие пассивацию металла, т.е. образование на его поверхности защитных плёнок из оксидов легирующих добавок. В качестве таких компонентов применяют хром, никель, вольфрам и т.д. За последние годы в строительной практике наблюдается тенденция роста потребления коррозионно-стойких сталей, в том числе нержавеющих. Защитные покрытия. Согласно общепринятой электрохимической теории, для протекания коррозионного процесса на поверхности металла необходимо наличие влаги и кислорода. Слои, искусственно создаваемые на поверхности металлов для предохранения их от коррозии, называются защитными покрытиями. Защитные слои подразделяются на металлические и неметаллические. Наиболее распространены неметаллические защитные покрытия – эмали, лаки, краски, пластмассы, различные смолы, полимеры. Защитное действие этих покрытий сводится в основном к изоляции металлов от окружающей среды. Достоинство этого способа защиты – простота технологии их нанесения. Недостаток – легко разрушаются из-за хрупкости и растрескивания при тепловых и механических ударах; эти покрытия защищают до тех пор, пока сохраняется их целостность. Лакокрасочные антикоррозионные покрытия особенно популярны в нашей стране, поскольку до 90% конструкций защищается именно так. Отечественная промышленность выпускает разнообразный ассортимент защитных лакокрасочных материалов. Современными тенденциями дальнейшего совершенствования лакокрасочных покрытий являются: - отказ от экологически опасных, токсичных составов, прежде всего органических растворителей; - увеличение процентного содержания твердого вещества; - использование в качестве растворителей синтетических смол, воды или их комбинаций.  Рисунок 4 - Защита от коррозии с помощью неметаллического и металлического покрытия [2] Современные лакокрасочные материалы, применяемые для защиты от коррозии - это масляные краски, битумные, фенолформальдегидные, флоркаучуковые, повинилхлоридные, полиуретановые, алкидные, эпоксидные и некоторые другие составы. В стоимости окрасочных работ, производимых по индустриальной технологии, на материалы приходится 20-45%. Долговечность лакокрасочного покрытия во многом зависит от качества подготовки Эффективность при выборе лакокрасочного покрытия можно определить из отношения стоимости поверхности (степени удаления ржавчины). По характеру поведения металлических покрытий при коррозии их можно разделить на катодные и анодные. К катодным покрытиям относятся покрытия из металлов, потенциалы которых в данной среде имеют большие значения, чем потенциал основного металла. В качестве примеров катодных покрытий на стали можно привести Cu, Ni, Ag, Sn. При повреждении покрытия (или наличии пор) возникает коррозионный элемент, в котором защищаемый материал (Fe) служит анодом и растворятся, а материал покрытия – катодом, следовательно, катодные покрытия могут защищать металл от коррозии лишь при отсутствии пор и повреждений покрытия. Анодные покрытия имеют более отрицательный потенциал, чем потенциал основного металла. В этом случае при нарушении целостности покрытия или возникновении пор в среде, имеющей ионную проводимость, основной металл (Fe) будет катодом возникающего коррозионного элемента и не будет корродировать, а разрушению подвергнется защитное покрытие, например, цинк. Металлические антикоррозионные покрытия, получившие широкое распространение в мировой строительной практике, - это защитные покрытия толщиной 20-200 мкм на основе цинка, алюминия или комбинации Zn-Al, Zn-Ni и некоторые другие. Для получения металлических защитных покрытий применяются различные способы: электрохимический (электролиз – нанесение гальванических покрытий), погружение в расплавленный металл, металлизация (распыление расплавленного металла с помощью струи сжатого воздуха), термодиффузионный (путём диффузии металла в металл при повышенной температуре), химический (восстановление соединений металла с помощью водорода, гидразина и других восстановителей). С помощью газотермического напыления на поверхности металла создается слой из другого металла/сплава, обладающий более высокой стойкостью к коррозии (изолирующий) или наоборот менее стойкий (протекторный). Такой слой позволяет остановить коррозию защищаемого металла. Метод распыления («холодное цинкование») позволяет покрывать изделия любого размера (например, мачты электропередач, резервуары, мостовые металлоконструкции, дорожные ограждения). Электролитическое цинкование ведётся в основном из кислых и щёлочно-цианистых электролитов; специальные добавки позволяют получать блестящие покрытия. Диффузионное цинкование, осуществляемое из паровой или газовой фазы при высоких температурах (375—850 °C), применяется для покрытия труб и др. конструкций. Толщина диффузионного слоя зависит от температуры и времени цинкования и может составлять 0,1—1,5 мм. Одним из перспективных направлений зашиты от коррозии является создание композиционных хромовых покрытий из сульфатно-оксалатных растворов-суспензий Cr(III)с добавками наночастиц SiC, Al2O3, SiO2 и MoS2. [5]. Авторами изучены физико-механические свойства покрытий. Обнаружено, что «чистые » хромовые покрытия из сульфатно-оксалатных растворов Cr(III) уже обладают лучшей износостойкостью, чем осадки из стандартных растворов Cr(VI), а включение частиц Al2O3 и SiC еще более повышает стойкость покрытий к износу. Спектрофотометрическими методами анализа подтверждена высокая стабильность сульфатно-оксалатных растворов Cr(III) при «старении», обеспечивающая неизменность технологических параметров осаждения хромовых покрытий из этих растворов в течение длительного времени. В литературе нередко упоминается о затруднениях в получении качественных осадков хрома из растворов на основе солей Cr(III) вследствие недостаточной их чистоты. Например, при содержании меди более 75 мг/л происходит резкое ухудщение качества покрытия. Также включение данных наночастиц в большом количестве может приводить к охрупчиванию покрытий и ухудшению их механических свойств. Карбидные соединения при этом играют роль катодной присадки, смещая бестоковый потенциал покрытия в область потенциалов пассивного состояния хрома. Выявленная пористость и неравномерность анодного растворения хромовых покрытий, осажденных из оксалатных растворов, является их существенным недостатком [6]. В настоящий момент одним из наиболее перспективных способов защиты металлов от агрессивного воздействия окружающей среды является формирование защитных покрытий посредством метода плазменного электролитического оксидирования (ПЭО). Данный способ модификации поверхности позволяет получать на своей основе покрытия, обладающие целым рядом ценных свойств, одним из которых является высокая коррозионная стойкость. Сущность метода заключается в том, что при пропускании тока через границу раздела металл-электролит при определенных условиях возникает высокая напряженность электрического поля (106–107 В/см), которая приводит к протеканию плазменных микрораздрядов на границе раздела электрод/электролит. В результате действия плазменных микроразрядов формируется слой покрытия, состоящего из окисленных форм элементов металла основы и компонентов электролита. Метод ПЭО позволяет создавать гетерооксидные покрытия на металлах и сплавах с определенным составом, структурой, морфологией и обладающих практически важными характеристиками. [7]. Недостатками данного способа являются сравнительно низкая коррозионная устойчивость получаемых покрытий на единицу толщины слоя и сложный, экологически опасный состав электролита, включающего фториды щелочных металлов. Ингибирование. Ингибиторы коррозии – вещества, которые, находясь в коррозионной среде в достаточной концентрации, сильно замедляют либо вообще прекращают коррозионное разрушение металла. Ингибитором коррозии может быть как одно соединение, так и смесь нескольких. Отличительная черта метода защиты конструкций от коррозии с помощью ингибиторов - это возможность при небольших капитальных затратах замедлить их коррозионное разрушение, даже если эти конструкции или оборудование давно находились в эксплуатации. Кроме того, введение ингибиторов в любой точке технологического процесса может оказать эффективное защитное действие и на оборудование последующих технологических стадий (подготовки и транспортировки продукции). Ингибиторная защита может быть применена как самостоятельный метод защиты от коррозии, а также в сочетании с другими методами - как комплексная защита. Адсорбционные ингибиторы коррозии адсорбируются на поверхности защищаемого изделия, образуя пленку, и тормозят электрохимические реакции. Иногда достаточно образование тонкой мономолекулярной пленки. Адсорбционными ингибиторами чаще всего являются ПАВ (поверхностно-активные вещества), а также органические соединения. При воздействии на изделие они дополнительно усиливают защитные свойства оксидной пленки. Пассивирующие ингибиторы коррозии играют важную роль при образовании на поверхности металла защитной пленки, которая пассивирует ее. Пассиваторами чаще всего являются неорганические соединения, обладающие окислительными свойствами (нитриты, молибдаты, хроматы). При обработке поверхности этими веществами коррозионный потенциал сдвигает эффективными, чем большая часть непассивирующих. Неорганические ингибиторы коррозии используются чаще всего. К ним относятся некоторые пассиваторы, катодные, анодные, пленкообразующие ингибиторы и т.д. Ингибирующий эффект таких соединений можно объяснить их составом. Некоторые анионы (PO43-, NO2-, CrO42-, SiO32-, Cr2O72-), а также катионы (Ni2+, Са2+, As3+, Sb3+, Zn2+, Bi3+) способствуют уменьшению скорости коррозионного процесса. Некоторыми учеными предложено в качестве ингибиторов коррозии использование триалкоксиланов [8]. Показано, что наиболее эффективные из них формируют на поверхности стали многослойные адсорбционные слои из силоксанов (Me-O-Si-O-Si-O-Si-), продуктов олигомеризации с сетчатой структурой, и адсорбционные слои, связанные с металлом органофункциональной группой X: [Ме-X-R1(OR) 3_ n], где n - число гидролизованных алкоксигрупп. По сравнению с традиционными процессами фосфатирования стали предлагаемый способ включает меньшее количество стадий подготовки металлической поверхности. Однако в некоторых условиях гидролизованные триалкоксиланы конденсируются между собой с образованием гелеобразных осадков, что делает раствор непригодным для формирования покрытия. В связи с тем, что составы импортных растворов триалкоксиланов и режимы используемых процессов не раскрываются, российскими учеными осуществляется разработка импортозамещающей технологии нанесения кремнийорганических покрытий [9] . Наиболее распространенный недостаток органических ингибиторов коррозии - это повышенное содержание смол, которые в процессе эксплуатации оборудования оседают на внутренних поверхностях, ухудшая теплопередачу, а иногда и нарушают работу контрольно-измерительных приборов Перспективным направлением борьбы с коррозией видится введение ингибиторов коррозии в состав грунтовок, наносимых перед покрытием лакокрасочными материалами. Это не только может улучшить защитные свойства грунтовок, но и создать новый вид лакокрасочных материалов - грунт-эмали, сочетающие достоинства как грунтовок, так и эмалей, т. е. избежать применения специальных грунтовок и получить покрытие с удовлетворительным внешним видом и высокими показателями физико-механических и защитных свойств. Используемые в рецептурах ингибиторы коррозии можно разделить на две группы: водорастворимые и маслорастворимые. Из водорастворимых ингибиторов, используемых в рецептурах водно-растворимых грунтовок, следует упомянуть в первую очередь хромовокислый гуанидин. Для снижения стоимости и уменьшения токсичности данный ингибитор рекомендуется применять совместно с фосфатом цинка в соотношении 1:75 (соответственно). Круг маслорастворимых ингибиторов весьма широк; ими могут быть разнообразные амины, аминокислоты, алкалоиды, сульфокислоты, тиосоединения и др. Предложено введение в состав грунтовок модификаторов, способствующих переводу оксидов железа (ржавчины) и прокатной окалины в нерастворимые, плотно сцепленные с поверхностью металла соединения, не нарушающие адгезию и коррозионную устойчивость покрытия. В качестве таких модификаторов используются производные фосфорной кислоты и некоторые дубильные вещества, например, таннин. Новым и весьма интересным направлением является использование в рецептурах грунтовок так называемых комплексонов - органических хелатообразующих соединений, содержащих в молекуле способные к координации атомы N,S и (или) P, а также карбоксильные, фосфоновые, фосфонистые и др. группы, и образующие, в частности, с ионами трехвалентного железа устойчивые, нерастворимые в воде комплексы [10]. Московская фирма "Браско Интер" производит состав СФ-1 - фосфатирующий модификатор ржавчины, который может использоваться в различных агрессивных средах (кислоты, щелочи, растворы солей) в широком температурном диапазоне (от -60оС до 600оС). Данный состав, наносимый тонким слоем (2,8-3,5 г/кв. м), можно наносить как на черный металл, так и на оцинкованную сталь, при этом покрытие не только не препятствует проведению сварочных работ, но и улучшает качество сварочного шва. Относительно высокая цена пока не позволяют использовать предлагаемый состав повсеместно. Деаэрация. Здесь применяется специальная обработка электролита или среды, в которой находится защищаемая конструкция. Вода, поступающая в котельные установки, подвергается деаэрации – удалению растворённого воздуха. Введение в электролит ингибиторов, их адсорбция на защищаемой детали резко замедляет процесс коррозии. В последние годы широко применяют летучие парофазные игибиторы. Их используют для защиты машин, аппаратов и других металлических изделий во время их эксплуатации в воздушной атмосфере, при перевозке и хранении. Летучие ингибиторы вводятся в контейнеры, в упаковочные материалы или помещаются в непосредственной близости от рабочего агрегата. Благодаря достаточно высокому давлению паров летучие ингибиторы достигают границы раздела металл – воздух и растворяются в плёнке влаги, покрывающей металл. Далее они адсорбируются на поверхности металла [11] . Недостатком летучих ингибиторов является высокая летучесть, резкий запах и возможность испарения ингибитора в атмосферу рабочей зоны. Рациональное конструирование изделий. Рациональное конструирование изделий должно исключать наличие или сокращать число и размеры особо опасных с точки зрения коррозии участков в изделиях или конструкциях (сварных швов, узких щелей, контактов разнородных по электродным потенциалам металлов и др.), а также предусматривать специальную защиту металла этих участков от коррозии. Контакт с металлами и неметаллами имеет большое значение для оценки опасности коррозии. В частности, при конструировании следует учитывать опасность контактной коррозии, в связи с чем, нельзя без соответствующей изоляции соприкасающихся поверхностей сочетать в конструкции металлы, существенно отличающиеся по величине потенциала. Важно учитывать использование в конструкции различных неметаллических материалов, в том числе теплоизоляционных, электроизоляционных и др. Известно, что некоторые из этих материалов, например войлок, асбест, древесина, могут впитывать и удерживать влагу и, таким образом, быть очагами усиленной коррозии. Скопление влаги в различных элементах конструкции способствует развитию коррозии. Поэтому при создании различных конструкций предусматривают возможность проветривания полостей, наличие дренажных отверстий и др. Исключительно опасно в коррозионном отношении наличие щелей и зазоров. На изделии не должно быть различных углублений, канавок и пазов, в которых может скапливаться влага. Элементы конструкции должны быть по возможности обтекаемыми; это облегчает испарение влаги. Электрохимическая защита. Этот метод противокоррозионной защиты позволяет предотвратить коррозионные и коррозионно-механические разрушения в водной среде (морская, речная, озерная вода) практически всех конструкционных металлических материалов, применяемых в гидротехнических сооружениях, судостроении, мелиорации и других отраслях, в том числе после различных технологических операций их обработки (сварки, гибки, правки и пр.). Различают две разновидности электрохимической защиты: - при питании анодных заземлителей от внешнего источника тока (выпрямителя, генератора) защита называется катодной; - при подключении к защищаемой конструкции анода из металла с более электроотрицательным электродным потенциалом (например, цинка) защита называется протекторной. Защищаемая от коррозии конструкция подвергается поляризации с помощью протектора, что приводит к смещению потенциала конструкции в отрицательную сторону и подщелачиванию слоя электролита, непосредственно прилегающего к металлу. Благодаря подщелачиванию на поверхности металла образуется осадок гидроокиси и карбонатов кальция и магния, похожий на накипь. Эти гидроокиси (карбонатные осадки) создают особые условия на поверхности металла: с одной стороны, они экранируют поверхность, а с другой - затрудняют диффузию кислорода, так как увеличивают толщину защитного слоя. Широкое распространение протекторной защиты объясняется ее высокой технико-экономической эффективностью, доступностью, простотой и надежностью в процессе эксплуатации. За весь период срока службы протектора защита не требует обслуживания. Для изготовления МО и СК гидротехнических сооружений применяют углеродистую сталь или низколегированную сталь, для защиты которой рекомендуется применять протекторы, изготовленные на основе цинка, алюминия и магния. Эти сплавы имеют высокие физико-химические характеристики, обеспечивающие возможность создания эффективных и долговечных систем защиты от коррозии без применения лакокрасочных покрытий. Совмещение протекторной защиты с использованием лакокрасочных покрытий позволяет значительно снижать расход протекторов и значительно увеличивать срок службы защиты [12]. В настоящее время существует большое количество методов защиты от коррозии. Однако, несмотря на то, что в нашей стране накоплен большой опыт проведения мероприятий с целью определения скорости протекания коррозионных процессов и способов защиты от коррозии, и ведутся разработки в области специализированных материалов и технологий, обеспечивающих большую степень защиты от коррозии, на данный момент нет универсального метода борьбы с этой проблемой. Список использованных источников: Андреев И.Н. Коррозия металлов и их защита. – Казань: Татарское книжное издательство, 2001. Основы электрохимической коррозии металлов и сплавов: учеб. пособие / Л.Г. Петрова, Г.Ю. Тимофеева, П.Е. Де- мин, А.В. Косачев; под общ. ред. Г.Ю. Тимофеевой. – М.: МА- ДИ, 2016. http://900igr.net/kartinki/khimija/Neorganicheskaja-khimija/148-Zaschita-ot-korrozii.html http://900igr.net/datas/khimija/Neorganicheskaja-khimija/0090-090-Zaschita-ot-korrozii.jpg Защитная способность композиционных хромовых покрытий из сульфатно-оксалатных растворов-суспензий Cr(III) с добавками наночастиц SiC, Al2O3, SiO2 и MoS2.Поляков Н.А., Абрашов А.А., Паутов Д.В., Данилов А.И. журнал Практика противокоррозионной защиты. 2013г, № 4 (70). Гасанова о. А. Электроосаждение покрытий на основе хрома из растворов CR(III), содержащих органические добавки и дисперсную фазу. диссертация на соискание ученой степени кандидата технических наук. Саратов 2016г. Осадчая А. А., Ползун У. А. Методы борьбы с коррозией. Плазменное электролитическое оксидирование как способ формирования антикоррозионных покрытий // Молодой ученый. — 2017. — №2.1. Исследование замещенных триалкоксисиланов в качестве ингибиторов коррозии Иванов Е.С., Ларьков А.П., Клюев А.Л. журнал Практика противокоррозионной защиты, 2013, № 3 Н. В. Кулюшина, И. А. Козлов, А. Е. Кутырев, Т. А. Ваграмян. Адгезионные покрытия на основе триалкоксиланов для алюминия и стали. Электронный журнал «Труды ВИАМ» 2015 г. № 8 СОСТАВ СФ-1 ДЛЯ ПОДГОТОВКИ ПОВЕРХНОСТИ. А. Э. Григорян, генеральный директор ЗАО «БРАСКО-ИНТЕР». Журнал «Промышленная окраска». 2011г. № 4. Новый метод защиты металлов от атмосферной коррозии. Лучкин А.Ю., Гончарова О.А., Андреев Н.Н., Кузнецов Ю.И. журнал Практика противокоррозионной защиты, № 4,2017г. Современные методы защиты строительных конструкций зданий, сооружений и технологического оборудования от коррозии. (ООО «Гипрогазоочистка инжиниринг»). СБОРНИК ДОКЛАДОВ МЕЖОТРАСЛЕВОЙ КОНФЕРЕНЦИИ «АНТИКОРРОЗИОННАЯ ЗАЩИТА - 2012». Москва |
