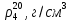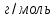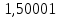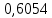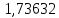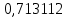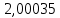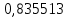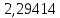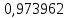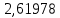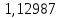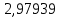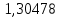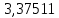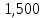РГР. Расчет ректификационной колонны по дисциплине Процессы и аппараты химической технологии
 Скачать 0.6 Mb. Скачать 0.6 Mb.
|
1 Теоретическая частьРектификация (от по поздне лат. rectificatio – выпрямление, исправление), разделение жидких смесей на практически чистые компоненты, отличающиеся температурами кипения, путем многократных испарения жидкости и конденсации паров. В этом основное отличие ректификации от дистилляции, при которой в результате однократного цикла частичного испарения-конденсации достигается лишь предварительное (грубое) разделение жидких смесей. Для ректификации обычно используют колонные аппараты, называемые ректификационными колоннами, в которых осуществляется многократный контакт между потоками паровой и жидкой фаз. Движущая сила ректификации – разность между фактическими (рабочими) и равновесными концентрациями компонентов в паровой фазе, отвечающими данному составу жидкой фазы. Парожидкостная система стремится к достижению равновесного состояния, в результате чего пар при контакте с жидкостью обогащается легколетучими (низкокипящими) компонентами (НКК), а жидкость - труднолетучими (высококипящими) компонентами (ВКК). Поскольку жидкость и пар движутся, как правило, противотоком (пар – вверх, жидкость – вниз), и при достаточно большой высоте колонны, в ее верхней части можно получить практически чистый целевой компонент. Ректификацию можно осуществлять непрерывно или периодически. Для непрерывной ректификации применяют колонны, состоящие из двух ступеней: верхняя – укрепляющая (в ней пар укрепляется, т.е. обогащается НКК) и нижней – отгонная (где происходит исчерпывание жидкой смеси, т. е. извлечение НКК и обогащение ее ВКК). При периодической ректификации в колонне производится только укрепление пара. Различают ректификации бинарных (двухкомпонентных) и многокомпонентных смесей. Рассмотрим сущность процесса ректификации на примере разделения двухкомпонентной смеси при наличии теоретических тарелок. На каждую, например, n-ую тарелку с вышележащей тарелки стекает жидкость в количестве gn1 , при температуре t n1 и 6 с нижерасположенной тарелки поднимаются пары в количестве Gn1 , при температуре t n1 . При теоретическом контакте на n-ой тарелке система достигает состояния равновесия, при этом пары Gn и жидкость gn будут иметь одинаковую температуру tn. Для осуществления процесса ректификации температурный режим в колонне должен быть таким, чтобы температура убывала в направлении движения потока паров (возрастала в направлении движения потока жидкости), т. е. tn1 tn tn1. При контакте фаз в результате массообменных процессов температура паровой фазы снизится, часть паров конденсируется и концентрация НКК в них возрастёт, а температура жидкой фазы увеличится, часть её испарится, и концентрация НКК в ней уменьшится. Изменение состава паров и жидкости удобно проследить по изобарным температурным кривым. На n-й теоретической тарелке в результате контакта концентрация НКК в паровой фазе увеличилась на величину yn yn1 , а в жидкой фазе уменьшилась на величину xn+1 xn , тем самым концентрация ВКК в жидкости увеличилась. При ректификации массообмен протекает в обоих направлениях. Если теплота испарения и теплоёмкости разделяемых компонентов различаются незначительно, то массы парового и жидкостного потоков по высоте аппарата изменяются мало. Очевидно, что при многократном повторении таких противоточных контактов на верху аппарата можно получить пары, обогащенные в любой степени НКК y 1,0, а снизу отбирать жидкость, обогащенную ВКК x 0. Подобное контактирование осуществляется до тех пор, пока пар на верху колонны не приобретает заданного состава по НКК yD, а жидкость внизу колонны не достигнет состава xW . Подобное контактирование фаз по схеме противотока в целом по аппарату осуществляется в ректификационных колоннах, заполненных различными контактными устройствами: тарелками, насадками и т.п. 2 Расчетная частьЦель: Рассчитать основные показатели работы и размеры ректификационной колонны для разделения бинарной смеси бензол-толуол .Исходные данные. Расчет основных показателей работы и размеров ректификационной колонны производим по следующим исходным данным: Давление верха колонны, ата π =1,50 атм; Мольная доля НКК в сырье x'F =0,48; Мольная доля НКК в дистилляте y'D=0,98; мольная доля НКК в остатке x'W=0,01; мольная доля отгона е'=0,57; коэффициент избытка тепло подвода n'=1,40; производительность колонны F=36 т/ч. Бензол – НКК, т. е. более легколетучий компонент. Толуол – ВКК, т. е. менее легколетучий компонент. 2.1 Построение зависимости давления насыщенных паров от температуры. Для построения кривых изобар необходимо определить крайние точки кривых, т.е. температуры кипения НКК и ВКК при заданном давлении в колонне 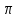 . . Уравнение Антуана: 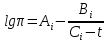 (1) (1)где 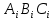 – постоянные Антуана; – постоянные Антуана;Представим эту формулу в следующем виде (2) и рассчитаем 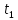 и и 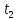 . .Коэффициенты Антуана подберём из табл. 2. Таблица 2 –Значения Ai, Bi, Ci, 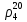 , M для бензола и толуола. , M для бензола и толуола.
Рассчитаем температуру кипения бензола tкипБ и толуола tкипТ по формуле: 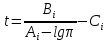 (2) (2)Температура кипения бензола 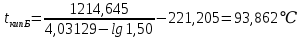 Температура кипения толуола 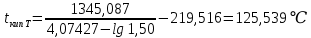 Таким образом, в данной бинарной системе низкокипящим компонентом является бензол, высококипящим – толуол. Полученный интервал температур разбиваем на 6 равных интервалов, и при данных температурах рассчитываются давления насыщенных паров компонентов РБ и РТ по уравнению (3), полученные данные приведем в таблице 3. Температуры будут меняться со следующим шагом: 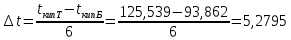 t1 = 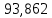 °С, °С,t2 = 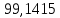 °С, °С,t3 = 104,421°С, t4 = 109,7005°С, t5 = 114,98°С, t6 = 120,2595°С, t7 = 125,539°С, 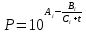 . (3)При температуре t1 = 93,862 °С: . (3)При температуре t1 = 93,862 °С: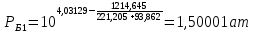 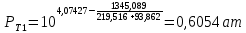 При температуре t2= 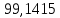 °С: °С: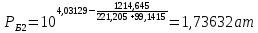 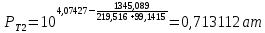 При температуре t3=104,421°С: 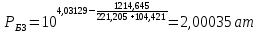 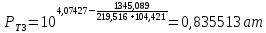 При температуре t4=109,7005°С 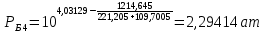 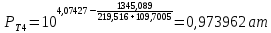 При температуре t5=114,98 С 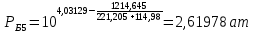 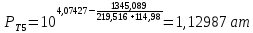 При температуре t6=120,2595 С 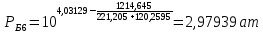 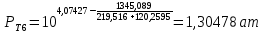 При температуре t7=125,539°С: 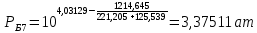 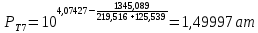 Таблица 3 – Зависимость между температурой t и давлением насыщенных паров
По полученным данным строим график зависимости давления насыщенных компонентов от температуры (рис. 1). Рисунок 1 -– График зависимости давления насыщенных паров от температуры |