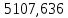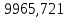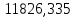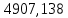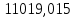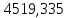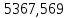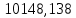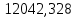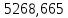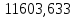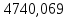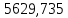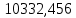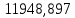РГР. Расчет ректификационной колонны по дисциплине Процессы и аппараты химической технологии
 Скачать 0.6 Mb. Скачать 0.6 Mb.
|
2.3 Построение энтальпийной диаграммыНайдем значение энтальпии в исследуемых точках, используя следующие эмпирические уравнения: 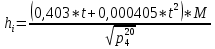 , ккал/кмоль, (11) , ккал/кмоль, (11)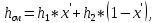 ккал/кмоль. (12) ккал/кмоль. (12)Для паровой фазы: 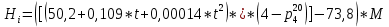 , ккал/кмоль, (13) , ккал/кмоль, (13)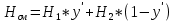 , ккал/кмоль. (14) , ккал/кмоль. (14)Энтальпийная диаграмма в координатах «содержание низкокипящего компонента в жидкой и паровой фазах – энтальпия жидкой и паровой фаз» включает линию (кривую) энтальпии кипящей жидкости и линию энтальпии равновесных паров. Отрезки линий, соединяющих точки энтальпий равновесных фаз, называются конодами. Крайние коноды соответствуют чистым компонентам, они занимают вертикальное положение, остальные коноды располагаются под разными углами к оси абсцисс. При температуре t1 =93,862 °С; 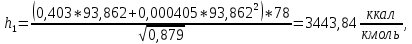 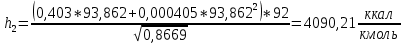 , ,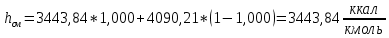 , ,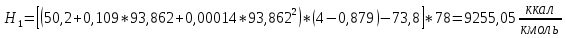 , ,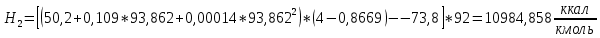 , ,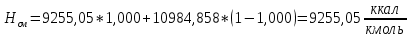 . .При температуре t2 = 99,1415°С 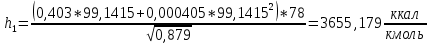 , ,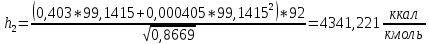 , ,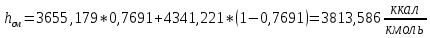 , ,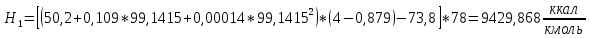 , ,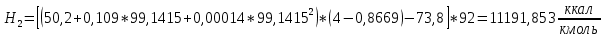 , ,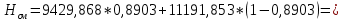 9623,158 9623,158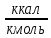 . .При температуре t3 =104,421°С 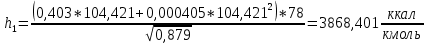 , ,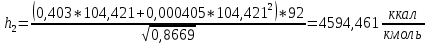 , ,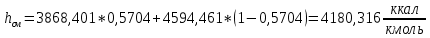 , ,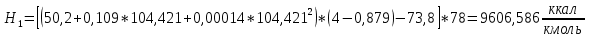 , ,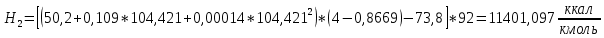 , ,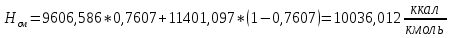 . .При температуре t4 = 109,7005°С 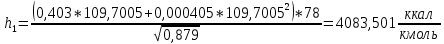 , ,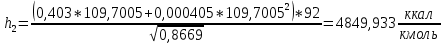 , ,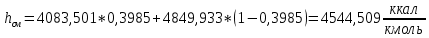 , ,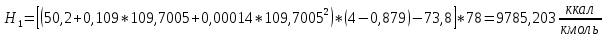 , ,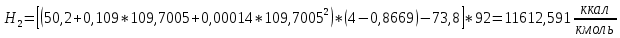 , ,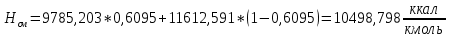 . .При температуре t5 = 114,98°С 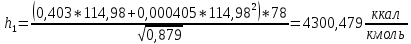 , ,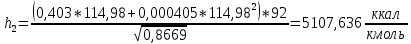 , ,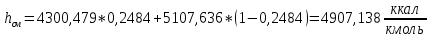 , ,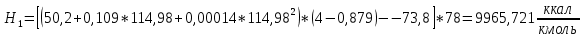 , ,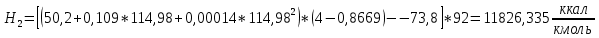 , ,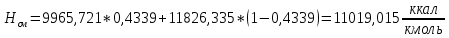 . .При температуре t6 = 120,2595°С 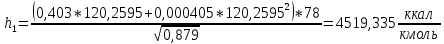 , ,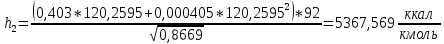 , ,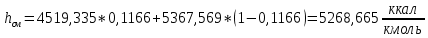 , ,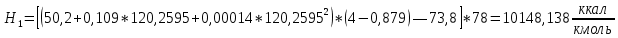 , ,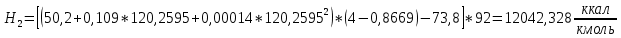 , ,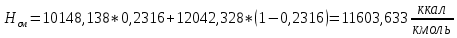 . .При температуре t7 = 125,539°С 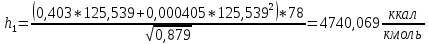 , ,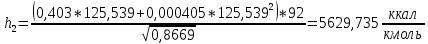 , ,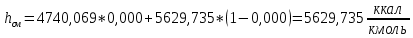 , ,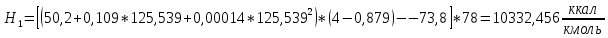 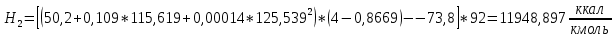 , ,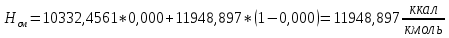 . .Результаты расчета энтальпий приведены в таблице 5. Таблица 5 – Результаты расчета энтальпий в жидкой и паровой фазах
Из результатов расчета видно, что с ростом температуры растут значения энтальпий каждого из компонентов и смеси как в жидкой, так и в паровой фазах. По данным таблицы 5 строим энтальпийную диаграмму. Рисунок 4 – Энтальпийная диаграмма |