Ректификационная колонна (метанол-вода). рект колонна 1 (метанол-вода). Расчёт ректификационной колонны
 Скачать 0.52 Mb. Скачать 0.52 Mb.
|
|
ПГТУ Кафедра МАПП Пояснительная записка к курсовой работе по курсу ПАХТ Тема: Расчёт ректификационной колонны Выполнил: студент группы АТП-01-1 Васильев А.Г. Проверил: Долганов В.Л. Пермь, 2004. Оглавление Введение 3 1. Технологическая схема установки 4 2. Задание на курсовое проектирование 5 3. Материальный баланс ректификационной колонны 6 4. Определение скорости пара и диаметра колонны 10 5. Гидравлический расчет тарелок 12 6. Определение числа тарелок и высоты колонны 15 7. Расчет условного диаметра штуцеров. 17 7.1. Штуцер для отвода дистиллята. 17 7.2. Штуцер для подвода флегмы. 17 7.3. Штуцера для входа парожидкостной смеси. 17 7.4. Штуцер для подвода исходной смеси. 17 7.5. Штуцер для отвода кубового остатка. 18 Выводы 19 Список используемой литературы 20 ВведениеОдним из наиболее распространенных методов разделения жидких однородных смесей, состоящих из двух или большего числа компонентов, является ректификация. Ректификация известна с начала XIX века как один из важнейших технологических процессов главным образом спиртовой и нефтяной промышленности. Ректификация представляет собой процесс многократного частичного испарения жидкости и паров. Процесс осуществляется путем контакта потоков паров и жидкости, имеющих различную температуру, и проводится обычно в колонных аппаратах. При каждом контакте из жидкости испаряется преимущественно низкокипящий компонент, которым обогащаются пары, а из паров конденсируется преимущественно высококипящий компонент, переходящий в жидкость. Такой двусторонний обмен компонентами, повторяемый многократно, позволяет получить, в конечном счете, пары, представляющие собой почти чистый НКК. Эти пары после конденсации в отдельном аппарате дают дистиллят и флегму – жидкость для орошения колонны и взаимодействия с поднимающимися парами. Пары получают путем частичного испарения снизу колонны остатка, являющегося почти чистым ВКК. Процесс ректификации может осуществляется периодически или непрерывно. В ректификационных установках используют главным образом аппараты двух типов: насадочные и тарельчатые. Кроме того, для ректификации под вакуумом применяют: пленочные и роторные колонны. Ректификационные колонны снабжены теплообменными устройствами – кипятильником (кубом) и дефлегматором. Кроме того, для уменьшения потерь тепла в окружающую среду ректификационные аппараты покрывают тепловой изоляцией. Если сравнивать тарельчатые и насадочные ректификационные аппараты, то отмечено, что тарельчатая колонна обладает значительно большей производительностью по сравнению с насадочной. Преимущество тарельчатой колонны так же в том, что насадочные колонны целесообразно использовать при диаметре не более 0,8 м. При дальнейшем увеличении диаметра ухудшается равномерное распределение флегмы по насадке, образуются каналы, по которым преимущественно устремляется флегма, и эффективность колонны резко снижается. В данном курсовом проекте процесс ректификации проводится под атмосферным давлением. Под вакуумом процесс ректификации проводится для разделения высококипящих жидких смесей. Повышенное давление – для разделения смесей находящихся в газообразном состоянии. Атмосферное давление применяют при разделении смесей, имеющих температуру кипения от 30 0С до 150 0С. 1. Технологическая схема установки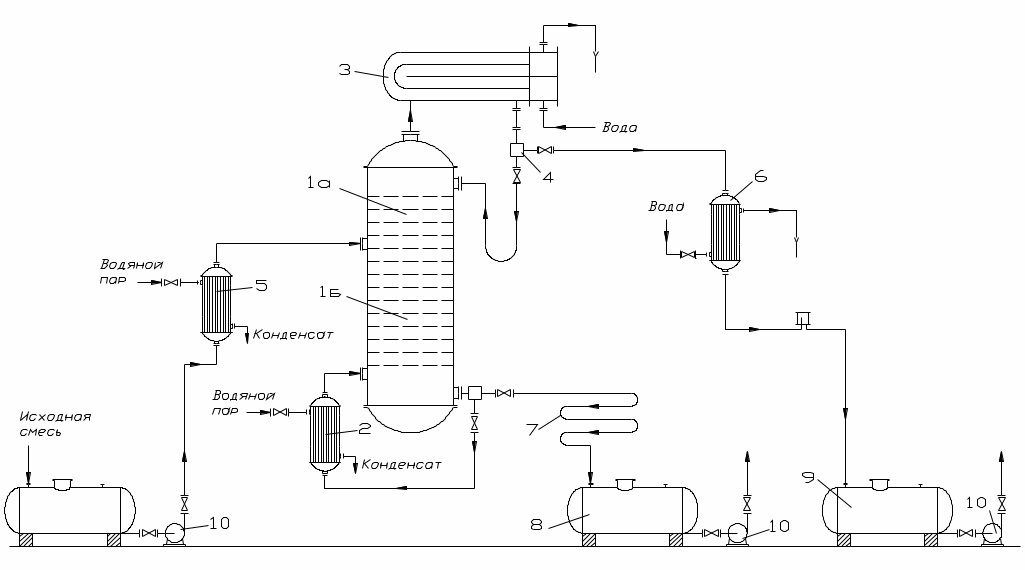 Рис. 1. Схема непрерывно действующей ректификационной установки. 1 – ректификационная колонна (а – укрепляющая часть, б – исчерпывающая часть); 2 – кипятильник; 3 – дефлегматор; 4 – делитель флегмы; 5 – подогреватель исходной смеси; 6 – холодильник дистиллята (или холодильник-конденсатор); 7 – холодильник остатка (или нижнего продукта); 8, 9 – сборники; 10 – насосы. 2. Задание на курсовое проектированиеРассчитать и запроектировать тарельчатую ректификационную колонну для смеси: метиловый спирт-вода Дано: Расход питания – 11 т/ч xF=42% xD=89% xW=4% Предоставить: Пояснительную записку (технологическая схема установки, расчёт материального и теплового балансов, выбор типа, конструкции и краткая характеристика аппарата, расчёт основных размеров аппарата и его гидравлического сопротивления). Чертежи общего вида аппарата, виды и разрезы. 3. Материальный баланс ректификационной колонныМатериальный баланс установки составляем для определения расходов флегмы и дистиллята, а так же для определения флегмового числа. Физико-химические свойства веществ, входящих в исходную смесь: Метиловый спирт: температура кипения: 64,7 0С; плотность (при температуре от 0 до 20 0С): 800 кг/м3; мольная масса: 32 кг/кмоль; давление насыщенного пара (при температуре 20 0С): 97,7 мм. рт. ст. вода: температура кипения: 100 0С; плотность (при температуре от 0 до 20 0С): 1000 кг/м3; мольная масса: 18 кг/кмоль; Пусть, согласно рис. 2, в колонну поступает F кмоль исходной смеси, состав которой хF мольных долей НКК. Сверху из колонны удаляется G кмоль, образующегося после конденсации флегма и дистиллят. Количество получаемого дистиллята – Р кмоль, его состав хР мольных долей НКК. На орошение колонны возвращается флегма в количестве Ф кмоль, причем ее состав равен составу дистиллята (хФ = хР мольных долей). Снизу из колонны удаляется W кмоль остатка состава хW мольных долей НКК. 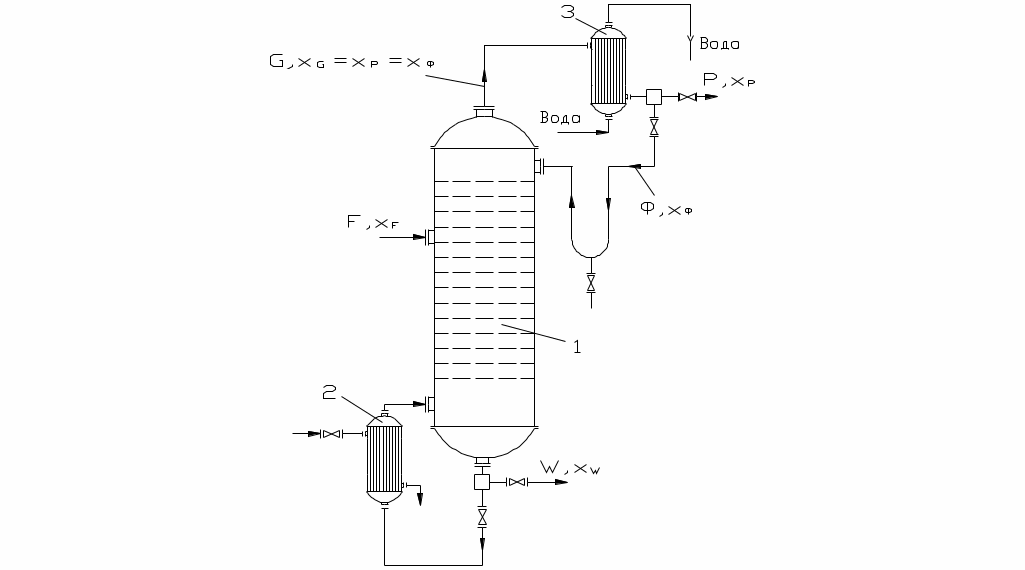 Рис. 2. К составлению материального баланса ректификационной колонны. 1 – колонна; 2 – куб; 3 – дефлегматор. Расчет будем производить по НКК. В данном процессе им является метиловый спирт. Уравнения материального баланса колонны будут иметь вид: 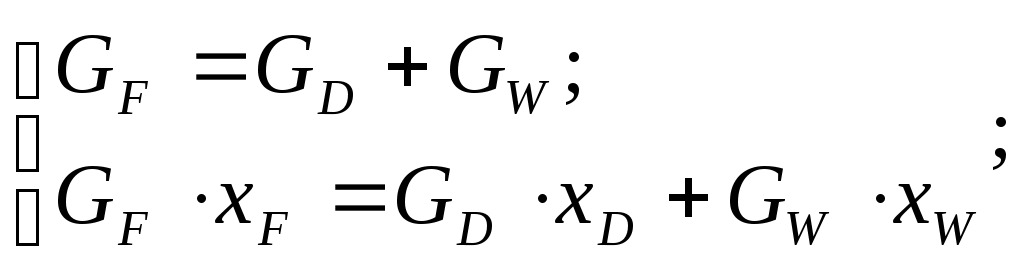 (4.1) (4.1)Обозначим массовый расход дистиллята через GD кг/ч, расход кубового остатка через GW кг/ч. Тогда из уравнений материального баланса запишем: Находим GD = 4918 кг/ч, GW = 6082 кг/ч. Запишем молярные массы компонентов. Выразим концентрации питания – хF, дистиллята – хD и кубового остатка – хW в мольных долях. Питание: 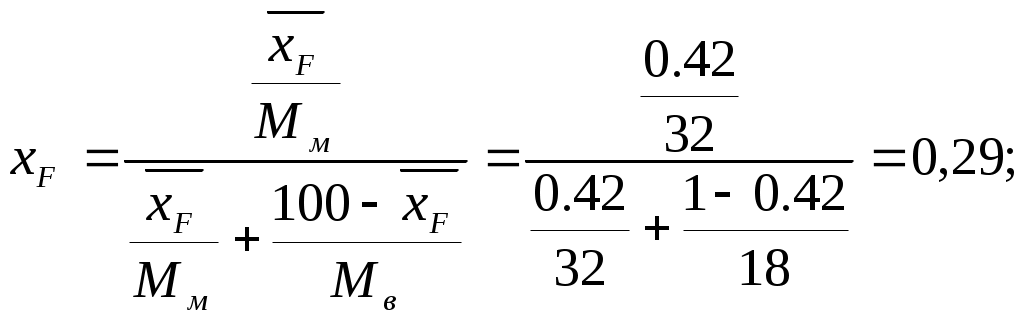 (4.3) (4.3)Дистиллят: 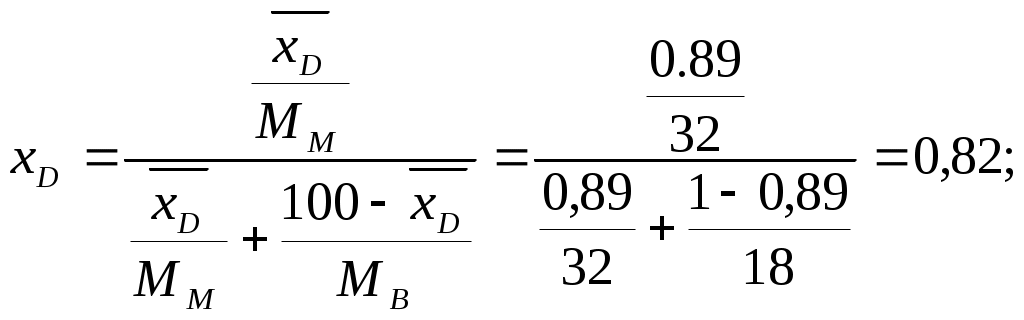 (4.4) (4.4)Кубовый остаток: 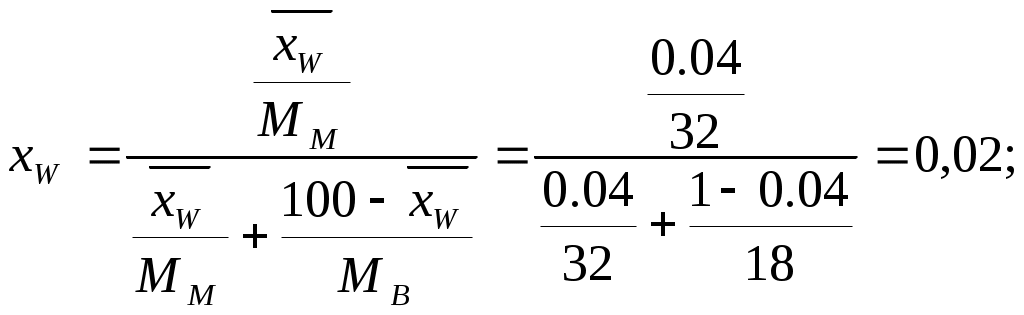 (4.5) (4.5)Определяем мольный расход питания: Строим кривую равновесия (см. рис. 3) по данным, приведенным в таблице 1: Зависимость массовой доли воды в жидкости и паре от температуры Таблица 1
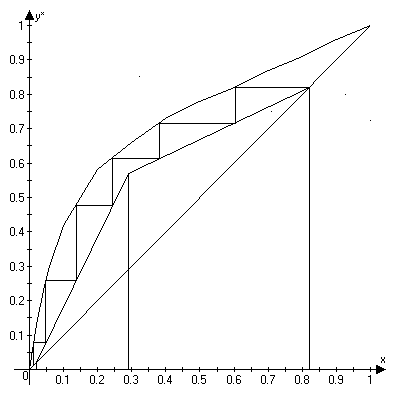 Рис. 3. y* – x диаграмма. 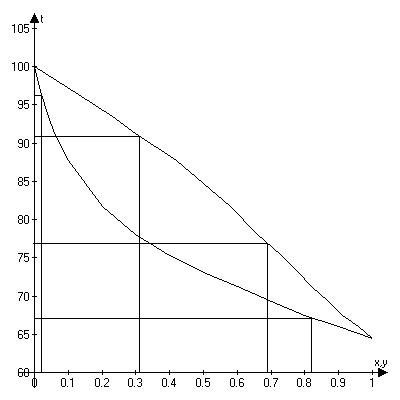 Рис. 4. t – х, у диаграмма. Как видно из рис. 3 кривая равновесия перегибов не имеет. Определяем минимальное число флегмы: где yF* = 0,655 – мольная доля метилового спирта в паре, равновесном с жидкостью питания, определяем по диаграмме y* – х на рис. 3. Рабочее число флегмы (/3/, с. 352): Определяем уравнения рабочих линий: верхней (укрепляющей) части колонны 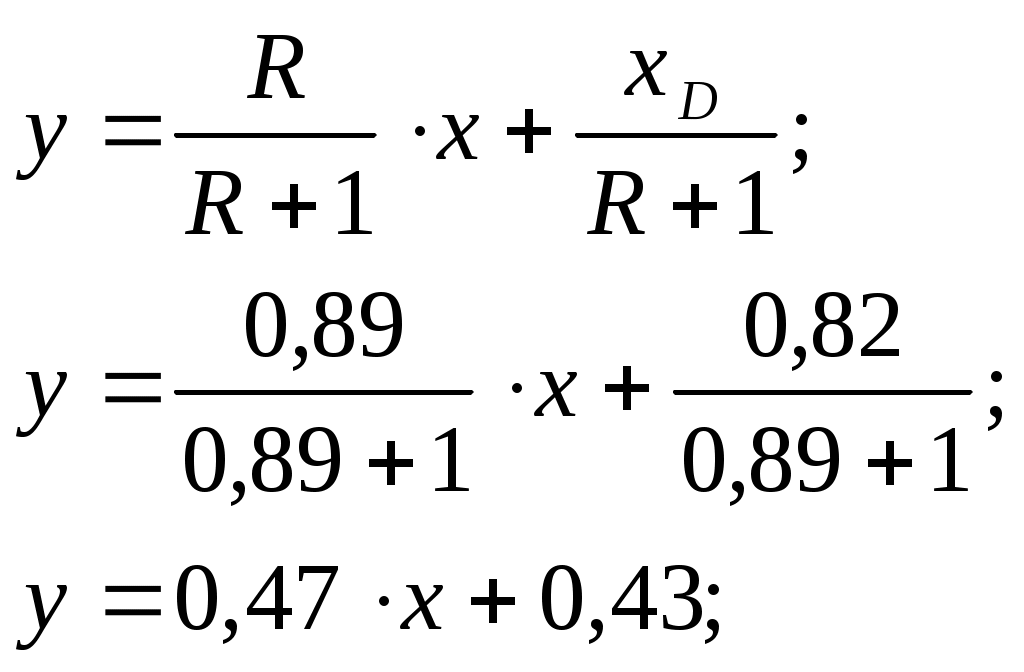 (4.9) (4.9)нижней (исчерпывающей) части колонны 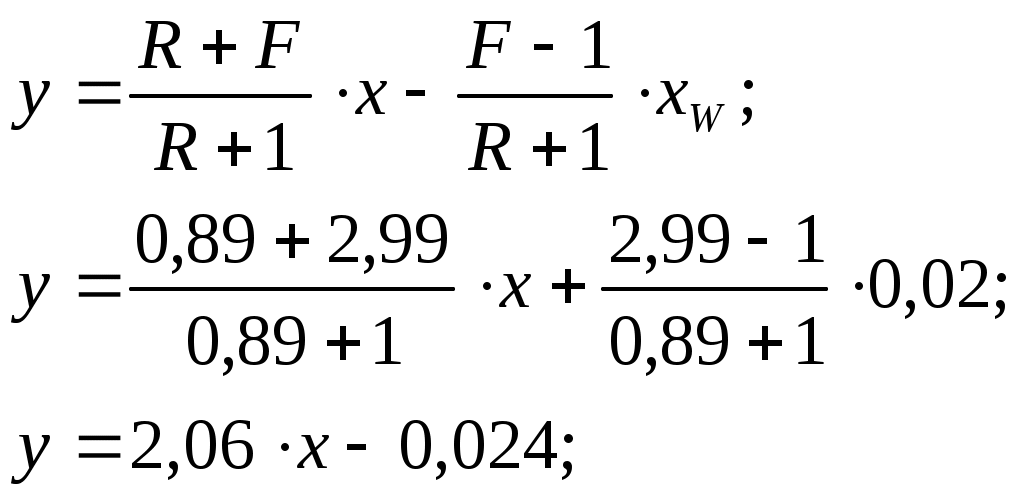 (4.10) (4.10)4. Определение скорости пара и диаметра колонныОпределяем средние концентрации жидкости: в верхней части колонны в нижней части колонны Средние концентрации пара находим по уравнениям рабочих линий: в верхней части колонны в нижней части колонны Средние температуры пара определяем по диаграмме t – x, y (рис. 4): при уср.в=0,69:tср.в=76,860С (Т`ср.в=tср.в+Т0=76,86+273=349,86К); при уср.н=0,31:tср.н=90,930С (Тср.н=tср.н+Т0=90,93+273=363,93К). Определяем средние мольные массы и плотности пара: Средняя плотность пара в колонне: Температура в верху колонны при xD=0,82 (см. рис. 4) равняется 67,24 0С, а в кубе–испарителе при хW=0,02 она равна 96,44 0С (см. рис. 4). Плотность воды при 96,44 0С: ρВ =960,492 кг/м3, а метилового спирта при 67,24 0С: ρм=748,76 кг/м3. (/3/, с. 512, табл. IV) Принимаем среднюю плотность жидкости в колонне: Определяем скорость пара в колонне по уравнению: где С – коэффициент, зависящий от конструкции тарелок, расстояния между тарелками, рабочего давления в колонне, нагрузки колонны по жидкости. ρж ρп– плотности жидкости и пара, кг/м3. Т. к. в нашем случае ρж ρп, то формулу (5.9) можно переписать следующим образом: Принимаем расстояние между тарелками h=0,5 м. Для ситчатых тарелок (/3/, с. 301, рис. 7-2) находим значение коэффициента С=0,075. (/3/, с. 323, рис. 7.2) Скорость пара в колонне: Определяем среднюю температуру в колонне: Определяем объемный расход проходящего через колонну пара при средней температуре: где MD – мольная масса дистиллята, равная: Определяем диаметр колонны: На основании полученного результата выбираем стандартный диаметр колонны (/3/, стр. 113, табл. VI.3) D=1200 мм. Тогда, с учетом выбранного диаметра, скорость пара в колонне будет: 5. Гидравлический расчет тарелокПо ОСТ 26-805-73 для колонны диаметром 1200 мм выбираем ситчатую однопоточную тарелку ТС-Р ([3], с. 113) со следующими конструктивными размерами: свободное сечение колонны: 1,13м2; рабочее сечение тарелки: 1,01м2; диаметр отверстия: 4мм; шаг между отверстиями: 12мм; относительное свободное сечение тарелки: 8%; сечение перелива: 0,06 м2; относительная площадь перелива: 5,3%; периметр слива: 0,722м; масса: 62кг. Рассчитаем гидравлические сопротивление тарелки в верхней и в нижней части колонны по формуле: Верхняя часть колонны. Определяем гидравлическое сопротивление сухой тарелки: где =1,82 – коэффициент сопротивления неорошаемых ситчатых тарелок со свободным сечением 7-10% (/3/, с. 28); Определяем сопротивление, обусловленное силами поверхностного натяжения: где =18,6810-3 Н/м – поверхностное натяжение жидкости при средней температуре в верхней части колонны при tср=67,24 0С (/3/, с. 526, табл. XXII); d0=0,004 м – диаметр отверстий тарелки.  Определяем сопротивление парожидкостного слоя на тарелке: Высота парожидкостного слоя (рис. 5): hП – высота сливной перегородки; h`– высота слоя над сливной перегородкой. Величину h рассчитываем по формуле: где V`Ж – объемный расход жидкости, м3/с; П – периметр сливной перегородки, м, Объемный расход жидкости в верхней части колонны: где Находим h`: По полученным данным определяем высоту парожидкостного слоя на тарелке: Определяем сопротивление парожидкостного слоя на тарелке: Общее гидравлическое сопротивление тарелки в верхней части колонны: Нижняя часть колонны. Расчет проводим аналогично расчету верхней части. где ``=16,0410-3 Н/м – поверхностное натяжение жидкости при средней температуре в нижней части колонны при tср=96,44 0С (/3/, с. 526, таблицы XXII); 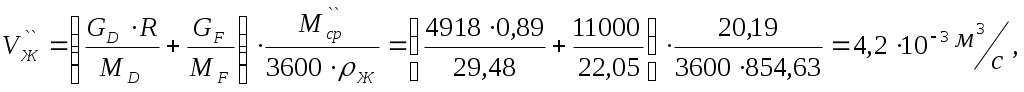 где Общее гидравлическое сопротивление тарелки в нижней части колонны: Проверяем, соблюдается ли при расстоянии между тарелками h=0,5 м необходимое для нормальной работы тарелок условие: Для тарелок нижней части колонны, у которых гидравлическое сопротивление Р больше, чем у тарелок верхней части: 0,5>0,21 следовательно, вышеуказанное условие соблюдается. Проверим равномерность работы тарелок – рассчитаем минимальную скорость пара в отверстиях 0 min достаточную для того, чтобы ситчатая тарелка работала всеми отверстиями: 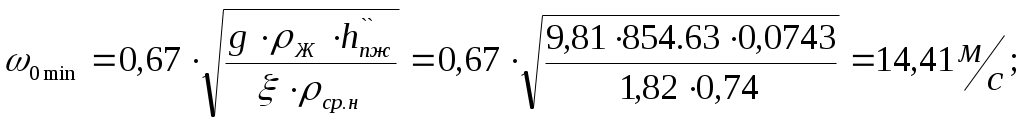 (6.10) (6.10)Т.к. 0 > 0 min (28,14 > 14,41), следовательно, тарелки будут работать всеми отверстиями. 6. Определение числа тарелок и высоты колонныНаносим на y – x диаграмму рабочие линии верхней и нижней части колонны (рис. 3) и находим число ступеней изменения концентрации nТ. В верхней части колонны 3, в нижней части колонны Число тарелок рассчитываем по уравнению: где - средний КПД тарелок. Для определения находим коэффициент относительной летучести разделяемых компонентов: Решая систему уравнений: 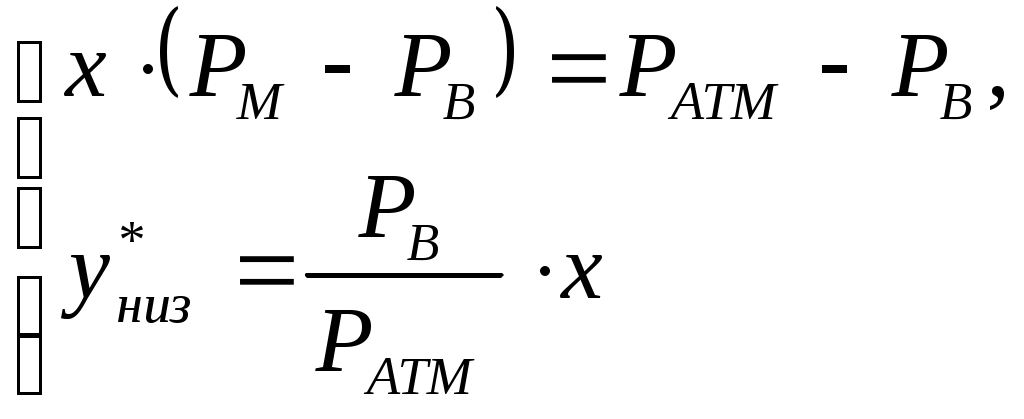 при заданных Определяем динамические коэффициенты вязкости (/3/, с. 516, табл. IX) (при 81,840С): Метилового спирта: 0,285 сП; воды: 0,350 сП. Принимаем динамический коэффициент вязкости исходной смеси: Тогда: По диаграмме для приближенного определения среднего КПД тарелок (/3/, с. 323, рис. 7.4) находим =0,492. Длина пути жидкости на тарелке: где D=1,2 м – диаметр колонны; LС=0,722 м – периметр слива. По графику (/3/, с. 324, рис. 7.5) определяем значение поправки на длину пути=0,035. Определяем средний КПД тарелок: Определяем число тарелок: в верхней части колонны в нижней части колонны Общее число тарелок n=12,с запасом n=16, из них в верхней части колонны 8 и в нижней части 8 тарелок. Высота тарельчатой части колонны: Общее гидравлическое сопротивление тарелок: 7. Расчет условного диаметра штуцеров.Условный диаметр рассчитываем исходя из объемного расхода и рекомендуемой скорости движения среды. Рекомендуемые скорости приведены в таблице 1.1 ([3] с.17). 7.1. Штуцер для отвода дистиллята.Дистиллят представляет собой пар. Принимаем для него скорость перемещения = 20 м/с. Массовый расход дистиллята равен 4918 кг/ч. Плотность пара в верхней части колонны равна 0,97 кг/м3. Тогда объемный расход пара будет равен Диаметр штуцера определяем по формуле: По ОСТ 231430-76 7.2. Штуцер для подвода флегмы.Рекомендуемая скорость для жидкости = 1 м/с. GF = 11000 кг/ч. Плотность флегмы (метиловый спирт) принимаем равной 748,76 кг/м3. Тогда По ОСТ 231430-76 7.3. Штуцера для входа парожидкостной смеси.Так как количество поступившего пара из колонны равно количеству пара ушедшего из колонны в виде дистиллята то площади этих штуцеров равны. В данном случае, для более равномерного распределения пара, мы принимаем два штуцера. По ОСТ 231430-76 7.4. Штуцер для подвода исходной смеси.Рекомендуемая скорость для жидкости = 1 м/с. По ОСТ 231430-76 7.5. Штуцер для отвода кубового остатка.Рекомендуемая скорость для жидкости = 1 м/с. GW= 6082 кг/ч. Плотность жидкости в колонне принимаем равной плотности воды В = По найденным диаметрам подбираем стандартные штуцера (/4/, с. 661, Таблица. 27.4). ОСТ 231423-76 ВыводыВ данной курсовой работе была рассчитана тарельчатая ректификационная колонна для разделения смеси метиловый спирт – вода и сделан чертеж общего вида колонны, ее виды и разрезы. В процессе выполнения курсовой работы были рассчитаны: материальный баланс, скорость пара и диаметр колонны, определение числа тарелок и диаметров штуцеров. Диаметр колонны D=1200 мм, общее число тарелок n=16 шт., общее гидравлическое сопротивление тарелок ∆P=0,15 атм. Список используемой литературыКасаткин А. Г. Основные процессы и аппараты химической технологии. М.: Химия, 1971. Основные процессы и аппараты химической технологии: Пособие по проектированию/ Под ред. Ю. И. Дытнерского. М.: Химия, 1983. Павлов К. Ф., Романков П. Г., Носков А. А. Примеры и задачи по курсу процессов и аппаратов химической технологии. Л.: Химия, 1976. Лащинский А. А. Конструирование сварных химических аппаратов. Л.: Машиностроение, 1981 г. - - | |||||||||||||||||||||||||||||||||||||||||||||||
