Цирроз печени. цирроз печени. Реферат цирроз печени Подготовила врачинтерн Минск,2022 Оглавление Введение
 Скачать 66.14 Kb. Скачать 66.14 Kb.
|
|
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ РЕФЕРАТ Цирроз печени Подготовила: врач-интерн Минск,2022 Оглавление Введение………………………………………………………….3 Этиология………………………………………………………...4 Клиническая картина……………………………………………5 Диагностика……………………………………………………...7 Лечение…………………………………………………………...8 Список используемых источников…………………………….18 ВВЕДЕНИЕ Цирроз печени — патологическое состояние, характеризующееся диффузным разрастанием соединительнотканных волокон с образованием фиброзных септ, узлов гиперрегенерации печеночной ткани, состоящих из функционально незрелых гепатоцитов, что приводит к изменению архитектоники органа и развитию псевдодолек. Цирроз печени сегодня является насущной медицинской и социально-экономической проблемой. По данным ВОЗ, цирроз печени является одной из шести ведущих причин смерти в экономически развитых странах в возрастной группе 35-60 лет. Среди причин смерти он занимает 4-е место в США и 10-е в Германии, в то время как в нашей стране насчитывается более 10 миллионов пациентов. Заболеваемость циррозом печени растет с каждым годом, что приводит к инвалидности среди населения, особенно в трудоспособном возрасте. гепатопротектор цирроза печени адсорбент Чаще всего у мужчин наблюдается цирроз печени. Соотношение мужчин и женщин составляет в среднем 3:1. Заболевание может встречаться во всех возрастных группах, но чаще всего после 40 лет. Цирроз печени соответствует следующей стадии морфогенеза хронического гепатита, основным отличием цирроза от хронического гепатита является развитие диффузного воспалительного процесса с высокой фибропластической активностью и фиброзированием печени. ЭТИОЛОГИЯ По данным литературы, более половины всех случаев цирроза печени в Европе, а также в странах бывшего СНГ связаны с употреблением алкоголя. Однако у четверти этих больных имеются указания на перенесенный в анамнезе гепатит. Наряду с алкоголем, вирусными гепатитами В, С, Д (роль вирусов 9 TTV- и SEN в патологии печени изучается) в этиологии циррозов также имеют значение метаболические нарушения (гемохроматоз, болезнь Вильсона–Коновалова, дефицит a1-антитрипсина, болезни накопления), заболевания сосудов (синдром Бадда–Киари-это обструкция печеночного венозного оттока с локализацией на любом уровне от мелких печеночных вен внутри печени до нижней полой вены и правого предсердия.), иммунологические факторы (аутоиммунный гепатит) и лекарственные препараты. Несмотря на большие диагностические возможности, даже в странах Западной Европы и США в 20% случаев этиология циррозов печени остается невыясненной (криптогенный цирроз). Классификация циррозов печени. По этиологии: 1. вирусные (В, С, Д); 2. алкогольные; – 3. токсические, в том числе лекарственные; 4. неалкогольный стеатогепатит; 5. болезнь Вильсона–Коновалова; – 6. вследствие дефицита α-1-антитрипсина; – 7. первичный билиарный цирроз; 8. вторичный билиарный цирроз. По морфологии: крупноузловой (диаметр узлов более 3 мм); мелкоузловой (диаметр узлов от 1 до 3 мм); неполный септальный; смешанный. КЛИНИЧЕСКАЯ КАРТИНА В клинической картине цирроза печени выделяют несколько синдромов: 1. Общие симптомы — слабость, пониженная трудоспособность, неприятные ощущения в животе, диспептические расстройства, повышение температуры тела, боли в суставах. Часто отмечается метеоризм, боль и чувство тяжести в верхней половине живота, похудание, астенизация. 2. Болевой синдром — как правило связан с дискинезией желчевыводящих путей или с некротическими изменениями в печени, особенно подкапсульными. 3. Синдром желтухи — обусловлен либо механическим нарушением оттока желчи вследствие внутрипеченочного холестаза, либо некротическими изменениями и всасыванием связанного билирубина в кровь. 4. Синдром гепатомегалии. 5. Синдром портальной гипертензии — обусловлен повышением давления в системе воротной вены. Он проявляется варикозным расширением вен в пищеводе, прямой кишке и на передней брюшной стенке, асцитом и спленомегалией. 6. Спленомегалия — может сопровождаться гиперспленизмом (лейкопения, тромбоцитопения и в тяжелых случаях — анемия). 7. Синдром портосистемной энцефалопатии. 8. Гепатопанкреатический синдром — снижение функции поджелудочной железы, приводящее к нарушению нормального пищеварения. При осмотре выявляют увеличение печени с уплотнением и деформацией ее поверхности (последняя часто не улавливается при мелкоузловой и септальной формах цирроза), край печени заострен. В начальной стадии обычно отмечается увеличение обеих долей печени, в последующем часто преобладает увеличение левой доли. Портальная гипертензия проявляется умеренной спленомегалией. В развернутой стадии цирроза печени клиническая картина разнообразна и отражает вовлечение в патологический процесс почти всех органов и систем. Основные, наиболее характерные симптомы связаны с наличием печеночно-клеточной недостаточности и портальной гипертензии. Наиболее частые жалобы — слабость, быстрая утомляемость, снижение работоспособности, ухудшение аппетита, диспептические расстройства (вздутие живота, плохая переносимость жирной пищи и алкоголя, тошнота, рвота, диарея), нарушение сна, раздражительность. Особенно часто отмечается чувство тяжести или боли в животе, преимущественно в правом подреберье и эпигастрии, импотенция, зуд кожи, нарушения менструального цикла у женщин. Наиболее частым объективным симптомом выступает гепатомегалия. Печень имеет уплотненную консистенцию, заостренный край, мало- или безболезненна. У 30 % больных пальпируют узловатую поверхность органа. В терминальной стадии болезни в 25 % случаев отмечается уменьшение размеров печени. Спленомегалия выявляется у 50 % больных. Часто обнаруживаются внешние симптомы цирроза: пальмарная или плантарная эритема, сосудистые звездочки, скудный волосяной покров в подмышечной области и на лобке, белые ногти, гинекомастия у мужчин. Характерно похудение, часто маскируемое одновременным накоплением жидкости. У половины больных повышена температура тела, в большинстве случаев — это субфебрилитет, который сохраняется несколько недель. Наблюдаются также изменения в сердечно-сосудистой системе, так как идет выброс большого количества гистамина, серотонина и недостаточная их инактивация в пораженной печени. Весьма часто выявляется гипотензия и в связи с этим тахикардия как компенсаторная реакция. К числу относительно поздних симптомов цирроза, характеризующих выраженную печеночно-клеточную недостаточность и портальную гипертензию, относятся желтуха, асцит, периферические отеки (прежде всего, отеки ног), внешние венозные коллатерали. Варикозные расширения вен пищевода, желудка, кишечника, в том числе и 12-перстной кишки, других венозных коллатеральных сосудов, включая мезентериальные расширения, выявляемые только при ангиографическом исследовании или оперативном вмешательстве, могут стать источником сильных внутренних кровотечений с летальным исходом. ДИАГНОСТИКА Для определения стадии цирроза печени используют критерии Чайлд–Пью (табл. 2). По сумме показателей выделяют 3 стадии заболевания: первая (класс А, компенсированный) — 5–6 баллов, вторая (класс В, субкомпенсированный) — 7–9 баллов, третья (класс С, декомпенсированный) — более 9 баллов 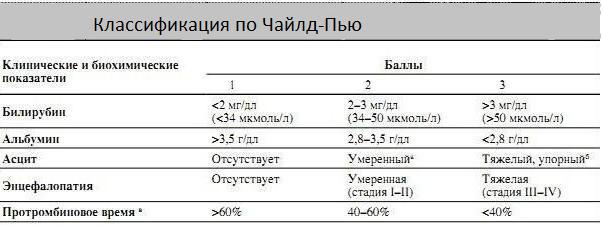 Одним из основных методов инструментальной диагностики циррозов печени является ультразвуковое исследование. Для цирроза печени достаточно типичны ультразвуковые признаки портальной гипертензии. Цирроз печени возможно диагностировать на основании исследования в режиме серой шкалы при визуализации печени с неоднородной структурой паренхимы и неровным бугристым контуром, принимая во внимания сопутствующие признаки портальной гипертензии (асцит, расширение вен воротной системы, спленомегалию). При отсутствии целостной ультразвуковой картины, характерной для цирроза, применение допплеровских методик позволяет получить дополнительную информацию, которая в ряде случаев определяет заключение протокола исследования. Используя ЦДК можно выявить кровоток в круглой связке печени при реканализации параумбиликальной вены, а также визуализировать другие порто-системные коллатерали (диафрагмальные, спленоренальные и спленогастральные, коллатерали в стенке желчного пузыря и т.д.). Общий анализ крови информативен для определения мегалобластной анемии у пациентов с циррозом печени. Биохимический анализ крови информативен для определения фракций биллирубина, АлАТ, АсАТ, щелочной фосфатазы, ГГТП, альбумин, также важно интерпретация коагулограммы в связи с тем, что у пациентов с циррозом печени наблюдается гипокоагуляция. ФГДС информативна для определения ВРВ пищевода, желудка, 12-персной кишки. ЛЕЧЕНИЕ Питание. Больные циррозом печени имеют тенденцию к гиперметаболическому статусу и для поддержания азотистого баланса нуждаются в большем, по сравнению со здоровыми, количестве белка. Большинство пациентов толерантны к потреблению нормального или повышенного количества белка без риска развития ПСЭ. У пациентов с тяжелой мальнутрицией могут использоваться препараты аминокислот. У части пациентов с интолерантностью к пищевому белку для поддержания нормального нервно-психического статуса могут использоваться препараты разветвленных аминокислот. Медикаментозное лечение цирроза печени состоит преимущественно в коррекции его осложнений и специфической терапии отдельных этиологических форм заболевания. Применение лекарственных препаратов у больных циррозом печени имеет свои ограничения с учетом их побочных действий. Вместе с тем имеется ряд лекарственных средств, которые направлены на улучшение метаболизма гепатоцитов, стабилизацию мембран, коррекцию холестаза и ослабление его симптомов. Эти препараты могут назначаться при различных этиологических формах цирроза при наличии признаков активности процесса холестаза. Появление урсодезоксихолевой кислоты является самым большим прогрессивным достижением в лечении заболеваний печени последних десятилетий. Несмотря на то, что механизмы благоприятного терапевтического действия УДХК пока еще окончательно не расшифрованы, препарат считается рациональным средством и имеет возрастающее значение при лечении заболеваний печени, особенно характеризующихся холестазом, вне зависимости от его этиологии улучшающим клинические и лабораторные показатели у больных. УДХК является третичной желчной кислотой и у человека составляет незначительную (менее 5 %) долю пула желчных кислот. В отличие от других желчных кислот человека, УДХК гидрофильна. УДХК конкурентно ингибирует всасывание в кишечнике эндогенных липофильных токсичных желчных кислот, что приводит к вытеснению их из энтеро-гепатической циркуляции и общего пула желчных кислот. Таким образом, на фоне лечения УДХК у пациентов происходит дозозависимое изменение соотношения желчных кислот — УДХК становится основным компонентом желчи, тогда как содержание эндогенных желчных кислот (ХДХК, дезоксихолевой, ХК) снижается. Лечебное действие УДХК связывают с рядом эффектов, основные их которых следующие: – образование небольших смешанных мицелл; – уменьшение количества липофильных желчных кислот; – образование неполярных димеров, которые включаются в мембраны гепатоцитов и обеспечивают прямое цитопротективное действие, направленное на стабилизацию мембран; – влияние на иммунную систему; – индукция холереза. Препараты УДХК (Ursofalk и Ursosan) выпускаются в капсулах по 250 мг. Назначаются по 10–15 мг/кг/сут , обычно в несколько приемов в течение суток. S-аденозил-L-метионин (Heptral). SAMe является естественным метаболитом организма человека. Синтезируется из метионина с участием SAM-синтетазы. Будучи очень активным, принимает участие в процессах метилирования, сульфатирования, аминопропиловом обмене, что приводит к образованию ряда активных продуктов. Продукты его метаболизма участвуют во многих процессах в печени. Участие в процессах метилирования имеет отношение к синтезу фосфолипидов, которые обеспечивают текучесть мембран гепатоцитов. Нарушение структуры и текучести мембран может стать причиной внутрипеченочного (внутридолькового) холестаза, например, при алкогольной или токсической болезни печени. Таурин используется в процессе конъюгации желчных кислот, что увеличивает их растворимость и экскрецию. Глютатион является универсальным детоксицирующим агентом, который участвует в инактивации токсичных продуктов, что уменьшает воздействие их на печень. Важную роль в детоксикации играют также сульфаты. Участие SAMe в аминопропиловом пути обуслов91 ливает его роль в регенерации печени. При заболеваниях печени отмечается дефицит SAMe, что явилось основанием для использования его в качестве лекарственного средства. Имеется большой опыт применения SAMe и показана его эффективность при циррозах печени для коррекции ряда нарушений, особенно холестаза, печеночной энцефалопатии, предупреждения фиброза. Особенно показан SAMe при циррозах печени лекарственной, токсической и алкогольной этиологии. Препарат SAMe Heptral выпускается в форме для инъекций (флаконы по 400 мг сухого вещества с приложением растворителя) и в таблетках по 400 мг. Может назначаться в/в, в/м и внутрь. Стандартный курс лечения — 14 ежедневных в/в вливаний по 800 мг и 14 дней приема таблеток по 1600 мг/день в 2 приема (утром и в 16 часов). Препарат практически не вызывает побочных явлений за исключением тошноты, изжоги. Кортикостероиды применяются в лечении первичного биллиарного цирроза. Основной механизм их действия — иммуносупрессивный. Дозы преднизолона — 10–20 мг/сут. Их назначение позволяет уменьшить клинические проявления и улучшить биохимические показатели. Недостатком кортикостероидной терапии является усугубление остеопороза, свойственного больным ПБЦ по причине мальабсорбции витамина Д, в связи с чем кортикостероиды используются нечасто. Профилактика геморрагических осложнений. Нарушения свертывания крови, свойственные больным циррозом, обычно не являются причиной спонтанных кровотечений. В случае необходимости инвазивных процедур при низких показателях ПТИ и числа тромбоцитов следует предварительно провести вливание свежезамороженной плазмы или тромбоцитов. Развитие больших подкожных гематом — беспричинных или после умеренной травмы — может быть обусловлено спонтанным фибринолизом и являться предвестником катастрофических кровотечений. У таких пациентов инвазивные процедуры, в том числе экстракция зуба или венепункция, должны выполняться под прикрытием вливания ε-аминокапроновой кислоты. Дефицит витамина К наблюдается при циррозе в случаях холестаза, плохого питания или подавления бактериальной кишечной продукции витаминов при антибактериальной терапии — у таких больных стоит производить осполнение его дефицита. Возможные методы лечения асцита: – ограничение приема натрия; – постельный режим; – прием диуретиков; – серийные парацентезы; – перитонеовенозный шунт; – портосистемное шунтирование; – трансъюгулярный портосистемный шунт (TIPS); – трансплантация печени. Диуретики называют средством, разрубающим гордиев узел при лечении асцита. Решение о диуретической терапии предпринимают обычно после 4 дней постельного режима и ограничения натрия. На фоне их приема больные должны соблюдать диету с ограничением натрия. При употреблении большого количества натрия даже прием диуретиков оказывается неэффективным. Существуют различные подходы к выбору диуретиков. Обычный рекомендуемый начальный режим — однократный утренний прием дозы спиронолактона и фуросемида, начиная со 100 мг первого и 40 мг последнего. Такое соотношение препаратов дает возможность оптимально поддерживать нормокалиемию. Однократный прием позволяет увеличить точность выполнения назначений. Оральная доза обоих диуретиков может быть увеличена, если соотношение (100 мг спиронолактона/40 мг фуросемида) не дает адекватного ответа — необходимого снижения массы тела и натрийуреза (обычно через 3 дня). Максимальные дозы составляют 400 мг/день спиронолактона и 160 мг/день фуросемида. 2. Изолированное использование спиронолактона имеет сторонников — это рекомендуется у пациентов с минимальным асцитом. Начальная доза спиронолактона — 100 или 200 мг. Примерно 1 /3 пациентов не отвечают на его изолированный прием. Период полувыведения спиронолактона составляет 5 дней, и контролируемые исследования показали, что эффект изолированного его приема проявляется спустя 2 недели; в связи с этим стабильные результаты можно оценивать через 4 недели после начала лечения или увеличения дозы. При неэффективности начальной дозы спиронолактона ее увеличивают (через каждые 3 дня), достигая максимальной (400 мг). Если отсутствует ответ на максимальную дозу спиронолактона, больному добавляют фуросемид. Спиронолактон наиболее эффективен при исходной экскреции натрия > 10 ммоль/л; при меньшей экскреции эффект препарата слабый. У части пациентов с изолированным приемом спиронолактона через 2 недели развивается гиперкалиемия . Изолированный прием фуросемида менее эффективен по сравнению со спиронолактоном, а, по мнению некоторых исследователей, у больных циррозом печени с асцитом не показан. Быстрый эффект натрийуреза в начале приема фуросемида приводит в дальнейшем — из-за периферической вазодилятации с последующей активацией гормональных и нервных стимулов — к феномену рикошета. Особенно быстро этот эффект развивается после в/в введения фуросемида. Хорошая усвояемость фуросемида у пациентов с циррозом, с одной стороны, и быстрое уменьшение клубочковой фильтрации, ассоциированное с в/в введением фуросемида, с другой, делают оральный прием этого диуретика предпочтительным. Изолированный прием фуросемида может сопровождаться гипокалиемией. Методы лечения варикозных кровотечений: 1. Лекарственная терапия. 2. Балонная тампонада (зонды Sengstaken–Blakemore, Linton–Nachlas). 3. Эндоскопические методы (склеротерапия, облитерация, лигирование). 4. Хирургические методы (прошивание варикозных вен, портосистемное шунтирование — декомпрессионные портокавальные анастомозы, транссекция пищевода). 5. Трансплантация печени. 6. Трансъюгулярный внутрипеченочный портосистемный шунт (TIPS). У каждого пациента с циррозом без осложнений портальной гипертензии должна быть проанализирована степень вероятности варикозного кровотечения. При наличии риска рассматривается вопрос о его профилактике. Согласно Baveno III, профилактическому лечению подлежат все пациенты с венами большого размера (более 5 мм), а дополнительные эндоскопические признаки не влияют на показания к лечению. Лекарственная терапия является основой профилактики первого кровотечения. В соответствии с соглашениями Baveno II и Baveno III препаратами первой линии профилактики первого эпизода варикозного кровотечения являются неселективные β-адреноблокаторы. Применяются с этой целью с 1981 г., их эффективность подтверждена 9 контролируемыми исследованиями и 3 метаанализами. Пропранолол высоко эффективен и применяется 103 в максимально переносимых дозах. Не установлено, насколько должно быть снижено портальное давление для предупреждения кровотечения, однако известно, что кровотечение не наблюдается при уменьшении градиента портокавального давления ниже 12 мм рт. ст. Доза пропранолола, снижающая частоту сердечных сокращений на 25 % через 12 часов, снижает давление в портальной системе на 30 %, хотя это соотношение непостоянно. β-блокаторы уменьшают риск кровотечения на 45 %. Используется комбинированное лечение: β-адреноблокаторы (например, надолол 40–60 мг/сут) + нитраты (изосорбид мононитрат 20 мг 2 раза/сут). Показано, что такая комбинация более целесообразна для применения больным пожилого возраста и с асцитом. Лечение острого кровотечения. Лечение больных с острым кровотечением из варикозных вен часто бывает интенсивным, требует немедленной госпитализации в стационар, совместных усилий гепатолога, эндоскописта, хирурга, врача интенсивной медицины и характеризуется высокой стоимостью. Неотложная терапия направлена, прежде всего, на предупреждение и/или осторожную коррекцию гемодинамических нарушений, связанных с гиповолемией и шоком. Обнаружение значимых симптомов гиповолемии (систолическое давление < 90 мм рт. ст., тахикардия > 120 уд./мин, признаки периферической гипоперфузии) диктуют необходимость ингаляции кислорода, быстрых вливаний плазмы и крови. Согласно консенсусу Baveno III, переливание плазмы рекомендуется для стабилизации гемодинамики, а эритроцитарной массы — при снижении гематокрита до 25–30 %. Установлено, что объем переливаемой крови и кровезамещающих растворов имеет значение для исхода эпизода кровотечения. Результаты лучше при неполном восполнении объема кровопотери, поэтому важно не производить больших гемотрансфузий и инфузий большими объемами растворов. Чем больше крови переливается, тем выше риск рецидивов. Очень важным является аспирация крови из дыхательных путей, особенно у пациентов, находящихся в бессознательном состоянии. Необходимость коррекции коагулопатии и тромбоцитопении не определена. Согласно Baveno III, эндоскопическое исследование после госпитализации должно быть выполнено по возможности быстро (в течение 12 часов), особенно у пациентов с клинически значимым кровотечением. Существует понятие «активное кровотечение» — ситуация, когда при эндоскопии видно истекание крови из варикозных вен. Активное кровотечение является предвестником недостаточности контроля кровотечения в последующие несколько дней и плохого прогноза. При нетяжелом кровотечении, отсутствии нарушений гемодинамики и необходимости коррекции гиповолемии эндоскопия не обязательна. 104 Лекарственная терапия вазоактивными средствами является основой лечения острого кровотечения и должна начинаться сразу, как только возможно, до диагностической эндоскопии Эффективны несколько средств: вазопрессин и его аналоги (терлипрессин), вазопрессин + нитроглицерин, соматостатин и его аналоги (октреотид). Лекарственная терапия может применяться и как начальное лечение перед эндоскопическими методами (склеротерапией или лигированием). Вазопрессин снижает портальное давление на 30 %, назначается в виде внутривенных инфузий и приводит к остановке кровотечения в 60 % случаев. Применение вазопрессина ассоциируется с осложнениями, обусловленными системной вазоконстрикцией и кардиотоксическим эффектом. Кардиоваскулярные проблемы включают коронарную вазоконстрикцию с ишемией миокарда и возможным развитием инфаркта, аритмии (особенно желудочковые), гипертензию, брадикардию. Периферическая артериальная вазоконстрикция может усиливать мезентериальную и церебральную ишемию, ишемию конечностей. Эффект вазопрессина на почки состоит в ослаблении экскреции воды, что может быть причиной гиперволемии, гипонатриемии и усиления асцита. Совместное применение вазопрессина и нитроглицерина оказывает положительный лечебный эффект по снижению портального давления и при этом уменьшает побочные эффекты возопрессина на сердце и системную гемодинамику. Нитроглицерин применяется в/в или сублингвально. Соматостатину не свойственны отрицательные эффекты вазопрессина на системную гемодинамику. Октреотид обладает более длительным периодом действия и может вводиться подкожно. Баллонная тампонада. Является методом контроля массивного варикозного кровотечения путем прямой компрессии варикозных вен в месте кровотечения. Имеется несколько вариантов зонда — зонд Sengstaken– Blakemore для пищевода, зонд Linton–Nachlas для желудка. Эффективность тампонады — 85–95 %. Метод имеет два недостатка: 1) ограниченный период нахождения баллона в месте компрессии; 2) высокая частота осложнений, которые могут быть летальными (наиболее частое — аспирационная пневмония). Согласно Baveno III, баллонная тампонада обычно рассматривается как «мост» к другим методам лечения. Эндоскопическое лечение. Существует несколько методов эндоскопического лечения: склеротерапия (используется с 1982 г.), облитерация и лигирование (с 1985 г.). Сущность склеротерапии заключается в тампонаде, тромбировании и индукции воспалительной реакции с последующим склерозированием варикозных сосудов с использованием различных веществ-склерозантов (тетрадецил-сульфат натрия, полидоканол, этаноламин). Облитерация производится введением в сосуд специальных веществ с немедленным их затвердеванием и чаще выполняется при варикозном расширении вен желудка. Эндоскопическое лигирование практикуется с 1985 г. и выполняется с помощью специальной насадки на эндоскоп. Использование эндоскопических методов возможно для профилактики первого кровотечения, лечения кровотечения и профилактики повторных кровотечений, что доказано рядом контролируемых исследований. Так, эффективность склеротерапии для первичной профилактики варикозных кровотечений доказана 19 контролируемыми исследованиями. Склеротерапия в Японии является стандартным методом профилактики кровотечений. 106 Вместе с тем, согласно Baveno III склеротерапия для профилактики первого эпизода варикозного кровотечения не рекомендуется, а эндоскопическое лигирование является альтернативой превентивного лечения β-блокаторами. Не рекомендуется и профилактическое комбинированное (лекарства + эндоскопическое) лечение. Склеротерапия и эндоскопическое лигирование рекомендуются для лечения варикозного кровотечения, причем рассматривается возможность комбинированной терапии (эндоскопической + лекарственной), когда лекарственная может предшествовать эндоскопической. Хирургическое лечение. Применяется для купирования кровотечения и профилактики рецидивирующих массивных кровотечений. Существует два принципиальных подхода: портальная декомпрессия и недекомпрессионные методики (пищеводная транссекция и деваскуляризация). Портальная декомпрессия достигается выполнением портосистемного шунтирования (различные виды селективных и неселективных декомпрессионных портокавальных анастомозов — спленоренальный и др.). Существенным недостатком портосистемного шунтирования является частое развитие ПСЭ. Лечение портосистемной энцефалопатии. Портосистемная энцефалопатия — синдромокомплекс потенциально обратимых психических и неврологических проявлений на фоне имеющегося заболевания печени. Когда нарушения достигают тяжелой степени, синдром приобретает имя печеночной комы. Клинические подходы к коррекции портосистемной энцефалопатии: 1. Исключение других причин нервно-психических расстройств. 2. Оценка необходимости дополнительного обследования (консультации невропатолога, М-эхо, КТ головного мозга, люмбальная пункция, исследование мочи на бензодиазепины, наркотики). 3. Исключение факта приема бензодиазепинов и других психотропных средств. 4. Активный поиск и устранение провоцирующих факторов. 5. Определение места лечения пациента (поликлиника, стационар, ОИТР). 6. Определение оптимального количества белка в диете. 7. Назначение разветвленных аминокислот внутрь. 8. Назначение фармакологических препаратов. Препараты, уменьшающие образование аммиака. Неабсорбируемые дисахариды. Лактулоза (бета-галактозидофруктоза) и лактитол (бетагалактозидосорбитол) являются синтетическими дисахаридами и используются в клинической практике соответственно с 1966 и 1982 гг. Будучи принятыми внутрь, они не подвергаются гидролизу кишечными ферментами человека (вследствие отсутствия таковых) и не всасываются. Их применение направлено на сокращение продукции аммиака и уменьшение его всасывания в кишечнике, что достигается благодаря следующим эффектам: а) увеличению осмотических свойств содержимого тонкой кишки и ускорению кишечного транзита, что усиливает удаление пищевых и эндогенных субстратов аммиака; б) в толстой кишке происходит бактериальная ферментация дисахаридов с продукцией органических кислот и снижением рН, в результате чего: – подавляется рост кишечных аммиакпродуцирующих бактерий с уменьшением продукции аммиака; – изменяется соотношения NH3/NH4 в сторону ионизированного NH4 + , что уменьшает абсорбцию аммиака и увеличивает поступление его из крови в просвет кишки; – усиливается перистальтика кишечника и учащается его опорожнение. Эффективность неабсорбируемых дисахаридов доказана контролируемыми исследованиями. Они практически не имеют побочных явлений (за исключением диареи). Являются главными препаратами для профилактики печеночной энцефалопатии, лечения латентной и манифестных форм. Препараты лактулозы — Lactulose sirop, Duphalak, Portalak, Lactofalk — имеют вид сиропа. Лактитол имеет вид кристаллического порошка. Дозы подбираются индивидуально: суточная доза титруется до получения мягкого стула от 2 до 3 раз в сутки с кислой реакцией (рН < 6,0). Для большинства пациентов в сутки требуется от 30 до 60 мл сиропа лактулозы, в некоторых случаях — до 120 мл. У тяжелых больных препарат может вводиться через зонд в 12-перстную кишку, а также в клизмах (клизмы выполняются 2 раза в день — 300 мл сиропа растворяют в 700 мл воды). Антибиотики. Эффект антибиотиков связан с подавлением бактерий, продуцирующих аммиак и другие токсины. Неомицин применяется с 50-х годов и считается «золотым стандартом» антибиотика, используемого с этой целью. Вместе с тем, из-за свойственных ему ото- и нефротоксичности, которые приходится принимать во внимание даже при незначительной всасываемости (1–3 %), используется редко и кратковременно — в течение 6–8 дней при лечении острых эпизодов ПСЭ. Вводится через рот или назогастральный зонд. Чаще используются другие антибактериальные препараты — метронидазол 800 мг/сут, ванкомицин 0,6–2,0 мг/сут, рифаксимин (неабсорбируемое производное рифампицина) 1200 мг/сут — обычно в течение 5–10 дней. Комбинации неабсорбируемых дисахаридов и антибиотиков применяются при рефрактерной ПСЭ. Такое сочетание допустимо, так как лактулоза метаболизируется популяцией бактерий, резистентных к антибиотикам. Заселение просвета толстой кишки неуреазопродуцирующими бактериями. Неуреазопродуцирующие бактерии — Lactobacillus acidophilus, Enterococcus faecium — выполняют роль антагонистов уреазопродуцирующих бактерий. Производится заселение оральным путем курсами по 4 недели. Препараты, повышающие метаболизм аммиака в тканях. Для повышения утилизации аммиака в тканях (печени, мышцах, головном мозге) используются вещества, усиливающие инкорпорацию его в мочевину и глютамин и являющиеся субстратами в цикле мочевины. Таковыми являются так называемые «снижающие аммиак» аминокислоты, опыт применения которых насчитывает уже около 25 лет. Препараты L-орнитин-L-аспартат (Hepa-merz,), Орнитин-α-кетоглютарат, Oxoglurate-L-ornithine (Ornicetil). L-орнитин-L-аспартат является дипептидом, который оказывает влияние на метаболизм аммиака благодаря нескольким механизмам: – орнитин включается в цикл мочевины в качестве субстрата (на этапе синтеза цитруллина); – орнитин включается в цикл мочевины (на этапе синтеза аргининсукцината); – орнитин служит субстратом для синтеза глютамина, участвуя в связывании аммиака. Возможно применение ингибиторов ГАМК-бензодиазепиновых рецепторов — флумазенил (Anexate) 0,3–2,0 мг/сут. Введение разветвленных аминокислот оказывается эффективным в уменьшении проявлений ПСЭ. Применяются препараты: Аминостерил N-гепа (5 % и 8 %), фалькамин (0,25 г/кг), лактострикт (30–40 г белка/сут.), лактострикт spezial по 0,3 г разветвленных аминокислот/сутки и другие. Так, один пакет фалькамина (9,33 г) содержит 3,62 г L-лейцина, 1,94 г L-валина, 1,45 г L-изолейцина. Имеются специальные растворы для энтерального питания (в качестве питья или питания через зонд), содержащие среди прочих питательных компонентов разветвленные аминокислоты, например, фрезубин hepa (печеночный). В лечении СБП не используют массивные парацентезы, интраабдоминальные промывания и введения через дренаж антибиотиков, так как последние хорошо проникают в асцитическую жидкость из крови. Лечение проводят антибиотиками широкого спектра действия до получения результатов анализа чувствительности к антибиотикам. Рекомендации в отношении выбора антибиотиков постоянно меняются. В настоящее время оптимальным считается парентеральное введение цефалоспорина III поколения — цефотаксима по 2,0 2 раза в сутки (и даже каждые 4, 6 или 8 часов) в течение 5–7–14 дней — эффективность достигает 78–95 %. Показан хороший эффект короткого (5 дней) курса внутривенного введения цефтриаксона (2,0 1 раз в сутки) — 110 95 %. Возможно пероральное применение цефтриаксона по 1,0 2 раза в сутки. Используется комбинация ампициллина/тобрамицина с цефотаксимом, которая эффективна в 95 % случаев. В качестве альтернативы предлагается сочетание 1,0 амоксициллина и 0,2 клавулановой кислоты каждые 6 часов в течение 14 дней (эффективность — 85 %). Показана эффективность орального приема офлоксацина 0,5 г 2 раза/сут внутрь у пациентов, не имеющих рвоты или других препятствий для орального приема (например, бессознательное состояние). Известны результаты многоцентрового рондомизированного исследования эффективности сочетанного введения цефотаксима и внутривенных инфузий альбумина (1,5 г/кг массы тела в первый день и 1 г/кг в последующие 3 дня) в сравнении с применением цефотаксима. Включение альбумина преследует цель увеличения объема плазмы и в итоге — предотвращение почечной недостаточности. Показано достоверное сокращение смертности больных с 29 % на фоне цефотаксима до 10 % при сочетании цефотаксима с альбумином в связи с улучшением функции почек. Через 2 дня после начала лечения антибиотиками рядом авторов рекомендуется контрольная пункция для оценки эффективности терапии: при отсутствии эффекта (оценивается по снижению числа лейкоцитов в жидкости) — смена антибиотика. Когда становится известна чувствительность флоры, выбор антибиотиков корригируется. Прогноз при СБП плохой, хотя накопленные знания в этой области и достижения антибактериальной терапии в 90-е годы позволили снизить смертность с 90 до 30–40 %. Основные причины смерти — гастроинтестинальные кровотечения, печеночная недостаточность, ГРС. Наиболее часто (30–40 %) больные СБП умирают от почечной недостаточности на фоне ГРС, имеющей гемодинамический генез как следствие активации систем вазоконстрикторов. Причина активации этих систем — снижение эффективного кровотока на фоне инфекции, что может вызывать ренальную вазоконстрикцию, снижать ренальную перфузию и клубочковую фильтрацию. Таким образом, при циррозе с СБП имеется комбинация циркуляторных нарушений — с одной стороны, свойственных циррозу и им обусловленных, с другой — наблюдающихся при септическом синдроме и связанных с инфекцией. Развитие циркуляторных нарушений, почечной недостаточности и летального исхода у больных циррозом с СБП тесно связаны. Неблагоприятными прогностическими факторами являются отклонения печеночных параметров — билирубин > 135 мкмоль/л, альбумин < 25 г/л — и осложнения цирроза (ПСЭ, ГРС, кровотечения из верхних отделов пищеварительного тракта). СПИСОК ИСПОЛЬЗУЕМЫХ ИСТОЧНИКОВ Циррозы печени: уч. пособие / Д.Х. Калимуллина [и др.] ; под общ. ред. А.Б. Бакирова – Уфа: Вагант, 2016. - 83 с. Хронические гепатиты и цирроз печени : учеб.-метод. пособие / А. И. Близнюк. – Минск : БГМУ, 2010. – 123 с. Вутренние болезни: Пособие В2 ч. Ч1 /А.А. Бова.- Минск: Зималетто, 2012 - 252 с. |
