Реферат. Химия и материалловедение. Бардиков В.Д. группа ИНз-29.. Реферат по дисциплине Химия и материаловедение
 Скачать 128.6 Kb. Скачать 128.6 Kb.
|
60 л/мин.МЕТОДЫ ПОЛУЧЕНИЯ МОНОКРИСТАЛЛОВВ исследовательских лабораториях и промышленности выращивают кристаллы из паров, расплавов и растворов, из твердой фазы, синтезируют путем химических реакций, осуществляют электролитическую кристаллизацию, кристаллизацию из гелей и др. В настоящее время для получения совершенных кристаллов большого диаметра чаще всего применяют следующие методы выращивания: из газовой (паровой) фазы при градиенте давления, из расплавов при температурном градиенте, из растворов при градиенте концентрации на границе раздела кристалл – раствор [3]. Выращивание монокристаллов из газовой фазыСуществующие способы выращивания монокристаллов из газовой фазы можно разделить на две группы: кристаллизация без участия химической реакции и кристаллизация с участием химической реакции. Кристаллизация без участия химической реакцииВ этом случае вещество переносится, к растущему кристаллу в результате возгонки. Поэтому процесс можно успешно вести лишь в том случае, если вещество ниже температуры плавления обладает заметной упругостью паров, которая к тому же достаточно сильно зависит от температуры. Таким образом, можно выращивать монокристаллы многих сульфидов, селенидов, теллуридов, галогенидов, а также органических веществ и даже таких тугоплавких соединений, как карбиды кремния и бора. Для получения пленок часто применяется и метод катодного напыления. Благодаря прямолинейности молекулярного пучка он позволяет использовать так называемые «маски» для получения единой пленки заданной, иногда довольно сложной конфигурации. Методом сублимации могут быть выращены и нитевидные кристаллы таких тугоплавких соединений, как оксида магния и карбида кремния. Метод сублимации позволяет получать кристаллы, не загрязненные посторонними примесями. Однако, широкое применение этого метода для получения полупроводниковых монокристаллов и пленок сталкивается с определенными трудностями, связанными с необходимостью создания глубокого вакуума, защищающего от вредного воздействия следов кислорода. Кристаллизация с участием химической реакцииЭта группа методов применяется для выращивания кристаллов веществ, не обладавших заметной упругостью пара ниже температуры плавления или нарушающих свою стехиометрию в процессе испарения. В нее входят методы, основанные на химических транспортных реакциях в замкнутой или открытой (проточной) системе и кристаллизация с применением так называемых парофазных реакций. Метод химических транспортных реакцийМетод основан на использовании обратимых гетерогенных реакций, в результате которых вещество переносится из зоны синтеза в зону роста. В зоне синтеза газообразное вещество В реагирует с подлежащим переносу твердым веще- ством А, образуя газообразный продукт АВ, который вследствие диффузии, конвекции или с газовым потоком переносится в зону кристаллизации, где в результате изменения температуры равновесие реакции смещается и на затравке кристаллизуется выделяющееся из газовой фазы вещество А: А(t)+В(r)↔AB(r). При эндотермической реакции вещество переносится из зоны с более высокой температурой Т2в зону с более низкой температурой Т1:  𝑇 А(t)+В(r)=AB(r),∆𝑟𝐻0,T2→T1. Стрелка указывает направление переноса вещества. При экзотермической реакции перенос вещества идет в зону с более высокой температурой:  𝑇 А(t)+В(r)=AB(r),−∆𝑟𝐻0,T1→T2. Таким образом, основа метода - обратимая гетерогенная реакция. Кристаллизацияизгазовойфазывзамкнутомреакционномсосуде (запаянной ампуле) принципиально схожа с выращиванием кристаллов из раствора (в том и числе и гидротермальным методом) в условиях температурного перепада, и отличается только сравнительно малой плотностью растворителя. В системе (рис.1) создаются две зоны: зона синтеза с температурой T1(или Т2) и зона кристаллизации с температурой T2(или Т1) 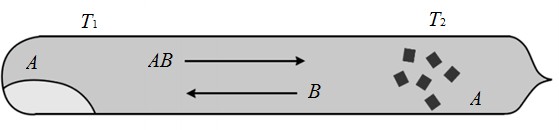 Рис. 1. Схема процесса в замкнутой ампуле Перенос вещества в указанной на рис. 1 ампуле происходит в результате диффузии. В тех случаях, когда наряду с диффузией имеет место и конвекция, количество перенесенного вещества увеличивается. При этом используются ампулы достаточно большого (> 20 мм) диаметра, наклонно установленные, причем нижний конец ампулы - более горячий (рис. 2). 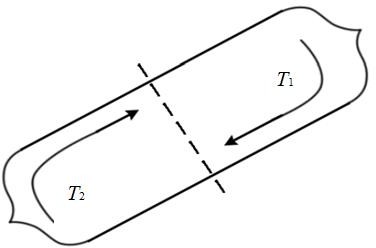 Рис. 2. Движение газа в ампуле вследствие конвекции (Т2>Т1) Реакциипереносавпроточнойсистеме. 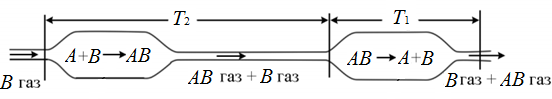 В проточной системе происходит одностороннее движение газового потока, поступающего в атмосферу после отложения вещества в зоне кристаллизации (рис. 3). В проточной системе происходит одностороннее движение газового потока, поступающего в атмосферу после отложения вещества в зоне кристаллизации (рис. 3).Рис. 3. Схема установки для транспорта вещества методом потока Этот метод целесообразно использовать в тех случаях, когда реакция про 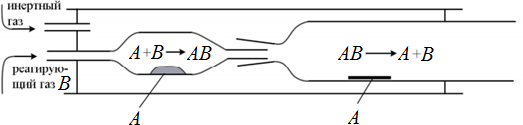 текает быстро и приводит к достаточно полному выделению транспортируемого вещества. Успешно применяется метод потока и при наличии перепада давления. Если газообразные продукты реакции, протекающей с уменьшением объема, продувать через сопло, то на выходе из сопла равновесие сместится; аналогичное влияние оказывает разбавление продуктов реакции инертным газом (рис. 4). текает быстро и приводит к достаточно полному выделению транспортируемого вещества. Успешно применяется метод потока и при наличии перепада давления. Если газообразные продукты реакции, протекающей с уменьшением объема, продувать через сопло, то на выходе из сопла равновесие сместится; аналогичное влияние оказывает разбавление продуктов реакции инертным газом (рис. 4).Рис. 4. Схема установки для транспорта вещества методом потока с подмешиванием инертного газа Хотя зачастую одной и той же реакцией можно пользоваться при кристаллизации в замкнутой и открытой системе, следует заметить, что замкнутая система дает определенные преимущества, когда экспериментатор располагает небольшим количеством вещества, а также при использовании медленно протекающих реакций. С другой стороны, транспорт вещества в открытой системе осуществляется быстрее и сам процесс кристаллизации легче поддается контролю и управлению. Кристаллизация с использованием парофазных реакцийМатериалом для кристаллизации служат пары летучего соединения, переносимые транспортирующим агентом (обычно – водородом). Проходя через нагретую реакционную камеру, захваченные пары, благодаря взаимодействию с водородом или термическому разложению, выделяют вещество, кристаллизующееся на стенках реакционной камеры и на затравке. Рассмотрим некоторые примеры получения монокристаллических пленок в результате разложения хлоридов в присутствии водорода: Получение монокристаллических пленок бора. Над подложкой, нагретой до 1000-1020 °C, пропускается смесь паров BCl3 и H2 со скоростью 1 л/мин: 2BCl3 + 3H2 → B + 6HCl. В течение 15 мин. образуется пленка бора толщиной |
