Ретросинтетический анали1-1. Ретросинтетический анализ это метод постепенного упрощения
 Скачать 0.76 Mb. Скачать 0.76 Mb.
|
|
Ретросинтетический анализ — это метод постепенного «упрощения» молекулярной структуры синтетической молекулы-мишени (TM от англ. target molecule) в более простые и коммерчески доступные вещества, из которых, в конечном итоге, будет синтезирована целевая молекула. При выборе конкретного пути реализации синтеза важнейшее значение имеет число стадий и выходы на стадиях синтеза. Как правило, органические реакции протекают с выходом, меньшим 100%. Поэтому чем меньше число стадий в запланированном синтезе и чем выше выход на каждой стадии, тем ценнее найденное решение. Предположим, что ТМ может быть получена из доступного соединения А1 десяти стадийным синтезом: A1 Такая синтетическая последовательность, представляющая собой последовательное изменение структуры соединения А 1 линейным синтезом (линейной стратегией). Допустим, выход на каждой из десяти стадий такого синтеза составляет 60%. В таком случае выход ТМ в расчете на исходное соединения А1 0,610 . 100 = 0,6% При таком подходе 99% всех синтетических усилий уйдут впустую. Образно эту ситуацию описывают как действие "арифметического демона". Существуют, по крайней мере, два способа борьбы с "арифметическим демоном". Первый из них – увеличение выхода на каждой из стадий. Если бы в рассматриваемом примере удалось поднять выход на каждой стадии до 90%, выход ТМ, считая на А1 составил бы 0,910 . 100 Второй способ разрешения данной ситуации – переход от линейных схем синтеза к сходящимся (конвергентным) [9]. Конвергентный синтез представляет собой две или более цепочки линейных синтезов с меньшим числом стадий. Завершающей стадией синтеза является взаимодействие продуктов таких цепочек, приводящее к ТМ: 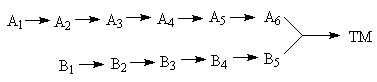 Общее число стадий при таком подходе не сократилось (10). Однако, при выходе на каждой стадии 60%, выход ТМ, считая на А1 составит уже0,66 . 100 = 4,6%. При выходе на стадиях 90%, общий выход ТМ будет равен 0,96 . 100 = 53%, что уже приемлемо для такого синтеза. Упрощение целевой молекулы осуществляется путём применения различных трансформов. Трансформ (Tf) — это мысленно проводимые реакции, обратные реакция синтеза. Конечно, для ТМ может существовать множество способов анализа и синтеза, которые, в совокупности, составляют так называемое «дерево промежуточных структур» Наиболее часто в анализе встречаются следующие типы трансформов: 1.Расчленение, D: расчленение цепи, CHD (chain disconnection); расчленение цикла, RGD (ring disconnection); отщепление функциональной группы, FGD (functional group disconnection); отщепление ответвления, APD (appendage disconnection). 2.Cочленение, R (reconnection): сочленение, например, вцикл, RR (ring reconnection). 3.Введение функциональной группы, FGA (functional group addition). 4.Замена одной функциональной группы на другую, FGI (functional group interconvertion). 5.Перегруппировка, Rt (rearrangement) Планирование синтеза этил 4-аминобензоата При планировании синтеза местного анестетика бензокаина (этил 4-аминобензоат, анастезин) (4.1) известно, что эфиры получаются из спиртов и кислот, следовательно, можно записать С–О-расчленение. Обычно расчленения будут маркироваться, чтобы показать мотив их выполнения. 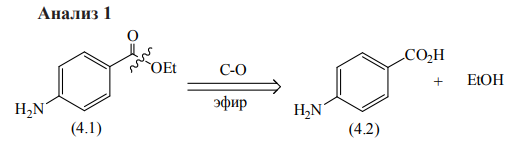 Теперь напрашивается самое простое решение: отчленить СООН- и NH2 -группы от ароматического кольца, но неизвестно ни одной хорошей реакции, соответствующей таким расчленениям. Значит, нужно сначала произвести взаимопревращение функциональных групп (ВФГ), чтобы заменить эти функциональные группы на другие, которые позволят провести расчленение. Ароматические кислоты можно получить окислением метильных групп, а аминогруппы – восстановлением нитрогрупп. Это можно записать следующим образом. 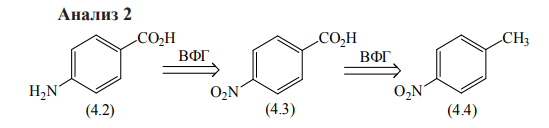 Теперь отчленение нитрогруппы рационально, так как нитрование толуола протекает легко, а сам толуол доступен. 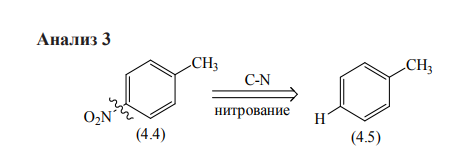 Это придаёт анализу законченный вид, и теперь можно записать синтез с предполагаемыми реагентами. 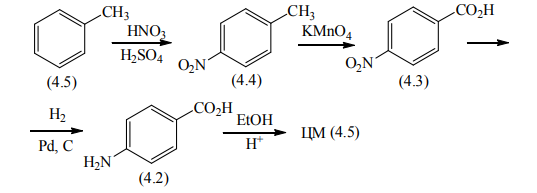 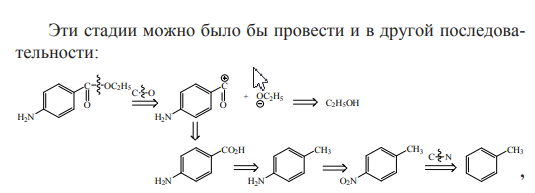 но, в отличие от указанного, альтернативный порядок превращения плох, так как предполагает окисление п-толуидина в п-аминобензойную кислоту — явно ненадежный процесс, поскольку хорошо известно, что электроно-донорная аминогруппа уменьшает стабильность ароматического кольца к окислителям и надеяться на хороший выход здесь вряд ли приходится. , 42 Решения по выбору наиболее перспективного пути синтеза составляют часть стратегии. Пример 2 Предположим, что TM можно расчленить несколькими способами. Из кусков, на которые мы разорвали молекулу не очевидно, какие именно реагенты мы должны использовать для создания соответствующей связи. Для решения этой проблемы, примем два основных для ретросинтетического анализа допущения: 1. Ключевые связи в ходе синтеза должны создаваться малой последовательностью реакций, а лучше – всего одной реакцией. 2. В ходе синтеза, связи будут создаваться реакциями, включающими ионные интермедиаты. Тогда припишем осколкам заряды. 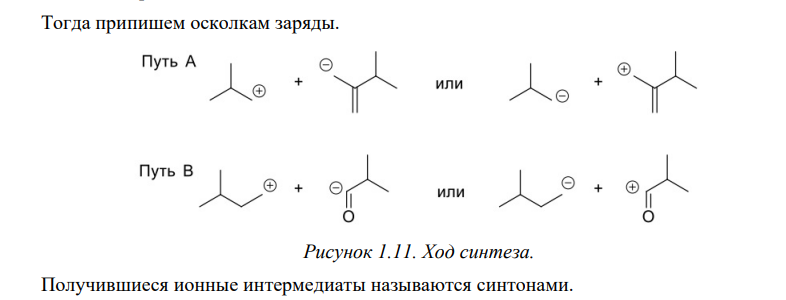 . Синтон – идеализированный фрагмент (катион, анион), возникающий в результате трансформа «расчленение (D)». • Синтон может быть, как реально образующейся частицей, так и виртуальной (то есть существующей только на бумаге). Реальные соединения, используемые для образования химической связи, называются реагентами Синтоны делятся на логичные (естественные) и нелогичные (не естественные). Эти термины применимы только к синтонам, содержащим функциональную группу. В случае рассматриваемых частиц: Неестественность нижнего синтона интуитивно понятна, формально указанный знак минус не соответствует известной полярности связи углерод-кислород в карбонильной группе. (Плюс на углероде, минус на кислороде). Более строгое обоснование терминов будет дано позднее. Остановимся на пути А. Полный анализ по ветви, представлен ниже. Для объяснения терминологии логичный/не логичный рассмотрим две различные модели распределения зарядов в молекуле 2,4-ен-пенталя. 1. Модель Ингрида – основана на химической реакционности, используется сегодня для описания того, как распределён заряд в молекуле. 2. Модель Лэпворда – основана на принципе альтернировании заряда в молекуле, то есть предположении о том, что один диполь (СО группа) наводит за собой другой и так далее. Для целей ретросинтетического анализа мы будем пользоваться моделью Лэпворда. Если заряд в синтоне соответствует альтернированию зарядов в исходной молекуле – то такой синтон называется логичным. Если такого соответствия не наблюдается, то синтон называют нелогичным. Пример Рассмотрим различные расчленения производного ацетилацетона c целью того, чтобы распланировать синтез. В случае расчленения D1 минус и плюс поставим так, как указано на рисунке, так как этот выбор зарядов для синтонов, сразу же приводит нас к реагентам: еноляну для частицы с минусом и хлорангидриду для синтона со знаком плюс. Очевидно, что в случае D2 так же не составляет труда подобрать реагенты. Анализируя распределение зарядов на рассматриваемых синтонах, видно, что в случае обоих расщеплений на центральном углероде находится отрицательный заряд, а на карбонильных положительный. Тогда, чисто формально можно написать схему исходной молекулы с распределением зарядов, которая будет обозначать то, какие синтоны будут образовываться при расчленении. Несложно заметить, что эта формальная схема согласуется с концепцией альтернирования зарядов. Пример 3. Планирование синтеза 1-(метоксифенил)этанона Другое полезное расчленение соответствует реакции Фриделя–Крафтса, которую можно использовать в синтезе 1-(метоксифенил)этанона (4.6) — душистого вещества цветов боярышника. Это одностадийный синтез из доступного эфира. 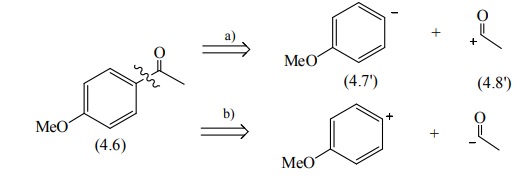 Проводим расчленение . Модели альтернатирования Лемпорда будет соответствовать путь а. Когда анализ завершён, синтоны должны быть заменены реагентами для практического использования. Для анионного синтона реагентом часто является соответствующий углеводород – для катионного синтона реагентом часто является соответствующий галогенид. 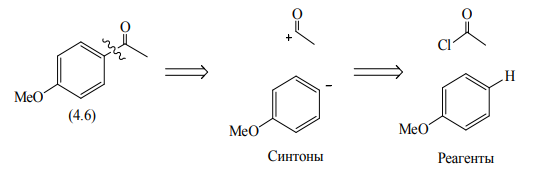 Мощные реакции – это такие реакции, которые в одну стадию сильноусложняют строение молекулы. Следовательно, расчленение следует проводить в соответствии с этими реакциями, например: Реакция Дильса-Альдера (карбоциклическая, с хинонами, гетеро реакция); Аннелирование по Робинсону; Парциальное восстановление по Бёрчу; Внитримолекулярная π-циклизация; Альдольная, ацилоиновая конденсация; Катионные, сигматропные перегруппировки; Конденсация Манниха; Олефинирование по Виттигу. Стратегические связи – связи, расчленение по которым приводит к значительному упрощению структуры. Стратегические связи можно выявить в соответствии с мощными реакциями. Помимо этого, не анализируя структуру на соответствие мощным реакциям, стратегическими зачастую являются: Ретронный подход — заключается в том, чтобы выделить из структуры ключевой фрагмент, который будет считаться главным. Этот фрагмент и называется ретроном. Ретрон — это совокупность необходимых и достаточных элементов в структуре молекулы, позволяющая провести определённый трансформ. Понятия трансформ, синтон, ретрон являются фундаментальными для ретросинтетического анализа. Ретроны именуются по названиям трансформа, то есть в соответствии с той синтетической реакцией, которая используется для перехода к соединению, содержащему ретрон. (В примерах 3-5 мы имели дело с ретроном Манниха, Ретроном Дильса-Альдера и Ретроном Гриньяра, соответственно). В некоторых случаях молекула содержит не полный, а частичный ретрон. Это происходит тогда, когда выполняется условие необходимости, но не достаточности. В таких случаях неполный синтон следует дополнить до полного. Сразу можно понять, что центральный цикл в молекуле является образуется в ходе реакции Дильса-Альдера. Ключевой фрагмент, который позволил провести нам это расчленение — шестичленный цикл с двойной связью.  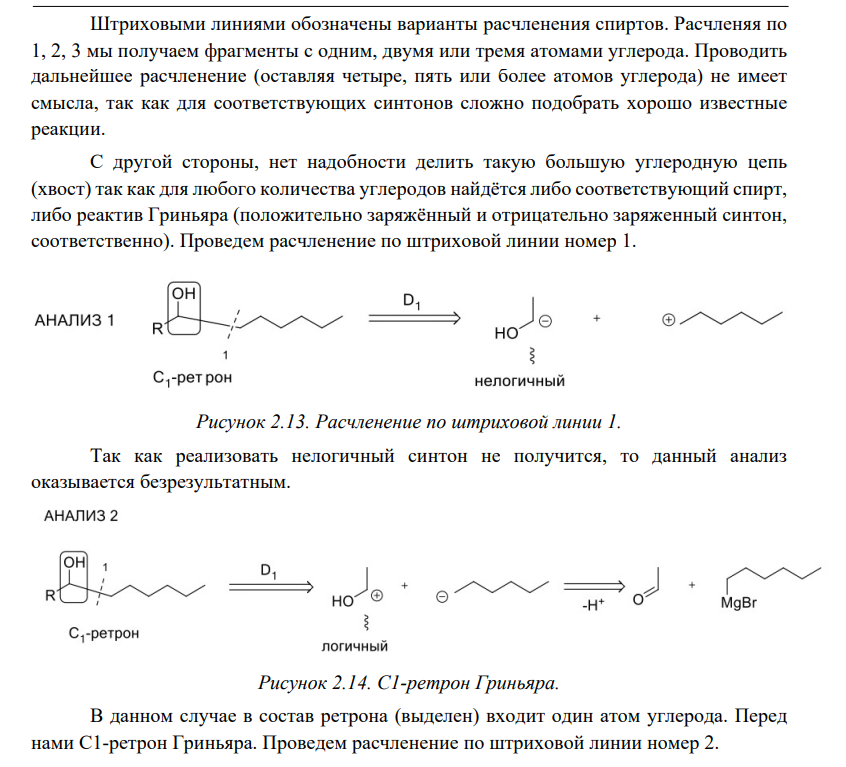 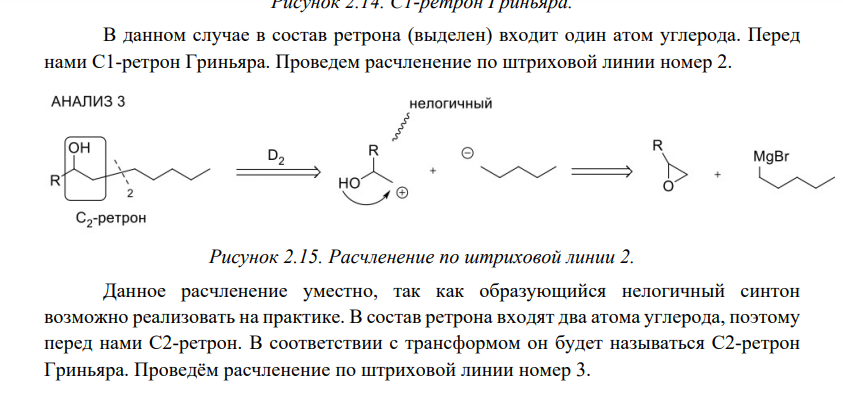 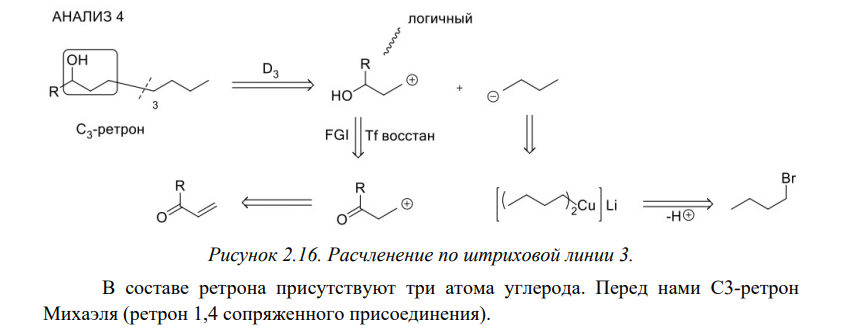 Несколько примеров, которые показывают ретрон в целевой молекуле (выделен красным) и трансформ, с помощью которого синтезируется данное соединение: Задания: Задания: 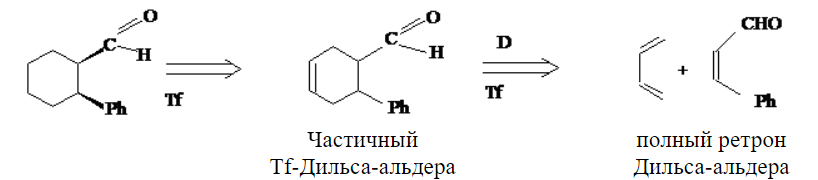 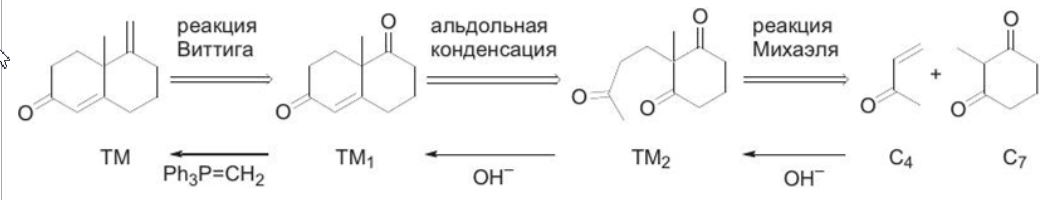 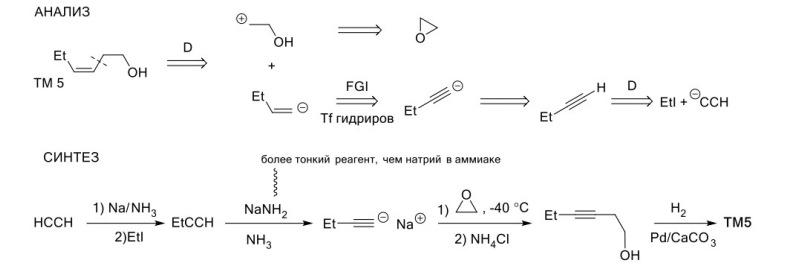 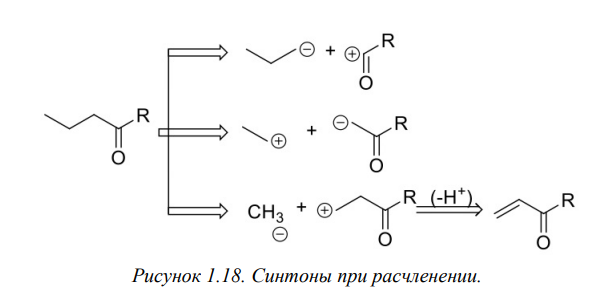 К сожалению, даже имея такое соединение, с ним будет невозможно провести реакцию Дильса-Альдера так, как и диен и диенофил содержат электроноакцепторную группу. Поэтому, можно заключить, что ТМ4 содержит ретрон Дильса-Альдера, но частичный. Для осуществления трансформа проведём модификацию ТМ4. 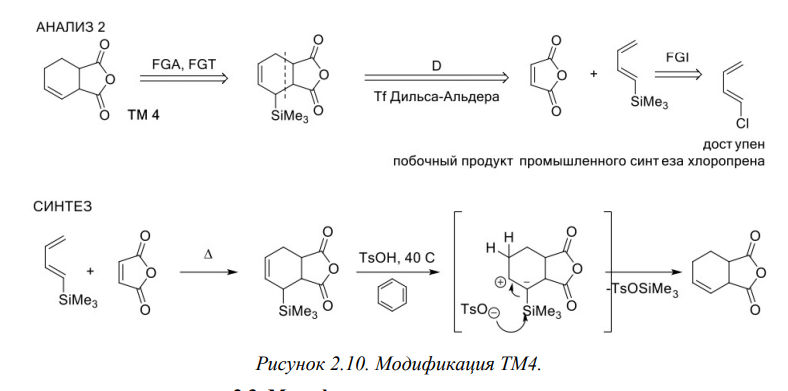 |
