Основные методы концентрирования и выделения продуктов биосинтеза (флотация, экстракция, осаждение, кристаллизация, ионный обмен. ПОПБ 2 концентрир. Рис принцип действия флотатора
 Скачать 1.67 Mb. Скачать 1.67 Mb.
|
|
Основные методы концентрирования и выделения продуктов биосинтеза (флотация, экстракция, осаждение, кристаллизация, ионный обмен, хроматография) ФЛОТАЦИЯ— это выделение клеток микроорганизмов из культуральной жидкости за счет адгезии (прилипания) микроорганизмов к поднимающимся в жидкости пузырькм воздуха и затем сбора пены и ее конденсации (коалесценции). Обычно чем меньше пузыри, тем медленнее они поднимаются и тем больше время пребывания их в жидкости и вероятность захвата клеток микроорганизмов. 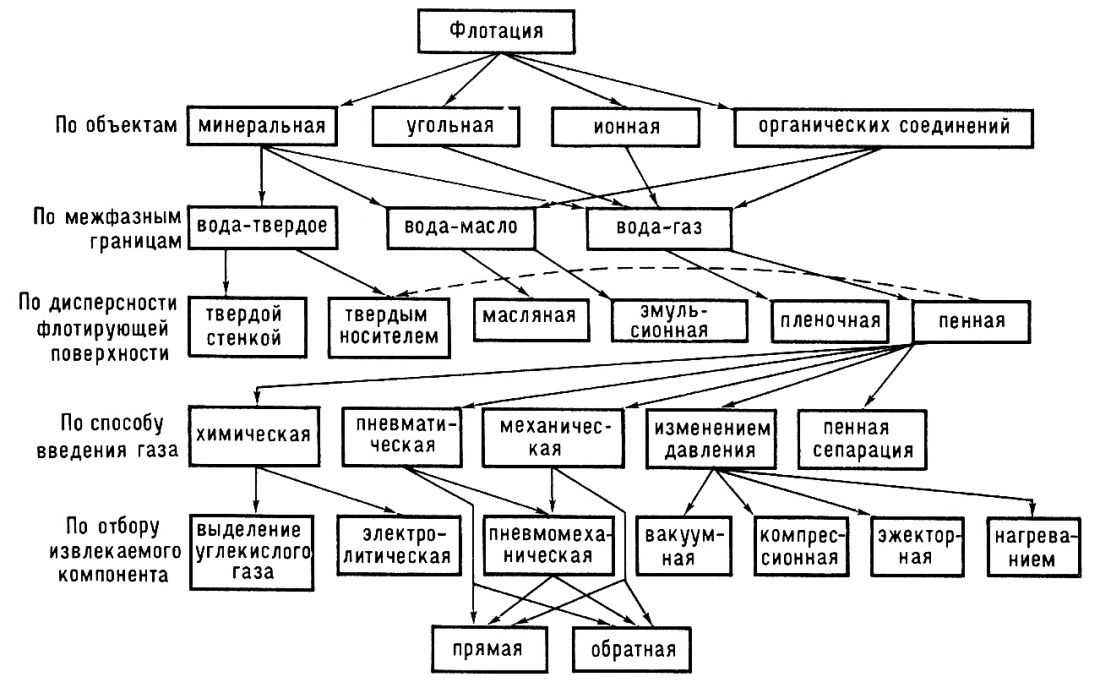 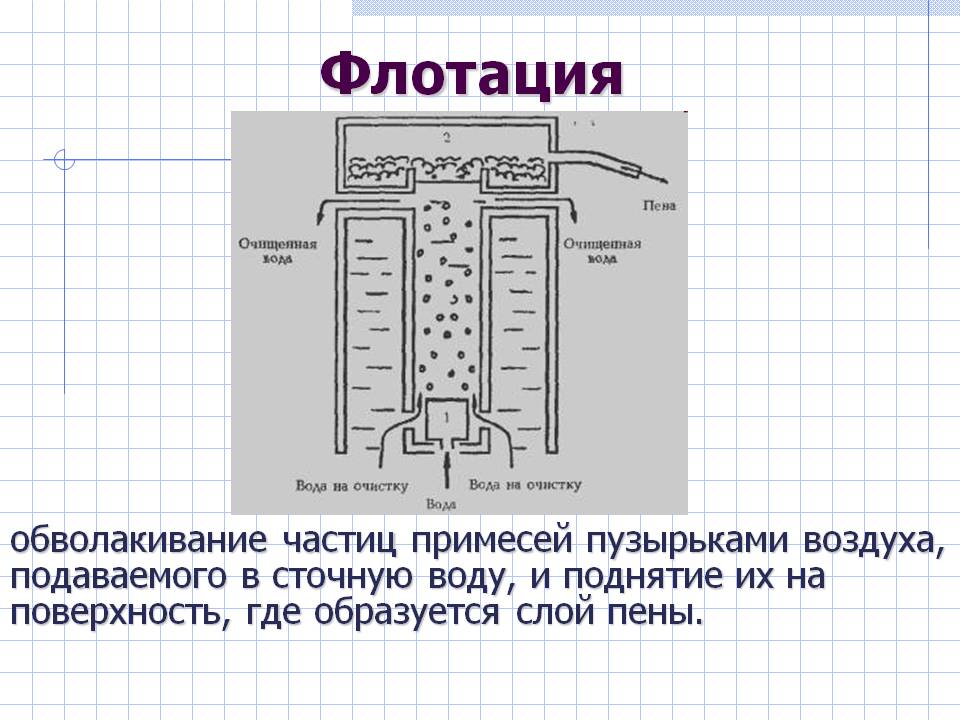  Процесс флотации протекает в несколько стадий: 1) закрепление клеток на поверхности всплывающего пузыря; 2) вынос их с пузырем в верхний слой структурированной пены; 3) удаление пены из флотатора вместе с твердыми частицами (микроорганизмами). Этот способ концентрирования суспензий наиболее эффективен в производстве дрожжей как первая стадия концентрирования, т.е. при небольших концентрациях твердой фазы. При флотации образуется пенный слой с концентрацией дрожжей в 4-6 раз большей, чем в исходной КЖ. Применение флотации в дрожжевом производстве позволяет сократить количество дорогостоящих сепараторов и снизить энергозатраты. Перспективно также применение флотаторов при сгущении и концентрировании активного ила при биологической очистке сточных вод. Флотируемые дрожжевые клетки взаимодействуют с газовыми пузырями как лиофобные (боящиеся растворения) твердые тела. Веществом, которое придает лиофобные свойства поверхности клеток, накапливаясь на них, является азотосодержащий полисахарид – хитин.[1] Влияет на процесс флотации и кислотность КЖ. Наилучшая флотируемость дрожжей при pH 4,5. 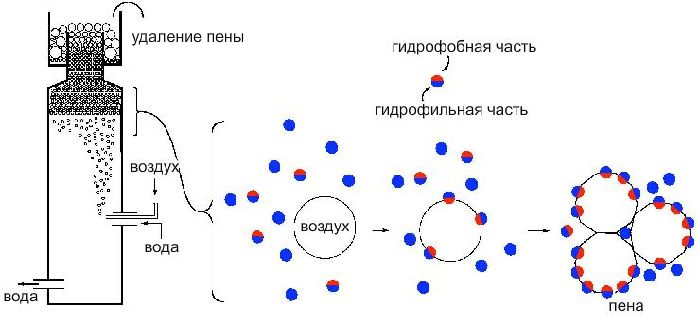 Рис – принцип действия флотатора Эффективность флотации зависит от способа образования пузырей и их размера. В связи с этим различают следующие способы флотации: диспергированным воздухом, растворенными газами и электрофлотация. Наиболее распространена флотация диспергированным воздухом, когда воздух диспергируется в жидкости до пузырьков диаметром >1мм с помощью различных диспергирующих устройств. Способ прост по аппаратурному оформлению, но требует больших расходов воздуха. Из-за относительно больших пузырей эффективность данного способа флотации невелика.[1] 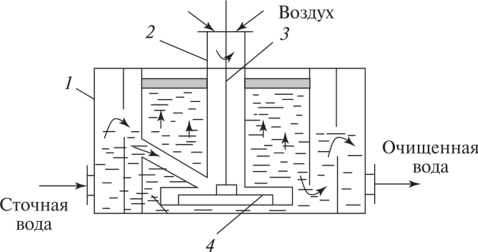 Флотация растворенным воздухом подразделяется на напорную и вакуумную флотацию. Суть напорной состоит в предварительном насыщении жидкости растворенным воздухом при избыточном давлении в 7 атм с последующей подачей ее во флотатор, работающий при атмосферном давлении. При этом воздух выделяется из пересыщенного раствора в виде мелких пузырей диаметром 0,1-0,5 мм, что обеспечивает высокую эффективность флотации. 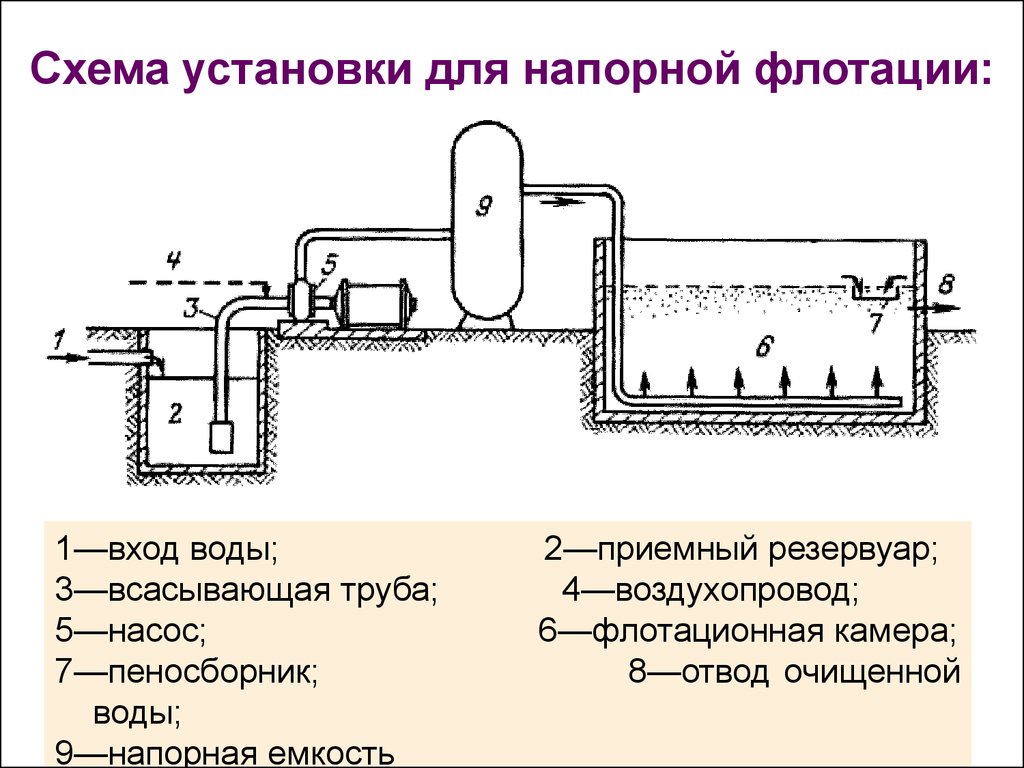 При вакуумной флотации создается разряжение над флотируемой средой и воздух также выделяется из жидкости, но уже в меньших количествах и в виде еще меньших пузырей. Вакуумная флотация лимитируется малым DP и используется при малых концентрациях суспензий С<0,03%. 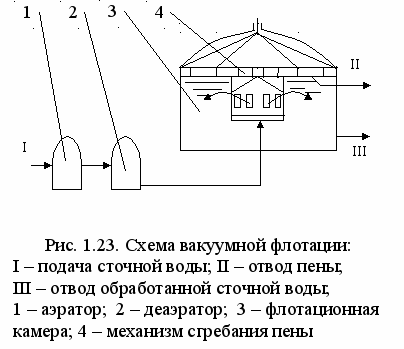 Электрофлотация. При электрофлотации на электродах в жидкой среде выделяются водород и кислород в виде пузырьков d<0,05мм. Но этот метод имеет ограниченное применение из-за взрыво-пожароопасности процесса, проблем загрязнения электродов, малой единичной мощности и энергоемкости. 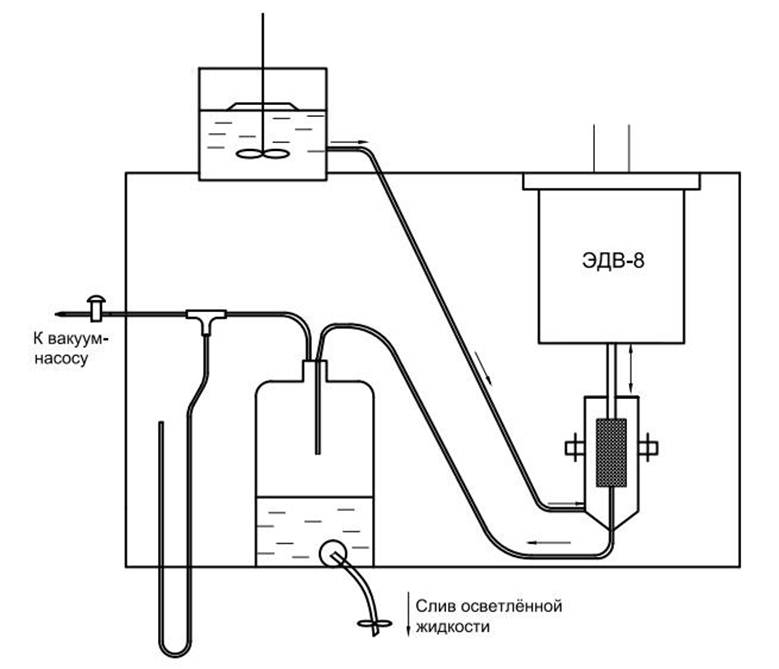 Рис – схема электрофлотационного аппарата Основным показателем процесса является коэффициент флотации, представляющий собой отношение концентрации биомассы в суспензии, выходящей из флотатора к концентрации биомассы в исходной суспензии. Коэффициент зависит от вязкости исходной среды и длительности отстаивания пены. В производственных условиях обычно равен 4-6; при увеличении его до 8-10 резко снижается производительность флотатора.[2] 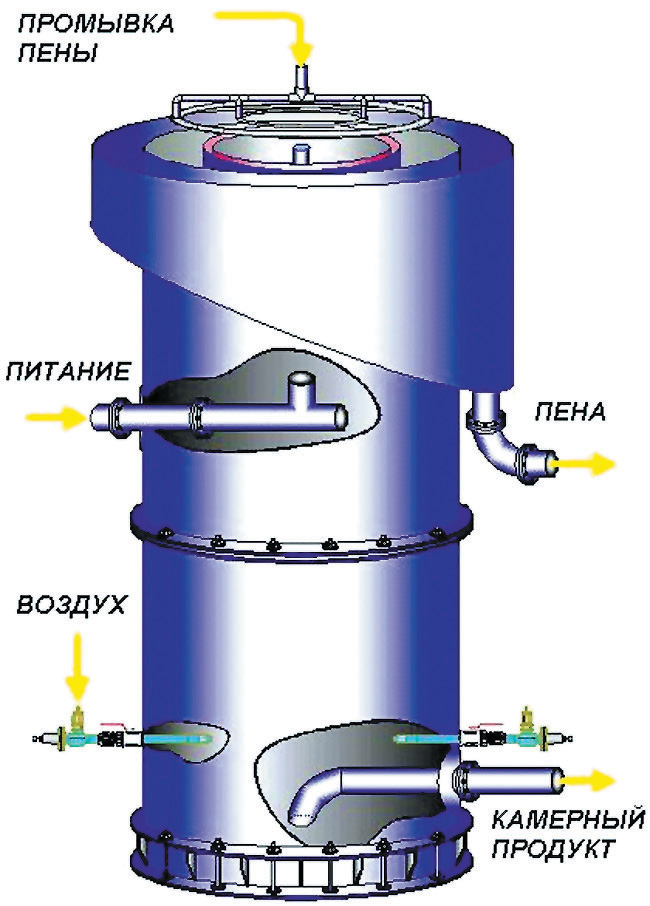 Рис – колонная флотация Экстракция Экстракцией называют процесс извлечения одного или нескольких компонентов из раствора с помощью избирательного растворителя. Экстракция широко используется для очистки производственных сточных вод от солей металлов, фенолов и других соединений. При экстракции исходный раствор и несмешивающийся с ним экстрагент приводят в контакт между собой, в результате чего экстрагируемое вещество переходит из раствора в экстрагент. В результате экстракции образуются экстракт – раствор извлекаемого вещества в экстрагенте и рафинат – остаточный исходный раствор, из которого в той или иной степени удалены экстрагируемые компоненты. Экстракт и рафинат отделяют друг от друга отстаиванием, после чего извлекают экстрагированное вещество из экстракта и проводят регенерацию экстрагента из рафината. Экстракция протекает в двухфазной трехкомпонентной системе. Компонентами этой системы являются: растворитель, из которого извлекается экстрагируемое вещество экстрагент и экстрагируемое вещество. Одной из фаз является раствор экстрагируемого вещества в воде, другой – раствор экстрагируемого вещества в экстрагенте. Не существует нерастворимых друг в друге жидкостей. Экстрагент частично растворяется в воде, а вода – в экстрагенте. Движущей силой процесса экстракции является разность химических потенциалов распределяемого вещества в воде и экстрагенте. Переход вещества из одной фазы в другую будет продолжаться до момента выравнивания этих потенциалов, т.е. до наступления равновесия. Методы экстракции. 1) Одноступенчатая (однократная) экстракция. Этот простейший метод экстракции заключается в том, что исходный раствор F, состоящий из двух компонентов: растворителя (воды) W и растворенного вещества B, перемешивают с экстрагентом S в смесителе периодического действия, после чего смесь сливают в сепаратор-отстойник. В отстойнике смесь разделяется на два слоя: экстракт E = S + B и рафинат R = W + B. При достаточном времени контакта могут быть получены близкие к равновесным концентрации распределяемого вещества B в экстракте и рафинате. 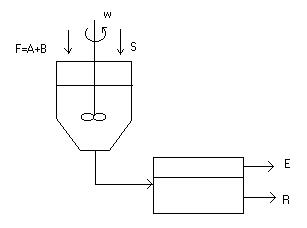 Рис. Схема одноступенчатой экстракции 2)Многоступенчатая экстракция при перекрестном потоке. Экстракция этим способом проводится в нескольких ступенях, через которые последовательно движется исходный раствор. Во всех ступенях, начиная со второй, исходным раствором является рафинат предыдущей ступени. Экстрагент подается во все ступени параллельно. 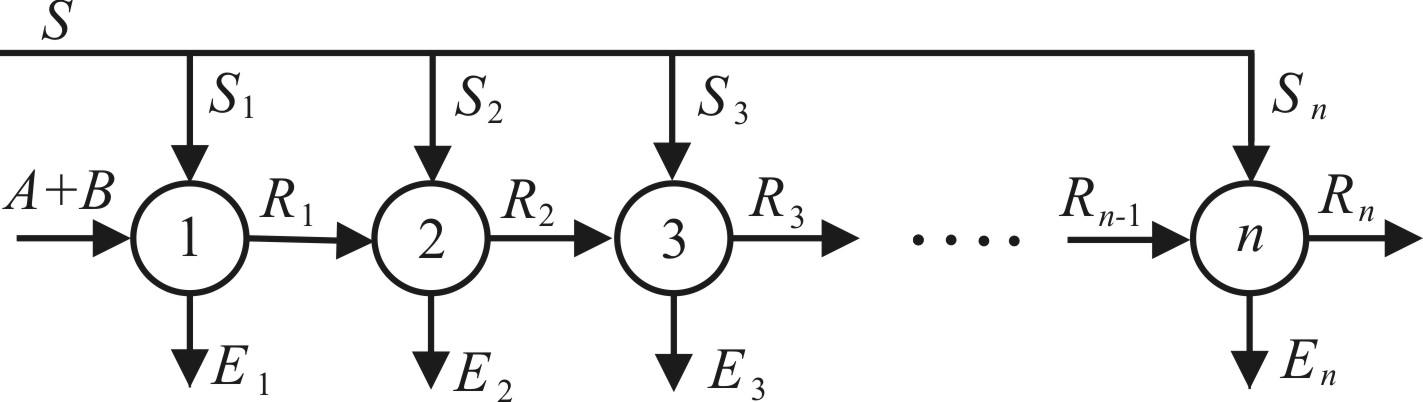 Рис.. Схема многоступенчатой экстракции На каждую следующую ступень подаются все более обедненные экстрагируемым веществом рафинаты, поэтому концентрации экстрактов снижаются от первой ступени к последней. В результате для получения рафината высокой чистоты требуются большие объемные соотношения экстрагента и исходного раствора, что связано с удорожанием всего процесса экстракции. Поэтому процессы такого типа применяют в промышленности в редких случаях, когда для экстракции можно применить дешевый экстрагент и утилизировать его без регенерации. 3) Многоступенчатая противоточная экстракция. По этой схеме исходный раствор и экстрагент поступают с противоположных концов установки и движутся противотоком друг к другу через ряд последовательных ступеней. 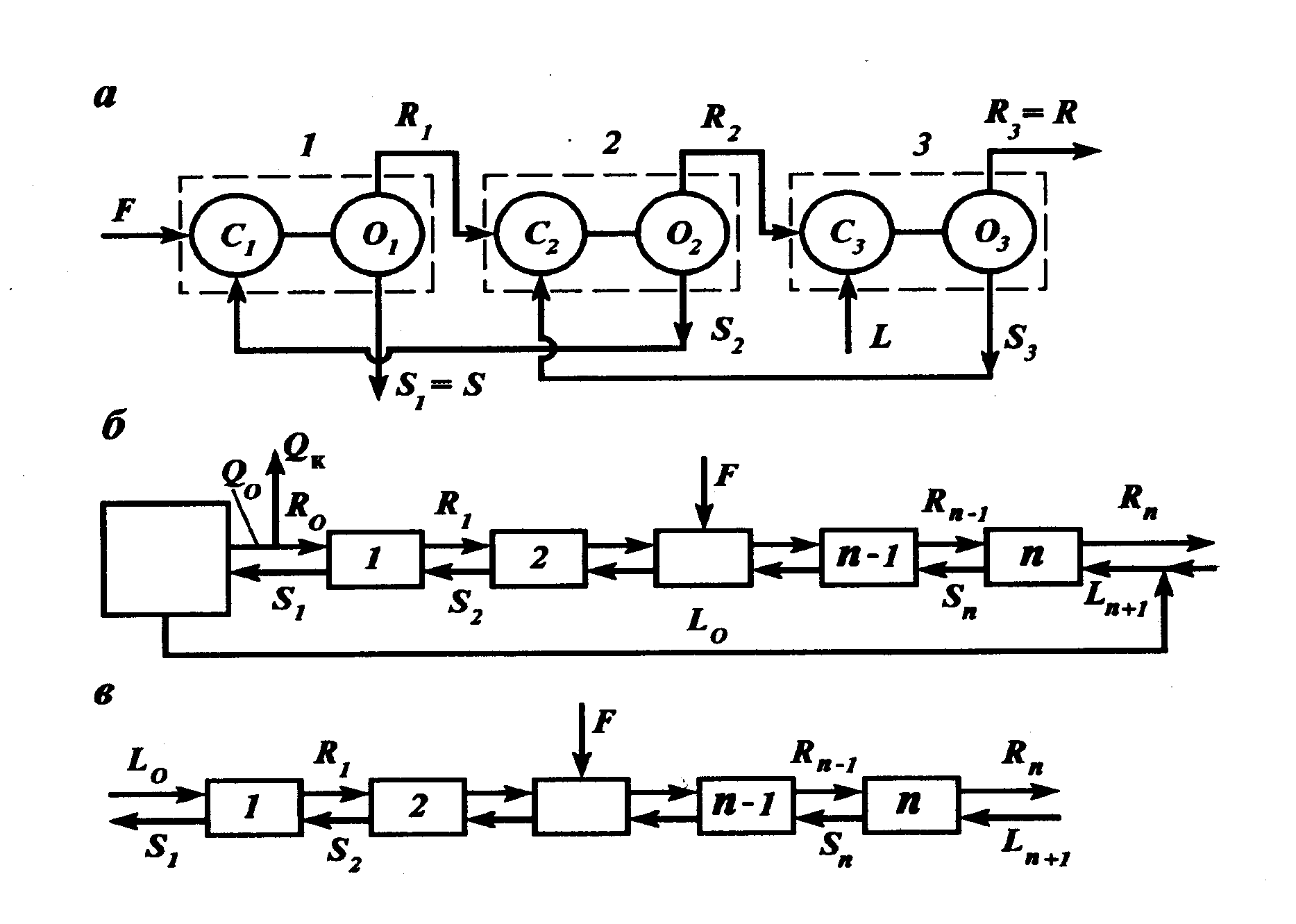 Рис. Схема многоступенчатой противоточной экстракции Смесительно-отстойные экстракторы. Экстракторы этого типа состоят из ряда ступеней, каждая из которых содержит смеситель и отстойник. Движение жидких фаз через ступени осуществляется в режиме противотока. Экстрагент подается в смеситель последней ступени. Туда же параллельным потоком подается рафинат из отстойника предыдущей ступени. После смешения фазы разделяются в отстойнике последней ступени, откуда конечный рафинат удаляется в качестве основного продукта, а экстракт направляется в смеситель предыдущей ступени.[2] Смешение жидкостей может происходить не только с помощью механических мешалок, но и посредством насосов, инжекторов и другими способами. Разделение фаз можно осуществлять не только в гравитационных отстойниках, но и в сепараторах центробежного типа. 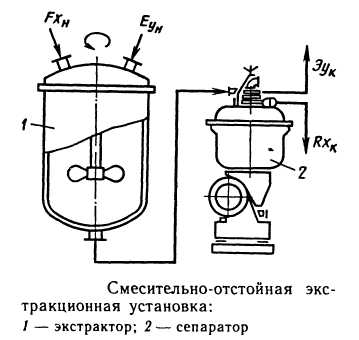 Недостатками экстракторов этого типа является сложность конструкции, обусловленная наличием мешалок в каждой ступени, и большая площадь, занимаемая установкой. Капитальные затраты и эксплуатационные расходы для таких экстракторов выше, чем для экстракторов других типов. Распылительные колонны. Распылительный колонный экстрактор представляет собой полую колонну, оборудованную устройствами для ввода и вывода фаз. Легкая фаза, которой может быть и экстрагент, и водный раствор, подается в нижнюю часть колонны. Проходя через отверстия распределителя, легкая фаза диспергируется на капли и движется снизу вверх через слой тяжелой фазы, которой заполнена колонна. В верхней части колонны находится верхняя отстойная зона, имеющая больший диаметр по сравнению с колонной.[2] 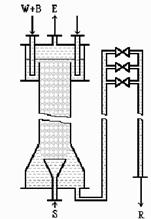 Рис - Распылительный колонный экстрактор В этой зоне происходит отделение легкой фазы от эмульсии и вывод ее из аппарата. Тяжелая фаза подается на дно верхней отстойной зоны, переливом поступает в колонну и собирается в нижней отстойной зоне. Вывод тяжелой фазы осуществляется через гидравлический затвор, с помощью которого достигается полное заполнение колонны жидкостью. Уровень раздела фаз в колонне регулируется высотой перелива тяжелой фазы с помощью вентилей. Каждому расходу тяжелой фазы соответствует некоторый оптимальный расход легкой фазы. С увеличением расхода легкой фазы возрастает число ее капель в единице объема аппарата, и уменьшается доля поперечного сечения, свободного для прохождения сплошной тяжелой фазы. Это, в свою очередь, вызывает возрастание локальных скоростей относительного движения фаз, и все большее число капель начинает двигаться вниз вместе с тяжелой фазой, т.е. навстречу основному потоку легкой фазы. Возникают циркуляционные токи дисперсной фазы (обратное перемешивание), которые существенно уменьшают среднюю движущую силу процесса и интенсивность экстракции. Дальнейшее увеличение расхода тяжелой фазы приведет к уносу капель из зоны экстракции, образованию второй поверхности раздела фаз в нижней отстойной зоне, нарушению противотока, т.е. к захлебыванию колонны.[2] С уменьшением расхода дисперсной (легкой) фазы резко снижается поверхность раздела фаз как за счет уменьшения числа капель в единице объема, так и за счет увеличения их размеров. При этом происходит пропорциональное снижение степени извлечения экстрагируемого компонента. Распылительные экстракторы характеризуются простотой конструкции, высокой производительностью, но вместе с тем очень низкой интенсивностью экстракции. Полочные колонные экстракторы. Полочные экстракторы представляют собой колонны с тарелками-перегородками различной конструкции. Перегородки имеют форму либо чередующихся дисков и колец, либо дисков с вырезами в виде сегментов. Расстояние между соседними полками составляет обычно 50 – 150 мм. 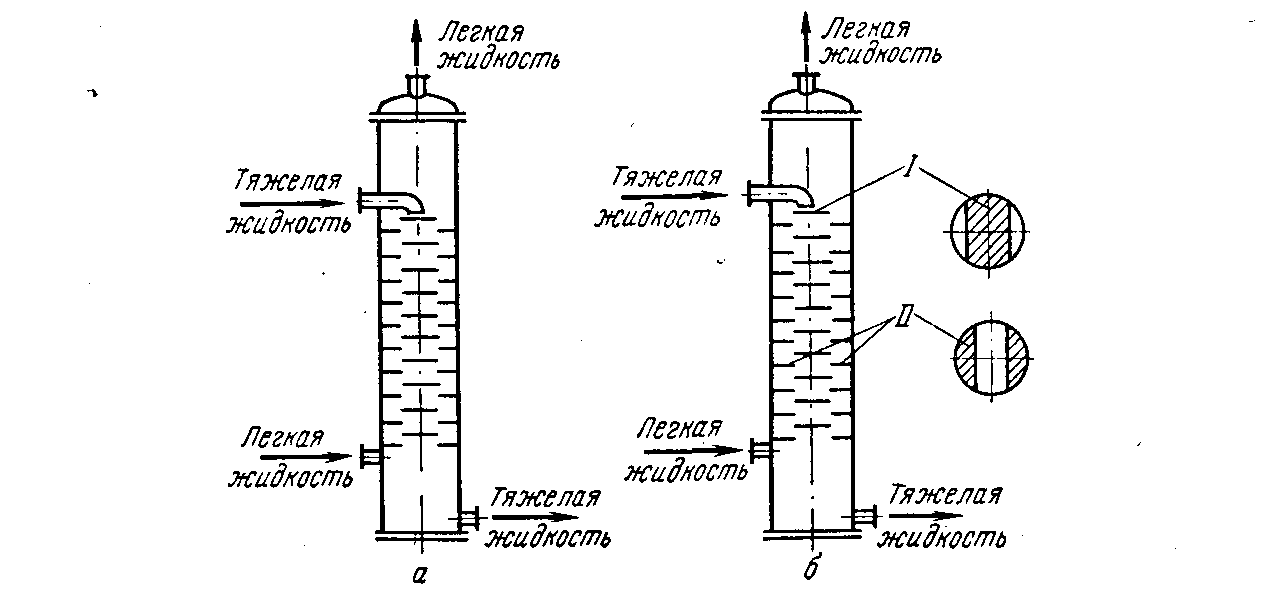 Рис. Полочный колонный экстрактор Легкая жидкость (экстрагент) при движении вверх разбивается на капли, которые под каждой полкой сливаются друг с другом и обтекают полку в виде ламинарной пленки, которая омывается сплошной фазой. Интенсивность массопередачи в полочных колоннах несколько выше, чем в распылительных, главным образом за счет уменьшения обратного перемешивания. Осаждение Осаждение — это образование твердого осадка в растворе в ходе химической реакции, например, добавлением соответствующих реагентов.  Различают два вида осаждения: физическое, которое иногда называют вакуумно-конденсационным напылением, и химическое или газофазное. Физическое осаждение. Осаждение тонких пленок в вакууме включает три этапа: генерацию атомов или молекул, перенос их к поверхности заготовки, наращивание пленки на подложке. Состав и структура образующейся пленки зависят от свойств исходных материалов, метода и режимов нанесения покрытий. Физическое осаждение обеспечивает необходимый энергомассоперенос материала на поверхность изделия. При этом могут использоваться любые твердые материалы: металлы, сплавы, полимеры, стекло, керамика, полупроводники, дерево, ткани и т. д.[3] Получение покрытий методом термического испарения осуществляется путем нагрева распыляемого материала лазерным лучом, потоком электронов и др. При температуре вещества, равной либо превышающей температуру испарения, атомы или молекулы покидают испаритель, переносятся в вакууме на подложку и конденсируются на ее поверхности в виде тонкой пленки . 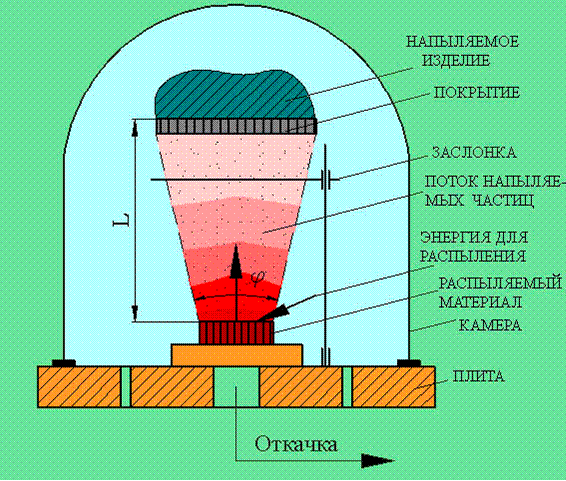 Рис. Обобщающая схема процесса физического осаждения покрытий К достоинствам этого метода относятся высокая чистота осаждаемого материала (процесс проводят в высоком и сверхвысоком вакууме) и универсальность (наносят пленки металлов, сплавов, полупроводников, диэлектриков). Ограничениями метода являются нерегулируемые скорость и энергия осаждаемых частиц. Среди методов физического осаждения большое значение приобретает алюминирование пластмассовых и стальных изделий путем термического испарения алюминия. Этот технологический процесс широко используется в оптической технике для получения тонких пленок металлических и неметаллических материалов, способных изменять прохождение световых волн. Особенностью технологии физического осаждения материала является возможность управлять параметрами тонкопленочных покрытий с помощью изменения структуры, толщины и состава пленки. Преимуществом физического осаждения является то, что заготовка находится при температуре окружающей среды. Для получения осадка в надлежащем месте температура изделия должна быть ниже температуры испаряемого вещества Химическое осаждение. Разложение карбонильных, галоидных и других соединений при химическом осаждении проводят при низком давлении, в результате чего получают осадок высокой степени чистоты и равномерности. 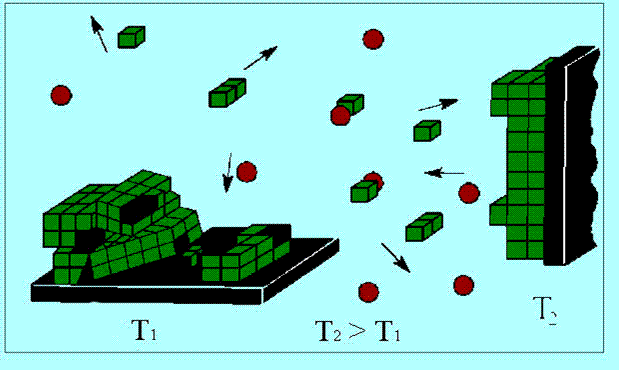 Рис.. Схема процесса химического осаждения из газовой фазы Главными преимуществами метода химического осаждения являются широкий диапазон скоростей осаждения и возможность получения заданной кристаллической структуры пленки (вплоть до монокристаллов). Основным недостатком является необходимость применения токсичных, экологически небезопасных газовых смесей. Оборудование для отстаивания и осаждения но принципу действия делится на гравитационные отстойники, отстойные центрифуги, гидроциклон и сепараторы. Отстойники бывают периодического, непрерывного и полунепрерывного действия. Отстойник периодического действия представляет собой плоский бассейн без перемешивающих устройств. Бассейн заполняется суспензией, которая отстаивается в нем в течение необходимого для разделения времени, затем осветленный слой жидкости сливают (декантируют) через штуцера расположенные выше слоя осадка. Осевший осадок (шлам) выгружают вручную. Размеры и форма отстойников зависят от концентрации дисперсной фазы и размеров частиц. С увеличением плотности и размеров частиц размеры отстойника уменьшаются. Продолжительность отстаивания зависит от вязкости дисперсионной фазы, которая снижается с повышением температуры Поэтому для ускорения процесса отстаиваемую суспензию подогревают (если это не противоречит технологии).[3] 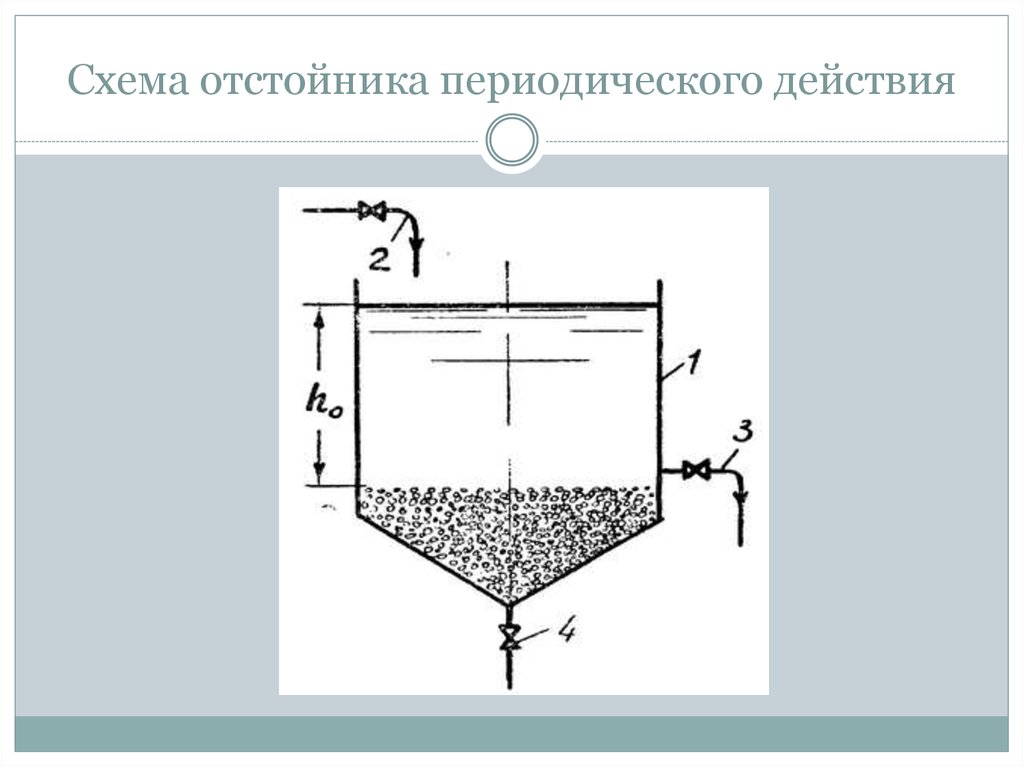 В отстойник полунепрерывного действия с наклонными перегородками суспензия подается через штуцер и направляется с помощью наклонных перегородок попеременно сверху вниз и снизу вверх. Устройство перегородок увеличивает продолжительность пребывания суспензии и площадь поверхности отстаивания. Шлам собирается в конических бункерах и по мере накопления удаляется из них через краны. Осветленная жидкость отводится из отстойника через верхний штуцер.  Наибольшее распространение в промышленности получили отстойники непрерывного действия. Непрерывнодействующий отстойник с гребковой мешалкой представляет собой цилиндрический резервуар с коническим днищем и внутренним кольцевым желобом вдоль верхнего края отстойника. Мешалка с наклонными лопастями, на которых расположены гребки для перемещения осадка к разгрузочному люку, вращается с переменной частотой от 0,02 до 0,5 мин-1 .  Рис. 2 Отстойник непрерывного действия с гребковой мешалкой: 1 — кольцевой желоб; 2 — мешалка; З — гребок; 4—люк; 5 — коническое днище; б— цилиндрический резервуар Суспензия непрерывно подается по трубе в середину резервуара. Осветленная жидкость переливается в кольцевой желоб и отводится из отстойника. Шлам удаляется при помощи диафрагменного насоса. Извлечение жидкости из шлама, если она является ценной для производства или ее извлечение необходимо по технологическим условиям, производится в установке для противоточной промывки. В таких отстойниках достигаются равномерная плотность осадка, эффективное его обезвоживание. Недостатком гребковых отстойников является их громоздкость. В многоярусных отстойниках, которые представляют собой несколько отстойников, поставленных один на другой, или цилиндрический резервуар с коническим днищем, внутри которого имеются конические перегородки, разделяющие отстойники на ярусы, значительно снижена громоздкость и увеличена площадь поверхности отстаивании. Такие отстойники используются на сахарных заводах для сгущения сатурационных соков.[3]  Рис. 3 Многоярусный отстойник: 1 —- распределительное устройство; 2— трубы; 3—стакан; 4 гребковая мешалка; 5 — разгрузочный конус; б— скребок; 7— коллектор; 8 — рама Центрифуги могут быть с вертикальным и горизонтальным расположением вала и барабана, периодического действия, полунепрерывного и непрерывного действия. Отстойная центрифуга периодического действия с ручной выгрузкой осадка состоит из барабана, насаженного на вращающийся вал и помещенного в корпус. Под действием центробежной силы, возникающей при вращении барабана, твердые частицы осаждаются в виде сплошного слоя осадка на стенке барабана, а осветленная жидкость переливается в кожух и удаляется через расположенный внизу патрубок. По окончании процесса осадок выгружается из центрифугу.[3] Процесс в отстойной центрифуге состоит из разделения (осаждения) суспензии и отжима или уплотнения осадка. Непрерывнодействующие отстойные горизонтальные центрифуги со шнековой выгрузкой осадка (НОГШ) применяются в крахмало-паточном производстве для получения концентрированного крахмального осадка и в других производствах. Центрифуга состоит из ротора и внутреннего шнекового устройства, заключенных в корпус. Суспензия подается через центральную трубу в полый вал шнека. На выходе из этойl трубы внутри шнека суспензия под действием центробежной силы распределяется в полости ротора. Ротор вращается в кожухе в полых цапфах. Шнек вращается в цапфах, находящихся внутри цапф ротора. Под действием центробежной силы твердые частицы отбрасываются к стенкам ротора, а жидкость образует внутреннее кольцо, толщина которого определяется положением сливных отверстии на торце ротора. Образовавшийся осадок переметается вследствие отставания скорости вращения шнека от скорости вращения ротора к отверстиям в роторе, через которые он выводится в камеру 6 и удаляется из центрифуги.[3] 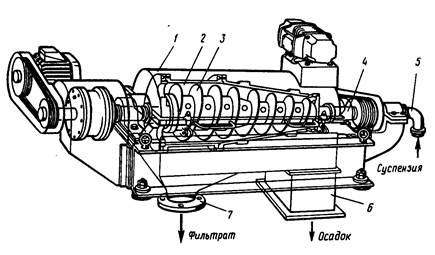 Рис.6 Непрерывнодействующая отстойная горизонтальная центрифуга со шнековой выгрузкой осадка: 1 корпус; 2 — ротор; З — шнековое устройство; 4 —. полый вал; 5 — центральная труба; б —камера осадка; 7— патрубок для фильтрата При движении вдоль ротора осадок уплотняется. При необходимости он может быть промыт. Осветленная жидкость отводится через сливные отверстия в камеру фильтрата и удаляется через патрубок 7. За счет изменения частоты вращения ротора и шнека можно регулировать режим работы центрифуги, изменяя продолжительность отстаивания и выгрузки осадка. Сепараторы применяются для разделения тонкодисперсных суспензий и эмульсий: обеспечивают эффективное отделение дрожжей от сброженной бражки, тонкое осветление виноматериалов, обезжиривание молока и др. Тарельчатый дрожжевой сепаратор с внутренними соплами состоит из барабана и пакета тарелок, заключенных в корпус, который смонтирован на общей раме с электродвигателем. Вал с насаженными на него тарелками приводится во вращение электродвигателем через ременную передачу. Сепаратор снабжен клапанами для его безразборной промывки. Клапаны автоматически открываются при снижении частоты вращения за счет накопления осадка.[4] 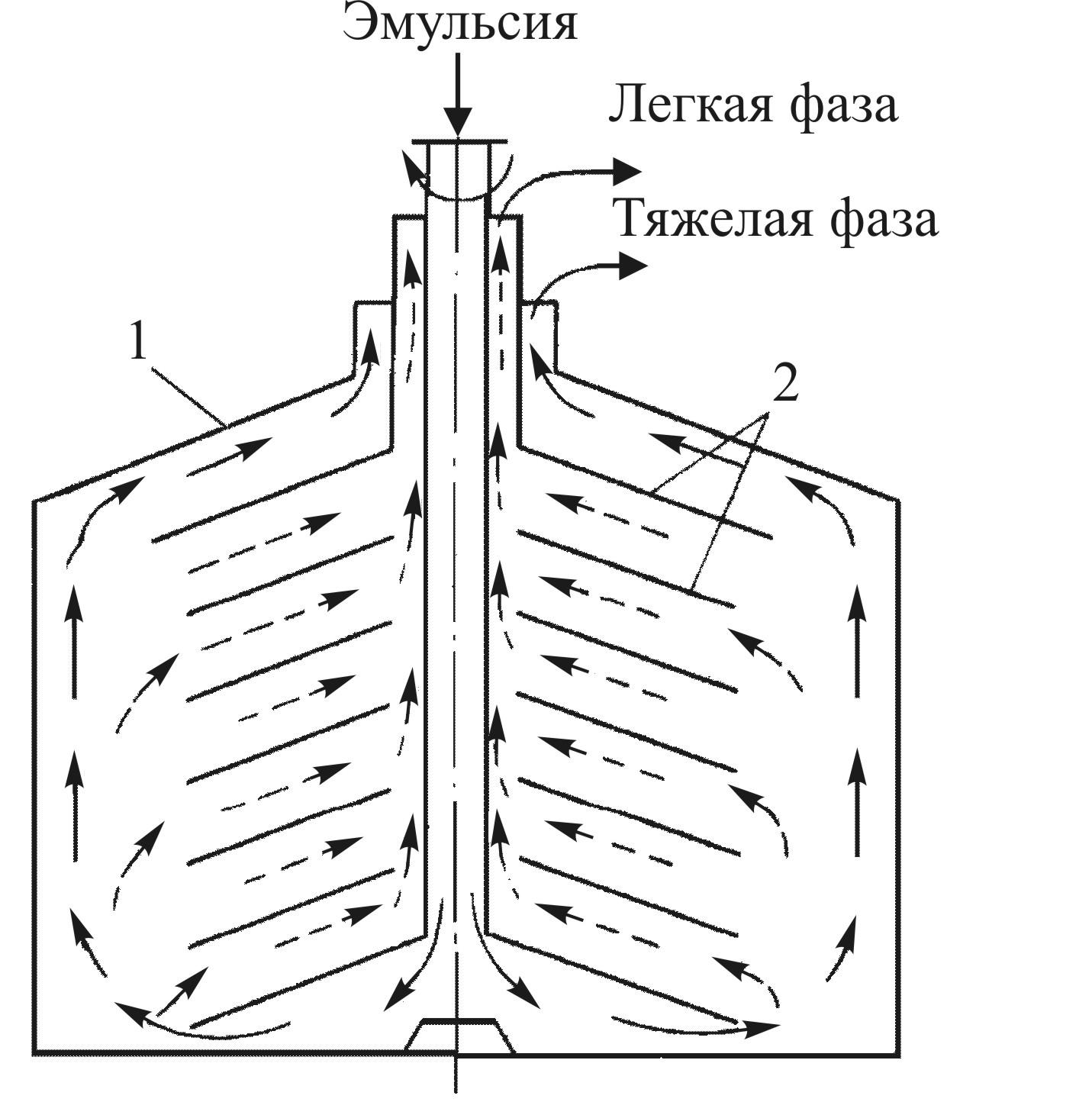 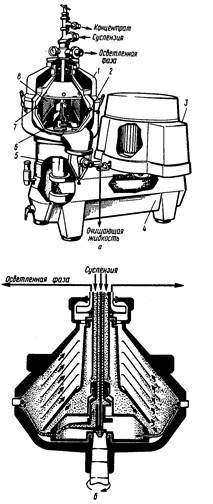 Рис. Дрожжевой сепаратор: а — общий вид; б—схема работы тарелок: 1 — корпус; 2 — внутреннее сопло; З — привод; 4 — рама; 5 — сменная втулка рабочего вала; б — регулируемая напорная труба; 7 — клапан системы безразборной мойки; 8 — пакет тарелок Гидроциклоны применяются для осветления, обогащения суспензий, классификации твердых частиц по размерам от 5 до 150 мкм, а также для очистки сточных вод после мойки пищевых агрегатов. 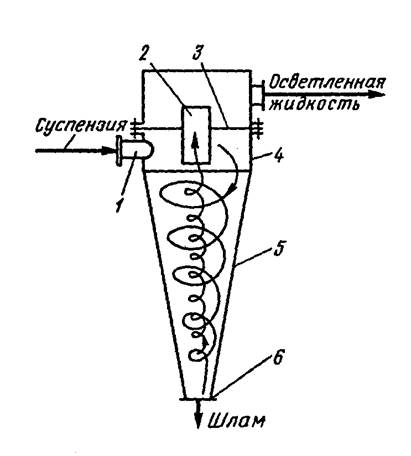 Рис. Гидроциклон 1 тангенциальный Штуцер: 2 патрубок; З — перегородка; 4 цилиндрический корпус; 5 — коническое днище; б — штуцер для выхода шлама Корпус гидроциклона состоит из верхней цилиндрической части и конического днища. Качество разделения в гидроциклонах зависит от угла конусности. Оптимальным считают угол, равный 10—15°. При таком угле удлиняются коническая часть гидроциклона и путь твердых частиц, следовательно, увеличиваются время пребывания частиц и качество разделения. Суспензия подается тангенциально в цилиндрическую часть и приобретает вращательное движение. Скорость суспензии на входе в гидроциклон составляет 5 - 25 м/с. Под действием центробежной силы твердые частицы отбрасываются к стенкам гидроциклона и движутся по спиральной траектории вдоль стенок вниз к штуцеру 6, через который отводятся в виде шлама. Осветленная жидкость движется во внутреннем спиральном потоке вверх вдоль оси гидроциклона и удаляется через патрубки 2. Гидроциклоны, применяемые в качестве классификаторов, имеют диаметр 300—350 мм и высоту 1,0—1.2 м. Для сгущения грубых суспензий используются гидроциклоны диаметром 100 мм, для сгущения и осветления тонких суспензий — гидроциклоны диаметром 10—15 мм, обычно объединяемые в общий агрегат, в котором они работают параллельно (мультигидроциклон).[4] Кристаллизация Кристаллизация — это процесс выделения твёрдой фазы в виде кристаллов из растворов или расплавов, в химической промышленности процесс кристаллизации используется для получения веществ в чистом виде. Виды кристаллизации Кристаллизация происходит, когда растворимость вещества в растворе понижается каким-либо способом. Стандартные методы снижения растворимости: a) охлаждение; b) добавление противорастворителя; c) испарение; d) реакция (осаждение).  Выбор метода кристаллизации зависит от имеющегося оборудования, целей процесса кристаллизации, растворимости и стабильности состояния вещества в выбранном растворителе. Типичные сложности при кристаллизации Кристаллизация происходит за счет нескольких взаимосвязанных процессов, на протекание которых влияют выбранные параметры. Основные этапы: образование активных центров (нуклеация); рост; образование новой жидкой фазы; агломерация; распад агломератов; полиморфные переходы. Данные процессы, которые часто протекают в скрытом виде, оказывают ключевое влияние на результат кристаллизации.  Технологический процесс кристаллизации из растворов состоит из следующих стадий: кристаллизация; отделение образовавшихся кристаллов; перекристаллизация; промывка и сушка кристаллов. Последние две стадии не являются обязательными и назначаются в соответствии с требованиями к конечному продукту. Первая из стадий осуществляется в аппаратах специальных конструкций – кристаллизаторах. По способу работы они делятся на аппараты периодического и непрерывного действия. Аппараты периодического действия используют обычно в кристаллизационных установках небольшой производительности. Они достаточно экономичны, просты по конструкции и обеспечивают требуемое качество продукта. Недостатком является относительно большая доля вспомогательных операций (загрузки, разгрузки и т. д.). Кристаллизаторы непрерывного действия применяют в условиях обеспечения высокой производительности. По способу создания пересыщения все кристаллизаторы можно разделить на выпарные, охладительные, испарительные, химические и др. Выпарные кристаллизаторы, используемые для проведения изотермической кристаллизации с удалением части растворителя в виде пара, чаще всего представляют выпарные аппараты с внутренней циркуляционной трубой, подвесной греющей камерой, выносной греющей камерой и другие, как при естественной, таки вынужденной циркуляции раствора. Однако при кристаллизации возникают специфические условия – наличие твердой фазы в растворе, возможность отложения кристаллов на стенках аппарата и греющих трубках, необходимость регулирования размера кристаллов в продукте. Все это требует ряда изменений в конструкции обычных выпарных аппаратов. На рис. 15.2 изображен выпарной аппарат – кристаллизатор 1 с подвесной нагревательной камерой 2 и двумя работающими поочередно нутч-фильтрами* 3 для отделения кристаллов. Выпарной аппарат – кристаллизатор 1 с вынесенной нагревательной камерой 2 и сборником кристаллов 3 показан на рис. 15.3. Охладительные кристаллизаторы применяют для изогидрической кристаллизации растворов веществ с прямой растворимостью. В малотоннажных производствах применяют кристаллизаторы, оборудованные перемешивающими устройствами, теплообменными рубашками или змеевиками. На рис. 15.4 показан кристаллизатор 1 емкостного типа со змеевиком 3, расположенным внутри аппарата, и лопастной мешалкой 2. Для непрерывной кристаллизации применяют барабанный кристаллизатор 1 (рис. 15.5), представляющий собой цилиндрический сосуд с водяной рубашкой 2, установленный на роликах 3 под небольшим углом к горизонту. Недостатком этих аппаратов является значительная кристаллизация внутренней поверхности    аппарата, поэтому для разрушения кристаллов на стенке в барабан могут помещать специальные насадки (цепи и штанги). Испарительные кристаллизаторы можно разделить на кристаллизаторы с воздушным охлаждением и вакуум-кристаллизаторы. В аппаратах первой группы охлаждение раствора производится путем непосредственного соприкосновения его с воздухом. Вследствие этого одновременно с охлаждением происходит испарение части растворителя. В вакуум-кристаллизаторах создается пониженное давление с помощью вакуум-насоса, что способствует испарению части растворителя с одновременным охлаждением раствора. 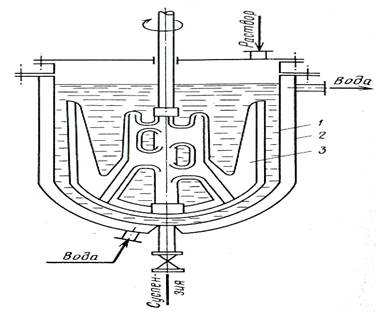 Рис – вакуумный кристализатор Химические кристаллизаторы используются для проведения в одном аппарате химической реакции и кристаллизации образующейся при этом твердой фазы.[5] Ионный обмен В основе метода ионного обмена лежит способность специальных сорбентов (ионообменных смол) сорбировать из раствора вещества, имеющие ионную природу (кислоты, основания, соли), за счет эквимолярного обмена ионов сорбента и ионов растворенного вещества. Ионообменные смолы (ИОС) — это высокомолекулярные органические соединения, полученные методом полимеризации или поликонденсации, имеющие сетчатую трехмерную структуру, нерастворимые в воде, но набухающие в ней с образованием гелей. На полимерной углеводородной матрице ионита закреплены ионогенные группы, способные к диссоциации. Их природа, количество и заряд определяются, подбираются и регулируются при синтезе ИОС.[5] Обменный ион, связанный с носителем, называется фиксированным. С ним электростатически связан ион противоположного знака — противоион или подвижный ион. Противоионы подвижны внутри матрицы и могут быть заменены другими ионами с зарядом того же знака. В зависимости от знака заряда обменивающихся ионов ИОС подразделяются: − на катиониты RAn– H+, − аниониты RKat+ OH– (Cl–), где RАn‑, RKat+ — заряженная полимерная матрица, нерастворимая в воде. Катиониты представляют собой полимерные поликислоты, содержащие в качестве ионогенных следующие группы: SO3H , PO H –3COOН–, OH–. Противоионами в катионитах являются: H+, Na+, K+, NH +4 . Аниониты — полимерные полиоснования. Ионогенные группы в анионитах в основном остатки алифатических или ароматических аминов. Противоионами для анионитов служат ионы OH– либо Cl–. Кроме двух основных групп, существуют амфолиты (амфотерные полиэлектролиты), обладающие свойствами катионитов и анионитов одновременно.[5] Таким образом, реакцию ионного обмена можно представить как обратимый стехиометрический обмен ионов двух электролитов в растворе: R An– H+ + Na+ + Cl– = R An– Na+ + H+ + Cl– R Kat+OH– + Na+ + Cl– = R Kat+ Cl– + Na+ + OH– Процесс ионного обмена слагается из нескольких этапов: 1) диффузия ионов растворенного электролита к поверхности сорбента; 2) диффузия ионов растворенного электролита внутри зерен ионита; 3) химическая реакция двойного обмена; 4) вытеснение подвижных ионов из сферы влияния неподвижных ионов; 5) диффузия вытесненного подвижного иона из фазы сорбента в раствор. Так как один из ионов раствора по мере реакции переходит в твердую фазу и выводится из раствора, равновесие реакции сдвигается в нужном направлении. 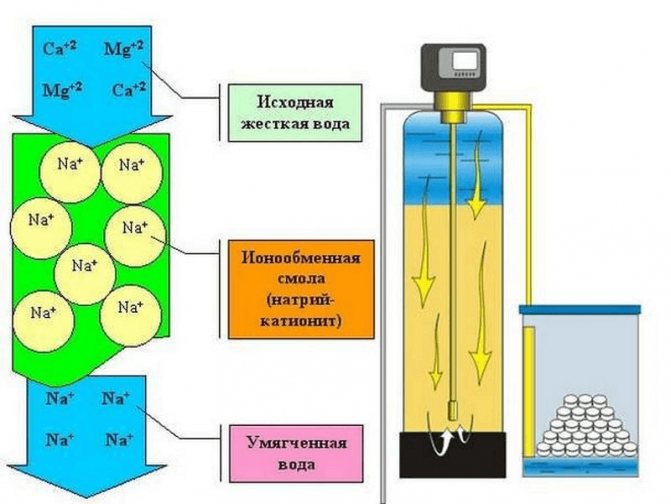 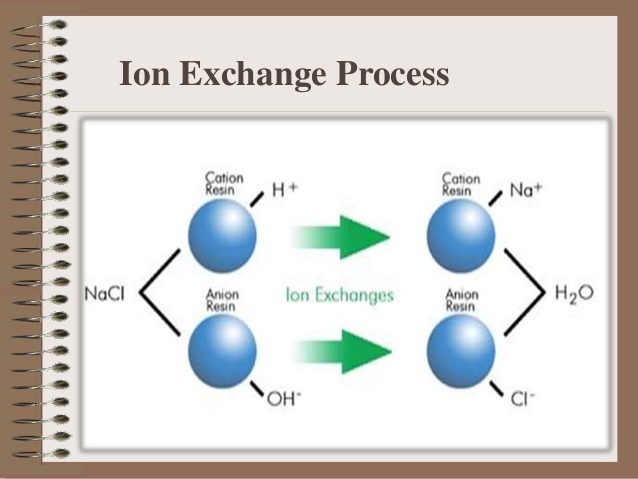 Хроматография  Рис – бумажная хроматография Основные понятия в хроматографии Хроматография – метод разделения смесей веществ, основанный на различии в скоростях их перемещения в системе несмешивающихся и движущихся относительно друг друга фаз. Подвижная фаза – поток жидкости или газа, перемещающий компоненты разделяемой смеси вдоль неподвижной фазы. Неподвижная фаза – твердый сорбент или несмешивающаяся с подвижной фазой жидкость, на которых осуществляется различное удерживание и разделение компонентов смеси. Сорбент – твердое вещество, жидкость или их смеси, способные удерживать газы, пары или растворенные вещества. Адсорбент – твердый сорбент, концентрирующий на своей поверхности газы, пары или растворенные вещества. Абсорбент – твердый или жидкий сорбент, растворяющий в своем объеме газы, пары или компоненты жидких смесей. Сорбат – вещество, удерживаемое сорбентом (в хроматографии – компоненты разделяемой смеси). Элюент – жидкость или газ, используемые в качестве подвижной фазы. Элюат – выходящий из колонки поток подвижной фазы с компонентами разделяемой смеси.[6] Классификация хроматографических методов В основу общепринятых классификаций многочисленных хроматографических методов положены следующие признаки: агрегатное состояние подвижной и неподвижной фаз, механизм взаимодействия сорбент – сорбат, форма слоя сорбента (техника выполнения), хроматографирования. По агрегатному состоянию фаз хроматографию разделяют на газовую и жидкостную. Газовая хроматография включает газожидкостную, газотвердофазную и газомезофазную; жидкостная хроматография –жидкостно- жидкостную, жидкостно-твердофазную и жидкостно-гелевую. Первое слово в названии метода характеризует агрегатное состояние подвижной фазы, второе – неподвижной.[6] По механизму взаимодействия сорбента и сорбата можно выделить несколько видов хроматографии. Распределительная хроматография основана на различии в растворимости разделяемых веществ в неподвижной фазе (газожидкостная хроматография) или на различии в растворимости веществ в подвижной и неподвижной жидких фазах. В ионообменной хроматографии используют различную способность веществ к ионному обмену. Адсорбционная хроматография основана на различии в адсорбируемости веществ твердым сорбентом. Эксклюзионная хроматография (гель- хроматография, гель-проникающая хроматография) – на различии в размерах и формах молекул разделяемых веществ. При этом используется неподвижная фаза, имеющая гелевую или жесткую пористую сетчатую структуру. Чем меньше размер молекул и доступнее для них поры неподвижной фазы, тем меньше скорость их движения. По технике выполнения хроматографического процесса различают колоночную (насадочную и капиллярную) хроматографию и плоскостную (планарную). По цели хроматографирования выделяют аналитическую хроматографию (идентификация веществ и количественное определение); препаративную хроматографию (для получения веществ в чистом виде, для концентрирования выделения микропримесей); промышленную (производственную) хроматографию для автоматического управления процессом (при этом целевой продукт из колонки поступает в датчик).[6] ГАЗОВЫЙ ХРОМАТОГРАФ. Любая газохроматографическая установка обязательно должна содержать следующий перечень узлов: • источник газа-носителя; • вентиль тонкой регулировки скорости потока газа-носителя; • устройство для ввода пробы; • хроматографическая колонка; • детектор; • термостат колонки и термостат детектора; • регистратор; • измеритель скорости потока газа-носителя. 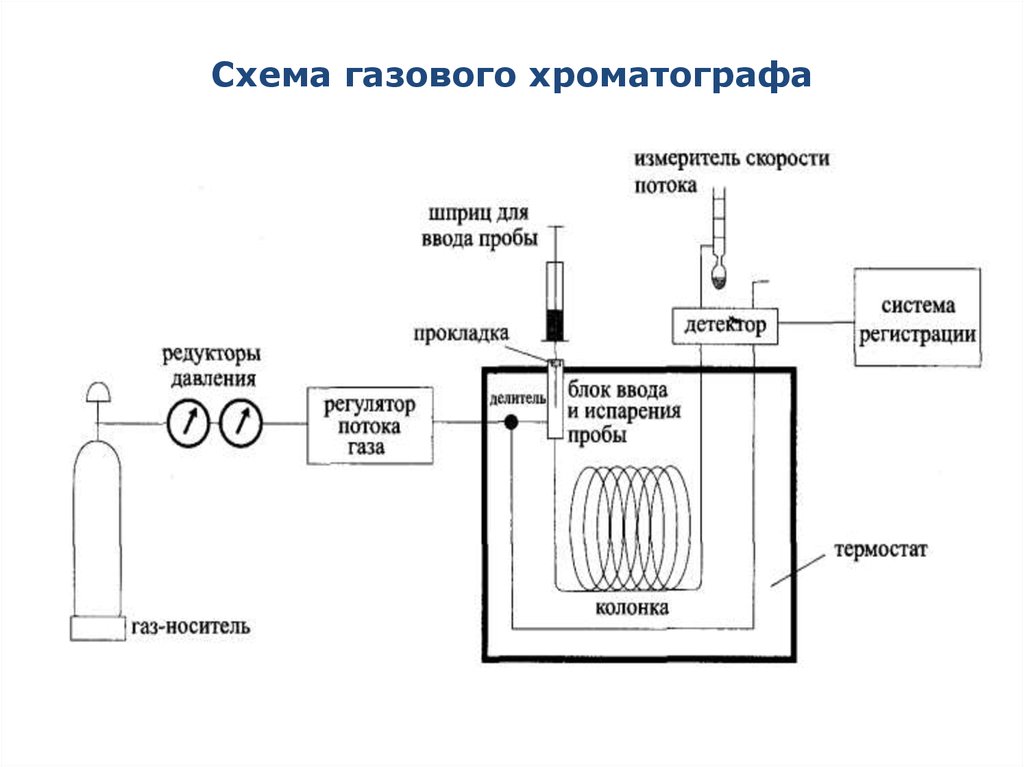  Рис- жидкостный хроматограф Список литературы 1 И.М. Грачева. Биотехнология биологически активных веществ. Учебное пособие для студентов высших учебных заведений./ Под редакцией д. б. н., проф. МГУШ1И.М. Грачевой ид.т.н., проф. МГУШІЛ.А. Ивановой. — М., Издательство НПО «Элевар»,2006. — 453 с.. 2006 2 Калишук Д.Г. Процессы и аппараты химической технологии Минск : БГТУ, 2011. – 426 с. 3 Пикалов, Е. С. Процессы и аппараты защиты окружающей среды. Механические и физические методы очистки промышленных выбросов в атмосферу и гидросферу : учеб. пособие / Е. С. Пикалов ;Владим. гос. ун-т им. А. Г. и Н. Г. Столетовых. ‒ Владимир : Изд-во ВлГУ, 2015 ‒ 79 с. 4 Кривошеин Д.А. Инженерная защита поверхностных вод от промышленных стоков: Учеб. пособие/Д.А. Кривошеин, П.П. Кукин, В.Л. Лапин и др. – М.: Высшая школа, 2003 – 344 с. 5 Берсенёва В. С. Сорбционные методы выделения продуктов биосинтеза / Берсенёва В. С. Бакулев В.А. : Екатеринбург, 2018 – 84 с. 6 Крылов В.А. Введение в хроматографические методы анализа. Часть 1 Ионный обмен и ионная хроматография. Практическая ионная хроматография./ Крылов В.А., Сергеев Г.М., Елипашева Е.В. Электронный учебно-методический комплекс. – Нижний Новгород: Нижегородский госуниверситет, 2010 – 91 с. |
