Роль печени в пигментном обмене
 Скачать 230.45 Kb. Скачать 230.45 Kb.
|
|
РОЛЬ ПЕЧЕНИ В ПИГМЕНТНОМ ОБМЕНЕ Пособие для подготовки к занятию Кафедра биохимии ЛФ составила д.х.н., проф. Орлова М.А. Пигменты в организме 1. гем-содержащие пигменты, входят в состав т.н. дыхательных пигментов: гемоглобина, миоглобина, цитохромов, каталазы, пероксидазы 2. предшественники гема – порфирины 3. продукты распада гема – желчные пигменты (билирубин желчи, уробилин мочи, стертобилин кала); 4. образующийся из аминокислоты Tyr в пигментных клетках меланоцитах меланин. Он находится в коже, волосах, радужной оболочке глаз. Большая часть пигментов человека – это гемохромагенные пигменты, которые образуются либо при синтезе, либо при распаде гема. Биосинтез гема Биосинтез гема идет в большинстве тканей, за исключением эритроцитов, которые не имеют митохондрий. В организме человека гем синтезируется из глицина и сукцинил-КоА, образованного в результате метаболических реакции ЦТК. Для активации глицина необходим витамин В6. В процессе первой метаболической реакции синтеза гема образуется аминолевулиновая кислота (АЛК). Скорость синтеза гема контролируется ферментом – аминолевулинат-синтазой. Наиболее активно эта реакция идет в печени. 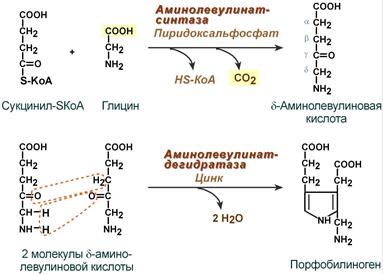 Первая из представленных реакций идет в митохондриях. Следующие реакции протекают в цитозоле: образование порфобилиногена (монопиррол) и далее из 4- молекул порфобилиногена образование гидроксиметилбилана, затем уропорфириногена (тетрапиррол) и копропорфириногена. Далее реакции снова проходят в митохондриях, кроме последней реакции соединения гема с белком с образованием гемоглобина, которая происходит снова в цитозоле. 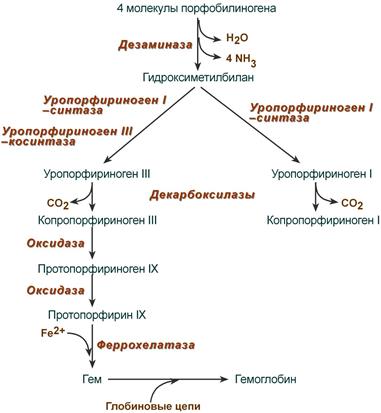 Скорость синтеза глобиновых цепей зависит от наличия гема, он ускоряет биосинтез "своих" белков. Фермент феррохелатаза катализирует встраивание ионов железа в порфириновое окружение с образованием гема. Гем является активным регулятором синтеза: напрямую оказывает отрицательный аллостерический эффект на регуляторный фермент – аминолевулинатсинтазу; влияет на транскрипцию фермента, формируя активный репрессорный комплекс. Ионы железа оказывает положительный эффект при синтезе молекулы аминолевулинатсинтазы. Железосвязывающий белок (IRP) в отсутствие ионов железа обладает сродством к железочувствительному участку IRE на матричной РНК фермента. Это связывание блокирует трансляцию мРНК в рибосоме, т.е. подавляет синтез белковой цепи. При наличии ионов железа они связываются с IRP, образуя с ним неактивный комплекс, и это инициирует синтез фермента. 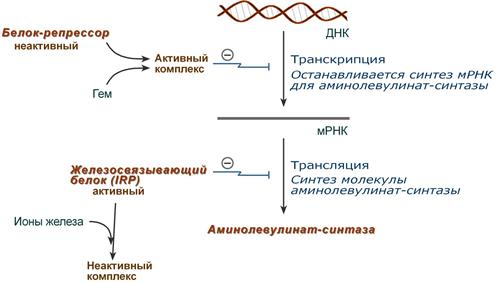 Регуляция синтеза аминолевулинатсинтазы Cоединения, усиливающие работу микросомальной системы (жирорастворимые вещества, стероиды) в печени способствуют повышению активности аминолевулинатсинтазы. При этом возрастает потребление гема для образования цитохрома Р450, за счет чего снижается внутриклеточная концентрация свободного гема и происходит усиление синтеза фермента. Порфирии При нарушении синтеза гема в организме человека, главным образом, в печени могут развиваться порфирии– группа заболеваний, возникших в результате блокирования отдельных стадий синтеза гема и сопровождающихся увеличенным содержанием порфиринов в организме. Причинами порфирий могут быть: наследственные болезни, когда из-за дефицита митохондрий и ферментов синтеза гема, нарушается пигментный обмен: Печеночные – группа заболеваний с аутосомно-доминантными нарушениями ферментов различных этапов синтеза протопорфирина IX. Эритропоэтические –аутосомно-рецессивные нарушения некоторых ферментов синтеза протопорфирина IX в эритроидных клетках. 2. приобретенные (токсические), которые вызываются действием ряда токсических соединений (гексохлорбензол, соли тяжелых металлов, алкоголь). Эти соединения могут ингибировать ферменты (порфобилиногенсинтазы, феррохелатазы и др.) в системе синтеза гема. Порфирии могут сопровождаться поражением кожи, сопровождаясь фотодерматозами (увеличение светочувствительности кожи). Моча таких больных – розовая или красная. Талассемии Для талассемий характерно снижение синтеза α-цепей гемоглобина (α-талассемия) или β-цепей (β-талассемия). Это приводит к нарушению эритропоэза, гемолизу и тяжелым анемиям. Распад гема Большая часть гемохромагенных пигментов в организме человека образуется при распаде гема. Главным источником гема является гемоглобин. В эритроцитах содержание гемоглобина составляет 80%, время жизни эритроцита 110-120 дней. В течение суток в организме взрослого человека массой 70 кг распадается около 6 г гемоглобина. Распад эритроцитов происходит в клетках мононуклеарных фагоцитов. Наибольшее число таких клеток в селезенке, печени, костном мозге. Первая реакция распада гемоглобина – это гидролиз его белковой части происходит в микросомальной фракции при участии сложной гем-оксигеназной ферментативной системы, требующей наличие НАДФН2 и кислорода. При поступлении гема в гемоксигеназную систему микросом ионы железа окисляются в ферри форму, т.е. гем превращается в гемин. Ферментная система гемоксигеназылокализована в мембране ЭР, в области электронтранспортных цепей микросомального окисления. В ходе реакции образуются линейный тетрапиррол – биливердин (пигмент жёлтого цвета) и монооксид углерода (СО). 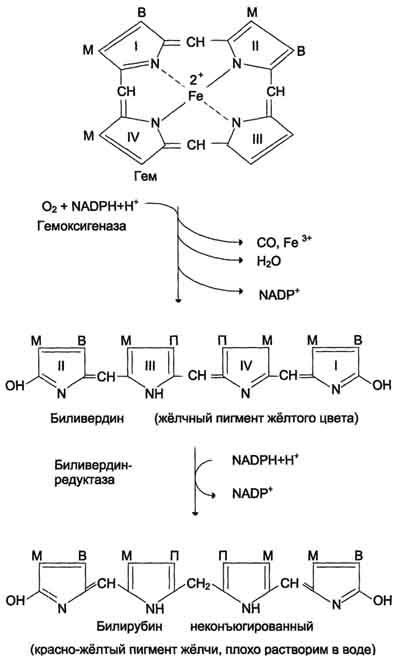 Ионы железа, освободившиеся при распаде гема, могут быть использованы для синтеза новых молекул гемоглобина или для синтеза других железосодержащих белков. Биливердин восстанавливается до билирубина NADPH-зависимым ферментом биливердинредуктазой. Билирубин образуется не только при распаде гемоглобина, но и при катаболизме других гемсодержащих белков, таких как цитохромы и миоглобин. При распаде 1 г гемоглобина образуется 35 мг билирубина, а в сутки у взрослого человека - примерно 250-350 мг билирубина. Дальнейший метаболизм билирубина происходит в печени. Билирубин, образованный в клетках РЭС (селезёнки и костного мозга), плохо растворим в воде, по крови транспортируется в комплексе с белком плазмы крови альбумином. Эту форму билирубина называют неконъюгированным билирубином. В гладком ЭР гепатоцитов к билирубину присоединяются (реакция конъюгации) полярные группы, главным образом от глюкуроновой кислоты. Билирубин имеет 2 карбоксильные группы, поэтому может соединяться с 2 молекулами глюкуроновой кислоты, образуя хорошо растворимый в воде конъюгат - диглюкуронид билирубина (конъюгированный, или прямой билирубин). 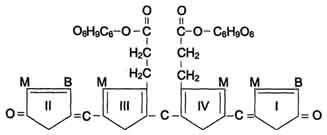 Специфические ферменты, УДФ-глюкуронилтрансферазы (уридиндифосфоглюкуронилтрансферазы) катализируют образование моно- и диглюкуронидов билирубина. 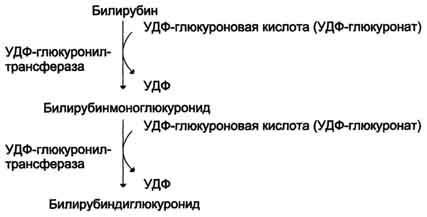 Далее секреция конъюгированного билирубина в жёлчь идёт по механизму активного транспорта, т.е. против градиента концентрации. Активный транспорт является скорость-лимитирующей стадией всего процесса метаболизма билирубина в печени. Скорость конъюгации билирубина и активный транспорт билирубинглюкуронида из гепатоцитов в жёлчь строго взаимосвязаны. Неконъюгированный билирубин: 1. токсичен; 2 - гидрофобен; 3 - адсорбирован на альбумине; 4 - не проходит через почечный эпителий; 5 - не дает прямой реакции с диазо-реактивом Эрлиха. Конъюгированный билирубин: 1. не токсичен; 2 - гидрофилен; 3 - не связан с белками; 4 - легко проникает через почечный барьер; 5 - дает прямую реакцию с диазо-реактивом Эрлиха. Этот билирубин может проникать в кровяные капилляры. В плазме крови на его долю приходиться 25%, от общего билирубина, который в норме составляет 8-20 мкмоль/л. В кишечнике поступившие билирубинглюкурониды гидролизуются специфическими бактериальными ферментами β-глюкуронидазами. Освободившийся билирубин под действием кишечной микрофлоры восстанавливается с образованием группы уробилиногенов. К ним относятся мезобилирубиноген и стеркобилиноген (или L-уробилиноген, окрашенные соединения). При этом небольшая часть мезобилирубиногена поступает через воротную вену в печень, где подвергается разрушению с образованием моно- и дипиррольных соединений. Кроме того, очень небольшая часть стеркобилиногена после всасывания через систему геморроидальных вен попадает в большой круг кровообращения, минуя печень, и в таком виде выводится почками с мочой. Таким образом, основная часть уробилиногена из печени в составе жёлчи выводится в кишечник и выделяется с фекалиями из организма, часть уробилиногена из печени поступает в кровь и удаляется с мочой в форме уробилина. В норме большая часть бесцветных уробилиногенов, образующихся в толстой кишке, под действием кишечной микрофлоры окисляется в прямой кишке до пигмента коричневого цвета уробилинаи удаляется с фекалиями. Цвет фекалий обусловлен присутствием уробилина. Ниже приведены структуры желчных пигментов 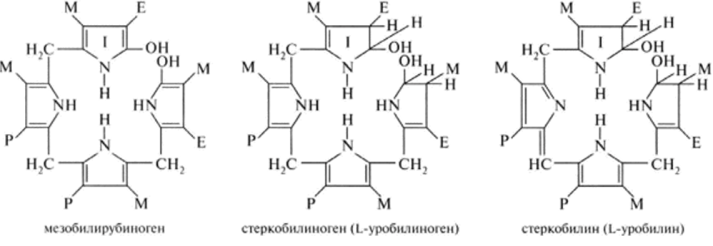 Желтухи Пожелтение тканей из-за отложения в них билирубина называют желтухой.Клинически желтуха может не проявляться до тех пор, пока концентрация билирубина в плазме крови не превысит 50 мкмоль/л. Желтуха у взрослых – это следствие патологических процессов, развивающихся в печени и жёлчных путях. В зависимости от причины возникновения такого процесса, можно выделить три вида желтух: 1.- надпеченочная или гемолитическая желтуха (из-за слишком быстрого распада билирубина) 2 - печеночная (из-за заболеваний печени) 3 -подпеченочная или механическая желтуха (из-за закрытых печеночных протоков) Надпеченочная желтуха Надпеченочная желтуха развивается на фоне избыточного образования и быстрого распада билирубина. В результате такого усиленного разрушения печень не в состоянии вывести весь билирубин, что приводит к его обратному поступлению в кровь и, как следствие, к развитию заболевания. Причины развития Гемолитические анемии; болезни неэффективного эритропоэза; результат обширных инфарктов; лекарственные и токсические повреждения. Может являться симптоматикой других заболеваний: крупозной пневмонии, малярии, злокачественных опухолей, поражения печени. Основные симптомы надпеченочной желтухи: лимонно-желтый оттенок кожи, слизистой и склер глаз, кожные покровы из-за анемии бледные, незначительное увеличение печени. Печеночная (паренхиматозная) желтуха. Возникает на фоне массивного повреждения клеток печени (их структур, функций), что вызывает нарушение потребления билирубина печеночными клетками и проблемы с его выводом. Паренхиматозная желтуха является одним из самых распространенных заболеваний печени. Причины развития Сначала необходимо исключить возможность инфекционного заболевания. Причины: острый вирусный гепатит; инфекционный мононуклеоз; лептоспироз; лекарственные или алкогольные поражения печени; хронический агрессивный гепатит; цирроз; гепатоцеллюлярный рак. Основные симптомы Красноватый, рубиновый оттенок кожи, увеличенная печень, боли в области печени, «печеночные ладони» (пятнистое покраснение), сосудистые звездочки, кожный зуд. Подпеченочная (механическая) желтуха Подпеченочная (механическая) желтуха у взрослых развивается из-за нарушения свободного тока желчи в двенадцатиперстную кишку по причине сужения желчных протоков. Сужение может развиться по разным причинам: наличие камней в общем желчном протоке; паразиты; рубцовые изменения после операций; аномалия развития желчных путей; опухоли желчных протоков; Симптомы: окрашивание кожи, слизистой и склер глаз в желтый цвет с зеленоватым оттенком, повышение температуры, кожный зуд. Физиологические желтухи новорожденных Наблюдаются у 65-75% новорожденных, но только у 10% они являются патологическими. Появление желтух у новорожденных связано 1. с повышенным образованием непрямого билирубина вследствие: укороченной продолжительности жизни эритроцитов (70-90 дней вместо 120); повышенного разрушения незрелых эритроцитов в костном мозге из-за несостоятельности эритропоэза; увеличения образования непрямого билирубина из неэритроцитарных источников гема (миоглобина, цитохромов); 2. со сниженной функциональной способностью печени к захвату, конъюгации и экскреции билирубина вследствие: транзиторной гипоальбуминемии; усиленной диссоциации молекул комплекса билирубин-альбумин в условиях гипоксии, ацидоза; замедленного созревания белков-переносчиков (лигандина и Z-протеина); сниженной активности ферментативной системы печени в связи с запаздыванием созревания глюкуронилтрансферазы; торможения процессов конъюгации из-за дефицита глюкозы, АТФ, гипоксии, а также высокого содержания в крови новорожденных некоторых стероидов, угнетающих глюкуронилтрансферазную активность печени; сниженной экскреции билирубина из гепатоцита из-за незрелости белков –переносчиков и узости желчных протоков; 3. с повышенной энтерогепатической циркуляцией билирубина вследствие: высокой активности кишечной β-глюкуронидазы; функционирования в первые дни жизни пути попадания непрямого билирубина в кровь из кишечника, а оттуда в портальный кровоток, минуя печень; стерильности кишечника. Патологические желтухи новорожденных делятся на наследственные и приобретенные, а также с преобладанием непрямого или прямого билирубина. Следует отметить гемолитическую неонатальную желтуху по резус- фактору вследствие иммунологического конфликта при несовместимости крови матери и плода. Может переходить в ядерную желтуху с гибелью плода. Для гемолитических желтух характерно: раннее появление желтухи из-за непрямой гипербилирубинемии; высокий почасовой прирост билирубина; цвет кожных покровов от ярко-желтого до лимонно-желтого; наличие нормохромной гиперрегенераторной анемии; гепатоспленомегалия; нормальная окраска кала и мочи; токсическое действие непрямого билирубина на все органы и ткани. К печеночным желтухам (пониженный клиренс билирубина) относится Синдром Жильбера. Часто сочетается с дефицитом глюкозо-6 фосфатдегидрогеназы, что вызывает более тяжелое и длительное течение болезни. Заболевание обусловлено дефектом синусоидальной мембраны гепатоцита с нарушением внутриклеточного транспорта билирубина и снижением активности процессов конъюгации до 50% от нормы. Синдром Криглера-НайяраI типа обусловлен отсутствием фермента глюкуронилтрансферазы в печени. Наблюдается резкий рост билирубина в печени, который сохраняется всю жизнь, и нет реакции на фенобарбитал. Кратковременное снижение билирубина наблюдается при фототерапии и заменном переливании крови. Обычно дети погибают от ядерной желтухи. II типа Наблюдается резкое снижение (до 5-10% от нормы) глюкуронилтрансферазной активности печени. (обычно результат нарушения конъюгации у одного из родителей). Лечение фенобарбиталом, при отмене препарата желтуха возвращается. Синдром Дубина-Джонса В основе дефект каналикулярной секреции билирубина из гепатоцита. Характеризуется умеренной желтухой и небольшим увеличением печени. При диагностике констатируется умеренная гипербилирубинемия с преобладанием прямого билирубина. При анализе мочи – копропорфирия. В печени наблюдаются коричневые включения и гранулы. Желтуха от материнского молока Ведущим в патогенезе считается нарушение экскреции, а не конъюгации билирубина. Желтуха при гипотиреозе из-за недостаточности гормонов щитовидной железы, которые способствуют созреванию фермента глюкуронилтрансферазы. Механические желтухи. Определяются пороками развития желчных путей (внутрипеченочная и внепеченочная атрезия). Муковисцидоз – закупорка желчных путей густой слизью. Гипербилирубинемия смешанного типа, стеаторея. У новорожденных повышен иммуннореактивный трипсин в крови. Биохимические маркеры синдромов: цитолиза Синдром цитолиза представляет собой клинико-лабораторный синдром, характеризующийся повышением уровней внутриклеточных ферментов трансаминаз (прежде всего, АСТ и АЛТ) в крови, как неспецифической реакции клеток на действие повреждающих факторов, и проявляется на клеточном уровне их повреждением и гибелью. В результате развития синдрома цитолиза или синдрома нарушения целостности гепатоцитов в плазме крови определяются повышенные уровни не только АЛТ и АСТ, но и билирубина (за счет обеих фракций), лактатдегидрогеназы (ЛДГ), альдолазы, глутатион-S-трансферазы, железа, вит. В12, глутамат-дегидрогеназы (ГлДГ), сорбит-дегидрогеназы (СДГ), орнитин-карбамоилтрансферазы (ОКТ). Последние три показателя являются печеночно-специфическими ферментами. При заболеваниях печени АЛТ является более специфичным маркером, чем АСТ. Повышение показателя до 5 нормальных значений свидетельствует о минимальной активности процесса, в 5–10 раз – об умеренной, более 10 раз – о высокой биохимической активности. 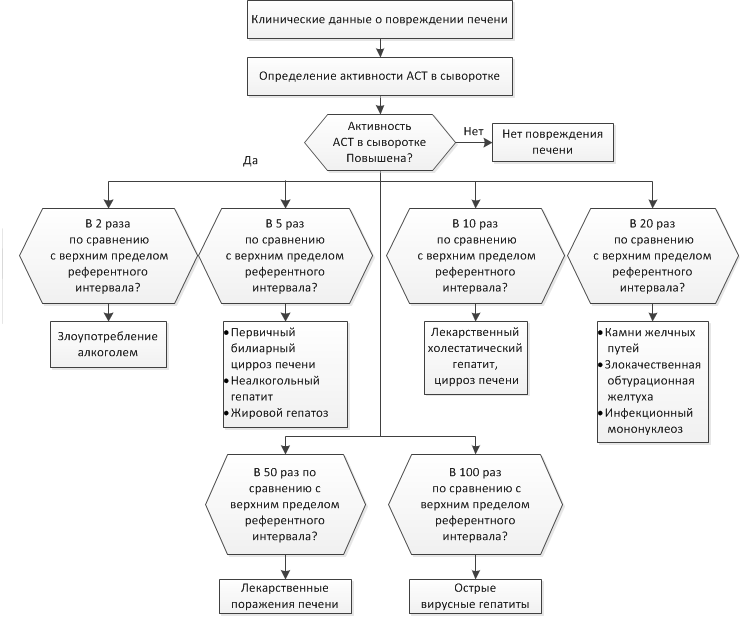 гемолиза Внутрисосудистый гемолиз приводит к гемоглобинемии, когда количество гемоглобина, высвобождаемого в плазму, превышает гемоглобин-связывающую способность плазматичекого связывающего белка гаптоглобина, концентрация которого в плазме в норме составляет около 100 мг/дл (1.0 г/л), что ведет к снижению несвязанного гаптоглобина плазмы. При наличии гемоглобинемии свободные димеры гемоглобина фильтруются в мочу и реабсорбируются в клетках почечных канальцев; когда способность к реабсорбции превышена, возникает гемоглобинурия. В канальцевых клетках железо, выделенное вследствие распада гемоглобина, включается в синтез гемосидерина; часть железа используется для реутилизации, остальное количество попадает в мочу в связи с перегрузкой канальцевых клеток. Маркеры: билирубин сыворотки крови, лактатдегидрогеназа (ЛДГ), гаптоглобин и аланинаминотрансфераза (АЛТ) холестаза Холестаз представляет собой нарушение синтеза, секреции и оттока жёлчи. Клинические признаки холестаза – слабость, кожный зуд и в ряде случаев желтуха. При бессимптомном течении холестаза ранние биохимические маркеры – повышение уровня щелочной фосфатазы (ЩФ) и -глютамилтранспептидазы (-ГТ), в дальнейшем присоединяется повышение уровня конъюгированного билирубина. Холестаз принято разделять на внутри- и внепеченочный. Внутрипеченочный холестаз может быть следствием функциональных дефектов образования жёлчи на уровне гепатоцита или обструкции на уровне внутрипеченочных желчных протоков. В развитии холестаза могут принимать участие оба механизма, например, при лимфомах. Холестаз считается хроническим, если он длится более 6 месяцев. Диагностическим уровнем повышения маркеров холестаза принято считать повышение ЩФ в 1,5 от верхней границы нормы (ВГН) и повышение -ГТ в 3 раза от ВГН. Активность -ГТ сыворотки возрастает при всех формах заболеваний печени. Она наиболее высока в случаях обструктивных поражений печени (внутри- или подпеченочной закупорке желчевыводящих путей), достигая повышения в 5-30 раз от нормальных значений. 5-нуклеотидаза (5-НТ) – фермент, содержащийся во многих тканях (печень, мышцы, легкие, почки, щитовидная железа). В печени 5-НТ наиболее активна в желчных канальцах, синусоидах и купферовских клетках. Повышение активности обычно обусловлено холестазом. Холестерин может рассматриваться как маркер холестаза только при его одновременном повышении с другими маркерами (билирубин, ЩФ, -ГТ и др.) Болезнь Ниманна-Пика является сфинголипидозом, наследственным нарушением обмена веществ, при которых сфингомиелин и другие фосфолипиды накапливаются в лизосомах и которое связано с недостаточной активностью сфингомиелиназы. Это приводит к накоплению сфингомиелина (церамидного фосфорилхолина) в ретикулоэндотелиальных клетках. Бывает трёх типов. Тип С связан с дефектами ферментов, вовлекающих аномальное хранение холестерина. |
