Санкт-Петербургский государственный педиатрический медицинский университет
Кафедра общей и медицинской химии
|
Специальность
«Педиатрия»
|
Дисциплина «Химия»
|
Семестр 1
|
БИЛЕТ № 15
Вопрос №1 (Тест)
Если температурный коэффициент химической реакции равен 2, то при повышении температуры от 30 °С до 70 °С скорость реакции
1) увеличивается в 27 раз 2) уменьшается в 8 раз 3) увеличивается в 16 раз 4) уменьшается в 9 раз
Верны ли следующие суждения о комплексных соединениях? А) Комплексообразователем называется центральный атом (ион) Б) Лигандами называются ионы слабых электролитов
1) верно только А 2) верно только Б 3) неверно А 4) оба суждения неверны
Коэффициент активности иона тем больше, чем
1) больше концентрация электролита 2) не зависит от концентрации электролита
3) меньше растворимость электролита 4) меньше концентрация электролита
Для вычисления рН раствора слабой кислоты используют уравнение
1) 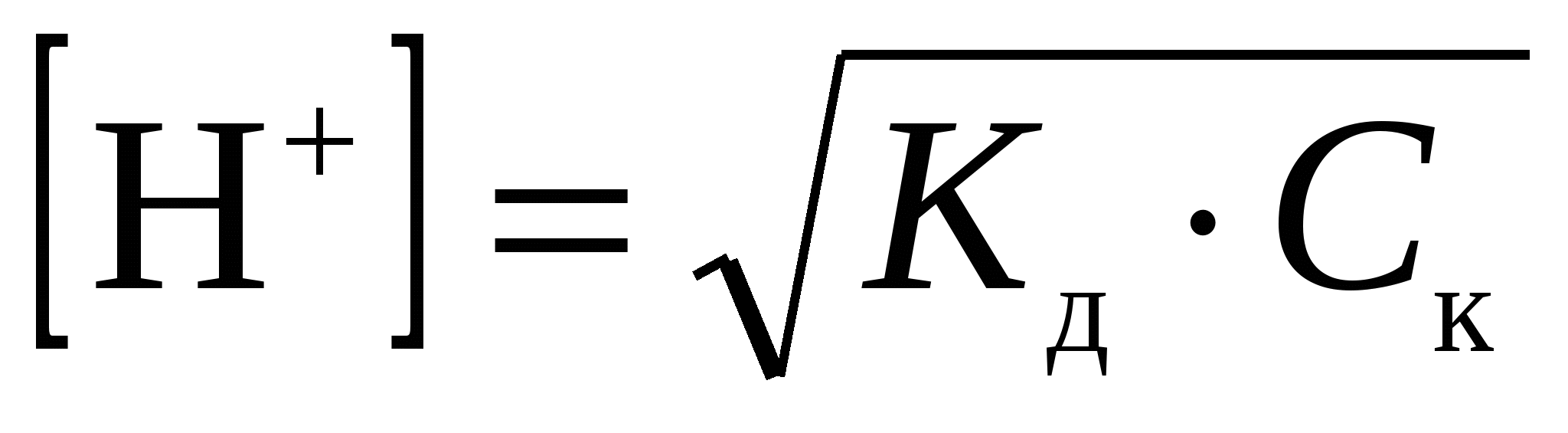 2) 2) 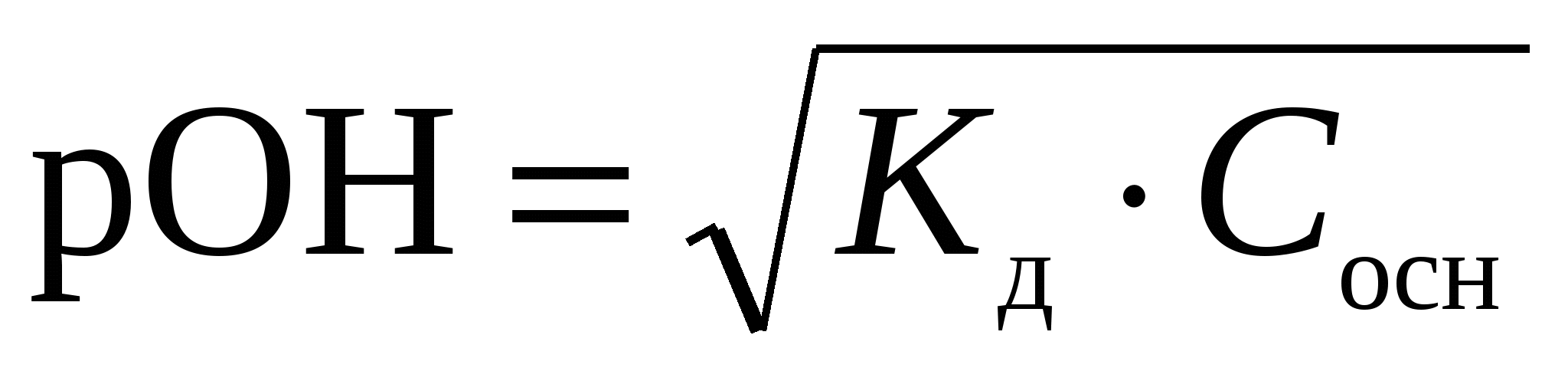 3) 3) 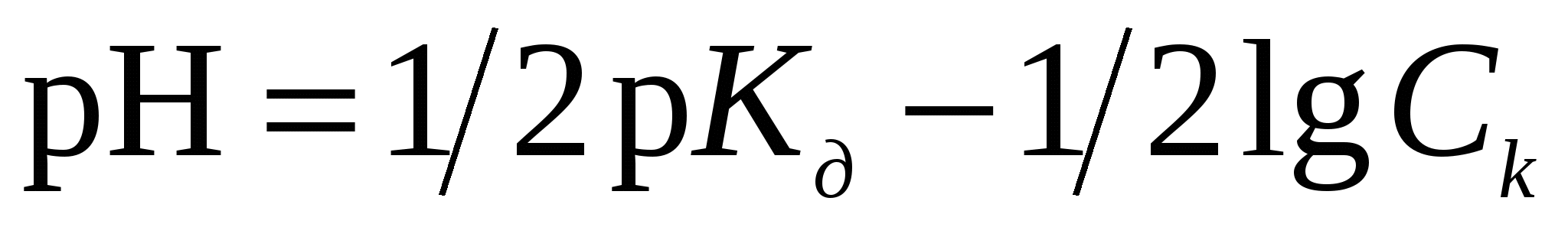 4) 4) 
Найдите верную фразу.
1) буферная емкость не зависит от количества добавленного сильного электролита
2) буферная емкость – величина постоянная
3) буферная емкость меняется только при добавлении сильной кислоты
4) максимальная буферная емкость при рН = рК слабого компонента системы
Какая полуреакция протекает на катоде гальванического элемента?
1) окисления 2) диспропорционирования 3) восстановления 4) обмен радикалами
Гемосорбция основана на таком явлении, как
1) десорбция 2) капиллярная конденсация
3) адсорбция на подвижной границе раздела фаз 4) адсорбция из раствора на твердом адсорбенте
Эмульсии – это дисперсные системы с
1) твердой дисперсной фазой и жидкой дисперсионной средой
2) жидкой дисперсной фазой и жидкой дисперсионной средой
3) твердой дисперсной фазой и газовой дисперсионной средой
4) газовой дисперсной фазой и жидкой дисперсионной средой
Для золя сульфата бария, полученного по реакции, уравнение которой BaCl2(изб) + Na2SO4 → BaSO4↓ + 2NaCl, коагуляцию вызывают
1) нейтральные молекулы 2) катионы электролита 3) анионы электролита 4) катионы и анионы
Денатурация белков – это
1) выпадение белка в осадок из раствора под действием больших количеств негидролизующихся солей
2) объединение частиц в коллоидных системах с твердой дисперсной фазой
3) переход свежеосажденного осадка в свободнодисперсное состояние
4) негидролитическое нарушение нативной структуры белка
Вопрос №2
Стандартная энергия Гиббса образования вещества, стандартная энергия Гиббса биологического окисления вещества. Стандартная энергия Гиббса реакции. Примеры экзергонических и эндергонических процессов, протекающих в организме. Принцип энергетического сопряжения.
Вопрос №3
Потенциометрическое определение рН с помощью гальванического элемента, составленного из стеклянного электрода и хлорсеребряного электродов. Электрохимическая схема гальванического элемента, формула для расчета рН.
Вопрос №4
Рассчитайте массу и количество молей растворенного вещества в 300 г 11,1% -ного раствора СаС12
Вопрос №5
В клинической лабораторной диагностике для создания буферных растворов широко используется органическое основание трис-гидроскиметиламинометан (Трис). Рассчитайте рН буферной смеси, полученной смешиванием 500 мл раствора трис-основания с концентрацией 0,2 моль/л и 10 мл 2 М раствора соляной кислоты. (рКд основания =5,92).
|
«Утверждаю»
Зав. кафедрой, профессор В.В.Хорунжий _______________________
| |
 Скачать 1.64 Mb.
Скачать 1.64 Mb.