Тағам биохим тест. 1Тағам химиясы ответы 2021. Сапалы талдау
 Скачать 51.45 Kb. Скачать 51.45 Kb.
|
|
Кондуктометрияда аналитикалық сигналдың пайда болуын қандай процестер анықтайды? (Екі дұрыс жауапты көрсетіңіз.) а) молекулалардың иондарға ыдырауы; б) электродтардың поляризациясы; в) сыртқы ток көзінің әсерінен иондардың көші-қоны; г) электрохимиялық реакция. 202. Электрөткізгіштіктің өлшем бірлігі: а) ампер; б) ом; в) сименс; г) кулон. Вольтампреометрия 203. Вольтамперометриялық ұяшықта қандай электрохимиялық процестер жүреді? а) анықталатын заттың толық электрге айналуы жүреді; б) электродтарда электрохимиялық реакция жүрмейді; в) электролизге анықталатын заттың аз мөлшері ұшырайды, жұмыс электродының бетіне жақын орналасқан; г) электролиз процесіне анықталатын зат пен фондық электролит қатысады. Орысшасы Какие электрохимические процессы протекают в вольтамперометрической ячейке? а) происходит полное электропревращение определяемого вещества; б) электрохимическая реакция на электродах не протекает; в) электролизу подвергается небольшое количество определяемого вещества, находящегося вблизи поверхности рабочего электрода; г) в процессе электролиза участвуют определяемое вещество и фоновый электролит. 204.. Тікелей вольтамперометрия әдістерінде аналитикалық сигнал ретінде қандай параметр қолданылады? а) жарты толқынның потенциалы; б) шекті диффузиялық ток; в) бөлу потенциалы; г) қалдық ток. Орысшасы Какой параметр используется в качестве аналитического сигнала в методах прямой вольтамперометрии? а) потенциал полуволны; б) предельный диффузионный ток; в) потенциал выделения; г) остаточный ток. 205.. Полярография әдістерінде аналитикалық сигналдың анықталатын заттың концентрациясына функционалды тәуелділігін қандай теңдеу сипаттайды? А) Илькович теңдеуімен; Ә) Фарадей Заңының теңдеуі; в) Нернст теңдеуі; г) Гейров теңдеуі ТЕСТ 2- ші ДЕҢГЕЙ: 206. Мына ТТР-дағы тотықтырғыштың, тотықсыздандырғыштың эквиваленттік массаларын есептеңіз: FeCl2 + KMnO4 + HCl --->FeCl3 + MnCl2 + KCl + H2O Осындай бірнеше сұрақ болады 207. Мына тотығу –тотықсыздану реакциясын теңестріңіз: NaNO2 + KMnO4 + H2SO4 ---> NaNO3 + MnSO4 + K2SO4 + H2O Теңдеудің оң жағының стехиометриялық коэффициенттерінің қосындысын анықтаныз. 5NaNO2 + 2KMnO4 + 3H2SO4 ---> 5NaNO3 + 2MnSO4 + K2SO4 + 3H2O Осындай бірнеше сұрақ болады 208. 1,5000 г Н2C2O42H2O кристаллогидратынан 0,25 л ерітінді дайындалды. Ерітіндінің титрін, нормальды концентрациясын есептеңіз Т=m/V, N=Tх1000/Э Осындай бірнеше есеп болады 209. Салмағы 2,5000 г Nа2С2О4-тен 1000 мл ерітінді дайындалды. Ерітіндінің молярлық, нормальды концентрацияларын және титрін есептеңіз. Т=m/V, N=Tх1000/Э, См= Tх1000/М э(Nа2С2О4)=134\2 = 67 Т=2,5000/1000 = 0,002500, N=0,002500х1000/67 = 0,0373, См= 0,002500х1000/134 = 0,187 Осындай бірнеше есеп болады 210. Егер T(KOH/ Н2SO4)= 0,004943 г/мл болса , N(H2SO4) анықтаңыз. :  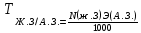 Э(H2SO4)=98\2=49 Э(H2SO4)=98\2=49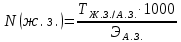 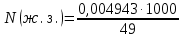 = =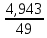 =0,100878= 0,1009 =0,100878= 0,1009Осындай бірнеше есеп болады 211. Егер T(Н2SO4 /KOH)= 0,005643 г/см3 болса , T(H2SO4) анықтаңыз (г/мл). 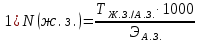 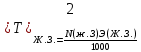 Осындай бірнеше есеп болады 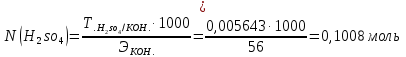 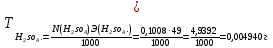 Жауап: 0,004940 г\мл 212. 1,6060 г натрий карбонатын V=100 мл өлшегіш колбада ерітті, осы ерітіндінің Т и СН табыңыз. m(Na₂CO₃)=1.6060г Э(Na₂CO₃)=106/2=53 V=100 мл T= 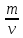 = =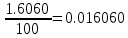 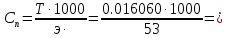 0.3030 0.3030Жауап: 0,016060; 0,3030 213. 15 мл NaОН ертіндісін 13 мл 0,1400 н НС1-мен титрледі. 250 мл ерітіндідегі натрий гидроксидының массасын анықтаңыз. Есептеуді пропорционалдылық ережесі бойынша анықталатын ерітіндінің нормалдығы арқылы жасаңыз. Э(NaОН)= 40 C(NаОН)= C(НСl)V(HCl)/ V(NаОН) = 0,1400*13/15 =0,1213 н m=C(NаОН)*Э(NаОН)*V= 0.1213*40*0,25 =1,2130 г 214. 15 мл NaОН ертіндісін 13 мл 0,1400 н НС1-мен титрледі. 250 мл ерітіндідегі натрий гидроксидының массасын анықтаңыз. Есептеуді Есептеуді титранттың анықталатын зат бойынша титры - T(HCl/NaOH) арқылы жасаңыз. Э(NaOH) = 40 Т = (0.1400*40)/1000 = 0.005600 г/мл 15х=13*250 Х=3250/15 х=216.7 M=T*v=0.005600*216.7 = 1.2135 г 215. 4,5100 г техникалық NaОН үлгісінен 250 мл ерітінді дайындалды. Осы ерітіндінің 15 мл NaОН ертіндісін 13 мл 0,1400 н НС1-мен титрледі. Үлгіде қанша NaОН пайызы бар? Есептеуді пропорционалдылық ережесі бойынша анықталатын ерітіндінің нормалдығы арқылы жасаңыз. Э(NaОН) = 40 C(NаОН)= C(НСl)V(HCl)/ V(NаОН)=0,1400*13\15 = 0,1213 m=C(NаОН)хЭ(NаОН)*v= 0,1213*40*0,25 = 1,213 г w = (1.213*100)/4.5100 = 26.89% С=а=0,1213н m=в=1,213г w=d=26,89% 216. 4,5100 г техникалық NaОН үлгісінен 250 мл ерітінді дайындалды. Осы ерітіндінің 15 мл NaОН ертіндісін 13 мл 0,1400 н НС1-мен титрледі. Үлгіде қанша NaОН пайызы бар? . Есептеуді Есептеуді титранттың анықталатын зат бойынша титры - T(HCl/NaOH) арқылы жасаңыз. Э(NaOH) = 40 T = N*Э(NaOH) / 1000 =( 0.1400 *40) /1000 = 0,005600 г/мл 15х = 13*250 Х = 216.7 m = T*v =0.005600*216.7= 1.2135 г W = (m*100)/mтех = (1.2135*100)/4.5100 = 26.9% T = 0,005600 г/мл m=1.2135 г w=26.9% Тотықсыздану процесiн көрсетiңiз. 2) SO42-SO32- 3) МnO2 Мn2+ Мn +4 O2-2 Мn 2+ тотықсыздану пр. 4) SO32-S2- H2S+4O32-S2- МnO42- МnO4- бір жауап болады Тотығу процесiн көрсетiңiз. As2O5As2O3 H3AsO4 As2O5 As2O3 AsH3 H3AsO3H3AsO4 +3----+5 As2O3 HАsO2 Тотықсыздану процесiн көрсетiңiз. 2O-2 O2о MnO4-MnO2о FeFe+3 2Br-Br20 NO2-NO3- Осындай ТТР сұрақтар көп болады Бейтарап ортада KMnO4–тің 500 мл 2 н. ертіндісін дайындау 3,3430 г KMnO4-ті 500мл өлшеуіш колбада ерітті. Бейтарап орта үшін ерітіндінің нормальды концентрациясы мен титрін табыңыз. 6,1530г KMnO4 –ті 2000 мл өлшеуіш колбада ерітті. Қышқыл орта үшін ерітіндінің нормальды концентрациясы мен титрін табыңыз. Э(KMnO4 ) = 31.61 г/моль T=m/v = 6.1530/2000 = 0.003077 N=(T*1000)/Э = (0.003077*1000)/31.61 = 0.0973 5,8890г KMnO4 2000 мл өлшеуіш колбада ерітті. Сілтілі орта үшін ерітіндінің нормальды концентрациясы мен титрін табыңыз. |
