лимонка. Схема 1 получение глицерина из пропилена
 Скачать 438.18 Kb. Скачать 438.18 Kb.
|
|
Предложите принципиальную технологическую схему получения лимонной кислоты из продуктов первичной переработки нефти и необходимого неорганического сырья. Запишите уравнения химических реакций, лежащие в основе технологической схемы, и условия их протекания. Покажите, какие процессы и аппараты будут использованы на каждой стадии производства. Оцените экологическую и экономическую составляющие предложенной схемы, опишите возможные способы переработки и утилизации отходов данного производства. Схема 1: получение глицерина из пропилена: 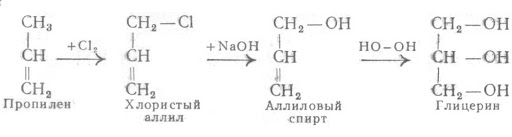 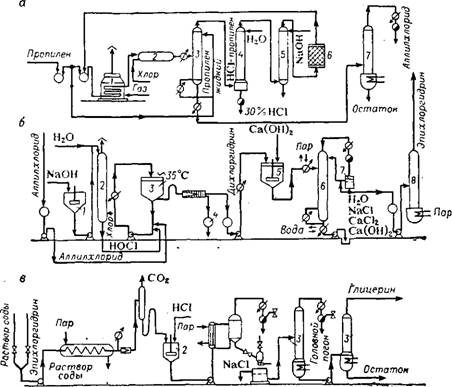 Рисунок 1. Технологическая схема химического цеха производства глицерина. а — хлорирование пропилена: 1 — нагреватель (от 20 до 400 °С); 2 — реактор; 3 — фракционная колонна; 4 — абсорбер; 5 — промывная колонна; в — сушильная башня; 7 — система из трех колонн для перегонки Аллилхлорида. б — хлоргидрирование аллилхлорида: I — растворитель щелочи; 2 — приготовление НОСІ; 3 — реактор; 4 — отбор трихлорпро - пена и тетрахлорпропилоного эфира; 5 — аппарат для отщепления НС1; в — колонна азео - ропной дистилляции; 7 — сепаратор; 8— система из дв^х колонн для обезвоживания и перегонки эпихлоргидрина; в — омыление эпихлоргидрина: 1 — подогреватель (Юо—180 °С, 10 кгс/см2); 2 — нейтрализатор; з — колонна для перегонки глицерина. Схема 2: получение лимонной кислоты из глицерина: 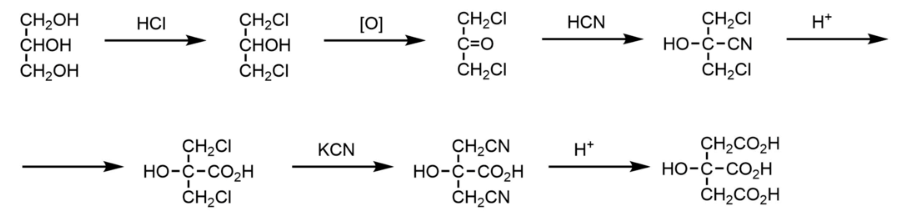 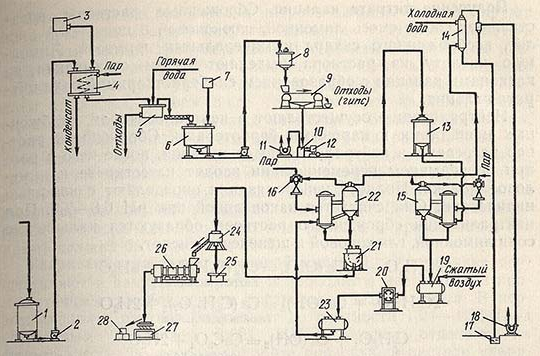 Рисунок 2. Технологическая схема химического цеха производства лимонной кислоты: 1 – сборник сброженных растворов; 2 – насос; 3 – сборник известкового молока; 4 – нейтрализатор; 5 – нутч-фильтр для отделения цитрата кальция; 6 – реактор; 7 – бачок-мерник серной кислоты; 8 – промежуточный сборник; 9 – ленточный вакуум-фильтр для отделения гипса; 10 – вакуум-сборник; 11 – вакуум-насос; 12 – насос; 13 – сборник раствора лимонной кислоты; 14 – барометрический конденсатор с ловушкой; 15 – вакуум-аппарат первой упарки; 16 – пароструйный компрессор; 17 – барометрический ящик; 18 – вакуум-насос; 19 – монтежю; 20 – фильтр-пресс; 21 – кристаллизатор; 22 – вакуум-аппарат второй упарки; 23 – промежуточный сборник; 24 – центрифуга; 25 – сборник маточного раствора; 26 – барабанная сушилка; 27 – трясосито; 28 – упакованная лимонная кислота. Получение глицерина. Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450-500°С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, CH2ClCHOHCH2Cl, которые при омылении щёлочью превращаются в глицерин. На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы. Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный ZnO — MgO катализатор образуется аллиловый спирт. Он при 190-270°C в водном растворе перекиси водорода превращается в глицерин. Получение лимонной кислоты. Впервые лимонную кислоту химическим синтезом получили Гримо (Grimaux) и Адам (Adam) в 1880 году. Исходным соединением в этом синтезе послужил глицерин. Первичные гидроксильные группы молекулы глицерина сначала замещали на атомы хлора, а затем на нитрильные группы, которые при гидролизе давали концевые карбоксильные группы. Вторичную же гидроксильную группу окисляли до кетогруппы, к которой затем присоединяли циановодород; полученный циангидрин также при гидролизе давал карбоксильную группу. Описание получения лимонной кислоты Сброженные растворы представляют собой смесь лимонной, глюконовой и щавелевой кислот, несброженного сахара и минеральных примесей. Лимонную кислоту из раствора выделяют путем связывания ее катионами кальция с образованием слаборастворимой соли цитрата кальция. Нейтрализацию осуществляют в нейтрализаторах, снабженных мешалками и паровыми барботерами. Сброженный раствор нагревают в нейтрализаторе до кипения, после чего в него при непрерывном перемешивании вводят известковое или меловое молоко. Полноту нейтрализации определяют с помощью индикатора. Она считается законченной при pH 6,8-7,5. При нейтрализации сброженного раствора образуются кальциевые соли лимонной, глюконовой и щавелевой кислот. Кальциевые соли лимонной и щавелевой кислот выпадают при этом в осадок, а кальциевая соль глюконовой кислоты и основная часть органических и минеральных веществ мелассы остаются в растворе. Для отделения образовавшегося осадка горячую реакционную массу передают на вакуум-фильтры. После отделения маточного раствора осадок на фильтре промывают горячей водой (температура около 95 °С). Об окончании промывки судят по отсутствию в промывных водах сахара. Для подсушивания через осадок в течение некоторого времени пропускают воздух. Перевод лимонной кислоты в свободное состояние и отделение ее от оксалата кальция достигается обработкой осадка серной кислотой с последующим фильтрованием. Разложение цитрата кальция осуществляют в реакторе, снабженном мешалкой и паровым барботером. В реактор подают воду из расчета 0,25-0,5 м3 на 1 т лимонной кислоты и при работающей мешалке загружают туда цитрат кальция с таким расчетом, чтобы после его разложения концентрация лимонной кислоты в растворе была не меньше 25%. В качестве осветлителя в реактор вводят активный уголь (2% к массе лимонной кислоты), содержимое реактора нагревают до 60 °С и при перемешивании подают из мерника серную кислоту (плотность 1,80-1,84) из расчета 0,425 л на 1 кг лимонной кислоты в цитрате. Смесь кипятят в течение 10-20 мин. После полного разложения цитрата кальция (контролируют по отсутствию в среде цитрата кальция и серной кислоты) в реактор вводят гранулированный сернистый барий (из расчета 0,10-0,15 кг на 100 кг лимонной кислоты) для осаждения тяжелых металлов. Для отделения раствора лимонной кислоты от осадка, содержащего гипс, оксалат кальция, уголь, сернистые соединения тяжелых металлов и берлинскую лазурь, горячую реакционную смесь направляют из реактора на вакуум-фильтр. Отфильтрованный раствор передают на дополнительное упаривание, а осадок на фильтре промывают горячей водой (90°С). Промывку осадка прекращают при содержании лимонной кислоты в промывной воде 0,1 %. Средняя концентрация раствора лимонной кислоты (вместе с промывными водами) должна быть не ниже 16%. Упаривание осуществляют в вакуум-аппаратах и проводят в две стадии с промежуточным освобождением раствора от осадка гипса. В первом аппарате раствор упаривают до плотности 1,24-1,26 (под остаточным давлением 0,021 МПа), осадок отделяют на фильтр-прессе. Во втором аппарате прозрачный раствор упаривают (под остаточным давлением 0,021 МПа) до плотности 1,35-1,36, что соответствует концентрации лимонной кислоты 80% (около 1070 г моногидрата в 1 л). Из вакуум-аппарата вторично упаренный раствор температурой 70 °С передают на кристаллизацию. После заполнения кристаллизатора раствор охлаждают до 35-37 °С и вносят в него затравку - кристаллы лимонной кислоты. Кристаллизацию проводят при непрерывном перемешивании и медленном охлаждении до температуры 8-10 °С. При конечной температуре кристаллизации раствор выдерживают не менее 30-45 мин. Кристаллы отделяют в центрифуге, промывают их небольшим количеством холодной воды, затем кристаллы влажностью 2-3% передают на сушку. Сушку проводят в ленточных или барабанных пневматических сушилках при температуре воздуха не более 35 °С. При: более высокой температуре происходит разрушение кристаллов вследствие потери ими кристаллизационной воды. В товарном продукте должно содержаться не менее 99,5% лимонной кислоты (в пересчете на моногидрат), зольность не более 0.1% для высшего сорта и 0,35% для I сорта. Экономическая составляющая производства Производство лимонной кислоты химическими способами экономически нецелесообразно: стоимость сырья значительно выше стоимости мелассы; технология многостадийна, требует применения сильно токсичных реагентов и дает относительно низкий выход целевого продукта. Поэтому несмотря на большой прогресс в области химического синтеза различных органических соединений, такие сравнительно простые вещества, как лимонная, молочная и некоторые другие кислоты, вырабатывают из сахаросодержащегося сырья с помощью микроорганизмов. Преимущества микробного способа в последовательном ферментативном осуществлении в клетке даже значительно большего числа химических реакций в одну производственную стадию - ферментацию. Это упрощает технологию, увеличивает выход кислот и снижает их себестоимость. Наиболее экономически выгодно производить лимонную кислоту поверхностным способом, так как себестоимость лимонной кислоты несколько ниже. Этот способ имеет и другие преимущества: выше концентрация лимонной кислоты в культуральной жидкости, значительно меньше образуется побочных кислот, вследствие чего затрачивается меньше мелассы при ферментации и меньше потери при химической переработке культуральных жидкостей. При поверхностном способе гриб менее чувствителен к перерывам в аэрации. Обслуживание и контроль процесса ферментации просты, проблемы возникают только при необходимости поддержания требующейся температуры воздуха в камере при высокой температуре наружного воздуха. Экологическая составляющая производства Данная схема экологически нецелесообразна, так как производство лимонной кислоты из глицерина имеет большое количество отходов и побочных продуктов, в частности отвалы гипса. Отвалы гипса можно перерабатывать в других отраслях производств, но для этого нужно учитывать тот факт, что завод по производству лимонной кислоты должен находиться неподалеку от завода по переработке гипса, либо же на самом заводе по производству ЛК нужен дополнительный цех для данных отходов. СОДЕРЖАНИЕ Схема 1: получение глицерина из пропилена Схема 2: получение лимонной кислоты из глицерина Получение глицерина. Получение лимонной кислоты Описание получения лимонной кислоты Экономическая составляющая производства Экологическая составляющая производства БИБЛИОГРАФИЯ Дьяконов И. А. Глицерин // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1988. — Т. 1: А—Дарзана. — С. 585. — 623 с. — 100 000 экз. — ISBN 5-85270-008-8. Verhoff F. H., Bauweleers H. Citric Acid (англ.) // Ullmann's Encyclopedia of Industrial Chemistry. — Wiley, 2014. http://www.spec-kniga.ru/tehnohimicheski-kontrol/obshchaya-tekhnologiya-mikrobiologicheskih-proizvodstv/organicheskie-kisloty-limonnaya-kislota.html |
