курсовая (Автосохраненный). Синтез новых веществ с уникальными свойствами
 Скачать 315.51 Kb. Скачать 315.51 Kb.
|
|
Глава 2. Нанотехнология 2.1 Основное понятие нанотехнологий В современном мире за последние несколько лет происходит стремительное развитие нанотехнологий. Особенность нанотехнологий заключается в возможности их применения в неограниченной сфере, поэтому они являются базисом для совершенно нового технологического уклада экономики. Нанотехнологии наряду с информационными и биотехнологиями служат фундаментом научно-технической революции в XXI в. Возможности их разностороннего применения в таких областях экономики, как производство полупроводников, медицина, сенсорная техника, экология, автомобилестроение, строительные материалы, биотехнологии, химия, авиация и космонавтика, машиностроение и текстильная промышленность, несут в себе огромный потенциал роста. Применение продукции нанотехнологий позволит сэкономить на сырье и потреблении энергии, сократить выбросы в атмосферу и, как следствие, будут способствовать устойчивому развитию экономики [3, с. 345]. 2.2 Нанообъекты В переводе с греческого слово "нано" означает карлик. Один нанометр (нм) — это одна миллиардная часть метра (10-9 м). Размеры объектов, с которыми имеют дело нанотехнологии, лежат в диапазоне от 0,1 до 100 нм. Большинство атомов имеют диаметр от 0,1 до 0,2 нм, а толщина нитей ДНК — около 2 нм. Нанометр во столько же раз меньше одного метра, во сколько толщина пальца меньше диаметра Земли. Идея о том, что вполне можно собирать устройства и работать с объектами, которые имеют наноразмеры, была впервые высказана Ричардом Фейнманом в 1959 г. По словам Фейнмана человек очень долго жил, не замечая, что рядом с ним живет целый мир объектов, разглядеть которые он не в состоянии. Тем не менее мы сами состоим из устройств, которые прекрасно научились работать с нанообъектами. Это наши клетки — кирпичики, из которых состоит наш организм. Клетка всю свою жизнь работает с нанообъектами, собирая из различных атомов молекулы сложных веществ. Собрав эти молекулы, клетка размещает их в различных своих частях — ядре, в цитоплазме, в мембране. Представьте себе возможности, которые открываются перед человечеством, если оно овладеет такими же нанотехнологиями, которыми уже владеет каждая клетка человека! Сейчас химики используют для синтеза новых веществ сложные и разнообразные приемы. Как только физики создадут устройства, способные оперировать отдельными атомами, многие методы традиционного химического синтеза могут быть заменены приемами "атомной сборки". Химики будут заказывать синтез, а физики — просто "укладывать" атомы в предлагаемом порядке. Развитие техники манипуляции на атомарном уровне позволит решить многие проблемы химии и биологии. Примерами нанообъектов образующих наноструктуры, являются углеродные нанотрубки, фуллерены, квантовые точки и дендримеры. Первыми устройствами, с помощью которых стало возможным наблюдать за нанообъектами и передвигать их, стали сканирующие Фондовые микроскопы — атомно-силовой микроскоп (АСМ) и туннельный микроскоп. Создание атомно-силового микроскопа дало возможность, наконец, "пощупать и увидеть" нанообъекты. Основой АСМ служит микрозонд, представляющий собой тонкую пластинку. На ее конце расположен очень острый шип (кантилевер), оканчивающийся одним или группой из нескольких атомов Заслуга нанотехнологий состоит и в том, что они способы придавать привычным на первый взгляд материалам дополнительные свойства. Одним из таких примеров является высокопрочный бетон. Специалисты утверждают, что новый бетон прослужит верой и правдой лет 500. На его основе можно возводить небоскребы, большие мосты. В химическом производстве применяют и нанокатализаторы. Примерами таких реакций могут служить следующие реакции: 1. Синтез бензола из ацетилена (палладий на пленке MgO): 2. Окисление угарного газа кислородом (нанокластеры золота): 3. Гидрирование монооксида углерода (наночастицы кобальта сферической формы): Последние годы вложений ознаменовались бурным рею том интереса к нанотехнологии и ростом вложений инвестиций в нее. И это вполне понятно, учитывая, что нанотехнологии обеспечивают высокий потенциал экономического роста, от которого зависят качество жизни населения, технологическая и оборонная безопасность, ресурсо- и энергосбережение. Сейчас практически во всех развитых странах действуют национальные программы в области нанотехнологии Графен. Графен был синтезирован российскими учеными А. Геймом и К. Новоселовым. Нанотехнологии позволили ученым изготовить углеродную пластину более твердую, чем алмаз, толщина которой составляет всего один атом. Состоит она как раз таки из графена. Это самый тонкий и прочный материал во всей Вселенной, который пропускает электричество намного лучше кремния компьютерных чипов. Графен представляет собой двухмерный кристалл. Его структура является гексагональной решеткой, состоящей из атомов углерода. На сегодняшний день химики, физики, а также инженеры-электронщики уже заинтересовались уникальными возможностями графена. К достоинствам графена можно отнести следующее: Высокая электропроводность. Графен может проводить электричество как обычная медь. На его основе можно создавать различные электрические приборы. Отличная оптическая чистота. Может поглощать только чуть более двух процентов видимого света вне зависимости от характеристик излучения. Вследствие этого данный материал практически бесцветен. Сторонний наблюдатель может назвать его невидимым. Высокая механическая прочность. По прочности превосходит алмаз. Гибкость. Является более гибким, чем кремний. По данным параметрам он превосходит даже резину. Благодаря однослойной структуре можно изменять форму и растягивать графен по мере необходимости. Рекордная теплопроводность. По данному показателю превосходит медь в десять раз. Медицина. Оксид графена убивает стволовые клетки, которые запрограммированы на преобразование в раковую опухоль. Он уменьшает размер опухоли, предотвращая ее дальнейший рост. К недостаткам графена можно отнести следующее: • Удается получить лишь небольшие по размерам листы графена. • Производство графена требует значительных затрат, что ограничивает его применение. Наноматериалы бывают внешними и внутренними. Важными материалами являются фуллерены, нанотрубки, графен. 2.3 Способы получения наноматериалов Наноматериалы синтезируют способами: химической конденсации, монохимической реакцией, термическим разложением и восстановлением. 1. Химическая конденсация Химические методы получения наночастиц и ультрадисперсных систем известны достаточно давно. Коллоидный раствор золя золота (красного) с размером частиц 20 нм был получен в 1857 г. М. Фарадеем. Наиболее простым и часто используемым способом является синтез наночастиц в растворах при протекании различных реакций. Для получения металлических наночастиц применяют реакции восстановления, при которых в качестве восстановителя используют алюмо- и борогидриды, тетрабораты, гипофосфиты и многие другие неорганические и органические соединения. Наноразмерные частицы солей и оксидов металлов получают чаще всего в реакциях обмена и гидролиза. Например, золь золота с размером частиц 7 нм может быть получен восстановлением хлорида золота боргидридом натрия с использованием в качестве стабилизатора тиолы. В качестве стабилизаторов используют и другие органические соединения, способные образовывать поверхностные комплексы. Реакцию гидролиза проводят в органических растворителях. Последующая полимеризация приводит к образованию геля: 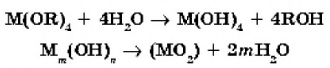 Этот метод обладает чрезвычайно широкими возможностями и позволяет получать материалы, содержащие и биологически активные макромолекулы. 2. Получение наночастиц с помощью топохимических реакций С помощью топохимических реакций (реакций в газовой среде) конденсации из паровой фазы можно получать наночастицы желаемых соединений. Газофазные химические реакции можно разделить на реакции разложения, протекающие с участием одного реагента по схеме: и реакции между двумя и более реагентов по схеме: Необходимым условием протекания первого типа химических реакций является существование реагента, содержащего все элементы конечного продукта, поэтому второй тип газофазных реакций находит более широкое распространение. При проведении газофазных химических реакций исходные реагенты должны быть легколетучими. В качестве исходных реагентов широко используются галогениды (особенно хлориды металлов), оксихлориды металлов МеОnСlm, алкооксиды Me(OR)n, алкильные соединения Me(R)n, пары металлов и так далее. Этим методом можно получать наноматериалы бора, газовой сажи, металлов, сплавов, нитридов, карбидов, силицидов, сульфидов и других соединений. 3. Термическое разложение и восстановление В процессах термического разложения обычно используют сложные металлорганические соединения, гидроксиды, карбонилы, формиаты, нитраты, оксалаты, амиды и амиды металлов, которые при определенной температуре распадаются с образованием синтезируемого вещества и выделением газовой фазы. В общем виде основную реакцию, например, пиролиза формиатов можно представить в виде следующего результирующего уравнения: По той же схеме происходит разложение формиатов Сu и Zn и других металлов. Термическое разложение оксалатов многих металлов (Mn, Fe, Сu) протекает по уравнению Пиролиз оксалатов, формиатов и других солей позволяет получать порошки с размером частиц около 100 нм. Путем термической диссоциации карбонилов при температуре до 773 К по реакции возможно получение полиметаллических пленок с размерами кристаллитов порядка 20 нм. Метод восстановления используют для получения наноматериалов (чаще всего металлов) из исходных кислородсодержащих соединений. При переработке оксидов металлов в качестве восстановителей используют газы — водород, монооксид углерода, конвертированный природный газ. Этим процессам соответствуют реакции, в результате которых получают нанопорошки металлов: Fe, W, Ni, Mo, Сu, Co. 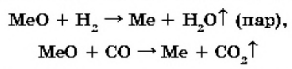 Наноматериалы синтезируют химической конденсацией, с помощью топохимических реакций и термических разложений. 2.4 Разработка новых полимеров Все современное развитие человечества неразрывно связано с развитием индустрии пластмасс — созданием новых и развитием существующих полимеров, способов их переработки, созданием изделий с новыми свойствами. Сегодняшний мир уже давно невозможно представить без пластмасс — начиная от предметов, окружающих нас в наших домах, и заканчивая деталями космических спутников и ракет. И эти пластмассовые предметы и детали поражают воображение и своими свойствами, и своими применениями, и размерами (от части корпуса трансатлантических авиалайнеров до наночастей медицинских устройств, вживляемых в организм человека). Ознакомимся с новыми видами полимеров, обладающими особыми свойствами. Кевлар. Кевлар был изобретен в 1964 году американской ученой-химиком Стефани Луизой Кволек во время ее работы в компании "Дюпон". К 1971 году группе ученых компании удалось доработать материал, и началось его массовое производство. Кевлар получается реакцией поликонденсации из терефталевой кислоты и па-рафенилендиамина. Кевларовое волокно обладает рядом уникальных свойств:  • оно в несколько раз прочнее стали; • сохраняет прочность при очень низких температурах, а при высоких (при том очень высоких: около 400°С) разлагается, не плавится, относительно легкий. Внешний вид кевларового волокна представляет собой нити характерного золотисто-желтого цвета. Диаметр элементарного волокна 10 мкм. Все перечисленные свойства позволяют использовать кевлар для производства непрокалываемых шин, бронежилетов, сверхпрочных тросов и прочих изделий, для которых такое качество, как прочность, является ключевым. Что делает кевлар столь прочным? Рассмотрим строение полимерной цепи. Кевлар — кристаллический полимер. В кристаллических веществах есть порядок. Кристаллические полимеры, как и вообще все кристаллические вещества, отличаются от полимеров как раз прочностью и высокими температурами плавления. Более компактной упаковке нитей полимера способствует транс-строение арамида: Пунктиром обозначены слабые водородные связи между цепями полимера. Как мы видим, заместители у бензольного кольца находятся в пара-положении (что отражено в названии: пара-арамид). Потому другие полиамиды и не отличаются прочностью: в цепях структурные звенья встречаются как цис-, так и транс-строения. Но вот с арамидами дела обстоят иначе: почти вся цепь имеет транс-строение.  Материал Кевлар — это пара-арамид. Компания DuPont также выпускает мета-арамид: Его торговое название Номекс. Он используется как огнеупорный компонент, тоже прочный. Из смеси номекса и кевлара изготавливают огнеупорную одежду. И ни в одном из перечисленных выше направлений развития человечества невозможно представить себе жизнь без пластмасс. Это и медицинские устройства, сохраняющие многие тысячи жизней, и упаковка, сберегающая миллионы тонн продуктов, и части устройств, помогающих получать энергию из альтернативных источников, и средства связи, и детали и части автомобилей, самолетов и космических ракет. Биоразлагаемые полимеры. Суммарный объем производства полимерных материалов во всем мире достигает многих десятков миллионов тонн. Свойства полимеров весьма разнообразны и определяются их областью применения. На основе полипропилена и ароматических полиамидов, например, созданы ценные конструкционные материалы, устойчивые к различным воздействиям. Эти материалы с успехом применяют, в частности, в строительстве и машиностроении. Однако не во всех областях требуются очень прочные и устойчивые к различным воздействиям полимеры. К таким областям относится, например, изготовление тары различного рода: мешки, пакеты, бутыли и т. д. Срок службы таких полимерных изделий невелик, вследствие чего многие миллионы тонн полиэтилена, полипропилена и других материалов ежегодно попадают на свалки. Эти материалы не гниют в почве и устойчивы к атмосферным воздействиям, так как в соответствующих организмах (грибы, бактерии) отсутствуют ферменты, способные разрушать синтетические полимерные материалы, поэтому проблема защиты окружающей среды от устойчивых полимеров превратилась в одну из актуальных глобальных задач. Создав исключительно прочные полимерные материалы, химики теперь озабочены прямо противоположной проблемой: как получить материалы, обладающие непродолжительным сроком эксплуатации и способные разлагаться в природных условиях. Исследования развиваются в двух направлениях: 1. Применение биополимеров. Биополимеры производятся живыми организмами и способны разлагаться в природных условиях. Речь при этом идет прежде всего о полисахаридах {крахмал, целлюлоза). 2. Синтез аналогов биополимеров, способных к разрушению под действием света или бактерий, а также полимеров, растворимых в воде. На пути создания синтетических биоразлагаемых полимеров достигнуты первые успехи. Разработан процесс изготовления предметов тары из полиэтилена, в который внедрены частицы крахмала. Крахмал весьма неустойчив в природных условиях, вследствие чего все изделия из такого полимера разлагаются значительно быстрее, чем обычные полимеры. Полезным полимером оказался поливинилацетат. При его гидролизе получают еще один биоразлагаемый материал — поливиниловый спирт. 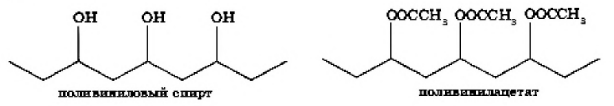 Его ценным качеством является растворимость в воде. Тара, изготовленная из поливинилового спирта, оказывается очень проста в утилизации. Специалисты в области "зеленой" химии, перед которой в странах Западной Европы и США поставлены задачи создания безотходных и безопасных для окружающей среды технологий, возлагают большие надежды на полимолочную кислоту (ПМК). ПМК — алифатический полиэфир, который получают поликонденсацией молочной кислоты или полимеризацией циклического димерного лактида.  ПМК легко разлагается в природных условиях или гидролизуется до молочной кислоты, которая может быть вновь превращена в полимер. Пленки ПМК обладают эластичностью, пригодны для изготовления тары, в том числе дня пищевых продуктов, так как защищают упакованный товар от запахов и загрязнений. Такой полимер может саморазлагаться в природе за несколько дней Полагают, что ПМК может оказаться особенно перспективной для изготовления синтетических ковров, поскольку пригодна для изготовления как лицевой стороны, так и основы ковра. Разработан новый метод производства полимолочной кислоты. По этому методу синтетический полимерный материал впервые производят из ежегодно возобновляемого растительного сырья — углеводов кукурузы. Процесс начинается с ферментативного расщепления декстрозы до молочной кислоты. Полученную кислоту очищают и конденсируют в непрерывном процессе до низкомолекулярного полимера (с молекулярной массой — 5000. Создание биоразлагаемых полимеров позволит решить экологическую проблему загрязнения окружающей среды. Но, конечно же, надо обратить внимание на развитие самих полимеров, ведь для решения глобальных проблем будут требоваться новые подходы, новые изделия (или новые компоненты существующих) с новыми назначениями и свойствами. Ученые из Технологического университета Делфта приступили к испытаниям уникального бетона, который самостоятельно восстанавливает трещины и повреждения с помощью бактерий. Голландские ученые решили проблему, создав "живой" бетон, трещины на котором затягиваются, как раны на человеческом теле. Для этого они добавили в состав гранулы, содержащие споры бактерий рода Bacillus и лактат кальция, который питает микроорганизмы. Споры могут в течение многих лет сохранять свои свойства. В случае появления трещины влага попадает внутрь гранул и бактерии переходят в активное состояние. При этом они потребляют питательное вещество и производят минерал кальцит, который заполняет образовавшиеся пустоты [14, с. 213]. |
